华师大版科学九年级上册 期中达标检测卷(含答案)
文档属性
| 名称 | 华师大版科学九年级上册 期中达标检测卷(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-09-20 17:28:16 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
期中达标检测卷
一、选择题(每小题4分,共60分)
1.
如图是物质X溶于水中发生电离的微观示意图,其中能说明X是一种酸的是(
)
2.
下面是用8mL蒸馏水稀释浓硫酸的实验操作过程,其中错误的环节是(
)
3.
某偏远山村学校食堂的中餐食谱为:主食:米饭;配菜:炒土豆、咸萝卜、白菜汤。为强壮身体、均衡营养,在“心连心”活动中,最好送去的是(
)
A.
猪油和菜油
B.
鸡蛋和牛肉
C.
小白菜和大白菜
D.
白糖和红糖
4.
(杭州中考)在试管中放入一根镁条(已去除氧化膜),往其中加入硝酸银溶液至浸没镁条,观察到如下现象:①镁条表面迅速覆盖一层疏松的固体物质,经检验发现生成的固体物质中有单质银;②镁条表面有明显的气泡现象,经检验发现气泡中有氢气。对于上述实验现象的分析错误的是(
)
A.
镁能从硝酸银溶液中置换出银
B.
镁跟硝酸银溶液反应会生成氢气
C.
镁投入硝酸银溶液中只发生2AgNO3+MgMg(NO3)2+2Ag
D.
根据该实验可判断镁比银化学活动性强
5.
金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用A表示):12HF+3Na2CO3+2Al(OH)32A+3CO2+9H2O,则A的化学式为
…………………(
)
A.
NaAlF6
B.
Na2AlF6
C.
Na3AlF6
D.
Na3Al2F6
6.
现有硫酸钠、碳酸钠、硝酸银三种无色溶液,滴入一种试剂可产生三种不同的现象,这种试剂可以是(
)
A.
氯化钡溶液
B.
稀硝酸
C.
稀盐酸
D.
氢氧化钠溶液
7.
下列物质不属于有机高分子化合物的是(
)
A.
淀粉
B.
油脂
C.
棉花
D.
蛋白质
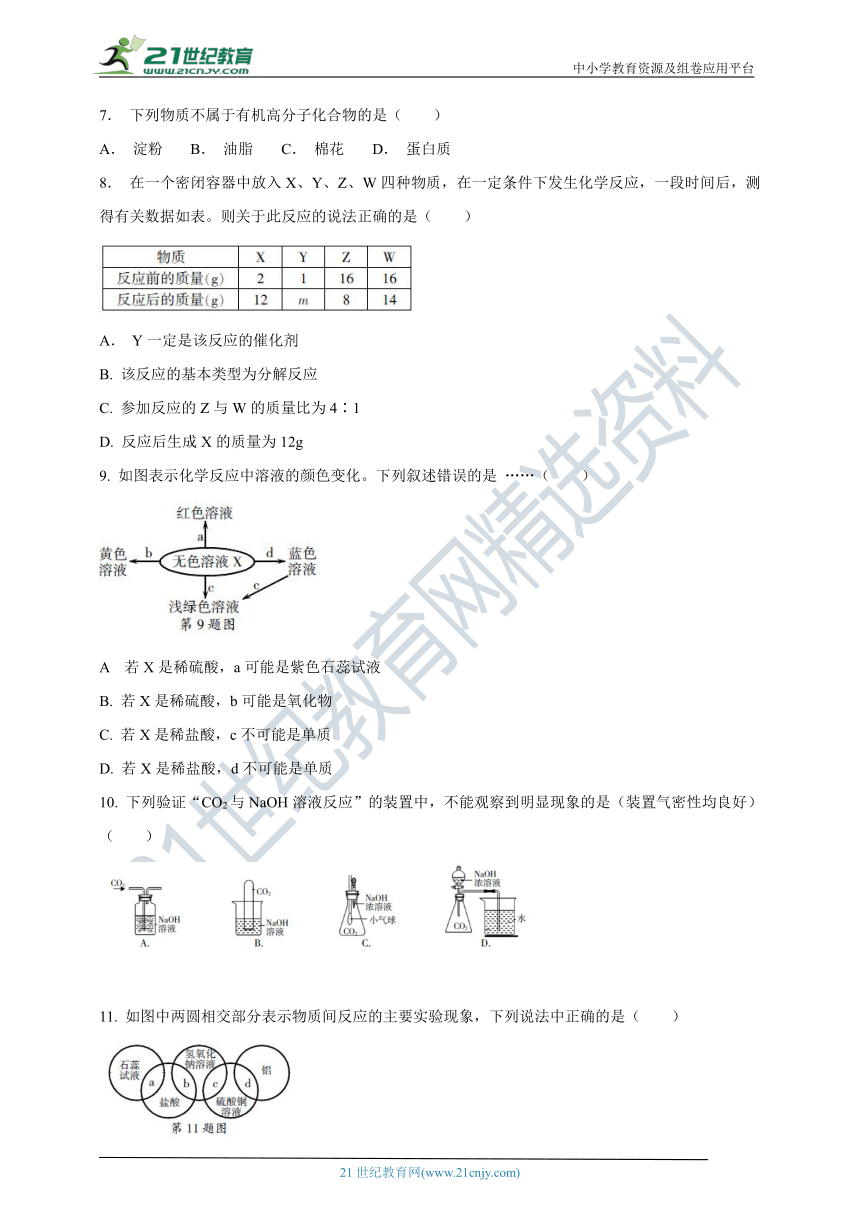
8.
在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表。则关于此反应的说法正确的是(
)
A.
Y一定是该反应的催化剂
B.
该反应的基本类型为分解反应
C.
参加反应的Z与W的质量比为4∶1
D.
反应后生成X的质量为12g
9.
如图表示化学反应中溶液的颜色变化。下列叙述错误的是
……(
)
A
若X是稀硫酸,a可能是紫色石蕊试液
B.
若X是稀硫酸,b可能是氧化物
C.
若X是稀盐酸,c不可能是单质
D.
若X是稀盐酸,d不可能是单质
10.
下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)(
)
11.
如图中两圆相交部分表示物质间反应的主要实验现象,下列说法中正确的是(
)
A.a处溶液呈蓝色
B.
b处反应后溶液的总质量增加
C.
c处产生白色沉淀
D.
d处银白色固体表面有红色固体析出
12.
甲、乙两工厂的生产污水中各含有下列五种离子中的三种(两厂含有一种相同的离子):H+、Cu2+、K+、NO-3、OH-。若两厂单独排放都会造成严重的污染。若将两厂的污水按一定比例混合,沉淀后污水会变成只含一种溶质的无色澄清溶液,此溶质可作化肥。下列关于污水的分析,正确的是(
)
A.
OH-和Cu2+来自同一工厂
B.
Cu2+和K+来自同一工厂
C.
K+和OH-来自同一工厂
D.
H+和K+来自同一工厂
13.
(宁波中考)下列实验中,根据有关现象得出结论,合理的是(
)
14.
(台州中考)语馨对Fe2O3做了如图探究活动,已知氯气在水溶液中能将Fe2+转变为Fe3+,且每一步都充分反应。下列分析正确的是
…………(
)
A.
无色气体可以使澄清石灰水变浑浊
B.
黑色粉末是Fe3O4
C.
①过程Fe2O3中的氧元素全部转入无色气体
D.
②过程有置换反应发生
15.
(绍兴中考)将质量均为10g的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,反应完成后,生成氢气的质量关系不可能的是(
)
二、填空题(每空3分,共66分)
16.
化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题:
(1)“沙里淘金”说明黄金在自然界中能够以
(填“单质”或“化合物”)形式存在。
(2)葡萄表皮上因喷洒“波尔多液”而呈现的蓝色斑点,可以用厨房调料
洗净。
17.
(湖州中考)有机物是自然界物质中的一个大家族。
(1)下列是生活中常见的物质:①尿素[CO(NH2)2];②纯碱(Na2CO3);③酒精(C2H5OH);④葡萄糖(C6H12O6),属于有机物的是
(填序号)。
(2)食醋是生活中常用的调味品,其主要成分是乙酸(CH3COOH),在乙酸分子中碳、氢、氧的原子个数比是
。
(3)一定质量的某有机化合物X与8克氧气恰好完全反应,生成8.8克二氧化碳和1.8克水。X中各元素的质量比为
。
18.
(丽水中考)“寓学于乐”是一种有效的学习方式,如图是“盖房子”的游戏示意图,其规则是根据“上下相邻两层的物质之间均可发生化学反应”来堆砌楼层。图中已放置好四种物质,还有二氧化碳、碳酸钠溶液、硫酸铜溶液三种物质待放置。请回答:
(1)二氧化碳应放在
处(填序号)。
(2)将氢氧化钠溶液滴到③中,产生的实验现象是
。
(3)第二层内的两物质间能相互转化,请写出其中的一个化学方程式:
。
19.
将一定质量的锌粒投入到含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液呈无色,则滤渣中一定含有
,滤液中一定含有的溶质是
,请任写出一个反应的化学方程式:
。
20.
乙醇汽油的使用,可以缓解石油危机。所谓乙醇汽油是在汽油中加入适量乙醇混合而成的一种燃料。
(1)乙醇汽油属于
(填“纯净物”或“混合物”)。
(2)从环境保护的角度看,下列燃料中最理想的是
(填字母编号)。
A.
氢气
B.
煤
C.
乙醇汽油
D.
煤气(主要含CO)
21.
(衢州中考)硫酸钡不容易被X射线透过,在医疗上可用作检查肠胃的内服剂,俗称“钡餐”。小柯将硫酸镁溶液滴入硝酸钡[Ba(NO3)2]溶液中得到硫酸钡,如图表示该实验过程中溶液总质量随加入硫酸镁溶液质量的变化情况。图线AB段对应的实验现象是
,C点处溶液中的溶质有
。
22.
(1)小明用滤纸折成一只纸蝴蝶,并在上面喷洒了试剂A,挂在铁架台上。另取一只盛有溶液B的烧杯,放在纸蝴蝶的下方,如图,过一会儿,纸蝴蝶的颜色变成红色。请从下面提供的试剂找出A、B可能的组合
(填序号)。
①石蕊试液
②酚酞试液
③浓盐酸
④浓硫酸
⑤氢氧化钠溶液
⑥浓氨水
(2)只用下列试剂中的一种进行实验,就能确定B的成分,则该试剂可能是
(填序号)。
①Na2CO3溶液
②BaCl2溶液
③铁钉
④NaCl溶液
23.
(绍兴中考)实验室制氧气的方法可以是:
方法一:2H2O22H2O+O2↑
方法二:2KMnO4K2MnO4+MnO2+O2↑
(1)这两种涉及到的化学反应基本类型都是
反应。
(2)用方法二制取一瓶氧气,可选择如图装置中的
(填字母)。
24.
小倩同学将妈妈的智能新手机屏幕解锁图形设置为如图所示,圆圈内每个数字分别代表初中化学常见的一种物质(“-”表示相连两种物质能发生化学反应,反应条件省略)。其中1为碳粉,7可用于工业上玻璃、造纸、洗涤剂的生产等,1、2、3、5、7分别为不同类别的物质。请完成下列问题:
(1)7代表的物质化学式为
。
(2)1和2发生的化学反应类型
(填“一定”或“不一定”)是置换反应。
(3)5和7发生反应的化学方程式可能为
(任写一个)。
三、实验探究题(第25题15分,第26题12分,共27分)
25.
小科和小敏利用下列装置进行O2、CO2的实验室制法和有关性质的研究。
(1)写出图中标记的仪器名称:①
;②
。
(2)小科要用过氧化氢溶液来制取并收集O2,应选用如图中的
装置(填字母编号)。
(3)小敏用
和大理石在B装置中反应,制CO2并检验CO2,能不能用火碱溶液代替图中的澄清石灰水来检验CO2?请说明理由。
。
26.
(衢州中考)某KCl固体样品中含有少量CaCl2杂质,实验室提纯氯化钾的流程如下。(氯化钾溶解度受温度影响较小)
(1)沉淀a是
。
(2)操作Ⅰ是
。
①冷却热饱和溶液
②蒸发结晶
(3)若KCl固体样品中还含有少量杂质K2SO4,语馨认为提纯该样品只要在上述方案基础上增加一步实验:在“加入过量K2CO3溶液”与“过滤”操作之间,加过量的硝酸钡溶液。小科认为这种方案不合理,会导致所得KCl固体中含有新的杂质,新杂质是
。
四、分析计算题(第27题12分,第28题15分,共27分)
27.
香椿被称为“树上蔬菜”,是香椿树的嫩芽,它不仅营养丰富,且具有极高的药用价值,如香椿中含有的皂甙具有抗菌、防癌的作用,皂甙的化学式为C27H42O3。请你计算:
(1)皂甙由
种元素组成,每个分子中有
个原子。
(2)皂甙中碳元素和氧元素的质量比为
。
(3)207g皂甙中有多少克碳元素?
28.
(温州中考)过氧化氢溶液保存时,因缓慢分解导致质量分数变小(化学方程式为2H2O2■2H2O+O2↑)。为探究酸碱性对过氧化氢分解快慢的影响,语馨利用图甲装置,每次实验往锥形瓶中加10g
30%过氧化氢溶液,再滴加调节剂,使其pH分别从3依次调至13,在60℃反应温度下进行实验,获得数据如图乙。
(1)氧气能用排水法收集,是因为
。
(2)根据本实验结果,对实验室常温保存过氧化氢溶液提出合理的建议:
。
(3)某次实验中,当10g溶质质量分数为30%的过氧化氢溶液分解产生0.32g氧气时,剩余过氧化氢溶液的溶质质量分数为多少?(滴加的试剂对溶液质量的影响忽略不计,计算结果精确到1%)
参考答案
期中测试
一、选择题
1—5.
CDBCC
6—10.
CBCCA
11—15.
DCABD
二、填空题
16.
(1)单质
(2)食醋
17.
(1)①③④
(2)1∶2∶1
(3)C∶H=12∶1
18.
(1)①
(2)有蓝色絮状沉淀产生
(3)CO2+2NaOHNa2CO3+H2O[或Na2CO3+Ca(OH)22NaOH+CaCO3↓(合理即可)]
19.
铜、铁
Zn(NO3)2
Zn+Cu(NO3)2Zn(NO3)2+Cu(或Zn+Fe(NO3)2Zn(NO3)2+Fe)
20.
(1)混合物
(2)A
21.
产生白色沉淀
Mg(NO3)2和MgSO4
22.
(1)①③或②⑥
(2)①、③
23.
(1)分解
(2)AE或AF
24.
(1)Na2CO3
(2)不一定
(3)Na2CO3+2HCl2NaCl+H2O+CO2↑(合理答案即可)
三、实验探究题
25.
(1)长颈漏斗
集气瓶
(2)C
(3)稀盐酸
不能,因为CO2与NaOH反应无明显现象
26.
(1)碳酸钙(CaCO3)
(2)②
(3)硝酸钾和硝酸钡
四、分析计算题
27.
(1)三
72
(2)27∶4
(3)162g
28.
(1)氧气不易溶于水
(2)在pH约为3~5的酸性条件下保存
(3)设当产生氧气0.32g时,消耗掉过氧化氢的质量为x。
2H2O22H2O+O2↑
68
32
x
0.32g
,x=0.68g,
剩余过氧化氢质量m=10g×30%-0.68g=2.32g,剩余过氧化氢溶液的溶质质量分数为×100%≈24%。
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
期中达标检测卷
一、选择题(每小题4分,共60分)
1.
如图是物质X溶于水中发生电离的微观示意图,其中能说明X是一种酸的是(
)
2.
下面是用8mL蒸馏水稀释浓硫酸的实验操作过程,其中错误的环节是(
)
3.
某偏远山村学校食堂的中餐食谱为:主食:米饭;配菜:炒土豆、咸萝卜、白菜汤。为强壮身体、均衡营养,在“心连心”活动中,最好送去的是(
)
A.
猪油和菜油
B.
鸡蛋和牛肉
C.
小白菜和大白菜
D.
白糖和红糖
4.
(杭州中考)在试管中放入一根镁条(已去除氧化膜),往其中加入硝酸银溶液至浸没镁条,观察到如下现象:①镁条表面迅速覆盖一层疏松的固体物质,经检验发现生成的固体物质中有单质银;②镁条表面有明显的气泡现象,经检验发现气泡中有氢气。对于上述实验现象的分析错误的是(
)
A.
镁能从硝酸银溶液中置换出银
B.
镁跟硝酸银溶液反应会生成氢气
C.
镁投入硝酸银溶液中只发生2AgNO3+MgMg(NO3)2+2Ag
D.
根据该实验可判断镁比银化学活动性强
5.
金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用A表示):12HF+3Na2CO3+2Al(OH)32A+3CO2+9H2O,则A的化学式为
…………………(
)
A.
NaAlF6
B.
Na2AlF6
C.
Na3AlF6
D.
Na3Al2F6
6.
现有硫酸钠、碳酸钠、硝酸银三种无色溶液,滴入一种试剂可产生三种不同的现象,这种试剂可以是(
)
A.
氯化钡溶液
B.
稀硝酸
C.
稀盐酸
D.
氢氧化钠溶液
7.
下列物质不属于有机高分子化合物的是(
)
A.
淀粉
B.
油脂
C.
棉花
D.
蛋白质
8.
在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表。则关于此反应的说法正确的是(
)
A.
Y一定是该反应的催化剂
B.
该反应的基本类型为分解反应
C.
参加反应的Z与W的质量比为4∶1
D.
反应后生成X的质量为12g
9.
如图表示化学反应中溶液的颜色变化。下列叙述错误的是
……(
)
A
若X是稀硫酸,a可能是紫色石蕊试液
B.
若X是稀硫酸,b可能是氧化物
C.
若X是稀盐酸,c不可能是单质
D.
若X是稀盐酸,d不可能是单质
10.
下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)(
)
11.
如图中两圆相交部分表示物质间反应的主要实验现象,下列说法中正确的是(
)
A.a处溶液呈蓝色
B.
b处反应后溶液的总质量增加
C.
c处产生白色沉淀
D.
d处银白色固体表面有红色固体析出
12.
甲、乙两工厂的生产污水中各含有下列五种离子中的三种(两厂含有一种相同的离子):H+、Cu2+、K+、NO-3、OH-。若两厂单独排放都会造成严重的污染。若将两厂的污水按一定比例混合,沉淀后污水会变成只含一种溶质的无色澄清溶液,此溶质可作化肥。下列关于污水的分析,正确的是(
)
A.
OH-和Cu2+来自同一工厂
B.
Cu2+和K+来自同一工厂
C.
K+和OH-来自同一工厂
D.
H+和K+来自同一工厂
13.
(宁波中考)下列实验中,根据有关现象得出结论,合理的是(
)
14.
(台州中考)语馨对Fe2O3做了如图探究活动,已知氯气在水溶液中能将Fe2+转变为Fe3+,且每一步都充分反应。下列分析正确的是
…………(
)
A.
无色气体可以使澄清石灰水变浑浊
B.
黑色粉末是Fe3O4
C.
①过程Fe2O3中的氧元素全部转入无色气体
D.
②过程有置换反应发生
15.
(绍兴中考)将质量均为10g的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,反应完成后,生成氢气的质量关系不可能的是(
)
二、填空题(每空3分,共66分)
16.
化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题:
(1)“沙里淘金”说明黄金在自然界中能够以
(填“单质”或“化合物”)形式存在。
(2)葡萄表皮上因喷洒“波尔多液”而呈现的蓝色斑点,可以用厨房调料
洗净。
17.
(湖州中考)有机物是自然界物质中的一个大家族。
(1)下列是生活中常见的物质:①尿素[CO(NH2)2];②纯碱(Na2CO3);③酒精(C2H5OH);④葡萄糖(C6H12O6),属于有机物的是
(填序号)。
(2)食醋是生活中常用的调味品,其主要成分是乙酸(CH3COOH),在乙酸分子中碳、氢、氧的原子个数比是
。
(3)一定质量的某有机化合物X与8克氧气恰好完全反应,生成8.8克二氧化碳和1.8克水。X中各元素的质量比为
。
18.
(丽水中考)“寓学于乐”是一种有效的学习方式,如图是“盖房子”的游戏示意图,其规则是根据“上下相邻两层的物质之间均可发生化学反应”来堆砌楼层。图中已放置好四种物质,还有二氧化碳、碳酸钠溶液、硫酸铜溶液三种物质待放置。请回答:
(1)二氧化碳应放在
处(填序号)。
(2)将氢氧化钠溶液滴到③中,产生的实验现象是
。
(3)第二层内的两物质间能相互转化,请写出其中的一个化学方程式:
。
19.
将一定质量的锌粒投入到含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液呈无色,则滤渣中一定含有
,滤液中一定含有的溶质是
,请任写出一个反应的化学方程式:
。
20.
乙醇汽油的使用,可以缓解石油危机。所谓乙醇汽油是在汽油中加入适量乙醇混合而成的一种燃料。
(1)乙醇汽油属于
(填“纯净物”或“混合物”)。
(2)从环境保护的角度看,下列燃料中最理想的是
(填字母编号)。
A.
氢气
B.
煤
C.
乙醇汽油
D.
煤气(主要含CO)
21.
(衢州中考)硫酸钡不容易被X射线透过,在医疗上可用作检查肠胃的内服剂,俗称“钡餐”。小柯将硫酸镁溶液滴入硝酸钡[Ba(NO3)2]溶液中得到硫酸钡,如图表示该实验过程中溶液总质量随加入硫酸镁溶液质量的变化情况。图线AB段对应的实验现象是
,C点处溶液中的溶质有
。
22.
(1)小明用滤纸折成一只纸蝴蝶,并在上面喷洒了试剂A,挂在铁架台上。另取一只盛有溶液B的烧杯,放在纸蝴蝶的下方,如图,过一会儿,纸蝴蝶的颜色变成红色。请从下面提供的试剂找出A、B可能的组合
(填序号)。
①石蕊试液
②酚酞试液
③浓盐酸
④浓硫酸
⑤氢氧化钠溶液
⑥浓氨水
(2)只用下列试剂中的一种进行实验,就能确定B的成分,则该试剂可能是
(填序号)。
①Na2CO3溶液
②BaCl2溶液
③铁钉
④NaCl溶液
23.
(绍兴中考)实验室制氧气的方法可以是:
方法一:2H2O22H2O+O2↑
方法二:2KMnO4K2MnO4+MnO2+O2↑
(1)这两种涉及到的化学反应基本类型都是
反应。
(2)用方法二制取一瓶氧气,可选择如图装置中的
(填字母)。
24.
小倩同学将妈妈的智能新手机屏幕解锁图形设置为如图所示,圆圈内每个数字分别代表初中化学常见的一种物质(“-”表示相连两种物质能发生化学反应,反应条件省略)。其中1为碳粉,7可用于工业上玻璃、造纸、洗涤剂的生产等,1、2、3、5、7分别为不同类别的物质。请完成下列问题:
(1)7代表的物质化学式为
。
(2)1和2发生的化学反应类型
(填“一定”或“不一定”)是置换反应。
(3)5和7发生反应的化学方程式可能为
(任写一个)。
三、实验探究题(第25题15分,第26题12分,共27分)
25.
小科和小敏利用下列装置进行O2、CO2的实验室制法和有关性质的研究。
(1)写出图中标记的仪器名称:①
;②
。
(2)小科要用过氧化氢溶液来制取并收集O2,应选用如图中的
装置(填字母编号)。
(3)小敏用
和大理石在B装置中反应,制CO2并检验CO2,能不能用火碱溶液代替图中的澄清石灰水来检验CO2?请说明理由。
。
26.
(衢州中考)某KCl固体样品中含有少量CaCl2杂质,实验室提纯氯化钾的流程如下。(氯化钾溶解度受温度影响较小)
(1)沉淀a是
。
(2)操作Ⅰ是
。
①冷却热饱和溶液
②蒸发结晶
(3)若KCl固体样品中还含有少量杂质K2SO4,语馨认为提纯该样品只要在上述方案基础上增加一步实验:在“加入过量K2CO3溶液”与“过滤”操作之间,加过量的硝酸钡溶液。小科认为这种方案不合理,会导致所得KCl固体中含有新的杂质,新杂质是
。
四、分析计算题(第27题12分,第28题15分,共27分)
27.
香椿被称为“树上蔬菜”,是香椿树的嫩芽,它不仅营养丰富,且具有极高的药用价值,如香椿中含有的皂甙具有抗菌、防癌的作用,皂甙的化学式为C27H42O3。请你计算:
(1)皂甙由
种元素组成,每个分子中有
个原子。
(2)皂甙中碳元素和氧元素的质量比为
。
(3)207g皂甙中有多少克碳元素?
28.
(温州中考)过氧化氢溶液保存时,因缓慢分解导致质量分数变小(化学方程式为2H2O2■2H2O+O2↑)。为探究酸碱性对过氧化氢分解快慢的影响,语馨利用图甲装置,每次实验往锥形瓶中加10g
30%过氧化氢溶液,再滴加调节剂,使其pH分别从3依次调至13,在60℃反应温度下进行实验,获得数据如图乙。
(1)氧气能用排水法收集,是因为
。
(2)根据本实验结果,对实验室常温保存过氧化氢溶液提出合理的建议:
。
(3)某次实验中,当10g溶质质量分数为30%的过氧化氢溶液分解产生0.32g氧气时,剩余过氧化氢溶液的溶质质量分数为多少?(滴加的试剂对溶液质量的影响忽略不计,计算结果精确到1%)
参考答案
期中测试
一、选择题
1—5.
CDBCC
6—10.
CBCCA
11—15.
DCABD
二、填空题
16.
(1)单质
(2)食醋
17.
(1)①③④
(2)1∶2∶1
(3)C∶H=12∶1
18.
(1)①
(2)有蓝色絮状沉淀产生
(3)CO2+2NaOHNa2CO3+H2O[或Na2CO3+Ca(OH)22NaOH+CaCO3↓(合理即可)]
19.
铜、铁
Zn(NO3)2
Zn+Cu(NO3)2Zn(NO3)2+Cu(或Zn+Fe(NO3)2Zn(NO3)2+Fe)
20.
(1)混合物
(2)A
21.
产生白色沉淀
Mg(NO3)2和MgSO4
22.
(1)①③或②⑥
(2)①、③
23.
(1)分解
(2)AE或AF
24.
(1)Na2CO3
(2)不一定
(3)Na2CO3+2HCl2NaCl+H2O+CO2↑(合理答案即可)
三、实验探究题
25.
(1)长颈漏斗
集气瓶
(2)C
(3)稀盐酸
不能,因为CO2与NaOH反应无明显现象
26.
(1)碳酸钙(CaCO3)
(2)②
(3)硝酸钾和硝酸钡
四、分析计算题
27.
(1)三
72
(2)27∶4
(3)162g
28.
(1)氧气不易溶于水
(2)在pH约为3~5的酸性条件下保存
(3)设当产生氧气0.32g时,消耗掉过氧化氢的质量为x。
2H2O22H2O+O2↑
68
32
x
0.32g
,x=0.68g,
剩余过氧化氢质量m=10g×30%-0.68g=2.32g,剩余过氧化氢溶液的溶质质量分数为×100%≈24%。
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
同课章节目录
