第二单元课题3 制取氧气课后培优—2021-2022学年九年级化学人教版上册(有答案)
文档属性
| 名称 | 第二单元课题3 制取氧气课后培优—2021-2022学年九年级化学人教版上册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 147.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-22 00:00:00 | ||
图片预览

文档简介
课题3
制取氧气
一、单选题
1.为了除去灯泡中可能混入的微量氧气,有些白炽灯在灯丝的支架上附着了少量的某种红色物质。该红色物质可能是
A.红色油漆
B.红磷
C.二氧化锰
D.高锰酸钾
2.实验室制取氧气时,必不可少的最简单的一组仪器是
A.试管、酒精灯、带导管的橡皮塞、集气瓶、铁架台
B.试管、酒精灯、水槽、集气瓶
C.集气瓶、铁架台、试管、带导管的橡皮塞
D.铁架台、烧瓶、集气瓶、玻璃片
3.小明为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据如下表:
实验1
实验2
MnO2的质量/克
0.5
0.5
5%的H2O2的体积/毫升
40
40
温度℃
20
80
实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,下列不属于偏大的原因是
A.锥形瓶内气体受热膨胀
B.收集到的氧气中混有空气
C.温度较高时水蒸发成水蒸气
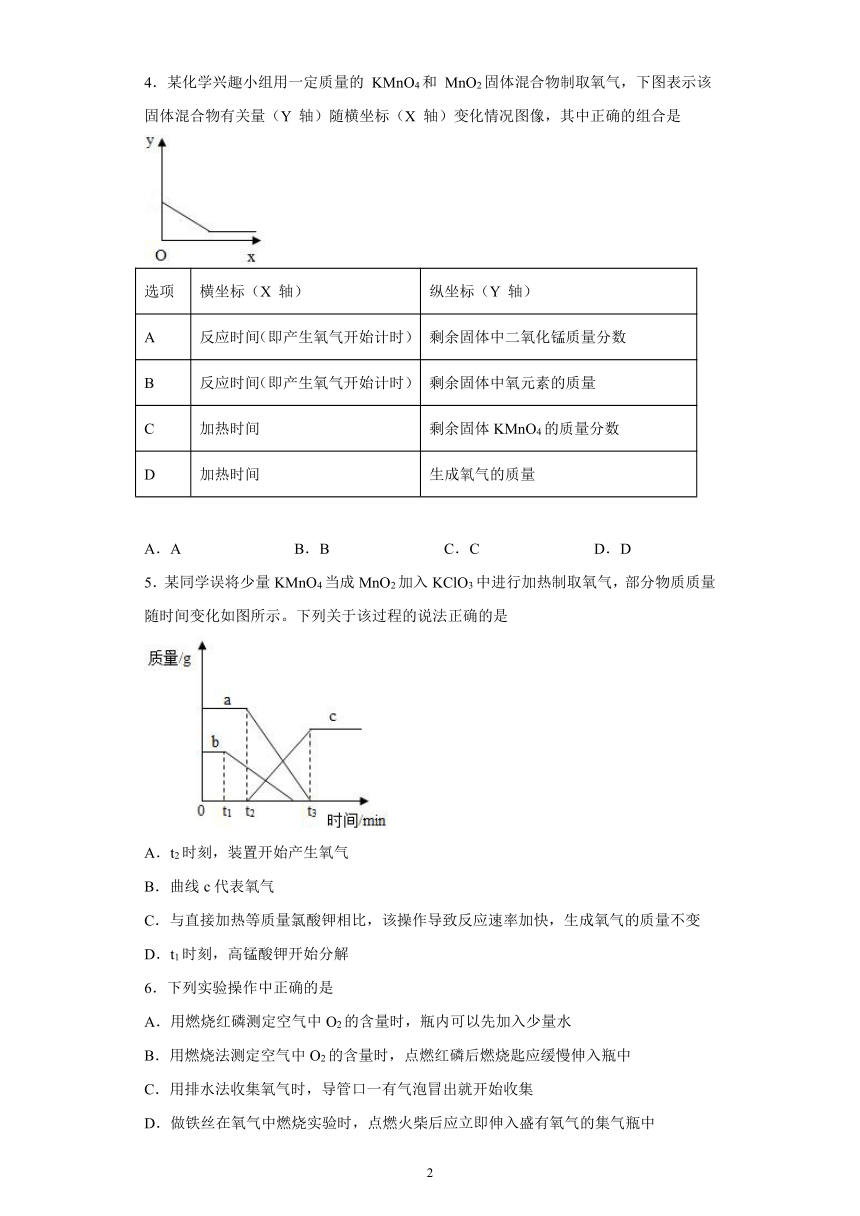
4.某化学兴趣小组用一定质量的
KMnO4和
MnO2固体混合物制取氧气,下图表示该固体混合物有关量(Y
轴)随横坐标(X
轴)变化情况图像,其中正确的组合是
选项
横坐标(X
轴)
纵坐标(Y
轴)
A
反应时间(即产生氧气开始计时)
剩余固体中二氧化锰质量分数
B
反应时间(即产生氧气开始计时)
剩余固体中氧元素的质量
C
加热时间
剩余固体KMnO4的质量分数
D
加热时间
生成氧气的质量
A.A
B.B
C.C
D.D
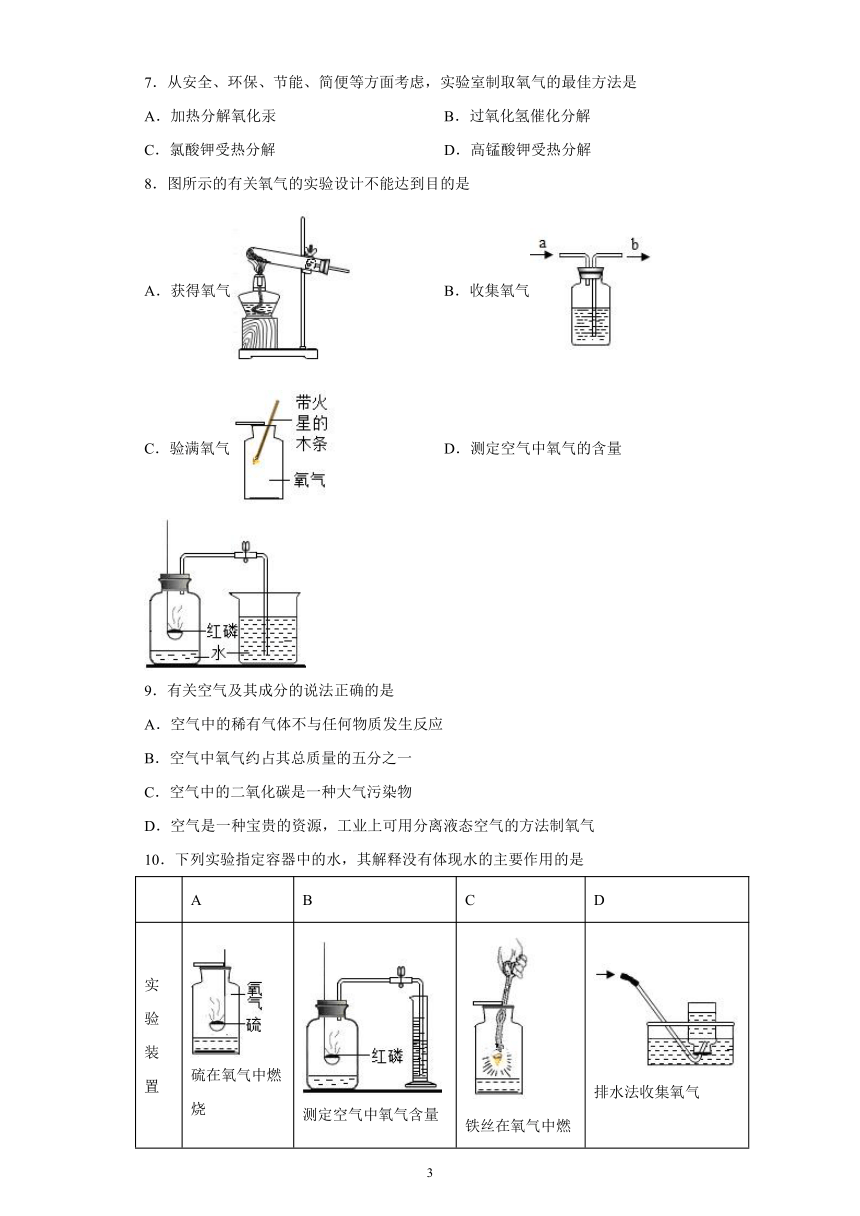
5.某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是
A.t2时刻,装置开始产生氧气
B.曲线c代表氧气
C.与直接加热等质量氯酸钾相比,该操作导致反应速率加快,生成氧气的质量不变
D.t1时刻,高锰酸钾开始分解
6.下列实验操作中正确的是
A.用燃烧红磷测定空气中O2的含量时,瓶内可以先加入少量水
B.用燃烧法测定空气中O2的含量时,点燃红磷后燃烧匙应缓慢伸入瓶中
C.用排水法收集氧气时,导管口一有气泡冒出就开始收集
D.做铁丝在氧气中燃烧实验时,点燃火柴后应立即伸入盛有氧气的集气瓶中
7.从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法是
A.加热分解氧化汞
B.过氧化氢催化分解
C.氯酸钾受热分解
D.高锰酸钾受热分解
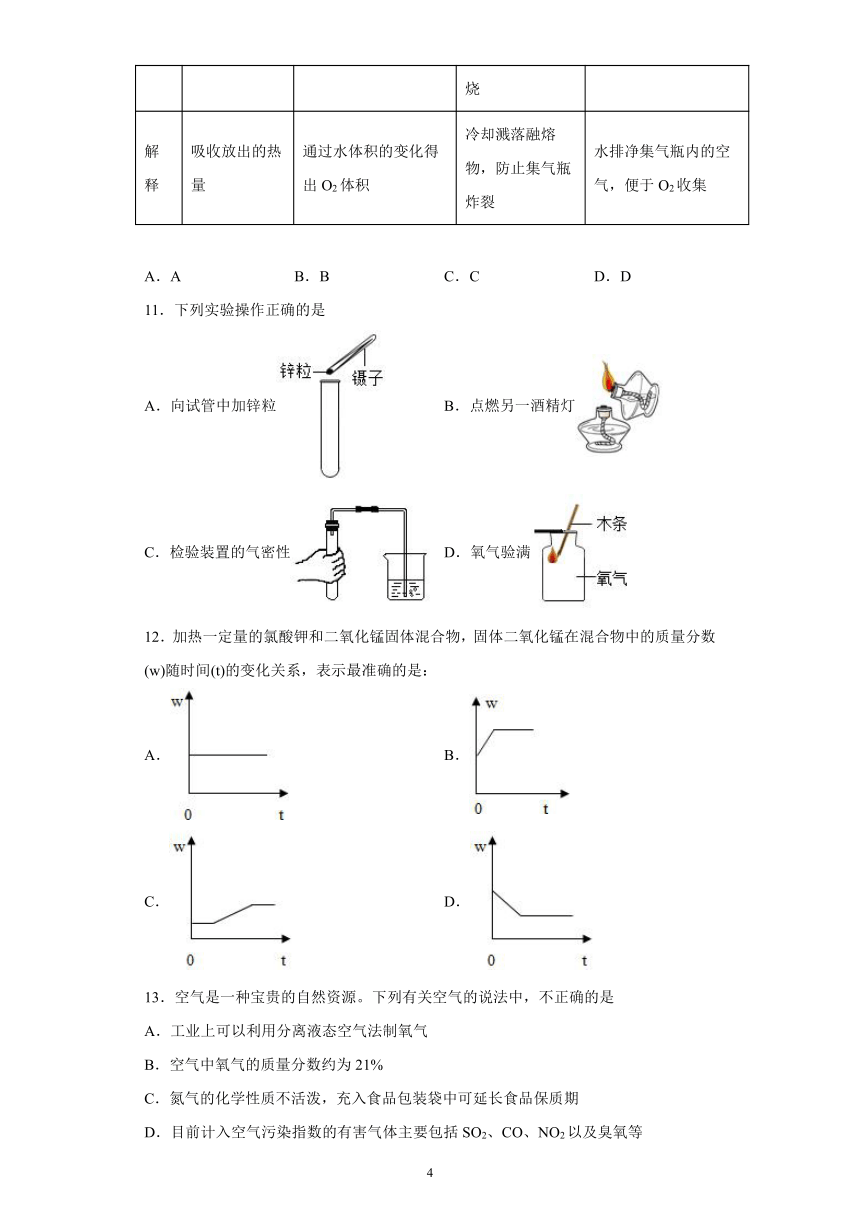
8.图所示的有关氧气的实验设计不能达到目的是
A.获得氧气
B.收集氧气
C.验满氧气
D.测定空气中氧气的含量
9.有关空气及其成分的说法正确的是
A.空气中的稀有气体不与任何物质发生反应
B.空气中氧气约占其总质量的五分之一
C.空气中的二氧化碳是一种大气污染物
D.空气是一种宝贵的资源,工业上可用分离液态空气的方法制氧气
10.下列实验指定容器中的水,其解释没有体现水的主要作用的是
A
B
C
D
实
验
装
置
硫在氧气中燃烧
测定空气中氧气含量
铁丝在氧气中燃烧
排水法收集氧气
解释
吸收放出的热量
通过水体积的变化得出O2体积
冷却溅落融熔物,防止集气瓶炸裂
水排净集气瓶内的空气,便于O2收集
A.A
B.B
C.C
D.D
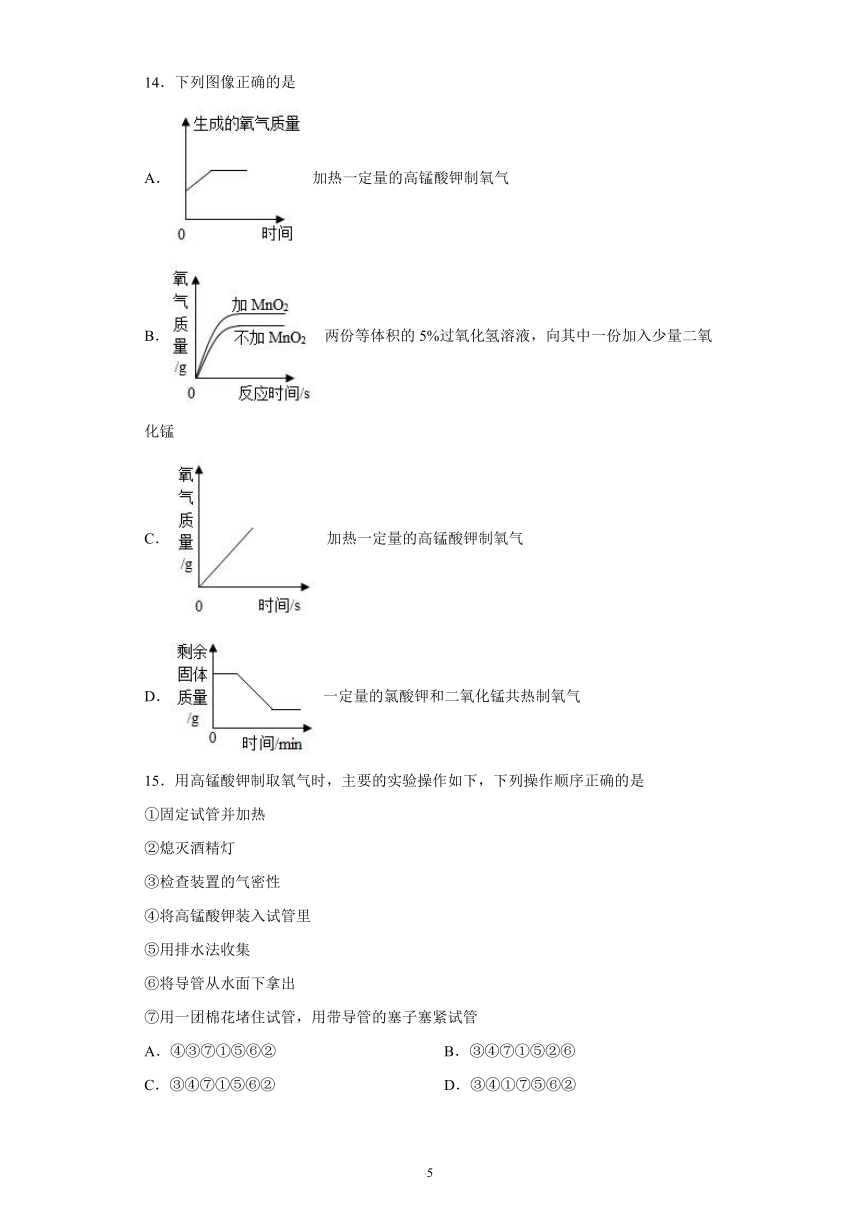
11.下列实验操作正确的是
A.向试管中加锌粒
B.点燃另一酒精灯
C.检验装置的气密性
D.氧气验满
12.加热一定量的氯酸钾和二氧化锰固体混合物,固体二氧化锰在混合物中的质量分数(w)随时间(t)的变化关系,表示最准确的是:
A.
B.
C.
D.
13.空气是一种宝贵的自然资源。下列有关空气的说法中,不正确的是
A.工业上可以利用分离液态空气法制氧气
B.空气中氧气的质量分数约为21%
C.氮气的化学性质不活泼,充入食品包装袋中可延长食品保质期
D.目前计入空气污染指数的有害气体主要包括SO2、CO、NO2以及臭氧等
14.下列图像正确的是
A.
加热一定量的高锰酸钾制氧气
B.
两份等体积的5%过氧化氢溶液,向其中一份加入少量二氧化锰
C.
加热一定量的高锰酸钾制氧气
D.
一定量的氯酸钾和二氧化锰共热制氧气
15.用高锰酸钾制取氧气时,主要的实验操作如下,下列操作顺序正确的是
①固定试管并加热
②熄灭酒精灯
③检查装置的气密性
④将高锰酸钾装入试管里
⑤用排水法收集
⑥将导管从水面下拿出
⑦用一团棉花堵住试管,用带导管的塞子塞紧试管
A.④③⑦①⑤⑥②
B.③④⑦①⑤②⑥
C.③④⑦①⑤⑥②
D.③④①⑦⑤⑥②
二、填空题
16.在①洁净的空气;②液态氧;③四氧化三铁;④高锰酸钾完全反应后剩余的固体;⑤二氧化碳;⑥稀有气体
(1)属混合物的是___________(填序号,下同);
(2)属于纯净物的是___________。
17.了解氧气的性质和用途;
(1)工业上用______的方法制氧气,这一变化属于______变化;而实验室通常可用氯酸钾在二氧化锰存在加热下制氧气,这种变化属于______变化。分解过氧化氢溶液制取氧气时,加入少量______(填物质名称),能加快氧气的生成速度。
(2)为纪念人类成功攀登珠穆朗玛峰50周年,中国登山协会业余登山队2003年5月21日再次登顶成功。登山队必备的物品之一是氧气瓶,此时氧气的作用是______。氧气与体内的葡萄糖发生反应,提供人体活动所需的能量,并生成二氧化碳和水,写出该反应的文字表达式______。燃料燃烧也需要氧气,这是利用了氧气的______性质。
18.化学是一门以实验为基础的科学。根据下图所示的装置,回答下列问题:
(1)图中标有序号①的仪器名称是_______。
(2)实验室用A装置制取氧气,发生反应的化学方程式是_______。
(3)用双氧水制取氧气并用于探究石蜡燃烧的产物,应选择装置B与_______、_______(填字母)组合。收集过程中,检验氧气已集满的方法是_______。
19.下列物质:①冰水混合物②液氮③氦气④氯酸钾⑤清新的空气⑥过氧化氢⑦硫粉⑧高锰酸钾⑨五氧化二磷⑩稀有气体。
请用序号回答:上述物质中为白色物质的是______;属于混合物的是______。
20.写出下列反应的文字表达式及基本反应类型
(1)铁在氧气中燃烧_______基本反应类型:_______
(2)过氧化氢溶液制氧气_______基本反应类型:_______
21.写出下列反应的文字表达式,并写出其反应的基本类型
(1)铁丝在氧气中燃烧:___________;___________
(2)加热高锰酸钾制取氧气:___________;___________
(3)硫在空气中燃烧:___________;___________
三、计算题
22.工业上用分离液态空气制取氧气,现用工业方法制取200L氧气。回答下列问题:
(1)至少要消耗空气多少L?
(2)制得的氧气质量为多少g?(氧气密度为1.429g?L﹣1)
23.现有一瓶过氧化氢溶液,取该溶液20g于锥形瓶内,再加入2g二氧化锰,立即塞紧橡皮塞。完全反应后,收集得到的氧气的体积为500mL。
(1)反应结束后,经过滤、洗涤、干燥后,所得固体质量为_____,在反应中,该固体所起的作用是_____。
(2)所得的氧气的质量是多少?(标准状况下,氧气密度约为1.4g/L)。
24.在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如图所示。请计算:
(1)完全反应时,生成氧气的质量为_____g。
(2)完全反应后,剩余的固体物质是_____。
(3)成年人每分钟大约需要吸入8L氧气,则成年人每分钟大致需要空气_____L;在标准状况下,8L氧气的质量是_____g,所需空气的质量为_____g。(O2的密度为1.429g/L,空气的密度为1.293g/L,精确到0.1)
25.小敏同学,想验证氧气的化学性质,她打算用加热高锰酸钾的方法来制取氧气,老师非常支持她,并且告知她加热高锰酸钾制取氧气,理论上生成氧气的质量约是高锰酸钾质量的。
(1)经老师允许她在实验室中称得11g高锰酸钾,大约能生成氧气的质量是多少?
(2)小敏打算将这些氧气装在容积为125mL的集气瓶中,请你计算一下大约需要几个集气瓶?(实验条件下,氧气密度为1.429g/L,写出详细的计算过程,最终结果保留整数)
参考答案
1.B
2.C
3.B
4.B
5.D
6.A
7.B
8.C
9.D
10.A
11.C
12.C
13.B
14.D
15.C
16.
(1)①④⑥
(2)②③⑤
17.
(1)
分离液态空气
物理
化学
二氧化锰
(2)
支持呼吸
氧气+葡萄糖二氧化碳+水
支持燃烧(助燃性)
18.
(1)集气瓶
(2)
(3)
F
E
将带火星的木条置于集气瓶口,若复燃则集满
19.④⑨
⑤⑩
20.
(1)
化合反应
(2)
分解反应
21.
(1)
化合反应
(2)
分解反应
(3)
化合反应
22.(1)氧气约占空气总体积的21%,至少要消耗空气的体积为200L÷21%≈952.4L。
(2)制得的氧气质量为m=ρV=1.429g?L﹣1×200L=285.8g。
答:(1)至少要消耗空气952.4L;
(2)制得的氧气质量为285.8g。
23.(1)2g;催化作用
(2)500mL=0.5L;所得的氧气的质量为
答:所得的氧气的质量为0.7g。
24.(1)9.6;
(2)氯化钾和二氧化锰;
(3)氧气约占空气体积分数的21%,故成年人每分钟大致需要空气8L÷21%≈38.1L;
在标准状况下,8L氧气的质量是:1.429g/L×8L≈11.4g;
所需空气的质量为1.293g/L×38.1L≈49.3g
25.(1)1.1g;
(2)解:生成氧气的体积为:≈0.77L=770mL
需要容积为125mL的集气瓶个数为:
答:需要容积为125mL的集气瓶个数为6个。
制取氧气
一、单选题
1.为了除去灯泡中可能混入的微量氧气,有些白炽灯在灯丝的支架上附着了少量的某种红色物质。该红色物质可能是
A.红色油漆
B.红磷
C.二氧化锰
D.高锰酸钾
2.实验室制取氧气时,必不可少的最简单的一组仪器是
A.试管、酒精灯、带导管的橡皮塞、集气瓶、铁架台
B.试管、酒精灯、水槽、集气瓶
C.集气瓶、铁架台、试管、带导管的橡皮塞
D.铁架台、烧瓶、集气瓶、玻璃片
3.小明为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据如下表:
实验1
实验2
MnO2的质量/克
0.5
0.5
5%的H2O2的体积/毫升
40
40
温度℃
20
80
实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,下列不属于偏大的原因是
A.锥形瓶内气体受热膨胀
B.收集到的氧气中混有空气
C.温度较高时水蒸发成水蒸气
4.某化学兴趣小组用一定质量的
KMnO4和
MnO2固体混合物制取氧气,下图表示该固体混合物有关量(Y
轴)随横坐标(X
轴)变化情况图像,其中正确的组合是
选项
横坐标(X
轴)
纵坐标(Y
轴)
A
反应时间(即产生氧气开始计时)
剩余固体中二氧化锰质量分数
B
反应时间(即产生氧气开始计时)
剩余固体中氧元素的质量
C
加热时间
剩余固体KMnO4的质量分数
D
加热时间
生成氧气的质量
A.A
B.B
C.C
D.D
5.某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是
A.t2时刻,装置开始产生氧气
B.曲线c代表氧气
C.与直接加热等质量氯酸钾相比,该操作导致反应速率加快,生成氧气的质量不变
D.t1时刻,高锰酸钾开始分解
6.下列实验操作中正确的是
A.用燃烧红磷测定空气中O2的含量时,瓶内可以先加入少量水
B.用燃烧法测定空气中O2的含量时,点燃红磷后燃烧匙应缓慢伸入瓶中
C.用排水法收集氧气时,导管口一有气泡冒出就开始收集
D.做铁丝在氧气中燃烧实验时,点燃火柴后应立即伸入盛有氧气的集气瓶中
7.从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法是
A.加热分解氧化汞
B.过氧化氢催化分解
C.氯酸钾受热分解
D.高锰酸钾受热分解
8.图所示的有关氧气的实验设计不能达到目的是
A.获得氧气
B.收集氧气
C.验满氧气
D.测定空气中氧气的含量
9.有关空气及其成分的说法正确的是
A.空气中的稀有气体不与任何物质发生反应
B.空气中氧气约占其总质量的五分之一
C.空气中的二氧化碳是一种大气污染物
D.空气是一种宝贵的资源,工业上可用分离液态空气的方法制氧气
10.下列实验指定容器中的水,其解释没有体现水的主要作用的是
A
B
C
D
实
验
装
置
硫在氧气中燃烧
测定空气中氧气含量
铁丝在氧气中燃烧
排水法收集氧气
解释
吸收放出的热量
通过水体积的变化得出O2体积
冷却溅落融熔物,防止集气瓶炸裂
水排净集气瓶内的空气,便于O2收集
A.A
B.B
C.C
D.D
11.下列实验操作正确的是
A.向试管中加锌粒
B.点燃另一酒精灯
C.检验装置的气密性
D.氧气验满
12.加热一定量的氯酸钾和二氧化锰固体混合物,固体二氧化锰在混合物中的质量分数(w)随时间(t)的变化关系,表示最准确的是:
A.
B.
C.
D.
13.空气是一种宝贵的自然资源。下列有关空气的说法中,不正确的是
A.工业上可以利用分离液态空气法制氧气
B.空气中氧气的质量分数约为21%
C.氮气的化学性质不活泼,充入食品包装袋中可延长食品保质期
D.目前计入空气污染指数的有害气体主要包括SO2、CO、NO2以及臭氧等
14.下列图像正确的是
A.
加热一定量的高锰酸钾制氧气
B.
两份等体积的5%过氧化氢溶液,向其中一份加入少量二氧化锰
C.
加热一定量的高锰酸钾制氧气
D.
一定量的氯酸钾和二氧化锰共热制氧气
15.用高锰酸钾制取氧气时,主要的实验操作如下,下列操作顺序正确的是
①固定试管并加热
②熄灭酒精灯
③检查装置的气密性
④将高锰酸钾装入试管里
⑤用排水法收集
⑥将导管从水面下拿出
⑦用一团棉花堵住试管,用带导管的塞子塞紧试管
A.④③⑦①⑤⑥②
B.③④⑦①⑤②⑥
C.③④⑦①⑤⑥②
D.③④①⑦⑤⑥②
二、填空题
16.在①洁净的空气;②液态氧;③四氧化三铁;④高锰酸钾完全反应后剩余的固体;⑤二氧化碳;⑥稀有气体
(1)属混合物的是___________(填序号,下同);
(2)属于纯净物的是___________。
17.了解氧气的性质和用途;
(1)工业上用______的方法制氧气,这一变化属于______变化;而实验室通常可用氯酸钾在二氧化锰存在加热下制氧气,这种变化属于______变化。分解过氧化氢溶液制取氧气时,加入少量______(填物质名称),能加快氧气的生成速度。
(2)为纪念人类成功攀登珠穆朗玛峰50周年,中国登山协会业余登山队2003年5月21日再次登顶成功。登山队必备的物品之一是氧气瓶,此时氧气的作用是______。氧气与体内的葡萄糖发生反应,提供人体活动所需的能量,并生成二氧化碳和水,写出该反应的文字表达式______。燃料燃烧也需要氧气,这是利用了氧气的______性质。
18.化学是一门以实验为基础的科学。根据下图所示的装置,回答下列问题:
(1)图中标有序号①的仪器名称是_______。
(2)实验室用A装置制取氧气,发生反应的化学方程式是_______。
(3)用双氧水制取氧气并用于探究石蜡燃烧的产物,应选择装置B与_______、_______(填字母)组合。收集过程中,检验氧气已集满的方法是_______。
19.下列物质:①冰水混合物②液氮③氦气④氯酸钾⑤清新的空气⑥过氧化氢⑦硫粉⑧高锰酸钾⑨五氧化二磷⑩稀有气体。
请用序号回答:上述物质中为白色物质的是______;属于混合物的是______。
20.写出下列反应的文字表达式及基本反应类型
(1)铁在氧气中燃烧_______基本反应类型:_______
(2)过氧化氢溶液制氧气_______基本反应类型:_______
21.写出下列反应的文字表达式,并写出其反应的基本类型
(1)铁丝在氧气中燃烧:___________;___________
(2)加热高锰酸钾制取氧气:___________;___________
(3)硫在空气中燃烧:___________;___________
三、计算题
22.工业上用分离液态空气制取氧气,现用工业方法制取200L氧气。回答下列问题:
(1)至少要消耗空气多少L?
(2)制得的氧气质量为多少g?(氧气密度为1.429g?L﹣1)
23.现有一瓶过氧化氢溶液,取该溶液20g于锥形瓶内,再加入2g二氧化锰,立即塞紧橡皮塞。完全反应后,收集得到的氧气的体积为500mL。
(1)反应结束后,经过滤、洗涤、干燥后,所得固体质量为_____,在反应中,该固体所起的作用是_____。
(2)所得的氧气的质量是多少?(标准状况下,氧气密度约为1.4g/L)。
24.在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如图所示。请计算:
(1)完全反应时,生成氧气的质量为_____g。
(2)完全反应后,剩余的固体物质是_____。
(3)成年人每分钟大约需要吸入8L氧气,则成年人每分钟大致需要空气_____L;在标准状况下,8L氧气的质量是_____g,所需空气的质量为_____g。(O2的密度为1.429g/L,空气的密度为1.293g/L,精确到0.1)
25.小敏同学,想验证氧气的化学性质,她打算用加热高锰酸钾的方法来制取氧气,老师非常支持她,并且告知她加热高锰酸钾制取氧气,理论上生成氧气的质量约是高锰酸钾质量的。
(1)经老师允许她在实验室中称得11g高锰酸钾,大约能生成氧气的质量是多少?
(2)小敏打算将这些氧气装在容积为125mL的集气瓶中,请你计算一下大约需要几个集气瓶?(实验条件下,氧气密度为1.429g/L,写出详细的计算过程,最终结果保留整数)
参考答案
1.B
2.C
3.B
4.B
5.D
6.A
7.B
8.C
9.D
10.A
11.C
12.C
13.B
14.D
15.C
16.
(1)①④⑥
(2)②③⑤
17.
(1)
分离液态空气
物理
化学
二氧化锰
(2)
支持呼吸
氧气+葡萄糖二氧化碳+水
支持燃烧(助燃性)
18.
(1)集气瓶
(2)
(3)
F
E
将带火星的木条置于集气瓶口,若复燃则集满
19.④⑨
⑤⑩
20.
(1)
化合反应
(2)
分解反应
21.
(1)
化合反应
(2)
分解反应
(3)
化合反应
22.(1)氧气约占空气总体积的21%,至少要消耗空气的体积为200L÷21%≈952.4L。
(2)制得的氧气质量为m=ρV=1.429g?L﹣1×200L=285.8g。
答:(1)至少要消耗空气952.4L;
(2)制得的氧气质量为285.8g。
23.(1)2g;催化作用
(2)500mL=0.5L;所得的氧气的质量为
答:所得的氧气的质量为0.7g。
24.(1)9.6;
(2)氯化钾和二氧化锰;
(3)氧气约占空气体积分数的21%,故成年人每分钟大致需要空气8L÷21%≈38.1L;
在标准状况下,8L氧气的质量是:1.429g/L×8L≈11.4g;
所需空气的质量为1.293g/L×38.1L≈49.3g
25.(1)1.1g;
(2)解:生成氧气的体积为:≈0.77L=770mL
需要容积为125mL的集气瓶个数为:
答:需要容积为125mL的集气瓶个数为6个。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
