第5节 物质的溶解 复习(溶质质量分数)(课件 28张PPT)
文档属性
| 名称 | 第5节 物质的溶解 复习(溶质质量分数)(课件 28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-09-23 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
溶质质量分数
课程内容
1.溶质质量分数概念及简单计算
2.溶液增浓及浓稀溶液混合计算
3.溶液稀释
溶质质量分数概念及简单计算
溶质质量分数——概念与表达式
10%葡萄糖注射液
0.9%氯化钠溶液
溶质质量分数——概念与表达式
概念
溶质质量与溶液质量之比
表达式
?
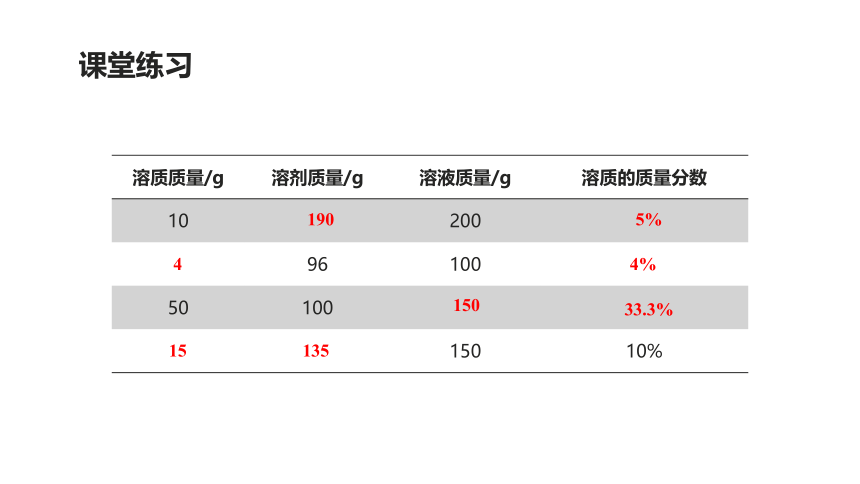
课堂练习
溶质质量/g
溶剂质量/g
溶液质量/g
溶质的质量分数
10
200
96
100
50
100
150
10%
190
5%
4
4%
150
33.3%
15
135
课堂练习
例5、向100g质量分数为20%的氯化钠溶液中加入3g氯化钠固体和12g水,使其完全溶解,所得溶液中氯化钠的质量分数是(
)
A.20%
B.22.5%
C.25%
D.30%
A
含义
判断:10%氯化钠溶液的含义
1)100g水中含有10g氯化钠
2)100g溶液中含有10g氯化钠
每100份质量的溶液中含有溶质的份数为多少
溶质质量分数——概念与表达式
课堂练习
例4、质量分数为25%的某溶液,其中溶质与溶液的质量比为(
)
1:4
B.
1:5
C.
4:1
D.
5:1
A
溶质质量分数——概念与表达式
?
溶质质量分数与溶解度
一定温度下,饱和溶液中的溶质的质量分数(P%)与溶解度(S)的关系
课堂练习
已知20℃时物质A的溶解度是60g,现将36g
A充分溶解在50g水中,所得到溶液中溶质的质量分数是多少?
饱和
?
课堂练习
例6、将100g质量分数为36%的饱和A溶液中,恒温蒸发掉50g水,则蒸发之后的溶液的溶质质量分数为(
)
18%
B.
20%
C.
36%
D.
72%
C
饱和:蒸发前后均为饱和溶液
恒温:溶解度不变
溶质质量分数不变
课堂练习
将一定质量的溶质质量分数为20.0%的某溶液,在一定温度下蒸发掉10.0克水时,有2.0克不含结晶水的的溶质晶体析出,此时溶液中溶质质量分数为24.0%。则该溶液在此温度下的溶解度是多少?
饱和
?
?
课堂练习
如图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是(
)
30℃时,氯化铵、硫酸钠的溶解度相同
氯化铵的溶解度随温度的升高而增大
将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出
将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变
C
溶质质量分数——增浓及浓稀混合计算
浓稀溶液混合
50克
30%硫酸溶液
50克
10%硫酸溶液
20%硫酸溶液
等质量混合:混合溶液的质量分数=(浓溶液质量分数+稀溶液质量分数)/2
课堂练习
例4、50g
10%的硫酸溶液与30g
20%的硫酸溶液混合后,溶液中溶质的质量分数为(
)
A.
30%
B.
15%
C.
20%
D.
13.75%
浓溶液质量=稀溶液质量:混合液质量分数=平均值
浓溶液质量>稀溶液质量:混合液质量分数>平均值
浓溶液质量<稀溶液质量:混合液质量分数<平均值
D
课堂练习
例5、用溶质质量分数60%的硫酸与10%的稀硫酸混合,配制质量分数为20%的硫酸溶液所需60%的硫酸与10%的稀硫酸的质量比为(
)
A.
1:6
B.
1:5
C.
1:4
D.
1:3
C
60%a+10%b=20%(a+b)
(60%-20%)a=(20%-10%)b
40%a=10%b
a:b=1:4
溶质质量分数——增浓及浓稀混合计算
100毫升
4%硫酸溶液
1.02g/mL
100毫升
16%硫酸溶液
1.11g/mL
10%硫酸溶液
等体积混合:混合溶液的质量分数≠平均值
若密度随质量分数增大而增大,则混合后质量分数>平均值
混合后质量分数10.3%
浓稀溶液混合
溶质质量分数——增浓及浓稀混合计算
100毫升
10%氨水
0.96g/mL
100毫升
20%氨水
0.92g/mL
15%氨水
若密度随质量分数增大而减小,则混合后质量分数<平均值
混合后质量分数14.9%
浓稀溶液混合
课堂练习
例6、溶液的配制是日常生活和化学实验中常见的操作。硫酸溶液和氨水密度与其溶质的质量分数对照表如下:(20℃)
1)20℃时,随着溶液中溶质的质量分数增大,氨水的密度逐渐_________。
2)取24%的氨水100g,加入100g水混匀后,所得溶液的质量分数为_______。
3)将100mL溶质的质量分数为16%的硫酸和100mL水混匀后,所得溶液的质量分数_______8%(填“>”“<”或“=”)
减小
12%
>
溶质质量分数——增浓及浓稀混合计算
溶液增浓
例1、20℃时,对100g
5%的食盐溶液做如下处理,求所得溶液溶质的质量分数(假设每次增加的溶质都完全溶解,列式计算,结果保留一位小数)
1)蒸发20g水后,溶质的质量分数为多少?
2)增加10g食盐后,溶质的质量分数为多少?
P%=溶质质量/溶液质量×100%
课堂练习
例2、电解水时,常在水中加入少量的稀硫酸以增强水的导电性。现用25克8%的硫酸进行电解水的实验,一段时间后,测得硫酸中溶质的质量分数为10%,则被电解的水的质量是多少?
电解前后溶质质量不变
电解水质量=电解前后溶液变化质量
课堂练习
例3、现有200克质量分数为10%的硝酸钠溶液,要使该溶液的溶质质量分数提高到15%,需要加入固体硝酸钠多少克?
(20g+X)/(200g+X)×100%=15%
X≈11.8g
课堂练习
在20℃时,有100克A物质的溶液,其溶质的质量分数为20%。加热蒸发掉20克溶剂后,恢复到20℃,析出3.2克A物质。则A物质在20℃时的溶解度是(
)
A.
28克
B.
25克
C.
20克
D.
16克
A
溶质质量分数——增浓及浓稀混合计算
溶液稀释
例1、把100mL溶质的质量分数为98%的浓硫酸稀释10倍,这时溶液所含溶质的质量是(
)
为原来的1/10
B.
增大10倍
C.
为原来的9/10
D.
不变
D
浓溶液加水稀释:溶质质量不变
溶质质量分数——增浓及浓稀混合计算
计算加水体积
①确定浓稀溶液质量;②计算加水质量;③换算加水体积
例2、二氧化氯消毒液是国际上公认的新一代强力、安全、高效的消毒剂,它能够迅速、彻底杀灭各种细菌和病毒。小亮发现超市一瓶二氧化氯消毒液(如图甲),他摘取了瓶上的部分标签信息如下表(如图乙)。现欲配制30千克质量分数为20%的二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液?加水多少升?
复习小结
谢谢!
溶质质量分数
课程内容
1.溶质质量分数概念及简单计算
2.溶液增浓及浓稀溶液混合计算
3.溶液稀释
溶质质量分数概念及简单计算
溶质质量分数——概念与表达式
10%葡萄糖注射液
0.9%氯化钠溶液
溶质质量分数——概念与表达式
概念
溶质质量与溶液质量之比
表达式
?
课堂练习
溶质质量/g
溶剂质量/g
溶液质量/g
溶质的质量分数
10
200
96
100
50
100
150
10%
190
5%
4
4%
150
33.3%
15
135
课堂练习
例5、向100g质量分数为20%的氯化钠溶液中加入3g氯化钠固体和12g水,使其完全溶解,所得溶液中氯化钠的质量分数是(
)
A.20%
B.22.5%
C.25%
D.30%
A
含义
判断:10%氯化钠溶液的含义
1)100g水中含有10g氯化钠
2)100g溶液中含有10g氯化钠
每100份质量的溶液中含有溶质的份数为多少
溶质质量分数——概念与表达式
课堂练习
例4、质量分数为25%的某溶液,其中溶质与溶液的质量比为(
)
1:4
B.
1:5
C.
4:1
D.
5:1
A
溶质质量分数——概念与表达式
?
溶质质量分数与溶解度
一定温度下,饱和溶液中的溶质的质量分数(P%)与溶解度(S)的关系
课堂练习
已知20℃时物质A的溶解度是60g,现将36g
A充分溶解在50g水中,所得到溶液中溶质的质量分数是多少?
饱和
?
课堂练习
例6、将100g质量分数为36%的饱和A溶液中,恒温蒸发掉50g水,则蒸发之后的溶液的溶质质量分数为(
)
18%
B.
20%
C.
36%
D.
72%
C
饱和:蒸发前后均为饱和溶液
恒温:溶解度不变
溶质质量分数不变
课堂练习
将一定质量的溶质质量分数为20.0%的某溶液,在一定温度下蒸发掉10.0克水时,有2.0克不含结晶水的的溶质晶体析出,此时溶液中溶质质量分数为24.0%。则该溶液在此温度下的溶解度是多少?
饱和
?
?
课堂练习
如图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是(
)
30℃时,氯化铵、硫酸钠的溶解度相同
氯化铵的溶解度随温度的升高而增大
将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出
将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变
C
溶质质量分数——增浓及浓稀混合计算
浓稀溶液混合
50克
30%硫酸溶液
50克
10%硫酸溶液
20%硫酸溶液
等质量混合:混合溶液的质量分数=(浓溶液质量分数+稀溶液质量分数)/2
课堂练习
例4、50g
10%的硫酸溶液与30g
20%的硫酸溶液混合后,溶液中溶质的质量分数为(
)
A.
30%
B.
15%
C.
20%
D.
13.75%
浓溶液质量=稀溶液质量:混合液质量分数=平均值
浓溶液质量>稀溶液质量:混合液质量分数>平均值
浓溶液质量<稀溶液质量:混合液质量分数<平均值
D
课堂练习
例5、用溶质质量分数60%的硫酸与10%的稀硫酸混合,配制质量分数为20%的硫酸溶液所需60%的硫酸与10%的稀硫酸的质量比为(
)
A.
1:6
B.
1:5
C.
1:4
D.
1:3
C
60%a+10%b=20%(a+b)
(60%-20%)a=(20%-10%)b
40%a=10%b
a:b=1:4
溶质质量分数——增浓及浓稀混合计算
100毫升
4%硫酸溶液
1.02g/mL
100毫升
16%硫酸溶液
1.11g/mL
10%硫酸溶液
等体积混合:混合溶液的质量分数≠平均值
若密度随质量分数增大而增大,则混合后质量分数>平均值
混合后质量分数10.3%
浓稀溶液混合
溶质质量分数——增浓及浓稀混合计算
100毫升
10%氨水
0.96g/mL
100毫升
20%氨水
0.92g/mL
15%氨水
若密度随质量分数增大而减小,则混合后质量分数<平均值
混合后质量分数14.9%
浓稀溶液混合
课堂练习
例6、溶液的配制是日常生活和化学实验中常见的操作。硫酸溶液和氨水密度与其溶质的质量分数对照表如下:(20℃)
1)20℃时,随着溶液中溶质的质量分数增大,氨水的密度逐渐_________。
2)取24%的氨水100g,加入100g水混匀后,所得溶液的质量分数为_______。
3)将100mL溶质的质量分数为16%的硫酸和100mL水混匀后,所得溶液的质量分数_______8%(填“>”“<”或“=”)
减小
12%
>
溶质质量分数——增浓及浓稀混合计算
溶液增浓
例1、20℃时,对100g
5%的食盐溶液做如下处理,求所得溶液溶质的质量分数(假设每次增加的溶质都完全溶解,列式计算,结果保留一位小数)
1)蒸发20g水后,溶质的质量分数为多少?
2)增加10g食盐后,溶质的质量分数为多少?
P%=溶质质量/溶液质量×100%
课堂练习
例2、电解水时,常在水中加入少量的稀硫酸以增强水的导电性。现用25克8%的硫酸进行电解水的实验,一段时间后,测得硫酸中溶质的质量分数为10%,则被电解的水的质量是多少?
电解前后溶质质量不变
电解水质量=电解前后溶液变化质量
课堂练习
例3、现有200克质量分数为10%的硝酸钠溶液,要使该溶液的溶质质量分数提高到15%,需要加入固体硝酸钠多少克?
(20g+X)/(200g+X)×100%=15%
X≈11.8g
课堂练习
在20℃时,有100克A物质的溶液,其溶质的质量分数为20%。加热蒸发掉20克溶剂后,恢复到20℃,析出3.2克A物质。则A物质在20℃时的溶解度是(
)
A.
28克
B.
25克
C.
20克
D.
16克
A
溶质质量分数——增浓及浓稀混合计算
溶液稀释
例1、把100mL溶质的质量分数为98%的浓硫酸稀释10倍,这时溶液所含溶质的质量是(
)
为原来的1/10
B.
增大10倍
C.
为原来的9/10
D.
不变
D
浓溶液加水稀释:溶质质量不变
溶质质量分数——增浓及浓稀混合计算
计算加水体积
①确定浓稀溶液质量;②计算加水质量;③换算加水体积
例2、二氧化氯消毒液是国际上公认的新一代强力、安全、高效的消毒剂,它能够迅速、彻底杀灭各种细菌和病毒。小亮发现超市一瓶二氧化氯消毒液(如图甲),他摘取了瓶上的部分标签信息如下表(如图乙)。现欲配制30千克质量分数为20%的二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液?加水多少升?
复习小结
谢谢!
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
