2021年高中化学新教材同步必修第一册 第1章 第一节 第1课时 物质的分类
文档属性
| 名称 | 2021年高中化学新教材同步必修第一册 第1章 第一节 第1课时 物质的分类 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-23 00:00:00 | ||
图片预览




文档简介
第一节 物质的分类及转化
第1课时 物质的分类
[核心素养发展目标] 1.能从元素组成(宏观)和构成微粒(微观)的角度分析认识物质,根据物质的组成和性质对物质进行分类,培养宏观辨识与微观探析的意识和能力。2.熟知溶液、浊液、胶体三种分散系的本质区别。认识胶体是一种常见的分散系。了解胶体的性质及其应用,会鉴别胶体和溶液。
一、根据物质的组成和性质分类
1.物质的元素组成
(1)物质都是由元素组成,单质都是由同一种元素组成,化合物是由不同种元素组成。
(2)金刚石、石墨和C60都是由碳元素组成的单质,它们的性质不同。
(3)同素异形体是由同一种元素形成的几种性质不同的单质。
(4)CO和CO2是由碳元素和氧元素以不同的方式组成的化合物,它们都属于非金属氧化物。
(1)只由一种元素组成的物质一定是纯净物吗?
提示 只由一种元素组成的物质不一定是纯净物,例如氧元素的同素异形体O2和O3形成的混合气体,只由氧元素组成,不是纯净物。
(2)从宏观上看物质由元素组成,从微观上看构成物质的微粒有哪些?
提示 构成物质的微粒有原子、分子或离子。如金刚石由原子构成,CO、CO2、H2、H2O等均由分子构成,NaCl、CaCO3等均由离子构成。
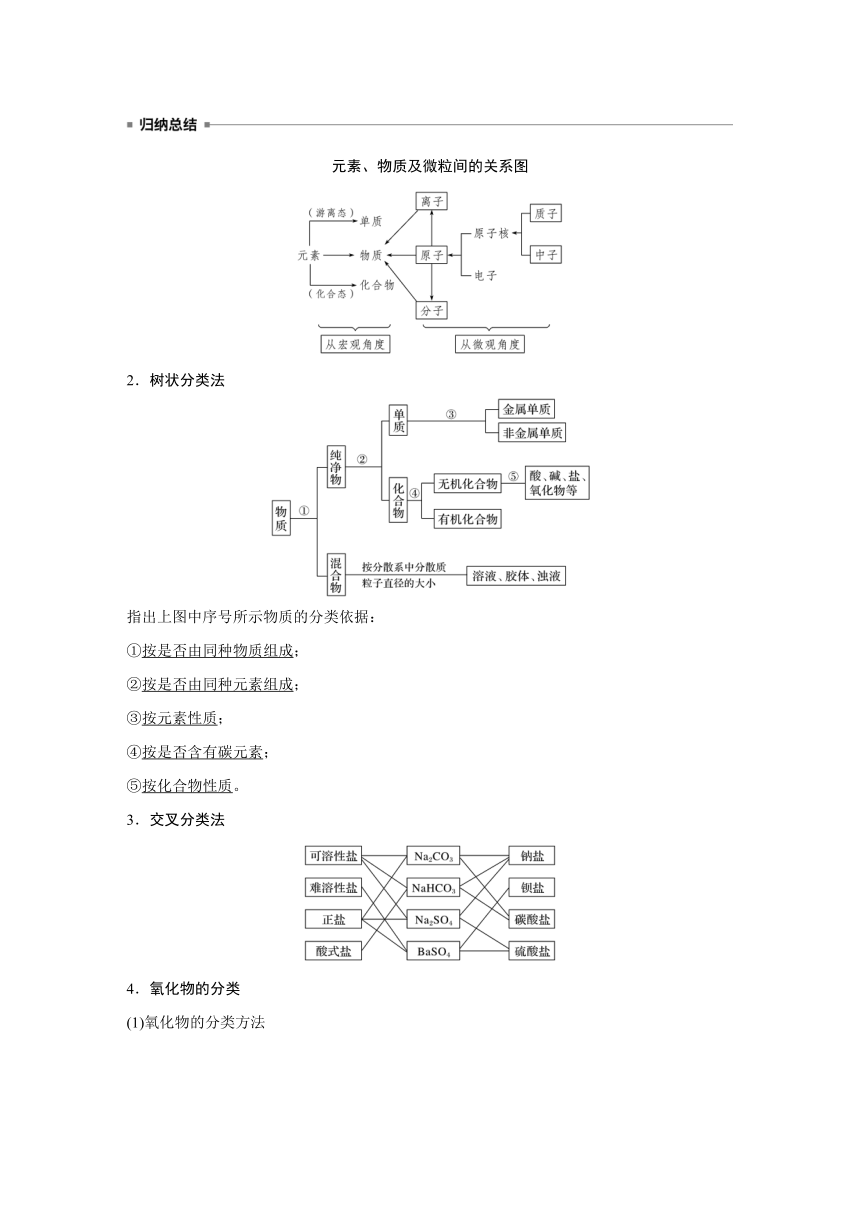
元素、物质及微粒间的关系图
2.树状分类法
指出上图中序号所示物质的分类依据:
①按是否由同种物质组成;
②按是否由同种元素组成;
③按元素性质;
④按是否含有碳元素;
⑤按化合物性质。
3.交叉分类法
4.氧化物的分类
(1)氧化物的分类方法
(2)各类氧化物之间的关系
(1)①酸、②碱、③盐、④氧化物四类物质的组成一定含有氧元素的是②④( )
(2)纯碱是碱( )
(3)CuSO4·5H2O属于混合物( )
(4)H2SO4既属于含氧酸又属于二元酸,这种分类方法是树状分类法( )
答案 (1)√ (2)× (3)× (4)×
(1)非金属氧化物一定是酸性氧化物吗?酸性氧化物一定是非金属氧化物吗?
提示 非金属氧化物不一定是酸性氧化物,如CO、NO。酸性氧化物不一定是非金属氧化物,如Mn2O7。
(2)金属氧化物一定是碱性氧化物吗?碱性氧化物一定是金属氧化物吗?
提示 金属氧化物不一定是碱性氧化物,如Mn2O7。碱性氧化物一定是金属氧化物。
(3)碳元素的物质家族如下表所示,请指出各物质的常见类别及碳元素的化合价:
碳元素化合价
+4
—
—
CO2
H2CO3
Na2CO3
NaHCO3
+2
—
—
CO
—
—
—
0
—
C60
—
—
—
—
-4
CH4
—
—
—
—
—
物质类别
氢化物
单质
氧化物
酸
碳酸盐
碳酸盐
(1)分类是根据研究对象的共同点和差异点,将它们区分为不同种类和层次的科学方法。
(2)物质的分类标准不同,其分类方式不同。对物质及其变化既可以从物质的组成和性质等宏观的角度进行分类,也可从物质的构成和参加化学反应的粒子等微观的角度分类。
相关链接
(1)根据物质的组成和性质对物质进行分类
(2)分类的标准不同,同一物质可以属于不同的类别:如NaHSO4可以属于纯净物、钠盐、硫酸氢盐、酸式盐、含氧酸盐、水溶性盐等。
二、分散系及其分类
1.分散系的概念与组成
(1)概念:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
(2)组成:分散系中被分散成粒子的物质叫做分散质,另一种物质叫做分散剂。
(3)常见分散系及其组成
分散系
分散质
分散剂
烟
微小尘埃(固)
空气(气)
雾
微小水滴(液)
空气(气)
碘酒
碘(固)
酒精(液)
食盐水
食盐(固)
水(液)
有色玻璃
金属氧化物(固)
玻璃(固)
2.分散系的分类及其依据
(1)按分散质和分散剂的状态不同,共有9种分散系。
(2)当分散剂是水或者其他液体时,根据分散质粒子直径的大小,分散系可分为三类:
①分散质粒子直径小于1
nm的分散系是溶液;
②分散质粒子直径大于100
nm的分散系是浊液;
③分散质粒子直径在1~100
nm之间的分散系是胶体。
3.胶体的制备和性质
(1)氢氧化铁胶体的制备
①制备实验:
在小烧杯中加入40
mL
蒸馏水,加热至沸腾,向沸水中慢慢滴入5~6滴氯化铁饱和溶液,继续煮沸至溶液呈红褐色,停止加热。即可得到氢氧化铁胶体。
②反应的化学方程式为
FeCl3+3H2OFe(OH)3(胶体)+3HCl。
(2)胶体的性质
①丁达尔效应
②聚沉
③电泳
(1)根据丁达尔效应将分散系分为溶液、浊液和胶体( )
(2)直径介于1~100
nm之间的粒子称为胶体( )
(3)Fe(OH)3胶体聚沉生成沉淀,发生了化学变化( )
答案 (1)× (2)× (3)×
(1)溶液、浊液、胶体三种分散系的本质区别是什么?
提示 溶液、浊液、胶体三种分散系本质的区别是分散质粒子的大小不同。
(2)可用过滤的方法除去氢氧化铁胶体中的泥沙吗?
提示 可以,胶体中的分散质粒子能透过滤纸孔隙,而泥沙不能透过,故可以用过滤的方法除去氢氧化铁胶体中的泥沙。
(3)下列事实与胶体性质有关的是________(填序号)。
①水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
②一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路
③往Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀生成,而后沉淀溶解
④医院里用血液透析的方法治疗肾功能衰竭等疾病引起的血液中毒
⑤FeCl3溶液和烧碱溶液混合会产生红褐色沉淀
提示 ①②③④
溶液、胶体、浊液三类分散系的比较
分散系
溶液
胶体
浊液
分散质粒子种类
分子、离子
较多分子集合体或大分子
大量分子集合体(固体小颗粒或小液滴)
分散质粒子直径
d<1
nm
1
nmnm
d>100
nm
外部特征
均一、透明、稳定
均一、透明、较稳定
不均一、不透明、不稳定
分散质能否透过滤纸
能
能
不能
鉴别方法
无丁达尔效应
有丁达尔效应
静置分层
实例
碘酒、蔗糖溶液、盐酸、酒精溶液
豆浆、云、雾、烟、淀粉溶液、蛋白质溶液
泥浆、油水混合物、氢氧化铁的悬浊液
相关链接
(1)分散系的组合方式及其实例
(2)胶体的分类
胶体
(3)图解胶体的制备与性质
1.(2018·吉林高一检测)某气体经过检验只含有一种元素,则该气体是( )
A.一种单质
B.一种化合物
C.单质与化合物的混合物
D.可能是一种单质,也可能是几种单质的混合物
答案 D
解析 只含有一种元素的物质可能是纯净物单质(如O2),也可能是混合物(如O2和O3的混合气体)。
2.在“加碘食盐”“含氟牙膏”“补钙保健品”“缺铁性贫血”中,“碘、氟、钙、铁”是指( )
A.单质
B.元素
C.化合物
D.物质
答案 B
解析 这些元素均以化合态形式存在,化合物不只是由一种元素组成。
3.国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种( )
A.氧化物
B.盐
C.碱
D.酸
答案 B
解析 胆矾、绿矾(FeSO4·7H2O)等结晶水合物都属于盐、纯净物。
4.根据某种共性,可将CO2、SO2归为一类氧化物,下列物质中与它们属于同一类的是( )
A.CaCO3
B.P2O5
C.CuO
D.KMnO4
答案 B
解析 CO2、SO2属于酸性氧化物,CaCO3、KMnO4属于盐,CuO属于碱性氧化物。
5.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A.分散质粒子直径在1~100
nm之间
B.都是混合物
C.都是无色、透明的溶液
D.都呈红褐色
答案 B
解析 氯化铁溶液与氢氧化铁胶体两种分散系,都属于混合物;氯化铁溶液为棕黄色,其分散质粒子直径小于1
nm;氢氧化铁胶体为红褐色,其分散质粒子直径在1~100
nm之间。
6.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9
m)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是( )
A.其分子直径比氯离子小
B.在水中形成的分散系属于悬浊液
C.在水中形成的分散系具有丁达尔效应
D.“钴酞菁”分子不能透过滤纸
答案 C
解析 分散质“钴酞菁”分子的直径(1.3×10-9
m)介于1~100
nm之间(大于氯离子的直径),为胶体粒子,其分散系为胶体,能透过滤纸,具有丁达尔效应。
7.回答下列问题:
(1)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是________(填字母)。
A.能全部透过滤纸
B.具有丁达尔效应
C.所得液体呈胶状
D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别淀粉溶液和淀粉胶体可以利用的方法是________________________________________________________________________。
答案 (1)AB
(2)用一束可见光分别照射两种无色液体,从侧面可以看到有一条光亮通路的为淀粉胶体
8.下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。
配料表
精制海盐、碘酸钾(KIO3)
含碘量
20~40
mg·kg-1
储藏方法
密封、避光、防潮
食用方法
烹调时待食品熟后加入碘盐
请根据此表,结合中学学过的化学知识,回答下列问题:
(1)据物质分类中的树状分类法的有关知识,在①HIO3、②NaIO3、③KOH、④I2O5、⑤NaCl五种__________(填“混合物”“化合物”“盐”或“氧化物”)中,与碘酸钾(KIO3)属于同类物质的是________(填序号)。
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾________(填“能”或“不能”)溶于水,化学性质:碘酸钾在受热时________。
答案 (1)化合物 ②⑤ (2)能 易分解
解析 (1)五种物质均属于化合物。碘酸钾属于盐,其中属于盐的有②和⑤。
(2)碘酸钾属于钾盐,能溶于水,根据“加碘盐”的食用方法“待食品熟后加入碘盐”可知碘酸钾受热易分解。
题组一 物质与组成元素
1.(2018·陕西高一检测)下列说法正确的是( )
A.含有氧元素的化合物一定是氧化物
B.纯净物一定由同种分子构成
C.只含一种元素的物质一定是单质
D.由同种分子构成的物质一定是纯净物
答案 D
解析 含有氧元素的化合物(如硫酸)不一定是氧化物;纯净物可由原子构成(如金刚石);只含一种元素的物质(如O2和O3的混合气体)不一定是单质。
2.经测定,一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是( )
A.一种化合物
B.一种单质和一种化合物的混合物
C.两种化合物
D.两种单质
答案 D
解析 由题意知,瓶中气体中含C、O两元素,在通常情况下,含C元素的单质为固体,故不能形成两种单质。
题组二 物质的分类
3.物质的分类如下图所示:
由图判断下列说法中不正确的是( )
A.甲图所示的分类方法属于树状分类法
B.乙图所示的分类方法属于交叉分类法
C.碱性氧化物一定是金属氧化物
D.非金属氧化物一定是酸性氧化物
答案 D
解析 非金属氧化物不一定是酸性氧化物,如CO、NO等。
4.(2019·河南龙泉中学月考)下列物质是生活中经常用到的物质,其中属于纯净物的是( )
A.煤
B.生铁
C.蒸馏水
D.矿泉水
答案 C
解析 煤是由含有碳、硫等多种物质构成的混合物;生铁是由铁和碳组成的混合物;矿泉水中除含有水外,还有其他多种矿物质,是混合物。
5.下列物质既属于纯净物又属于化合物的是( )
A.石墨
B.干冰
C.盐酸
D.食盐水
答案 B
解析 石墨属于单质;盐酸和食盐水属于混合物;干冰是固体二氧化碳,属于纯净物、化合物。
6.胃药“达喜”中含有碳酸镁(MgCO3),碳酸镁属于( )
A.酸
B.碱
C.盐
D.氧化物
答案 C
解析 碳酸镁是由镁离子和碳酸根离子组成的化合物,属于盐。
7.(2019·晋江市季延中学测试)下列物质的分类正确的是( )
碱
酸
盐
碱性氧化物
酸性氧化物
A
KOH
HNO3
CaCO3
CaO
SO2
B
NaOH
HCl
NaHSO4
Na2O
CO
C
Cu2(OH)2CO3
CH3COOH
CaF2
CO
SO2
D
Na2CO3
H2SO4
NaOH
SO2
CO2
答案 A
解析 一氧化碳不是酸性氧化物,也不是碱性氧化物;二氧化硫是酸性氧化物。
8.将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
答案 C
解析 选项A中的食盐为混合物;选项B中的碘酒为混合物,硫酸氢钠属于盐而不属于酸;选项D中的石灰水为混合物。
题组三 分散系及胶体
9.“云蒸霞蔚”出自《世说新语·寓言》,表示霞光透过云层的绚丽灿烂。“云”从化学角度分析属于下列分散系中的( )
A.溶液
B.悬浊液
C.乳浊液
D.胶体
答案 D
解析 “云”是小液滴分散在空气中形成的气溶胶。
10.溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否是大量分子或离子的集合体
B.分散质微粒直径的大小
C.能否透过滤纸或半透膜
D.是否均一、稳定、透明或是否具有丁达尔效应
答案 B
解析 分散系按照分散质微粒直径的大小来分类。
11.(2019·上饶市“山江湖”协作体月考)下列叙述中正确的是( )
A.FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔效应
B.根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
C.将几滴汽油加入装有10
mL水的试管中,用力振荡形成胶体
D.胶体、分散系、混合物概念间的从属关系可用下图表示
答案 D
解析 胶体区别于其他分散系的本质特征是分散质粒子直径的大小不同,A错误;根据分散质粒子直径大小来分类,B错误;将几滴汽油加入装有10
mL水的试管中,用力振荡形成浊液,C错误。
12.(2019·扬州中学月考)某同学在实验室进行了如图所示的实验,下列说法中错误的是( )
A.X、Z烧杯中分散质相同
B.利用过滤的方法,可将Z中固体与液体分离
C.Y中产生的气体为CO2
D.Z中分散系能产生丁达尔效应
答案 A
解析 X是氯化铁溶液,分散质是氯离子和三价铁离子,Z是氢氧化铁胶体,分散质是氢氧化铁胶粒,故A错误。
13.近年来,人类生产、生活所产生的污染,如机动车、燃煤、工业等排放的尾气,使灰霾天气逐渐增多。灰霾粒子比较小,平均直径大约在1
000~2
000
nm左右。下列有关说法正确的是( )
A.灰霾是一种分散系
B.灰霾能发生丁达尔效应
C.灰霾形成的是非常稳定的体系
D.戴口罩不能阻止吸入灰霾粒子
答案 A
解析 灰霾粒子分散在空气中形成分散系,其粒子直径远大于胶体粒子的直径,不能发生丁达尔效应;该分散系不稳定,灰霾粒子不能透过纱布。
14.(2018·金华高一检测)用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。其操作步骤如下:
①取20%白磷的乙醚溶液0.5
mL,加蒸馏水60
mL。
②先滴加1%氯化金水溶液0.75
mL,再滴加0.1
mol·L-1的碳酸钾0.6
mL,振荡变成棕红色。
③加热煮沸至溶液变成透明红色。
④分离提纯,除去无机溶质。
所得分散系中,金颗粒直径为5~12
nm。
请回答下列问题:
(1)该分散系属于________,其分散质是________。
(2)用一束强光照射该分散系,从侧面可看到_____________________________________。
(3)所得红色溶液________(填“能”或“不能”)继续加热。
答案 (1)胶体 金颗粒 (2)分散系中形成一条明亮的“通路” (3)不能
15.某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。
(1)将饱和氯化铁溶液分别滴入沸腾的下列物质中,能形成胶体的是________(填字母)。
A.自来水
B.蒸馏水
C.氢氧化钠溶液
D.氯化钠溶液
(2)现有甲、乙、丙三名同学进行氢氧化铁胶体的制备,其中正确的是________(填序号)。
①甲同学的操作:取一小烧杯,加入25
mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2
mL
氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热
②乙直接加热饱和氯化铁溶液
③丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟
(3)制备氢氧化铁胶体的化学方程式是_______________________________________________
_______________________________________________________________________________。
证明有氢氧化铁胶体生成的实验操作是______________________________________________
_______________________________________________________________________________。
(4)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是__________________________,
这种现象称为胶体的_____________________________________________________________。
答案 (1)B (2)① (3)FeCl3+3H2OFe(OH)3(胶体)+3HCl 让一束可见光通过制得的分散系,从侧面观察到一条光亮的“通路”,说明制得的是胶体 (4)产生红褐色沉淀 聚沉
16.纯净物根据其组成和性质可进行如下分类。
(1)如图所示的分类方法属于________(填字母)。
A.交叉分类法
B.树状分类法
(2)用H、O、S、N、K、Ca六种元素中任意两种或三种元素组成合适的常见物质,分别将其中一种常见物质的化学式填在下表相应类别中:
物质类别
酸
碱
盐
氧化物
化学式
(3)从上表中选出一种酸和一种氧化物,写出其反应的化学方程式:_______________________
_______________________________________________________________________________。
答案 (1)B (2)H2SO4 KOH KNO3 K2O(答案合理即可)
(3)K2O+H2SO4===K2SO4+H2O(答案合理即可)
解析 (1)题图中是对同类事物按照某种属性进行再分类的分类法,属于树状分类法。
(2)题干中的六种元素可以形成H2SO4、HNO3、H2S等酸;可以形成KOH、Ca(OH)2、NH3·H2O等碱;可以形成Ca(NO3)2、KNO3、K2SO4、CaSO4、NH4NO3等盐;可以形成的氧化物有H2O、SO2、NO、NO2、K2O、CaO等。
(3)能够与酸反应的氧化物一般为金属氧化物,如CaO+2HNO3===Ca(NO3)2+H2O、K2O+H2SO4===K2SO4+H2O。
第1课时 物质的分类
[核心素养发展目标] 1.能从元素组成(宏观)和构成微粒(微观)的角度分析认识物质,根据物质的组成和性质对物质进行分类,培养宏观辨识与微观探析的意识和能力。2.熟知溶液、浊液、胶体三种分散系的本质区别。认识胶体是一种常见的分散系。了解胶体的性质及其应用,会鉴别胶体和溶液。
一、根据物质的组成和性质分类
1.物质的元素组成
(1)物质都是由元素组成,单质都是由同一种元素组成,化合物是由不同种元素组成。
(2)金刚石、石墨和C60都是由碳元素组成的单质,它们的性质不同。
(3)同素异形体是由同一种元素形成的几种性质不同的单质。
(4)CO和CO2是由碳元素和氧元素以不同的方式组成的化合物,它们都属于非金属氧化物。
(1)只由一种元素组成的物质一定是纯净物吗?
提示 只由一种元素组成的物质不一定是纯净物,例如氧元素的同素异形体O2和O3形成的混合气体,只由氧元素组成,不是纯净物。
(2)从宏观上看物质由元素组成,从微观上看构成物质的微粒有哪些?
提示 构成物质的微粒有原子、分子或离子。如金刚石由原子构成,CO、CO2、H2、H2O等均由分子构成,NaCl、CaCO3等均由离子构成。
元素、物质及微粒间的关系图
2.树状分类法
指出上图中序号所示物质的分类依据:
①按是否由同种物质组成;
②按是否由同种元素组成;
③按元素性质;
④按是否含有碳元素;
⑤按化合物性质。
3.交叉分类法
4.氧化物的分类
(1)氧化物的分类方法
(2)各类氧化物之间的关系
(1)①酸、②碱、③盐、④氧化物四类物质的组成一定含有氧元素的是②④( )
(2)纯碱是碱( )
(3)CuSO4·5H2O属于混合物( )
(4)H2SO4既属于含氧酸又属于二元酸,这种分类方法是树状分类法( )
答案 (1)√ (2)× (3)× (4)×
(1)非金属氧化物一定是酸性氧化物吗?酸性氧化物一定是非金属氧化物吗?
提示 非金属氧化物不一定是酸性氧化物,如CO、NO。酸性氧化物不一定是非金属氧化物,如Mn2O7。
(2)金属氧化物一定是碱性氧化物吗?碱性氧化物一定是金属氧化物吗?
提示 金属氧化物不一定是碱性氧化物,如Mn2O7。碱性氧化物一定是金属氧化物。
(3)碳元素的物质家族如下表所示,请指出各物质的常见类别及碳元素的化合价:
碳元素化合价
+4
—
—
CO2
H2CO3
Na2CO3
NaHCO3
+2
—
—
CO
—
—
—
0
—
C60
—
—
—
—
-4
CH4
—
—
—
—
—
物质类别
氢化物
单质
氧化物
酸
碳酸盐
碳酸盐
(1)分类是根据研究对象的共同点和差异点,将它们区分为不同种类和层次的科学方法。
(2)物质的分类标准不同,其分类方式不同。对物质及其变化既可以从物质的组成和性质等宏观的角度进行分类,也可从物质的构成和参加化学反应的粒子等微观的角度分类。
相关链接
(1)根据物质的组成和性质对物质进行分类
(2)分类的标准不同,同一物质可以属于不同的类别:如NaHSO4可以属于纯净物、钠盐、硫酸氢盐、酸式盐、含氧酸盐、水溶性盐等。
二、分散系及其分类
1.分散系的概念与组成
(1)概念:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
(2)组成:分散系中被分散成粒子的物质叫做分散质,另一种物质叫做分散剂。
(3)常见分散系及其组成
分散系
分散质
分散剂
烟
微小尘埃(固)
空气(气)
雾
微小水滴(液)
空气(气)
碘酒
碘(固)
酒精(液)
食盐水
食盐(固)
水(液)
有色玻璃
金属氧化物(固)
玻璃(固)
2.分散系的分类及其依据
(1)按分散质和分散剂的状态不同,共有9种分散系。
(2)当分散剂是水或者其他液体时,根据分散质粒子直径的大小,分散系可分为三类:
①分散质粒子直径小于1
nm的分散系是溶液;
②分散质粒子直径大于100
nm的分散系是浊液;
③分散质粒子直径在1~100
nm之间的分散系是胶体。
3.胶体的制备和性质
(1)氢氧化铁胶体的制备
①制备实验:
在小烧杯中加入40
mL
蒸馏水,加热至沸腾,向沸水中慢慢滴入5~6滴氯化铁饱和溶液,继续煮沸至溶液呈红褐色,停止加热。即可得到氢氧化铁胶体。
②反应的化学方程式为
FeCl3+3H2OFe(OH)3(胶体)+3HCl。
(2)胶体的性质
①丁达尔效应
②聚沉
③电泳
(1)根据丁达尔效应将分散系分为溶液、浊液和胶体( )
(2)直径介于1~100
nm之间的粒子称为胶体( )
(3)Fe(OH)3胶体聚沉生成沉淀,发生了化学变化( )
答案 (1)× (2)× (3)×
(1)溶液、浊液、胶体三种分散系的本质区别是什么?
提示 溶液、浊液、胶体三种分散系本质的区别是分散质粒子的大小不同。
(2)可用过滤的方法除去氢氧化铁胶体中的泥沙吗?
提示 可以,胶体中的分散质粒子能透过滤纸孔隙,而泥沙不能透过,故可以用过滤的方法除去氢氧化铁胶体中的泥沙。
(3)下列事实与胶体性质有关的是________(填序号)。
①水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
②一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路
③往Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀生成,而后沉淀溶解
④医院里用血液透析的方法治疗肾功能衰竭等疾病引起的血液中毒
⑤FeCl3溶液和烧碱溶液混合会产生红褐色沉淀
提示 ①②③④
溶液、胶体、浊液三类分散系的比较
分散系
溶液
胶体
浊液
分散质粒子种类
分子、离子
较多分子集合体或大分子
大量分子集合体(固体小颗粒或小液滴)
分散质粒子直径
d<1
nm
1
nm
d>100
nm
外部特征
均一、透明、稳定
均一、透明、较稳定
不均一、不透明、不稳定
分散质能否透过滤纸
能
能
不能
鉴别方法
无丁达尔效应
有丁达尔效应
静置分层
实例
碘酒、蔗糖溶液、盐酸、酒精溶液
豆浆、云、雾、烟、淀粉溶液、蛋白质溶液
泥浆、油水混合物、氢氧化铁的悬浊液
相关链接
(1)分散系的组合方式及其实例
(2)胶体的分类
胶体
(3)图解胶体的制备与性质
1.(2018·吉林高一检测)某气体经过检验只含有一种元素,则该气体是( )
A.一种单质
B.一种化合物
C.单质与化合物的混合物
D.可能是一种单质,也可能是几种单质的混合物
答案 D
解析 只含有一种元素的物质可能是纯净物单质(如O2),也可能是混合物(如O2和O3的混合气体)。
2.在“加碘食盐”“含氟牙膏”“补钙保健品”“缺铁性贫血”中,“碘、氟、钙、铁”是指( )
A.单质
B.元素
C.化合物
D.物质
答案 B
解析 这些元素均以化合态形式存在,化合物不只是由一种元素组成。
3.国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种( )
A.氧化物
B.盐
C.碱
D.酸
答案 B
解析 胆矾、绿矾(FeSO4·7H2O)等结晶水合物都属于盐、纯净物。
4.根据某种共性,可将CO2、SO2归为一类氧化物,下列物质中与它们属于同一类的是( )
A.CaCO3
B.P2O5
C.CuO
D.KMnO4
答案 B
解析 CO2、SO2属于酸性氧化物,CaCO3、KMnO4属于盐,CuO属于碱性氧化物。
5.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A.分散质粒子直径在1~100
nm之间
B.都是混合物
C.都是无色、透明的溶液
D.都呈红褐色
答案 B
解析 氯化铁溶液与氢氧化铁胶体两种分散系,都属于混合物;氯化铁溶液为棕黄色,其分散质粒子直径小于1
nm;氢氧化铁胶体为红褐色,其分散质粒子直径在1~100
nm之间。
6.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9
m)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是( )
A.其分子直径比氯离子小
B.在水中形成的分散系属于悬浊液
C.在水中形成的分散系具有丁达尔效应
D.“钴酞菁”分子不能透过滤纸
答案 C
解析 分散质“钴酞菁”分子的直径(1.3×10-9
m)介于1~100
nm之间(大于氯离子的直径),为胶体粒子,其分散系为胶体,能透过滤纸,具有丁达尔效应。
7.回答下列问题:
(1)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是________(填字母)。
A.能全部透过滤纸
B.具有丁达尔效应
C.所得液体呈胶状
D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别淀粉溶液和淀粉胶体可以利用的方法是________________________________________________________________________。
答案 (1)AB
(2)用一束可见光分别照射两种无色液体,从侧面可以看到有一条光亮通路的为淀粉胶体
8.下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。
配料表
精制海盐、碘酸钾(KIO3)
含碘量
20~40
mg·kg-1
储藏方法
密封、避光、防潮
食用方法
烹调时待食品熟后加入碘盐
请根据此表,结合中学学过的化学知识,回答下列问题:
(1)据物质分类中的树状分类法的有关知识,在①HIO3、②NaIO3、③KOH、④I2O5、⑤NaCl五种__________(填“混合物”“化合物”“盐”或“氧化物”)中,与碘酸钾(KIO3)属于同类物质的是________(填序号)。
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾________(填“能”或“不能”)溶于水,化学性质:碘酸钾在受热时________。
答案 (1)化合物 ②⑤ (2)能 易分解
解析 (1)五种物质均属于化合物。碘酸钾属于盐,其中属于盐的有②和⑤。
(2)碘酸钾属于钾盐,能溶于水,根据“加碘盐”的食用方法“待食品熟后加入碘盐”可知碘酸钾受热易分解。
题组一 物质与组成元素
1.(2018·陕西高一检测)下列说法正确的是( )
A.含有氧元素的化合物一定是氧化物
B.纯净物一定由同种分子构成
C.只含一种元素的物质一定是单质
D.由同种分子构成的物质一定是纯净物
答案 D
解析 含有氧元素的化合物(如硫酸)不一定是氧化物;纯净物可由原子构成(如金刚石);只含一种元素的物质(如O2和O3的混合气体)不一定是单质。
2.经测定,一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是( )
A.一种化合物
B.一种单质和一种化合物的混合物
C.两种化合物
D.两种单质
答案 D
解析 由题意知,瓶中气体中含C、O两元素,在通常情况下,含C元素的单质为固体,故不能形成两种单质。
题组二 物质的分类
3.物质的分类如下图所示:
由图判断下列说法中不正确的是( )
A.甲图所示的分类方法属于树状分类法
B.乙图所示的分类方法属于交叉分类法
C.碱性氧化物一定是金属氧化物
D.非金属氧化物一定是酸性氧化物
答案 D
解析 非金属氧化物不一定是酸性氧化物,如CO、NO等。
4.(2019·河南龙泉中学月考)下列物质是生活中经常用到的物质,其中属于纯净物的是( )
A.煤
B.生铁
C.蒸馏水
D.矿泉水
答案 C
解析 煤是由含有碳、硫等多种物质构成的混合物;生铁是由铁和碳组成的混合物;矿泉水中除含有水外,还有其他多种矿物质,是混合物。
5.下列物质既属于纯净物又属于化合物的是( )
A.石墨
B.干冰
C.盐酸
D.食盐水
答案 B
解析 石墨属于单质;盐酸和食盐水属于混合物;干冰是固体二氧化碳,属于纯净物、化合物。
6.胃药“达喜”中含有碳酸镁(MgCO3),碳酸镁属于( )
A.酸
B.碱
C.盐
D.氧化物
答案 C
解析 碳酸镁是由镁离子和碳酸根离子组成的化合物,属于盐。
7.(2019·晋江市季延中学测试)下列物质的分类正确的是( )
碱
酸
盐
碱性氧化物
酸性氧化物
A
KOH
HNO3
CaCO3
CaO
SO2
B
NaOH
HCl
NaHSO4
Na2O
CO
C
Cu2(OH)2CO3
CH3COOH
CaF2
CO
SO2
D
Na2CO3
H2SO4
NaOH
SO2
CO2
答案 A
解析 一氧化碳不是酸性氧化物,也不是碱性氧化物;二氧化硫是酸性氧化物。
8.将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
答案 C
解析 选项A中的食盐为混合物;选项B中的碘酒为混合物,硫酸氢钠属于盐而不属于酸;选项D中的石灰水为混合物。
题组三 分散系及胶体
9.“云蒸霞蔚”出自《世说新语·寓言》,表示霞光透过云层的绚丽灿烂。“云”从化学角度分析属于下列分散系中的( )
A.溶液
B.悬浊液
C.乳浊液
D.胶体
答案 D
解析 “云”是小液滴分散在空气中形成的气溶胶。
10.溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否是大量分子或离子的集合体
B.分散质微粒直径的大小
C.能否透过滤纸或半透膜
D.是否均一、稳定、透明或是否具有丁达尔效应
答案 B
解析 分散系按照分散质微粒直径的大小来分类。
11.(2019·上饶市“山江湖”协作体月考)下列叙述中正确的是( )
A.FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔效应
B.根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
C.将几滴汽油加入装有10
mL水的试管中,用力振荡形成胶体
D.胶体、分散系、混合物概念间的从属关系可用下图表示
答案 D
解析 胶体区别于其他分散系的本质特征是分散质粒子直径的大小不同,A错误;根据分散质粒子直径大小来分类,B错误;将几滴汽油加入装有10
mL水的试管中,用力振荡形成浊液,C错误。
12.(2019·扬州中学月考)某同学在实验室进行了如图所示的实验,下列说法中错误的是( )
A.X、Z烧杯中分散质相同
B.利用过滤的方法,可将Z中固体与液体分离
C.Y中产生的气体为CO2
D.Z中分散系能产生丁达尔效应
答案 A
解析 X是氯化铁溶液,分散质是氯离子和三价铁离子,Z是氢氧化铁胶体,分散质是氢氧化铁胶粒,故A错误。
13.近年来,人类生产、生活所产生的污染,如机动车、燃煤、工业等排放的尾气,使灰霾天气逐渐增多。灰霾粒子比较小,平均直径大约在1
000~2
000
nm左右。下列有关说法正确的是( )
A.灰霾是一种分散系
B.灰霾能发生丁达尔效应
C.灰霾形成的是非常稳定的体系
D.戴口罩不能阻止吸入灰霾粒子
答案 A
解析 灰霾粒子分散在空气中形成分散系,其粒子直径远大于胶体粒子的直径,不能发生丁达尔效应;该分散系不稳定,灰霾粒子不能透过纱布。
14.(2018·金华高一检测)用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。其操作步骤如下:
①取20%白磷的乙醚溶液0.5
mL,加蒸馏水60
mL。
②先滴加1%氯化金水溶液0.75
mL,再滴加0.1
mol·L-1的碳酸钾0.6
mL,振荡变成棕红色。
③加热煮沸至溶液变成透明红色。
④分离提纯,除去无机溶质。
所得分散系中,金颗粒直径为5~12
nm。
请回答下列问题:
(1)该分散系属于________,其分散质是________。
(2)用一束强光照射该分散系,从侧面可看到_____________________________________。
(3)所得红色溶液________(填“能”或“不能”)继续加热。
答案 (1)胶体 金颗粒 (2)分散系中形成一条明亮的“通路” (3)不能
15.某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。
(1)将饱和氯化铁溶液分别滴入沸腾的下列物质中,能形成胶体的是________(填字母)。
A.自来水
B.蒸馏水
C.氢氧化钠溶液
D.氯化钠溶液
(2)现有甲、乙、丙三名同学进行氢氧化铁胶体的制备,其中正确的是________(填序号)。
①甲同学的操作:取一小烧杯,加入25
mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2
mL
氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热
②乙直接加热饱和氯化铁溶液
③丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟
(3)制备氢氧化铁胶体的化学方程式是_______________________________________________
_______________________________________________________________________________。
证明有氢氧化铁胶体生成的实验操作是______________________________________________
_______________________________________________________________________________。
(4)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是__________________________,
这种现象称为胶体的_____________________________________________________________。
答案 (1)B (2)① (3)FeCl3+3H2OFe(OH)3(胶体)+3HCl 让一束可见光通过制得的分散系,从侧面观察到一条光亮的“通路”,说明制得的是胶体 (4)产生红褐色沉淀 聚沉
16.纯净物根据其组成和性质可进行如下分类。
(1)如图所示的分类方法属于________(填字母)。
A.交叉分类法
B.树状分类法
(2)用H、O、S、N、K、Ca六种元素中任意两种或三种元素组成合适的常见物质,分别将其中一种常见物质的化学式填在下表相应类别中:
物质类别
酸
碱
盐
氧化物
化学式
(3)从上表中选出一种酸和一种氧化物,写出其反应的化学方程式:_______________________
_______________________________________________________________________________。
答案 (1)B (2)H2SO4 KOH KNO3 K2O(答案合理即可)
(3)K2O+H2SO4===K2SO4+H2O(答案合理即可)
解析 (1)题图中是对同类事物按照某种属性进行再分类的分类法,属于树状分类法。
(2)题干中的六种元素可以形成H2SO4、HNO3、H2S等酸;可以形成KOH、Ca(OH)2、NH3·H2O等碱;可以形成Ca(NO3)2、KNO3、K2SO4、CaSO4、NH4NO3等盐;可以形成的氧化物有H2O、SO2、NO、NO2、K2O、CaO等。
(3)能够与酸反应的氧化物一般为金属氧化物,如CaO+2HNO3===Ca(NO3)2+H2O、K2O+H2SO4===K2SO4+H2O。
