湖北省沙市高级中学校2021-2022学年高一上学期9月月考化学试题(Word版含答案)
文档属性
| 名称 | 湖北省沙市高级中学校2021-2022学年高一上学期9月月考化学试题(Word版含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 110.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-24 22:20:10 | ||
图片预览


文档简介
沙市高级中学校2021-2022学年高一上学期9月月考
化学试卷
时间:75分钟
满分:100分
考试时间:2021年9月23日
第Ⅰ卷(选择题
共48分)
一、选择题(本题包括16个小题,每小3分,共48分,每小题只有1个选项符合题意)
1.化学与生活、社会发展息息相关,下列说法不正确的是(
)
A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B.“千淘万漉虽辛苦,吹尽狂沙始到金”体现了运用化学方法的淘金方式
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.“春蚕到死丝方尽,蜡炬成灰泪始干”诗句中涉及氧化还原反应
2.下列物质组,按强电解质、弱电解质、非电解质的顺序排列的是(
)
A.烧碱、纯碱、苛性钾
B.硫酸氢钠、NH3、乙醇
C.氯酸钾、醋酸、铜
D.硫酸铵、碳酸、SO2
3.下列不是Fe(OH)3胶体和MgCl2溶液共同具备的性质是(
)
A.都比较稳定,密封放置不产生沉淀
B.都有丁达尔效应
C.加入NaOH溶液都可产生沉淀
D.分散质微粒均可透过滤纸
4.下列各组中的离子,能在无色透明的溶液中大量共存的是(
)
A.Mg2+、H+、Cl–、OH–
B.Na+、Ba2+、CO32–、NO3–
C.Na+、H+、Cu2+、SO42–
D.K+、Zn2+、NO3–、SO42–
5.纳米材料是指粒子直径为1~100
nm的材料,纳米碳就是其中的一种。下列有关纳米碳的说
法正确的是(
)
A.纳米碳是一种新的化合物
B.纳米碳属于胶体,能产生丁达尔效应
C.纳米碳极易燃烧,产物能使澄清石灰水变浑浊
D.纳米碳与金刚石是碳元素的同素异形体,性质相同
6.下列反应既属于离子反应又属于氧化还原反应的是(
)
A.NaCl溶液与AgNO3溶液反应
B.Fe在O2中燃烧
C.CO与Fe2O3在高温下反应
D.Zn与稀硫酸反应
7.下列关于氧化还原反应的说法中错误的是(
)
A.氧化还原反应的实质是电子的转移
B.氧化还原反应中一定存在元素化合价的变化
C.氧化还原反应一定有氧元素参加
D.发生氧化反应的物质也可能同时发生还原反应
8.下列变化过程中,需要加入氧化剂才能实现的是(
)
A.H2O2O2
B.SO3H2SO4
C.CuCu(NO3)2
D.MnO2Mn2+
9.下列叙述正确的是(
)
A.氨水能导电,所以氨水是电解质
B.既有单质参加又有单质生成的反应一定是氧化还原反应
C.溶于水后能电离出H?+的化合物都是酸
D.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
10.下列反应的离子方程式书写正确的是(
)
A.金属镁与稀盐酸反应:Mg+2H++2Cl-===MgCl2+H2↑
B.氯化钡溶液与稀硫酸反应:Ba2++SO===BaSO4↓
C.碳酸钠溶液与稀盐酸反应:Na2CO3+2H+===2Na++H2O+CO2↑
D.氢氧化镁与稀硫酸反应:OH-+H+===H2O
11.下列反应能用H++OH–=H2O表示的是(
)
A.稀盐酸和大理石反应
B.H2SO4溶液和NaOH溶液反应
C.醋酸溶液和NaOH溶液反应
D.稀硫酸和Ba(OH)2溶液反应
12.离子方程式BaCO3+2H+=CO2↑+H2O+Ba2+中的H+不能代表的物质是(
)
①HCl ②H2SO4 ③HNO3 ④NaHSO4
⑤CH3COOH
A.②④⑤
B.①④⑤
C.①③
D.①⑤
13.高锰酸钾在医药上用作防腐剂、消毒剂、除臭剂及解毒剂;在水质净化及废水处理中,作
水处理剂。高锰酸钾受热分解可以制得氧气,反应为2KMnO4△K2MnO4+MnO2+O2↑,有关该反应,下列说法错误的是(
)
A.氧化剂和还原剂都是KMnO4
B.该反应的还原产物只有MnO2
C.该反应的氧化产物是O2
D.KMnO4中Mn元素被还原,O元素被氧化
14.某溶液中含有较大量的Cl–、、OH–三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中,正确的是(
)
①滴加Mg(NO3)2溶液
②过滤
③滴加AgNO3溶液
④滴加Ba(NO3)2溶液
A.④②①②③
B.④②③②①
C.①②③②④
D.①②④②③
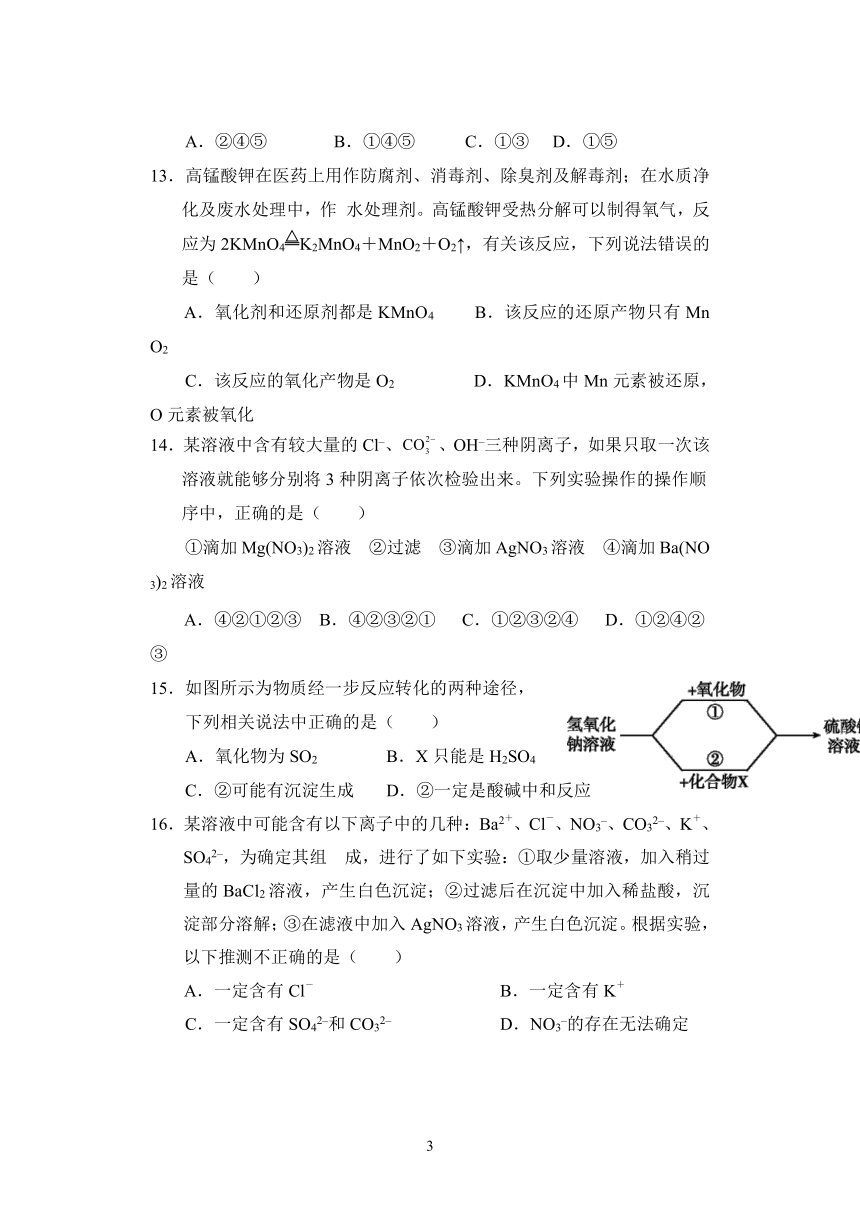
15.如图所示为物质经一步反应转化的两种途径,
下列相关说法中正确的是(
)
A.氧化物为SO2
B.X只能是H2SO4
C.②可能有沉淀生成
D.②一定是酸碱中和反应
16.某溶液中可能含有以下离子中的几种:Ba2+、Cl-、NO3–、CO32–、K+、SO42–,为确定其组
成,进行了如下实验:①取少量溶液,加入稍过量的BaCl2溶液,产生白色沉淀;②过滤后在沉淀中加入稀盐酸,沉淀部分溶解;③在滤液中加入AgNO3溶液,产生白色沉淀。根据实验,以下推测不正确的是(
)
A.一定含有Cl-
B.一定含有K+
C.一定含有SO42–和CO32–
D.NO3–的存在无法确定
第Ⅱ卷(非选择题
共55分)
17.(12分)对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的。
(1)现有下列5种物质:CO、CaO、MgO、Fe2O3、Na2O。按照不同的分类标准,它们中有
1种物质与其他4种物质有明显的不同,找出这种物质,并写出依据(写出两种分类方法):
①______________________________________________;
②______________________________________________。?
(2)从(1)中的物质中找出两种能相互反应的物质,写出一个氧化还原反应的化学方程式:
____________________________________。?
(3)生活中的食醋和豆浆分别属于分散系中的______和______,用______
(填化学专用名词)
可以鉴别两者。?
18.(14分)已知反应:
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥SiO2+2NaOH=Na2SiO3+H2O。
(1)上述反应中,不属于氧化还原反应的是________(填序号,下同)。
(2)H2O被氧化的是________;H2O被还原的是_______;属于氧化还原反应,但其中的H2O
既不被氧化又不被还原的是_____________。
(3)反应②中,氧化剂和还原剂的质量之比为_______;反应③中,当有1个O2分子生成时,
转移的电子数目是_____个。
(4)写出反应⑥的离子方程式:______________________________________________。
19.(14分)Ⅰ.现有以下物质:①NaOH溶液;②液氯;③Ba(OH)2固体,④熔融KHSO4;
⑤Fe(OH)3胶体:⑥水银;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩NaHCO3。
(1)以上物质中属于电解质的是______(填序号);以上纯净物中能导电的是______(填序号)。
(2)写出⑩在水溶液中的电离方程式______________________________。
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向
Ba(OH)2溶液中滴加盐酸,测定导电率的变化如图所示,回答下列问题:
(3)Ba(OH)2在水中以离子形式存在的实验证据是
_____________。
(4)A—B段,发生的离子反应方程式是____________。
(5)B点恰好完全反应,此时溶液中存在的微粒主要有H2O、
______________。
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应
的实质相同的是___________。
A.Ba(OH)2和H2SO4???
?
B.NaOH?和H2SO4
C.Ba(OH)2与HNO3
20.(12分)有五种物质A、B、C、D、E,其中一种是碱,其余四种是盐。它们溶于水后电
离只产生下表中的离子:
阳离子
Na+、H+、Ba2+
阴离子
OH–、CO32–、SO42–
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E
可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X的名称是___________,X______
(填“是”或“不是”)电解质。?
(2)B在水中的电离方程式为____________________。鉴别B溶液中阴离子的实验操作方法
___________________________________________________________________________。?
(3)写出以下水溶液中反应的离子方程式。
①A溶液与B溶液反应生成无色气体X:_______________________________________。?
②B溶液与C溶液反应至溶液呈中性:_________________________________________。?
沙市高级中学校2021-2022学年高一上学期9月月考
化学答案
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
B
D
B
D
C
D
C
C
D
B
B
A
B
A
C
A
17.(12分)(1)①CO常温常压下是气体,其余是固体(2分)
②CO是非金属氧化物,其余是金属氧化物(2分)
(2)Fe2O3+3CO2Fe+3CO2(2分)
(3)溶液(2分);胶体(2分);丁达尔效应(2分)
18.(14分)(1)①⑤⑥(2分)
(2)③(2分);④(2分);②(2分)
(3)1︰2(2分);4(2分)
(4)SiO2+2OH–=SiO32–+H2O(2分)
19.(14分)(1)③④⑧⑩(2分);④⑥(2分)
(2)NaHCO3=Na++HCO3–(2分)
(3)A点导电率高(2分)
(4)H++OH–=H2O(2分)
(5)Ba2+、Cl–(2分)
(6)BC(2分)
20.(12分)(1)二氧化碳(2分);不是(2分)
(2)NaHSO4=Na++H++SO42–(2分);取少量B溶液放入试管中,先加入足量盐酸,不生
成沉淀;再加入BaCl2溶液,生成白色沉淀,证明溶液中含有SO42–(2分)
(3)CO32–+2H+=CO2↑+H2O(2分);2H++SO42–+Ba2++2OH-=BaSO4↓+2H2O(2分)
7
化学试卷
时间:75分钟
满分:100分
考试时间:2021年9月23日
第Ⅰ卷(选择题
共48分)
一、选择题(本题包括16个小题,每小3分,共48分,每小题只有1个选项符合题意)
1.化学与生活、社会发展息息相关,下列说法不正确的是(
)
A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B.“千淘万漉虽辛苦,吹尽狂沙始到金”体现了运用化学方法的淘金方式
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.“春蚕到死丝方尽,蜡炬成灰泪始干”诗句中涉及氧化还原反应
2.下列物质组,按强电解质、弱电解质、非电解质的顺序排列的是(
)
A.烧碱、纯碱、苛性钾
B.硫酸氢钠、NH3、乙醇
C.氯酸钾、醋酸、铜
D.硫酸铵、碳酸、SO2
3.下列不是Fe(OH)3胶体和MgCl2溶液共同具备的性质是(
)
A.都比较稳定,密封放置不产生沉淀
B.都有丁达尔效应
C.加入NaOH溶液都可产生沉淀
D.分散质微粒均可透过滤纸
4.下列各组中的离子,能在无色透明的溶液中大量共存的是(
)
A.Mg2+、H+、Cl–、OH–
B.Na+、Ba2+、CO32–、NO3–
C.Na+、H+、Cu2+、SO42–
D.K+、Zn2+、NO3–、SO42–
5.纳米材料是指粒子直径为1~100
nm的材料,纳米碳就是其中的一种。下列有关纳米碳的说
法正确的是(
)
A.纳米碳是一种新的化合物
B.纳米碳属于胶体,能产生丁达尔效应
C.纳米碳极易燃烧,产物能使澄清石灰水变浑浊
D.纳米碳与金刚石是碳元素的同素异形体,性质相同
6.下列反应既属于离子反应又属于氧化还原反应的是(
)
A.NaCl溶液与AgNO3溶液反应
B.Fe在O2中燃烧
C.CO与Fe2O3在高温下反应
D.Zn与稀硫酸反应
7.下列关于氧化还原反应的说法中错误的是(
)
A.氧化还原反应的实质是电子的转移
B.氧化还原反应中一定存在元素化合价的变化
C.氧化还原反应一定有氧元素参加
D.发生氧化反应的物质也可能同时发生还原反应
8.下列变化过程中,需要加入氧化剂才能实现的是(
)
A.H2O2O2
B.SO3H2SO4
C.CuCu(NO3)2
D.MnO2Mn2+
9.下列叙述正确的是(
)
A.氨水能导电,所以氨水是电解质
B.既有单质参加又有单质生成的反应一定是氧化还原反应
C.溶于水后能电离出H?+的化合物都是酸
D.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
10.下列反应的离子方程式书写正确的是(
)
A.金属镁与稀盐酸反应:Mg+2H++2Cl-===MgCl2+H2↑
B.氯化钡溶液与稀硫酸反应:Ba2++SO===BaSO4↓
C.碳酸钠溶液与稀盐酸反应:Na2CO3+2H+===2Na++H2O+CO2↑
D.氢氧化镁与稀硫酸反应:OH-+H+===H2O
11.下列反应能用H++OH–=H2O表示的是(
)
A.稀盐酸和大理石反应
B.H2SO4溶液和NaOH溶液反应
C.醋酸溶液和NaOH溶液反应
D.稀硫酸和Ba(OH)2溶液反应
12.离子方程式BaCO3+2H+=CO2↑+H2O+Ba2+中的H+不能代表的物质是(
)
①HCl ②H2SO4 ③HNO3 ④NaHSO4
⑤CH3COOH
A.②④⑤
B.①④⑤
C.①③
D.①⑤
13.高锰酸钾在医药上用作防腐剂、消毒剂、除臭剂及解毒剂;在水质净化及废水处理中,作
水处理剂。高锰酸钾受热分解可以制得氧气,反应为2KMnO4△K2MnO4+MnO2+O2↑,有关该反应,下列说法错误的是(
)
A.氧化剂和还原剂都是KMnO4
B.该反应的还原产物只有MnO2
C.该反应的氧化产物是O2
D.KMnO4中Mn元素被还原,O元素被氧化
14.某溶液中含有较大量的Cl–、、OH–三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中,正确的是(
)
①滴加Mg(NO3)2溶液
②过滤
③滴加AgNO3溶液
④滴加Ba(NO3)2溶液
A.④②①②③
B.④②③②①
C.①②③②④
D.①②④②③
15.如图所示为物质经一步反应转化的两种途径,
下列相关说法中正确的是(
)
A.氧化物为SO2
B.X只能是H2SO4
C.②可能有沉淀生成
D.②一定是酸碱中和反应
16.某溶液中可能含有以下离子中的几种:Ba2+、Cl-、NO3–、CO32–、K+、SO42–,为确定其组
成,进行了如下实验:①取少量溶液,加入稍过量的BaCl2溶液,产生白色沉淀;②过滤后在沉淀中加入稀盐酸,沉淀部分溶解;③在滤液中加入AgNO3溶液,产生白色沉淀。根据实验,以下推测不正确的是(
)
A.一定含有Cl-
B.一定含有K+
C.一定含有SO42–和CO32–
D.NO3–的存在无法确定
第Ⅱ卷(非选择题
共55分)
17.(12分)对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的。
(1)现有下列5种物质:CO、CaO、MgO、Fe2O3、Na2O。按照不同的分类标准,它们中有
1种物质与其他4种物质有明显的不同,找出这种物质,并写出依据(写出两种分类方法):
①______________________________________________;
②______________________________________________。?
(2)从(1)中的物质中找出两种能相互反应的物质,写出一个氧化还原反应的化学方程式:
____________________________________。?
(3)生活中的食醋和豆浆分别属于分散系中的______和______,用______
(填化学专用名词)
可以鉴别两者。?
18.(14分)已知反应:
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥SiO2+2NaOH=Na2SiO3+H2O。
(1)上述反应中,不属于氧化还原反应的是________(填序号,下同)。
(2)H2O被氧化的是________;H2O被还原的是_______;属于氧化还原反应,但其中的H2O
既不被氧化又不被还原的是_____________。
(3)反应②中,氧化剂和还原剂的质量之比为_______;反应③中,当有1个O2分子生成时,
转移的电子数目是_____个。
(4)写出反应⑥的离子方程式:______________________________________________。
19.(14分)Ⅰ.现有以下物质:①NaOH溶液;②液氯;③Ba(OH)2固体,④熔融KHSO4;
⑤Fe(OH)3胶体:⑥水银;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩NaHCO3。
(1)以上物质中属于电解质的是______(填序号);以上纯净物中能导电的是______(填序号)。
(2)写出⑩在水溶液中的电离方程式______________________________。
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向
Ba(OH)2溶液中滴加盐酸,测定导电率的变化如图所示,回答下列问题:
(3)Ba(OH)2在水中以离子形式存在的实验证据是
_____________。
(4)A—B段,发生的离子反应方程式是____________。
(5)B点恰好完全反应,此时溶液中存在的微粒主要有H2O、
______________。
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应
的实质相同的是___________。
A.Ba(OH)2和H2SO4???
?
B.NaOH?和H2SO4
C.Ba(OH)2与HNO3
20.(12分)有五种物质A、B、C、D、E,其中一种是碱,其余四种是盐。它们溶于水后电
离只产生下表中的离子:
阳离子
Na+、H+、Ba2+
阴离子
OH–、CO32–、SO42–
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E
可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X的名称是___________,X______
(填“是”或“不是”)电解质。?
(2)B在水中的电离方程式为____________________。鉴别B溶液中阴离子的实验操作方法
___________________________________________________________________________。?
(3)写出以下水溶液中反应的离子方程式。
①A溶液与B溶液反应生成无色气体X:_______________________________________。?
②B溶液与C溶液反应至溶液呈中性:_________________________________________。?
沙市高级中学校2021-2022学年高一上学期9月月考
化学答案
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
B
D
B
D
C
D
C
C
D
B
B
A
B
A
C
A
17.(12分)(1)①CO常温常压下是气体,其余是固体(2分)
②CO是非金属氧化物,其余是金属氧化物(2分)
(2)Fe2O3+3CO2Fe+3CO2(2分)
(3)溶液(2分);胶体(2分);丁达尔效应(2分)
18.(14分)(1)①⑤⑥(2分)
(2)③(2分);④(2分);②(2分)
(3)1︰2(2分);4(2分)
(4)SiO2+2OH–=SiO32–+H2O(2分)
19.(14分)(1)③④⑧⑩(2分);④⑥(2分)
(2)NaHCO3=Na++HCO3–(2分)
(3)A点导电率高(2分)
(4)H++OH–=H2O(2分)
(5)Ba2+、Cl–(2分)
(6)BC(2分)
20.(12分)(1)二氧化碳(2分);不是(2分)
(2)NaHSO4=Na++H++SO42–(2分);取少量B溶液放入试管中,先加入足量盐酸,不生
成沉淀;再加入BaCl2溶液,生成白色沉淀,证明溶液中含有SO42–(2分)
(3)CO32–+2H+=CO2↑+H2O(2分);2H++SO42–+Ba2++2OH-=BaSO4↓+2H2O(2分)
7
同课章节目录
