3.3.1元素(课件25页)
图片预览







文档简介
(共25张PPT)
第三单元
课题3
第1课时
人教版-化学-九年级上册
元素
学习目标-新知导入-新知探究-课堂小结-课堂达标
【重点】认识元素的存在。
【难点】形成元素的概念。
1.了解元素的概念,将对物质的宏观组成与微观结构的认识统一起来;
2.了解各种元素在地壳中的含量及在生物细胞中的含量。
学习目标
新知导入
这些不都是日常生活中的一些物品吗?
是的,一些广告常宣传”含人体必需的营养元素”,这里的“元素”是指什么?今天我们就来一起学习。
新知导入
新知探究
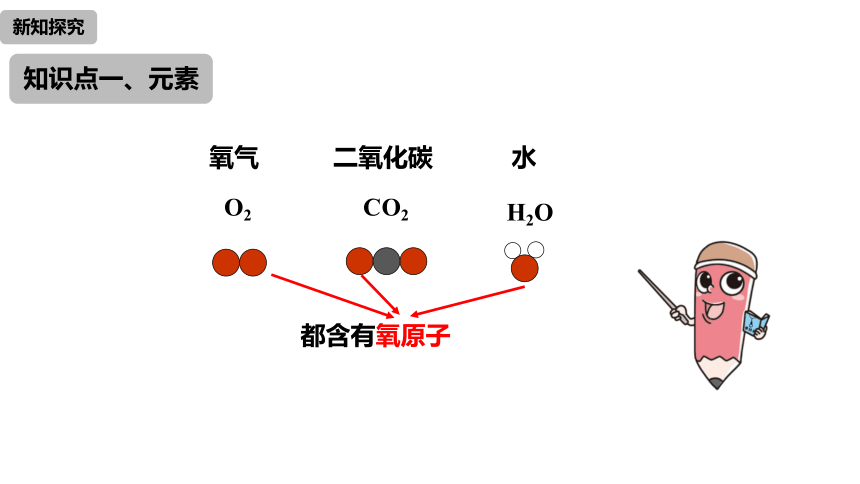
知识点一、元素
都含有氧原子
O2
氧气
CO2
二氧化碳
H2O
水
新知探究
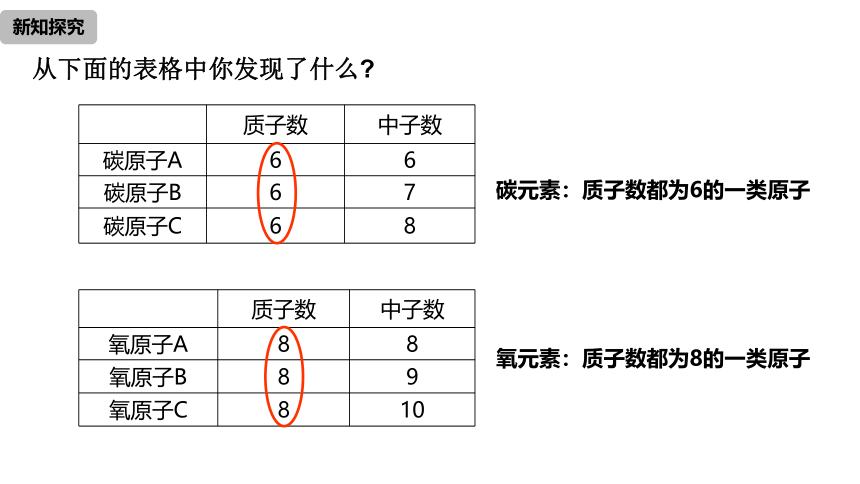
从下面的表格中你发现了什么?
质子数
中子数
碳原子A
6
6
碳原子B
6
7
碳原子C
6
8
质子数
中子数
氧原子A
8
8
氧原子B
8
9
氧原子C
8
10
氧元素:质子数都为8的一类原子
碳元素:质子数都为6的一类原子
新知探究
元素的定义
把质子数(即核电荷数)为8的原子统称为氧元素。
把质子数(即核电荷数)为1的原子统称为氢元素。
把质子数(即核电荷数)为6的原子统称为碳元素。
元素是质子数(即核电荷数)相同的一类原子的总称
新知探究
不同元素的根本区别是质子数(即核电荷数)不同,元素的种类由质子数决定。如氢的质子数是1,氧的质子数是8。
元素是同一类原子的“总称”,是一个宏观概念,因此元素只讲种类,不讲个数。
对“一类原子”的理解:
核电荷数(即质子数)相同,中子数不同的几种原子;如氢原子(质子数为1,中子数有0、1、2)。
核电荷数(即质子数)相同,核外电子数不同的原子和离子。如钠原子和钠离子。
1
3
2
新知探究
元素的性质
从微观角度来看,化学反应的实质是分子破裂为原子,原子重新组成新的分子,化学变化前后原子的种类、数目不变,则元素种类也不变。
元素的化学性质与其原子的核外电子排布,特别是最外层电子的数目有关,即最外层电子数决定元素的化学性质,最外层电子数相同的元素具有相似的化学性质。
新知探究
元素与原子的比较
元
素
原
子
概
念
质子数(即核电荷数)相同的一类原子的总称
化学变化中的最小粒子
区
别
宏观概念,只讲种类,不讲个数
微观概念,既讲种类,又讲个数
适用范围
描述物质的宏观组成,如水是由氢、氧两种元素组成的
描述物质的微观构成,如1个水分子由2个氢原子和1个氧原子构成
联
系
元素是质子数相同的一类原子总称,原子是元素的个体(即最小单位),元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系
新知探究
元素的存在
从19世纪末开始,科学家们对地壳的岩石、天然水、矿物、土壤等进行了普遍分析,他们总结了五千多个样品分析数据,历尽千辛万苦得出了元素在地壳中的平均含量,这种勇于探索的科学精神是值得我们学习的。
氧O
硅Si
铝Al
铁Fe
钙
Ca
地壳中含量前五位元素
养闺女贴盖
新知探究
元素的分布
元素的分布
地壳中:
生物细胞中:
空气中:
海水中:
氮(N)、氧(O)
氧(O)、碳(C)、氢(H)、氮(N)
氧(O)、硅(Si)、铝(Al)、铁(Fe)
氧(O)、氢(H)、氯(Cl)、钠(Na)
新知探究
元素的分类
非金属元素
金属元素:元素名称带“?钅”字旁(汞、金除外)如:铁、铜等
气态非金属元素:元素名称带“?气”字头
如:氢、氧等
液态非金属元素:元素名称带“?氵”字旁
如:溴
固态非金属元素:元素名称带“?石”字旁
如:碳、硅等
元素的分类
稀有气体元素
“含氟牙膏”中的“氟”指的是( )
典例1
新知探究
A.分子
B.原子
C.离子
D.元素
D
(北京中考)
方法点拨:本题主要考查的是元素的概念。含氟牙膏中的“氟”不是以单质、分子、原子、离子等形式存在的,这里的“氟”是存在的元素,与具体形态无关。
方法点拨:决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是质子数不同。
典例2
新知探究
不同种元素最本质的区别是( )
A.质子数不同
B.核外电子数不同
C.中子数不同
D.最外层电子数不同
A
(兰州中考)
新知探究
知识点二、物质的组成、构成
物质的组成可从宏观和微观两个方面进行描述:其中元素是从宏观上描述物质的组成,即“宏观对宏观”;原子、分子是从微观上描述物质的构成,即“微观对微观”。
自然界中,由一百多种元素组成的几千万种物质都是由原子、分子或离子构成的。
1
2
新知探究
元素与物质、微粒间的关系
构成
分解
得失电子
失得电子
物质的组成用元素描述,物质的构成用分子、原子或离子描述,分子的构成用原子描述。
元素
组成
氧气、氢气、水等
铁、汞、金刚石等
硫酸铜、氯化钠等
构成
构成
构成
分子
原子
离子
新知探究
物质
分子
原子
元素
具有相同核电荷数的一类原子的总称
组
成
构
成
构
成
构
成
破
裂
失得电子
得失电子
宏观概念
只讲种类
不讲个数
微观概念
既讲种类
又讲个数
离子
构
成
典例1
新知探究
二氧化碳(CO2)是植物进行光合作用的原料之一。下列关于二氧化碳的说法错误的是( )
A.二氧化碳由碳元素和氧元素组成
B.二氧化碳由二氧化碳分子构成
C.二氧化碳分子由碳元素和氧元素组成
D.一个二氧化碳分子由一个碳原子和两个氧原子构成
解析:元素只能用于描述物质的宏观组成,不能用于描述分子的构成。
C
典例2
新知探究
1.氧气、氢气、氨等物质是由________构成的;
2.铁、汞、金刚石等物质是由________构成的;
3.氯化钠、硫酸铜等是由________构成的。
分子
原子
离子
将正确答案填写在题中划线处。
课堂小结
元素
分类
分子、原子、元素、离子与物质之间的关系
概念
含量
地壳中:氧、硅、铝、铁等
生物细胞中:氧、碳、氢、氮等
金属元素、非金属元素、稀有气体元素
元素是质子数(即核电荷数)相同的一类原子的总称
下列关于物质的组成与构成的说法正确的是( )
A.水是由氢原子和氧原子构成的
B.汞是由汞分子构成的
C.氧分子由氧元素组成
D.二氧化碳是由碳、氧两种元素组成的
(包头中考)
D
课堂达标
1
方法点拨:
①从宏观角度讲物质是由元素组成的,可描述为“某物质是由某元素组成的”;②从微观角度讲物质是由分子、原子、离子等粒子构成的,可描述为“某物质是由某种粒子(分子、原子、离子)构成的”;③分子的构成用原子来描述。
课堂达标
2
过氧化氢(H2O2) 由氢原子和氧原子构成
过氧化氢分子 由2个氢原子和2个氧原子构成
1个过氧化氢分子
由氢元素和氧元素组成
根据下列所给要求进行连线。
下列关于元素的叙述中正确的是(
)
D
课堂达标
3
A.质子数相同的两种粒子属于同种元素
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素原子的核外电子数
D.不同种元素的根本区别是核内质子数不同
方法点拨:元素的种类是由质子数来决定的,质子数相同的原子或离子属于同种元素。
下列物质中含金属元素的是( )
课堂达标
4
解析:铝(Al)属于金属元素,其他的氢(H)、硫(S)、氧(O)、氮(N)、磷(P)均为非金属元素。
A.硫酸
(H2SO4)
B.氧化铝
(Al2O3)
C.二氧化氮
(NO2)
D.五氧化二磷
(P2O5)
(北京中考)
B
第三单元
课题3
第1课时
人教版-化学-九年级上册
元素
学习目标-新知导入-新知探究-课堂小结-课堂达标
【重点】认识元素的存在。
【难点】形成元素的概念。
1.了解元素的概念,将对物质的宏观组成与微观结构的认识统一起来;
2.了解各种元素在地壳中的含量及在生物细胞中的含量。
学习目标
新知导入
这些不都是日常生活中的一些物品吗?
是的,一些广告常宣传”含人体必需的营养元素”,这里的“元素”是指什么?今天我们就来一起学习。
新知导入
新知探究
知识点一、元素
都含有氧原子
O2
氧气
CO2
二氧化碳
H2O
水
新知探究
从下面的表格中你发现了什么?
质子数
中子数
碳原子A
6
6
碳原子B
6
7
碳原子C
6
8
质子数
中子数
氧原子A
8
8
氧原子B
8
9
氧原子C
8
10
氧元素:质子数都为8的一类原子
碳元素:质子数都为6的一类原子
新知探究
元素的定义
把质子数(即核电荷数)为8的原子统称为氧元素。
把质子数(即核电荷数)为1的原子统称为氢元素。
把质子数(即核电荷数)为6的原子统称为碳元素。
元素是质子数(即核电荷数)相同的一类原子的总称
新知探究
不同元素的根本区别是质子数(即核电荷数)不同,元素的种类由质子数决定。如氢的质子数是1,氧的质子数是8。
元素是同一类原子的“总称”,是一个宏观概念,因此元素只讲种类,不讲个数。
对“一类原子”的理解:
核电荷数(即质子数)相同,中子数不同的几种原子;如氢原子(质子数为1,中子数有0、1、2)。
核电荷数(即质子数)相同,核外电子数不同的原子和离子。如钠原子和钠离子。
1
3
2
新知探究
元素的性质
从微观角度来看,化学反应的实质是分子破裂为原子,原子重新组成新的分子,化学变化前后原子的种类、数目不变,则元素种类也不变。
元素的化学性质与其原子的核外电子排布,特别是最外层电子的数目有关,即最外层电子数决定元素的化学性质,最外层电子数相同的元素具有相似的化学性质。
新知探究
元素与原子的比较
元
素
原
子
概
念
质子数(即核电荷数)相同的一类原子的总称
化学变化中的最小粒子
区
别
宏观概念,只讲种类,不讲个数
微观概念,既讲种类,又讲个数
适用范围
描述物质的宏观组成,如水是由氢、氧两种元素组成的
描述物质的微观构成,如1个水分子由2个氢原子和1个氧原子构成
联
系
元素是质子数相同的一类原子总称,原子是元素的个体(即最小单位),元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系
新知探究
元素的存在
从19世纪末开始,科学家们对地壳的岩石、天然水、矿物、土壤等进行了普遍分析,他们总结了五千多个样品分析数据,历尽千辛万苦得出了元素在地壳中的平均含量,这种勇于探索的科学精神是值得我们学习的。
氧O
硅Si
铝Al
铁Fe
钙
Ca
地壳中含量前五位元素
养闺女贴盖
新知探究
元素的分布
元素的分布
地壳中:
生物细胞中:
空气中:
海水中:
氮(N)、氧(O)
氧(O)、碳(C)、氢(H)、氮(N)
氧(O)、硅(Si)、铝(Al)、铁(Fe)
氧(O)、氢(H)、氯(Cl)、钠(Na)
新知探究
元素的分类
非金属元素
金属元素:元素名称带“?钅”字旁(汞、金除外)如:铁、铜等
气态非金属元素:元素名称带“?气”字头
如:氢、氧等
液态非金属元素:元素名称带“?氵”字旁
如:溴
固态非金属元素:元素名称带“?石”字旁
如:碳、硅等
元素的分类
稀有气体元素
“含氟牙膏”中的“氟”指的是( )
典例1
新知探究
A.分子
B.原子
C.离子
D.元素
D
(北京中考)
方法点拨:本题主要考查的是元素的概念。含氟牙膏中的“氟”不是以单质、分子、原子、离子等形式存在的,这里的“氟”是存在的元素,与具体形态无关。
方法点拨:决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是质子数不同。
典例2
新知探究
不同种元素最本质的区别是( )
A.质子数不同
B.核外电子数不同
C.中子数不同
D.最外层电子数不同
A
(兰州中考)
新知探究
知识点二、物质的组成、构成
物质的组成可从宏观和微观两个方面进行描述:其中元素是从宏观上描述物质的组成,即“宏观对宏观”;原子、分子是从微观上描述物质的构成,即“微观对微观”。
自然界中,由一百多种元素组成的几千万种物质都是由原子、分子或离子构成的。
1
2
新知探究
元素与物质、微粒间的关系
构成
分解
得失电子
失得电子
物质的组成用元素描述,物质的构成用分子、原子或离子描述,分子的构成用原子描述。
元素
组成
氧气、氢气、水等
铁、汞、金刚石等
硫酸铜、氯化钠等
构成
构成
构成
分子
原子
离子
新知探究
物质
分子
原子
元素
具有相同核电荷数的一类原子的总称
组
成
构
成
构
成
构
成
破
裂
失得电子
得失电子
宏观概念
只讲种类
不讲个数
微观概念
既讲种类
又讲个数
离子
构
成
典例1
新知探究
二氧化碳(CO2)是植物进行光合作用的原料之一。下列关于二氧化碳的说法错误的是( )
A.二氧化碳由碳元素和氧元素组成
B.二氧化碳由二氧化碳分子构成
C.二氧化碳分子由碳元素和氧元素组成
D.一个二氧化碳分子由一个碳原子和两个氧原子构成
解析:元素只能用于描述物质的宏观组成,不能用于描述分子的构成。
C
典例2
新知探究
1.氧气、氢气、氨等物质是由________构成的;
2.铁、汞、金刚石等物质是由________构成的;
3.氯化钠、硫酸铜等是由________构成的。
分子
原子
离子
将正确答案填写在题中划线处。
课堂小结
元素
分类
分子、原子、元素、离子与物质之间的关系
概念
含量
地壳中:氧、硅、铝、铁等
生物细胞中:氧、碳、氢、氮等
金属元素、非金属元素、稀有气体元素
元素是质子数(即核电荷数)相同的一类原子的总称
下列关于物质的组成与构成的说法正确的是( )
A.水是由氢原子和氧原子构成的
B.汞是由汞分子构成的
C.氧分子由氧元素组成
D.二氧化碳是由碳、氧两种元素组成的
(包头中考)
D
课堂达标
1
方法点拨:
①从宏观角度讲物质是由元素组成的,可描述为“某物质是由某元素组成的”;②从微观角度讲物质是由分子、原子、离子等粒子构成的,可描述为“某物质是由某种粒子(分子、原子、离子)构成的”;③分子的构成用原子来描述。
课堂达标
2
过氧化氢(H2O2) 由氢原子和氧原子构成
过氧化氢分子 由2个氢原子和2个氧原子构成
1个过氧化氢分子
由氢元素和氧元素组成
根据下列所给要求进行连线。
下列关于元素的叙述中正确的是(
)
D
课堂达标
3
A.质子数相同的两种粒子属于同种元素
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素原子的核外电子数
D.不同种元素的根本区别是核内质子数不同
方法点拨:元素的种类是由质子数来决定的,质子数相同的原子或离子属于同种元素。
下列物质中含金属元素的是( )
课堂达标
4
解析:铝(Al)属于金属元素,其他的氢(H)、硫(S)、氧(O)、氮(N)、磷(P)均为非金属元素。
A.硫酸
(H2SO4)
B.氧化铝
(Al2O3)
C.二氧化氮
(NO2)
D.五氧化二磷
(P2O5)
(北京中考)
B
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
