2021-2022学年高一上学期化学鲁科版(2019)必修第一册第1章 认识化学科学 单元测试 (含答案)
文档属性
| 名称 | 2021-2022学年高一上学期化学鲁科版(2019)必修第一册第1章 认识化学科学 单元测试 (含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 225.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-27 00:00:00 | ||
图片预览



文档简介
第1章
认识化学科学课后题含答案2021—2022学年(上学期)高一化学鲁科版(2019)必修第一册
鲁科版(2019)必修第一册第1章
认识化学科学
一、选择题。(15题)
1、下列说法错误的是(
)
A.面粉厂严禁烟火
B.活性炭具有除异味和杀菌作用
C.实验中用到电器,禁止湿手操作
D.不可以用甲醛溶液浸泡海鲜产品来延长保质期
2、家庭使用漂白粉时为了增强漂白粉的漂白能力,可在漂白粉中加入少量的( )
A.NaCl
B.Na2CO3
C.水
D.食用醋
3、漂白粉主要成分可表示为:Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为(
)
A.7.5
B.8.0
C.9.5
D.11.0
4、将4.34克Na、Na2O、Na2O2混合物与足量的水反应,在标准情况下得到672ml气体,将该混合气体通过电火花点燃,恰好完全反应,则它们的物质的量之比为(
)
A.1:1:1
B.1:1:2
C.1:2:1
D.4:3:2
5、由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是(
)
A.水分子的化学性质改变
B.水分子中氧氢键长缩短
C.小分子团水是一种新化合物
D.水分子间结构、物理性质改变
6、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe
B.Mg
C.Cu
D.Ag
7、氯化碘(ICl)的化学性质跟Cl2相似,预计它与H2O反应的最初生成物是(
)
A.HI和HClO
B.HCl和HIO
C.HClO3和HIO
D.HCl和HI
8、配制一定物质的量浓度的溶液,造成浓度偏高的操作是(
)
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
9、下列化学药品与其危险化学品图形标志不一致的一组是(
)
A.烧碱——1
B.甲烷——2
C.酒精——3
D.白磷——4
10、下列说法中正确的是( )
A.Cl-和Cl2都有毒
B.液氯和氯水都有漂白性
C.将NaCl溶液滴入AgNO3溶液中或将氯气通入AgNO3溶液中均会出现白色沉淀
D.含Cl-的溶液和氯水一样均呈黄绿色
11、在空气中久置而不易变质的物质是(
)
A.过氧化钠
B.亚硫酸钠
C.硅酸钠溶液
D.纯碱
12、下列溶液中,Cl-的物质的量浓度最大的是(
)
A.1
mL
0.5
mol·L-1的NaCl溶液
B.100
mL
0.01
mol·L-1的MgCl2溶液
C.100
mL
0.1
mol·L-1的AlCl3溶液
D.10
mL
1
mol·L-1的KClO3溶液
13、晋朝葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍,绞取汁,尽服之……”,受此启发为人类做出巨大贡献的科学家是(
)
A.屠呦呦
B.钟南山
C.侯德榜
D.张青莲
14、下列关于氯气及其化合物的叙述不正确的是( )
A.新制氯水久置后酸性增强
B.氯气在常温下能与铁反应,故不能用铁罐存放液氯
C.氯水具有杀菌、漂白作用是因为氯水中含有次氯酸
D.新制备的氯水可使蓝色石蕊溶液先变红后褪色
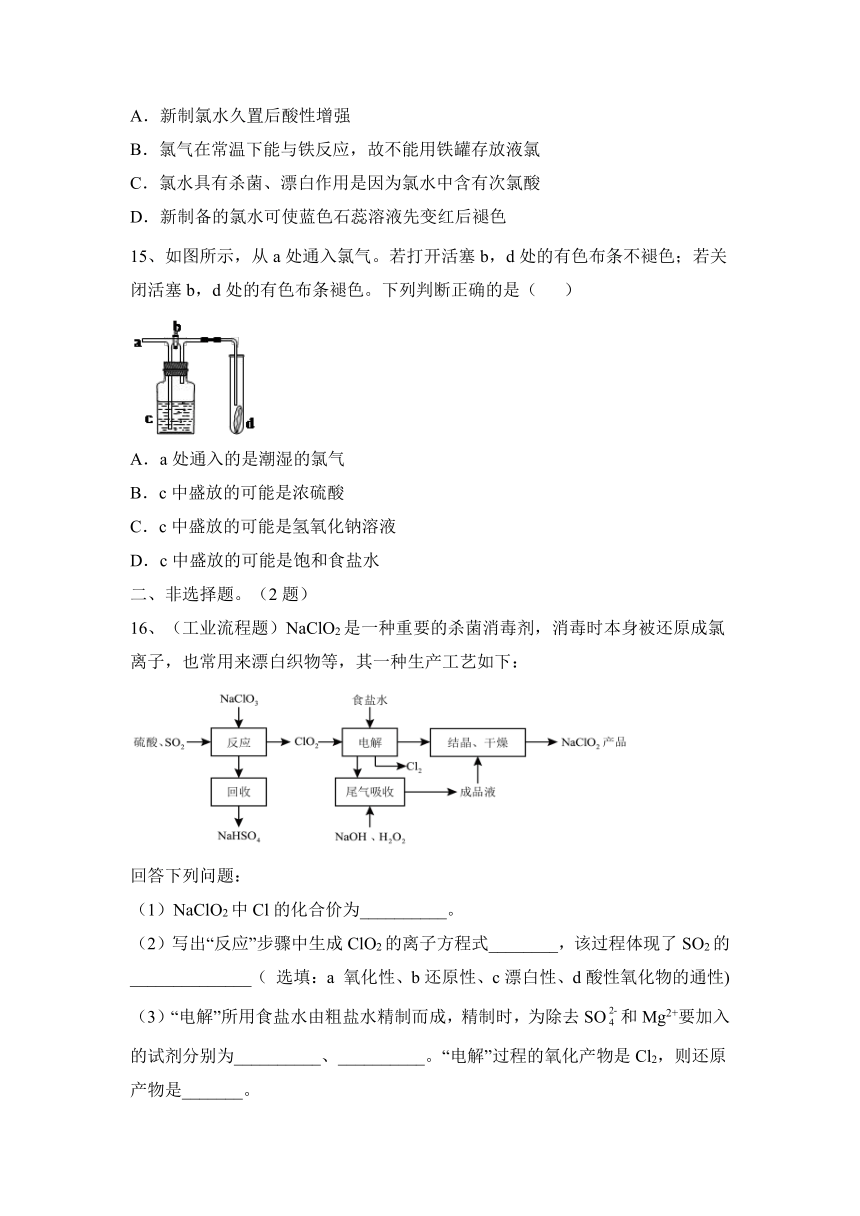
15、如图所示,从a处通入氯气。若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色。下列判断正确的是(
)
A.a处通入的是潮湿的氯气
B.c中盛放的可能是浓硫酸
C.c中盛放的可能是氢氧化钠溶液
D.c中盛放的可能是饱和食盐水
二、非选择题。(2题)
16、(工业流程题)NaClO2是一种重要的杀菌消毒剂,消毒时本身被还原成氯离子,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)NaClO2中Cl的化合价为__________。
(2)写出“反应”步骤中生成ClO2的离子方程式________,该过程体现了SO2的______________(
选填:a
氧化性、b还原性、c漂白性、d酸性氧化物的通性)
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去SO和Mg2+要加入的试剂分别为__________、__________。“电解”过程的氧化产物是Cl2,则还原产物是_______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应的化学方程式为__________,实验室进行结晶操作使用的仪器有铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳和__________。
(5)消毒能力可用单位质量消毒剂得电子多少来衡量。NaClO2与Cl2消毒能力比为___________。(不必化简)。
17、将200mlBaCl2溶液等分为两份,一份中加入100ml物质的量浓度为0.1mol/L的稀硫酸,恰好完全沉淀;另一份中加入足量AgNO3溶液,使其充分沉淀。试计算:
(1)此BaCl2溶液的物质的量浓度是________
(2)上述反应中生成的AgCl沉淀的质量是________
第1章
认识化学科学课后题含答案2021—2022学年(上学期)高一化学鲁科版(2019)必修第一册
鲁科版(2019)必修第一册第1章
认识化学科学
一、选择题。(15题)
1、下列说法错误的是(
)
A.面粉厂严禁烟火
B.活性炭具有除异味和杀菌作用
C.实验中用到电器,禁止湿手操作
D.不可以用甲醛溶液浸泡海鲜产品来延长保质期
【答案】B
2、家庭使用漂白粉时为了增强漂白粉的漂白能力,可在漂白粉中加入少量的( )
A.NaCl
B.Na2CO3
C.水
D.食用醋
【答案】D
3、漂白粉主要成分可表示为:Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为(
)
A.7.5
B.8.0
C.9.5
D.11.0
【答案】B
4、将4.34克Na、Na2O、Na2O2混合物与足量的水反应,在标准情况下得到672ml气体,将该混合气体通过电火花点燃,恰好完全反应,则它们的物质的量之比为(
)
A.1:1:1
B.1:1:2
C.1:2:1
D.4:3:2
【答案】D
5、由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是(
)
A.水分子的化学性质改变
B.水分子中氧氢键长缩短
C.小分子团水是一种新化合物
D.水分子间结构、物理性质改变
【答案】D
6、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe
B.Mg
C.Cu
D.Ag
【答案】B
7、氯化碘(ICl)的化学性质跟Cl2相似,预计它与H2O反应的最初生成物是(
)
A.HI和HClO
B.HCl和HIO
C.HClO3和HIO
D.HCl和HI
【答案】B
8、配制一定物质的量浓度的溶液,造成浓度偏高的操作是(
)
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
【答案】B
9、下列化学药品与其危险化学品图形标志不一致的一组是(
)
A.烧碱——1
B.甲烷——2
C.酒精——3
D.白磷——4
【答案】A
10、下列说法中正确的是( )
A.Cl-和Cl2都有毒
B.液氯和氯水都有漂白性
C.将NaCl溶液滴入AgNO3溶液中或将氯气通入AgNO3溶液中均会出现白色沉淀
D.含Cl-的溶液和氯水一样均呈黄绿色
【答案】C
11、在空气中久置而不易变质的物质是(
)
A.过氧化钠
B.亚硫酸钠
C.硅酸钠溶液
D.纯碱
【答案】D
12、下列溶液中,Cl-的物质的量浓度最大的是(
)
A.1
mL
0.5
mol·L-1的NaCl溶液
B.100
mL
0.01
mol·L-1的MgCl2溶液
C.100
mL
0.1
mol·L-1的AlCl3溶液
D.10
mL
1
mol·L-1的KClO3溶液
【答案】A
13、晋朝葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍,绞取汁,尽服之……”,受此启发为人类做出巨大贡献的科学家是(
)
A.屠呦呦
B.钟南山
C.侯德榜
D.张青莲
【答案】A
14、下列关于氯气及其化合物的叙述不正确的是( )
A.新制氯水久置后酸性增强
B.氯气在常温下能与铁反应,故不能用铁罐存放液氯
C.氯水具有杀菌、漂白作用是因为氯水中含有次氯酸
D.新制备的氯水可使蓝色石蕊溶液先变红后褪色
【答案】B
15、如图所示,从a处通入氯气。若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色。下列判断正确的是(
)
A.a处通入的是潮湿的氯气
B.c中盛放的可能是浓硫酸
C.c中盛放的可能是氢氧化钠溶液
D.c中盛放的可能是饱和食盐水
【答案】D
二、非选择题。(2题)
16、(工业流程题)NaClO2是一种重要的杀菌消毒剂,消毒时本身被还原成氯离子,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)NaClO2中Cl的化合价为__________。
(2)写出“反应”步骤中生成ClO2的离子方程式________,该过程体现了SO2的______________(
选填:a
氧化性、b还原性、c漂白性、d酸性氧化物的通性)
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去SO和Mg2+要加入的试剂分别为__________、__________。“电解”过程的氧化产物是Cl2,则还原产物是_______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应的化学方程式为__________,实验室进行结晶操作使用的仪器有铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳和__________。
(5)消毒能力可用单位质量消毒剂得电子多少来衡量。NaClO2与Cl2消毒能力比为___________。(不必化简)。
【答案】+3
2ClO+SO2=2ClO2+SO
b
BaCl2
NaOH
NaClO2
2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2
蒸发皿
142:90.5
17、将200mlBaCl2溶液等分为两份,一份中加入100ml物质的量浓度为0.1mol/L的稀硫酸,恰好完全沉淀;另一份中加入足量AgNO3溶液,使其充分沉淀。试计算:
(1)此BaCl2溶液的物质的量浓度是________
(2)上述反应中生成的AgCl沉淀的质量是________
【答案】0.1mol/L
2.87g
认识化学科学课后题含答案2021—2022学年(上学期)高一化学鲁科版(2019)必修第一册
鲁科版(2019)必修第一册第1章
认识化学科学
一、选择题。(15题)
1、下列说法错误的是(
)
A.面粉厂严禁烟火
B.活性炭具有除异味和杀菌作用
C.实验中用到电器,禁止湿手操作
D.不可以用甲醛溶液浸泡海鲜产品来延长保质期
2、家庭使用漂白粉时为了增强漂白粉的漂白能力,可在漂白粉中加入少量的( )
A.NaCl
B.Na2CO3
C.水
D.食用醋
3、漂白粉主要成分可表示为:Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为(
)
A.7.5
B.8.0
C.9.5
D.11.0
4、将4.34克Na、Na2O、Na2O2混合物与足量的水反应,在标准情况下得到672ml气体,将该混合气体通过电火花点燃,恰好完全反应,则它们的物质的量之比为(
)
A.1:1:1
B.1:1:2
C.1:2:1
D.4:3:2
5、由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是(
)
A.水分子的化学性质改变
B.水分子中氧氢键长缩短
C.小分子团水是一种新化合物
D.水分子间结构、物理性质改变
6、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe
B.Mg
C.Cu
D.Ag
7、氯化碘(ICl)的化学性质跟Cl2相似,预计它与H2O反应的最初生成物是(
)
A.HI和HClO
B.HCl和HIO
C.HClO3和HIO
D.HCl和HI
8、配制一定物质的量浓度的溶液,造成浓度偏高的操作是(
)
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
9、下列化学药品与其危险化学品图形标志不一致的一组是(
)
A.烧碱——1
B.甲烷——2
C.酒精——3
D.白磷——4
10、下列说法中正确的是( )
A.Cl-和Cl2都有毒
B.液氯和氯水都有漂白性
C.将NaCl溶液滴入AgNO3溶液中或将氯气通入AgNO3溶液中均会出现白色沉淀
D.含Cl-的溶液和氯水一样均呈黄绿色
11、在空气中久置而不易变质的物质是(
)
A.过氧化钠
B.亚硫酸钠
C.硅酸钠溶液
D.纯碱
12、下列溶液中,Cl-的物质的量浓度最大的是(
)
A.1
mL
0.5
mol·L-1的NaCl溶液
B.100
mL
0.01
mol·L-1的MgCl2溶液
C.100
mL
0.1
mol·L-1的AlCl3溶液
D.10
mL
1
mol·L-1的KClO3溶液
13、晋朝葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍,绞取汁,尽服之……”,受此启发为人类做出巨大贡献的科学家是(
)
A.屠呦呦
B.钟南山
C.侯德榜
D.张青莲
14、下列关于氯气及其化合物的叙述不正确的是( )
A.新制氯水久置后酸性增强
B.氯气在常温下能与铁反应,故不能用铁罐存放液氯
C.氯水具有杀菌、漂白作用是因为氯水中含有次氯酸
D.新制备的氯水可使蓝色石蕊溶液先变红后褪色
15、如图所示,从a处通入氯气。若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色。下列判断正确的是(
)
A.a处通入的是潮湿的氯气
B.c中盛放的可能是浓硫酸
C.c中盛放的可能是氢氧化钠溶液
D.c中盛放的可能是饱和食盐水
二、非选择题。(2题)
16、(工业流程题)NaClO2是一种重要的杀菌消毒剂,消毒时本身被还原成氯离子,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)NaClO2中Cl的化合价为__________。
(2)写出“反应”步骤中生成ClO2的离子方程式________,该过程体现了SO2的______________(
选填:a
氧化性、b还原性、c漂白性、d酸性氧化物的通性)
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去SO和Mg2+要加入的试剂分别为__________、__________。“电解”过程的氧化产物是Cl2,则还原产物是_______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应的化学方程式为__________,实验室进行结晶操作使用的仪器有铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳和__________。
(5)消毒能力可用单位质量消毒剂得电子多少来衡量。NaClO2与Cl2消毒能力比为___________。(不必化简)。
17、将200mlBaCl2溶液等分为两份,一份中加入100ml物质的量浓度为0.1mol/L的稀硫酸,恰好完全沉淀;另一份中加入足量AgNO3溶液,使其充分沉淀。试计算:
(1)此BaCl2溶液的物质的量浓度是________
(2)上述反应中生成的AgCl沉淀的质量是________
第1章
认识化学科学课后题含答案2021—2022学年(上学期)高一化学鲁科版(2019)必修第一册
鲁科版(2019)必修第一册第1章
认识化学科学
一、选择题。(15题)
1、下列说法错误的是(
)
A.面粉厂严禁烟火
B.活性炭具有除异味和杀菌作用
C.实验中用到电器,禁止湿手操作
D.不可以用甲醛溶液浸泡海鲜产品来延长保质期
【答案】B
2、家庭使用漂白粉时为了增强漂白粉的漂白能力,可在漂白粉中加入少量的( )
A.NaCl
B.Na2CO3
C.水
D.食用醋
【答案】D
3、漂白粉主要成分可表示为:Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为(
)
A.7.5
B.8.0
C.9.5
D.11.0
【答案】B
4、将4.34克Na、Na2O、Na2O2混合物与足量的水反应,在标准情况下得到672ml气体,将该混合气体通过电火花点燃,恰好完全反应,则它们的物质的量之比为(
)
A.1:1:1
B.1:1:2
C.1:2:1
D.4:3:2
【答案】D
5、由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是(
)
A.水分子的化学性质改变
B.水分子中氧氢键长缩短
C.小分子团水是一种新化合物
D.水分子间结构、物理性质改变
【答案】D
6、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe
B.Mg
C.Cu
D.Ag
【答案】B
7、氯化碘(ICl)的化学性质跟Cl2相似,预计它与H2O反应的最初生成物是(
)
A.HI和HClO
B.HCl和HIO
C.HClO3和HIO
D.HCl和HI
【答案】B
8、配制一定物质的量浓度的溶液,造成浓度偏高的操作是(
)
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
【答案】B
9、下列化学药品与其危险化学品图形标志不一致的一组是(
)
A.烧碱——1
B.甲烷——2
C.酒精——3
D.白磷——4
【答案】A
10、下列说法中正确的是( )
A.Cl-和Cl2都有毒
B.液氯和氯水都有漂白性
C.将NaCl溶液滴入AgNO3溶液中或将氯气通入AgNO3溶液中均会出现白色沉淀
D.含Cl-的溶液和氯水一样均呈黄绿色
【答案】C
11、在空气中久置而不易变质的物质是(
)
A.过氧化钠
B.亚硫酸钠
C.硅酸钠溶液
D.纯碱
【答案】D
12、下列溶液中,Cl-的物质的量浓度最大的是(
)
A.1
mL
0.5
mol·L-1的NaCl溶液
B.100
mL
0.01
mol·L-1的MgCl2溶液
C.100
mL
0.1
mol·L-1的AlCl3溶液
D.10
mL
1
mol·L-1的KClO3溶液
【答案】A
13、晋朝葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍,绞取汁,尽服之……”,受此启发为人类做出巨大贡献的科学家是(
)
A.屠呦呦
B.钟南山
C.侯德榜
D.张青莲
【答案】A
14、下列关于氯气及其化合物的叙述不正确的是( )
A.新制氯水久置后酸性增强
B.氯气在常温下能与铁反应,故不能用铁罐存放液氯
C.氯水具有杀菌、漂白作用是因为氯水中含有次氯酸
D.新制备的氯水可使蓝色石蕊溶液先变红后褪色
【答案】B
15、如图所示,从a处通入氯气。若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色。下列判断正确的是(
)
A.a处通入的是潮湿的氯气
B.c中盛放的可能是浓硫酸
C.c中盛放的可能是氢氧化钠溶液
D.c中盛放的可能是饱和食盐水
【答案】D
二、非选择题。(2题)
16、(工业流程题)NaClO2是一种重要的杀菌消毒剂,消毒时本身被还原成氯离子,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)NaClO2中Cl的化合价为__________。
(2)写出“反应”步骤中生成ClO2的离子方程式________,该过程体现了SO2的______________(
选填:a
氧化性、b还原性、c漂白性、d酸性氧化物的通性)
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去SO和Mg2+要加入的试剂分别为__________、__________。“电解”过程的氧化产物是Cl2,则还原产物是_______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应的化学方程式为__________,实验室进行结晶操作使用的仪器有铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳和__________。
(5)消毒能力可用单位质量消毒剂得电子多少来衡量。NaClO2与Cl2消毒能力比为___________。(不必化简)。
【答案】+3
2ClO+SO2=2ClO2+SO
b
BaCl2
NaOH
NaClO2
2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2
蒸发皿
142:90.5
17、将200mlBaCl2溶液等分为两份,一份中加入100ml物质的量浓度为0.1mol/L的稀硫酸,恰好完全沉淀;另一份中加入足量AgNO3溶液,使其充分沉淀。试计算:
(1)此BaCl2溶液的物质的量浓度是________
(2)上述反应中生成的AgCl沉淀的质量是________
【答案】0.1mol/L
2.87g
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
