第1章 物质及其变化(1-4)小练(无答案)
文档属性
| 名称 | 第1章 物质及其变化(1-4)小练(无答案) | 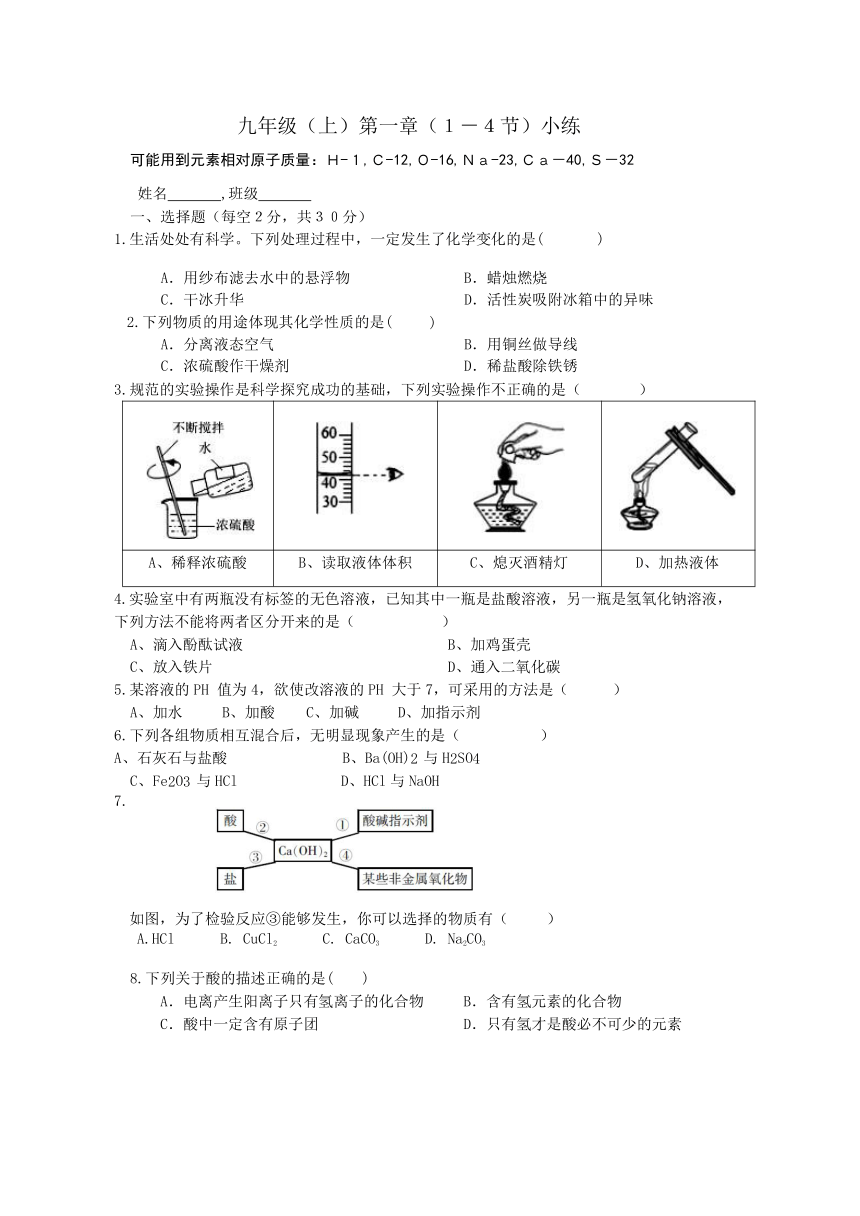 | |
| 格式 | zip | ||
| 文件大小 | 121.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-09-28 14:30:16 | ||
图片预览


文档简介
九年级(上)第一章(1-4节)小练
可能用到元素相对原子质量:H-1,C-12,O-16,Na-23,Ca-40,S-32
姓名
,班级
一、选择题(每空2分,共30分)
1.生活处处有科学。下列处理过程中,一定发生了化学变化的是(
)
A.用纱布滤去水中的悬浮物
B.蜡烛燃烧
C.干冰升华
D.活性炭吸附冰箱中的异味
2.下列物质的用途体现其化学性质的是(
)
A.分离液态空气
B.用铜丝做导线
C.浓硫酸作干燥剂
D.稀盐酸除铁锈
3.规范的实验操作是科学探究成功的基础,下列实验操作不正确的是(
)
A、稀释浓硫酸
B、读取液体体积
C、熄灭酒精灯
D、加热液体
4.实验室中有两瓶没有标签的无色溶液,已知其中一瓶是盐酸溶液,另一瓶是氢氧化钠溶液,下列方法不能将两者区分开来的是(
)
A、滴入酚酞试液
B、加鸡蛋壳
C、放入铁片
D、通入二氧化碳
5.某溶液的
PH
值为
4,欲使改溶液的
PH
大于
7,可采用的方法是(
)
A、加水
B、加酸
C、加碱
D、加指示剂
6.下列各组物质相互混合后,无明显现象产生的是(
)
A、石灰石与盐酸
B、Ba(OH)2
与
H2SO4
C、Fe2O3
与
HCl
D、HCl
与
NaOH
7.
如图,为了检验反应③能够发生,你可以选择的物质有(
)
A.HCl
B.
CuCl2
C.
CaCO3
D.
Na2CO3
8.下列关于酸的描述正确的是(
)
A.电离产生阳离子只有氢离子的化合物
B.含有氢元素的化合物
C.酸中一定含有原子团
D.只有氢才是酸必不可少的元素
9.为探究盐酸的化学性质,某学习小组做了如下实验。下列反应中无现象的是(
)
10.能用BaCl2溶液鉴别的一组物质是(
)
A.HCl、KNO3
B.Na2SO4、H2SO4
C.KNO3、NaNO3
D.HCl、H2SO4
11.盛石灰水的试剂瓶存放久了,内壁常附有一层白膜,除去这层白膜最合适的试剂是
(
)
A、蒸馏水
B、稀盐酸
C、硫酸铜溶液
D、氢氧化钠溶液
12.下列化学方程式符合事实的是(
)
铁粉与稀盐酸混合后有大量气泡产生:Fe+6HCl===2FeCl3+3H2↑
稀盐酸洒到大理石表面上有气泡产生:CaCO3+2HCl===CaCl2+H2O+CO2↑
C.用盐酸除锈:Fe2O3+4HCl===2FeCl2+3H2O
D.黑色的氧化铜粉末与稀盐酸混合后,溶液变成蓝色:CuO+2HCl===CuCl2+H2↑
13.欲除去氢氧化钠溶液中的碳酸钠杂质,可以选用下列试剂中的(
)
A、二氧化碳气体
B、澄清石灰水
C、氯化钙溶液
D、稀盐酸
14.将下列试剂分别加入
KOH
溶液,饱和石灰水和稀
H2SO4
中,能出现三种不同现象的是
(
)
A、紫色石蕊试液
B、Na2CO3
溶液
C、CuCl2
溶液
D、NaCl
溶液
用如图所示装置进行实验。将
a
中的
NaOH
浓溶液挤入盛满
CO2
气体的
b
中,打开止水夹.可能看到的现象是(
)
A.c
中的水倒吸入导管中
B.导管处有气泡冒出C.气球胀大
D.无明显现象
二、填空题(每空2分,共28分)
16、打开浓盐酸盖子,看到瓶口上方有
,这其实是
(填化学式)跟空气中的水结合生成的盐酸小液滴,长时间敞开瓶口,浓盐酸质量分数
(填“增大”、“减小”
或“不变”。
17、浓硫酸具有
,不小心把浓硫酸滴在纸上,纸张会变黑炭化.浓硫酸还有
性,
可以用来干燥
等气体。
18、氢氧化钠固体暴露在空气会吸收空气中的水分而
,
还会与空气中的二氧化碳反应而变质,请写出化学方程式
.
19、小明想知道柠檬酸和醋酸的酸性哪个强,他先使用紫色石蕊进行检测,发现溶液都变
,并且颜色很接近。于是,他又利用
PH
试纸进行检测,具体操作是
,与标准比色卡对照,PH值都在3附近,还是难以分辨。最后,向又向实验室借来PH计
,得到柠檬酸PH值2.1,醋酸PH值2.9
,小明得出结论:柠檬酸酸性比醋酸
。
20.小明学习了酸和碱之后,发现它们其实离我们很近,我们的胃液中含有
,刷墙壁的石灰浆是
,家里请了阿姨来洗油烟机,阿姨居然拿出了一瓶苛性钠,苛性钠其实就是
。
三、实验探究(每空
3
分,24题6分,共
24
分)
21、为验证“酸的化学通性”,某班同学在实验室进行如下实验。请分析并回答相关问题:
A
B
C
D
写出能证明B
中反应发生的现象
。
要全面验证酸的化学通性,D
试管中能与酸反应的固体单质是
(写一种即可)。(3)实验完成后,将全部废液倒入废液缸内,测得
pH=2,则该废液中可能含有溶质
(写化学式)。
22、铜丝表面上常有一层氧化铜,某同学于是把该铜丝放到稀硫酸中浸泡一会,很快铜表面的黑色氧化铜就没有了,该同学想知道是稀硫酸中的哪种粒子使氧化铜溶解,请你和他一起通过图中的三个实验完成这次探究活动:(另取纯的氧化铜粉末做实验)
你提出的假设是
。
通过实验
I
无明显变化,可以证明
。
证明另外两种粒子能否溶解氧化铜,还要进行两组实验,其中在Ⅲ中应加入
。
23、某小组同学在实验室,发现两瓶丢失了标签的试剂,掉落的标签上分别写着氢氧化钙溶液和氢氧化钠溶液,请你用学过的知识来鉴别哪瓶是氢氧化钠溶液,哪瓶是氢氧化钙溶液。请写出具体的操作过程、现象及预测结果。
四、分析计算题(8
分,10
分)
24、某硫酸厂每天排放
3.2
千克二氧化硫尾气,工作人员用
20%的氢氧化钠溶液来吸收这些尾气,同时生成的产物Na2SO3(对眼睛、皮肤、粘膜有刺激作用,可污染水源,受高热分解产生有毒烟气)可用于制作有机化学药品、漂白织物等,应用广泛。请计算:
每天可制得
Na2SO3
晶体多少千克
求每天至少需要配置质量分数
20%的氢氧化钠溶液多少千克?
已知反应化学方程式:SO2+2NaOH=Na2SO3+H2O.
25、小明想知道鸡蛋壳中碳酸钙的含量,取得一只鸡蛋壳,清洗干燥后,称量得到蛋壳质量
4.8
克,与稀盐酸反应,加入稀盐酸的质量与生成气体的质量关系如图所示,已知
m=1.76。
求生成二氧化碳的质量为
克。
这个鸡蛋壳含碳酸钙的质量分数是多少?
(3)当加入
120
克稀盐酸后,经充分反应,溶液中的溶质有
。
可能用到元素相对原子质量:H-1,C-12,O-16,Na-23,Ca-40,S-32
姓名
,班级
一、选择题(每空2分,共30分)
1.生活处处有科学。下列处理过程中,一定发生了化学变化的是(
)
A.用纱布滤去水中的悬浮物
B.蜡烛燃烧
C.干冰升华
D.活性炭吸附冰箱中的异味
2.下列物质的用途体现其化学性质的是(
)
A.分离液态空气
B.用铜丝做导线
C.浓硫酸作干燥剂
D.稀盐酸除铁锈
3.规范的实验操作是科学探究成功的基础,下列实验操作不正确的是(
)
A、稀释浓硫酸
B、读取液体体积
C、熄灭酒精灯
D、加热液体
4.实验室中有两瓶没有标签的无色溶液,已知其中一瓶是盐酸溶液,另一瓶是氢氧化钠溶液,下列方法不能将两者区分开来的是(
)
A、滴入酚酞试液
B、加鸡蛋壳
C、放入铁片
D、通入二氧化碳
5.某溶液的
PH
值为
4,欲使改溶液的
PH
大于
7,可采用的方法是(
)
A、加水
B、加酸
C、加碱
D、加指示剂
6.下列各组物质相互混合后,无明显现象产生的是(
)
A、石灰石与盐酸
B、Ba(OH)2
与
H2SO4
C、Fe2O3
与
HCl
D、HCl
与
NaOH
7.
如图,为了检验反应③能够发生,你可以选择的物质有(
)
A.HCl
B.
CuCl2
C.
CaCO3
D.
Na2CO3
8.下列关于酸的描述正确的是(
)
A.电离产生阳离子只有氢离子的化合物
B.含有氢元素的化合物
C.酸中一定含有原子团
D.只有氢才是酸必不可少的元素
9.为探究盐酸的化学性质,某学习小组做了如下实验。下列反应中无现象的是(
)
10.能用BaCl2溶液鉴别的一组物质是(
)
A.HCl、KNO3
B.Na2SO4、H2SO4
C.KNO3、NaNO3
D.HCl、H2SO4
11.盛石灰水的试剂瓶存放久了,内壁常附有一层白膜,除去这层白膜最合适的试剂是
(
)
A、蒸馏水
B、稀盐酸
C、硫酸铜溶液
D、氢氧化钠溶液
12.下列化学方程式符合事实的是(
)
铁粉与稀盐酸混合后有大量气泡产生:Fe+6HCl===2FeCl3+3H2↑
稀盐酸洒到大理石表面上有气泡产生:CaCO3+2HCl===CaCl2+H2O+CO2↑
C.用盐酸除锈:Fe2O3+4HCl===2FeCl2+3H2O
D.黑色的氧化铜粉末与稀盐酸混合后,溶液变成蓝色:CuO+2HCl===CuCl2+H2↑
13.欲除去氢氧化钠溶液中的碳酸钠杂质,可以选用下列试剂中的(
)
A、二氧化碳气体
B、澄清石灰水
C、氯化钙溶液
D、稀盐酸
14.将下列试剂分别加入
KOH
溶液,饱和石灰水和稀
H2SO4
中,能出现三种不同现象的是
(
)
A、紫色石蕊试液
B、Na2CO3
溶液
C、CuCl2
溶液
D、NaCl
溶液
用如图所示装置进行实验。将
a
中的
NaOH
浓溶液挤入盛满
CO2
气体的
b
中,打开止水夹.可能看到的现象是(
)
A.c
中的水倒吸入导管中
B.导管处有气泡冒出C.气球胀大
D.无明显现象
二、填空题(每空2分,共28分)
16、打开浓盐酸盖子,看到瓶口上方有
,这其实是
(填化学式)跟空气中的水结合生成的盐酸小液滴,长时间敞开瓶口,浓盐酸质量分数
(填“增大”、“减小”
或“不变”。
17、浓硫酸具有
,不小心把浓硫酸滴在纸上,纸张会变黑炭化.浓硫酸还有
性,
可以用来干燥
等气体。
18、氢氧化钠固体暴露在空气会吸收空气中的水分而
,
还会与空气中的二氧化碳反应而变质,请写出化学方程式
.
19、小明想知道柠檬酸和醋酸的酸性哪个强,他先使用紫色石蕊进行检测,发现溶液都变
,并且颜色很接近。于是,他又利用
PH
试纸进行检测,具体操作是
,与标准比色卡对照,PH值都在3附近,还是难以分辨。最后,向又向实验室借来PH计
,得到柠檬酸PH值2.1,醋酸PH值2.9
,小明得出结论:柠檬酸酸性比醋酸
。
20.小明学习了酸和碱之后,发现它们其实离我们很近,我们的胃液中含有
,刷墙壁的石灰浆是
,家里请了阿姨来洗油烟机,阿姨居然拿出了一瓶苛性钠,苛性钠其实就是
。
三、实验探究(每空
3
分,24题6分,共
24
分)
21、为验证“酸的化学通性”,某班同学在实验室进行如下实验。请分析并回答相关问题:
A
B
C
D
写出能证明B
中反应发生的现象
。
要全面验证酸的化学通性,D
试管中能与酸反应的固体单质是
(写一种即可)。(3)实验完成后,将全部废液倒入废液缸内,测得
pH=2,则该废液中可能含有溶质
(写化学式)。
22、铜丝表面上常有一层氧化铜,某同学于是把该铜丝放到稀硫酸中浸泡一会,很快铜表面的黑色氧化铜就没有了,该同学想知道是稀硫酸中的哪种粒子使氧化铜溶解,请你和他一起通过图中的三个实验完成这次探究活动:(另取纯的氧化铜粉末做实验)
你提出的假设是
。
通过实验
I
无明显变化,可以证明
。
证明另外两种粒子能否溶解氧化铜,还要进行两组实验,其中在Ⅲ中应加入
。
23、某小组同学在实验室,发现两瓶丢失了标签的试剂,掉落的标签上分别写着氢氧化钙溶液和氢氧化钠溶液,请你用学过的知识来鉴别哪瓶是氢氧化钠溶液,哪瓶是氢氧化钙溶液。请写出具体的操作过程、现象及预测结果。
四、分析计算题(8
分,10
分)
24、某硫酸厂每天排放
3.2
千克二氧化硫尾气,工作人员用
20%的氢氧化钠溶液来吸收这些尾气,同时生成的产物Na2SO3(对眼睛、皮肤、粘膜有刺激作用,可污染水源,受高热分解产生有毒烟气)可用于制作有机化学药品、漂白织物等,应用广泛。请计算:
每天可制得
Na2SO3
晶体多少千克
求每天至少需要配置质量分数
20%的氢氧化钠溶液多少千克?
已知反应化学方程式:SO2+2NaOH=Na2SO3+H2O.
25、小明想知道鸡蛋壳中碳酸钙的含量,取得一只鸡蛋壳,清洗干燥后,称量得到蛋壳质量
4.8
克,与稀盐酸反应,加入稀盐酸的质量与生成气体的质量关系如图所示,已知
m=1.76。
求生成二氧化碳的质量为
克。
这个鸡蛋壳含碳酸钙的质量分数是多少?
(3)当加入
120
克稀盐酸后,经充分反应,溶液中的溶质有
。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
