第五单元课题2如何正确书写化学方程式课时练习-2021-2022学年九年级化学人教版上册(word版 含解析
文档属性
| 名称 | 第五单元课题2如何正确书写化学方程式课时练习-2021-2022学年九年级化学人教版上册(word版 含解析 |

|
|
| 格式 | zip | ||
| 文件大小 | 187.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-28 00:00:00 | ||
图片预览


文档简介
第五单元化学方程式课题2如何正确书写化学方程式课时练习人教版初中化学九年级上册
一、单选题(共12题)
1.根据化学方程式不能获得该反应的信息是(
)
A.反应物和生成物
B.反应中各物质间粒子个数比
C.化学反应的快慢
D.反应的条件
2.过氧化钠(Na2O2)是淡黄色粉末,常用于呼吸面具和潜水艇中,反应方程式:2Na2O2
+
2X
=
2Na2CO3+O2,则X
的化学式为(?
)
A.CO
B.NaHCO3
C.CO2
D.C
3.对于化学反应:4P+5O22P2O5,下列说法正确的是( )
①反应前后原子的种类和数目不变②反应前后分子总数不变③反应前后元素的种类和质量不变④反应前后元素的化合价不变.⑤反应前后物质的总质量不变⑥每4份质量的磷和5份质量氧气在点燃的条件下恰好完全反应生成2份质量的五氧化二磷
A.①③⑤
B.①③⑤⑥
C.①③④⑤
D.①②③⑤⑥
4.《本草纲目》记载:“雄黄,乃治疮杀毒要药也……”,雄黄主要成分为As4S4,在空气中加热到一定温度可以被氧化成剧毒物质三氧化二砷,其反应的化学方程式为:。则X的化学式为(
)
A.S
B.O2
C.SO2
D.SO3
5.下列化学方程式与事实相符且书写正确的是(
)
A.利用红磷测定空气中氧气含量:4P+5O22P2O5
B.实验室用过氧化氢溶液制氧气
2H2O2=2H2O+O2↑
C.铁在氧气中燃烧:4Fe
+3O22Fe2O3
D.用高锰酸钾制取氧气:2KMnO4K2MnO2+MnO2+
O2↑
6.超氧化钾(KO2)常备于急救器和消防队员背包中,能迅速与水反应放出氧气:,则X的化学式为(
)
A.H2O2
B.H2O
C.H2
D.CO2
7.容器内有甲、乙、丙、丁四种物质,一定条件下发生了化学反应,各物质的质量变化如图所示。下列说法正确的是(
)
A.X=0
B.丙可能为该反应的催化剂
C.乙、丁两物质变化的质量比为2:3
D.甲和丁的相对分子质量之比为1:2
8.由CO2制取C的太阳能工艺流程如图,利用铁的氧化物作催化剂,可提高效益。下列关于该原理说法错误的是(
)
A.该流程可以缓解温室效应
B.转化①为:
C.转化②中发生分解反应
D.每用一定量CO2制取C,须向体系中再添加一定量FeO
9.从陶瓷、玻璃、水泥到集成电路芯片,硅的用途非常广泛。工业制取高纯硅的部分反应原理的微观示意图如下图,有关判断错误的是(
)
A.甲的化学式是SiCl4
B.反应前后原子个数不变
C.X的化学式是HCl
D.反应前后分子个数不变
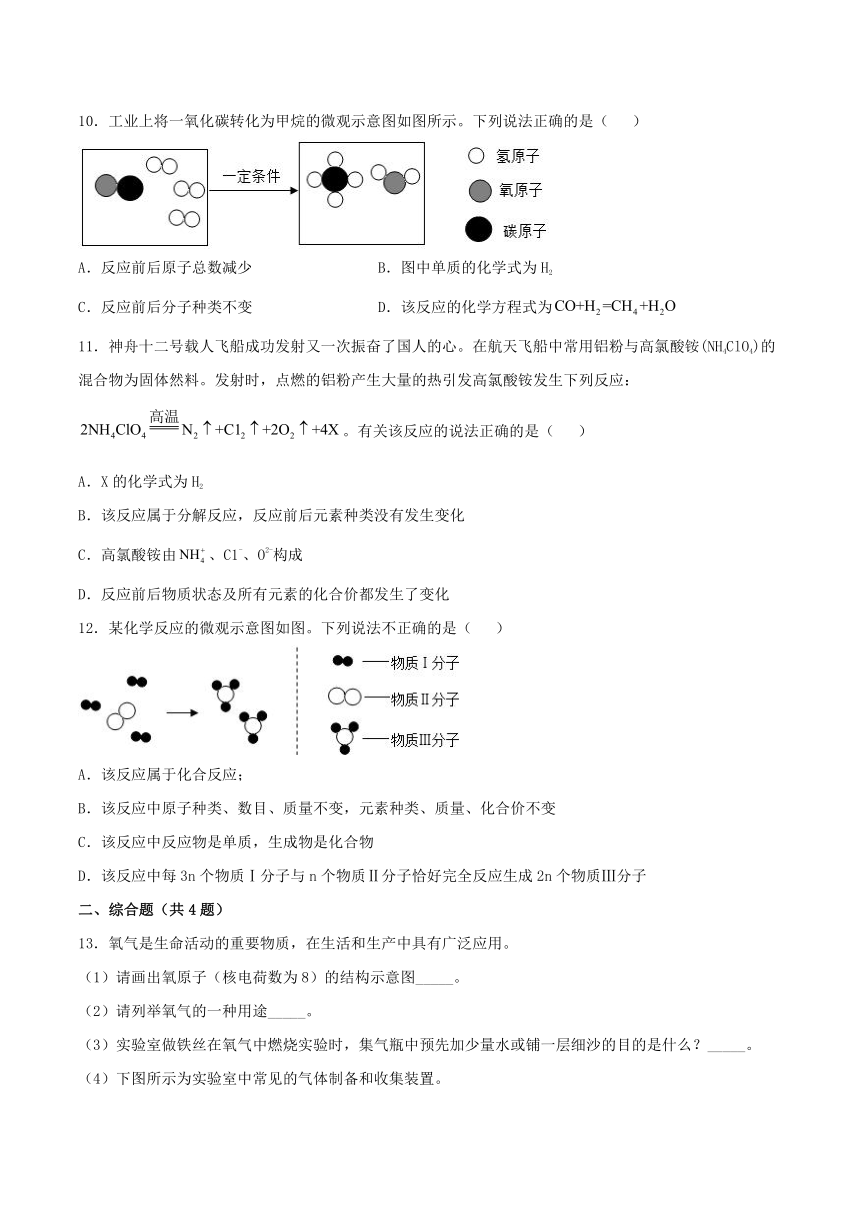
10.工业上将一氧化碳转化为甲烷的微观示意图如图所示。下列说法正确的是(
)
A.反应前后原子总数减少
B.图中单质的化学式为H2
C.反应前后分子种类不变
D.该反应的化学方程式为
11.神舟十二号载人飞船成功发射又一次振奋了国人的心。在航天飞船中常用铝粉与高氯酸铵(NH4ClO4)的混合物为固体然料。发射时,点燃的铝粉产生大量的热引发高氯酸铵发生下列反应:。有关该反应的说法正确的是(
)
A.X的化学式为H2
B.该反应属于分解反应,反应前后元素种类没有发生变化
C.高氯酸铵由、C1-、O2-构成
D.反应前后物质状态及所有元素的化合价都发生了变化
12.某化学反应的微观示意图如图。下列说法不正确的是(
)
A.该反应属于化合反应;
B.该反应中原子种类、数目、质量不变,元素种类、质量、化合价不变
C.该反应中反应物是单质,生成物是化合物
D.该反应中每3n个物质Ⅰ分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子
二、综合题(共4题)
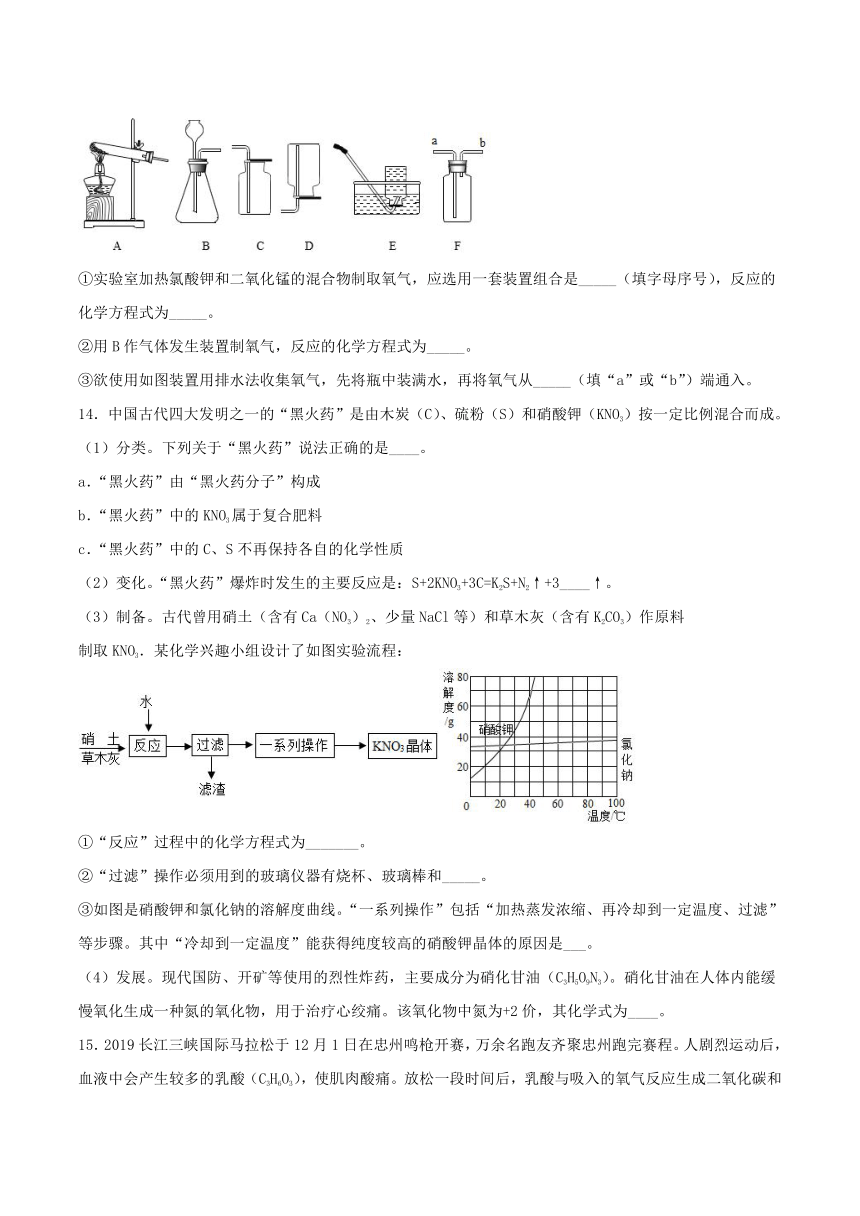
13.氧气是生命活动的重要物质,在生活和生产中具有广泛应用。
(1)请画出氧原子(核电荷数为8)的结构示意图_____。
(2)请列举氧气的一种用途_____。
(3)实验室做铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是什么?_____。
(4)下图所示为实验室中常见的气体制备和收集装置。
①实验室加热氯酸钾和二氧化锰的混合物制取氧气,应选用一套装置组合是_____(填字母序号),反应的化学方程式为_____。
②用B作气体发生装置制氧气,反应的化学方程式为_____。
③欲使用如图装置用排水法收集氧气,先将瓶中装满水,再将氧气从_____(填“a”或“b”)端通入。
14.中国古代四大发明之一的“黑火药”是由木炭(C)、硫粉(S)和硝酸钾(KNO3)按一定比例混合而成。
(1)分类。下列关于“黑火药”说法正确的是____。
a.“黑火药”由“黑火药分子”构成
b.“黑火药”中的KNO3属于复合肥料
c.“黑火药”中的C、S不再保持各自的化学性质
(2)变化。“黑火药”爆炸时发生的主要反应是:S+2KNO3+3C=K2S+N2↑+3____↑。
(3)制备。古代曾用硝土(含有Ca(NO3)2、少量NaCl等)和草木灰(含有K2CO3)作原料
制取KNO3.某化学兴趣小组设计了如图实验流程:
①“反应”过程中的化学方程式为_______。
②“过滤”操作必须用到的玻璃仪器有烧杯、玻璃棒和_____。
③如图是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括“加热蒸发浓缩、再冷却到一定温度、过滤”等步骤。其中“冷却到一定温度”能获得纯度较高的硝酸钾晶体的原因是___。
(4)发展。现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C3H5O9N3)。硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。该氧化物中氮为+2价,其化学式为____。
15.2019长江三峡国际马拉松于12月1日在忠州鸣枪开赛,万余名跑友齐聚忠州跑完赛程。人剧烈运动后,血液中会产生较多的乳酸(C3H6O3),使肌肉酸痛。放松一段时间后,乳酸与吸入的氧气反应生成二氧化碳和水,肌肉酸痛感消失。
(1)乳酸中碳、氢、氧的质量比为______。
(2)写出乳酸与氧气反应的化学方程式______。
(3)180g乳酸中碳元素与______g蔗糖(C12H22O11)中碳元素的质量相等。
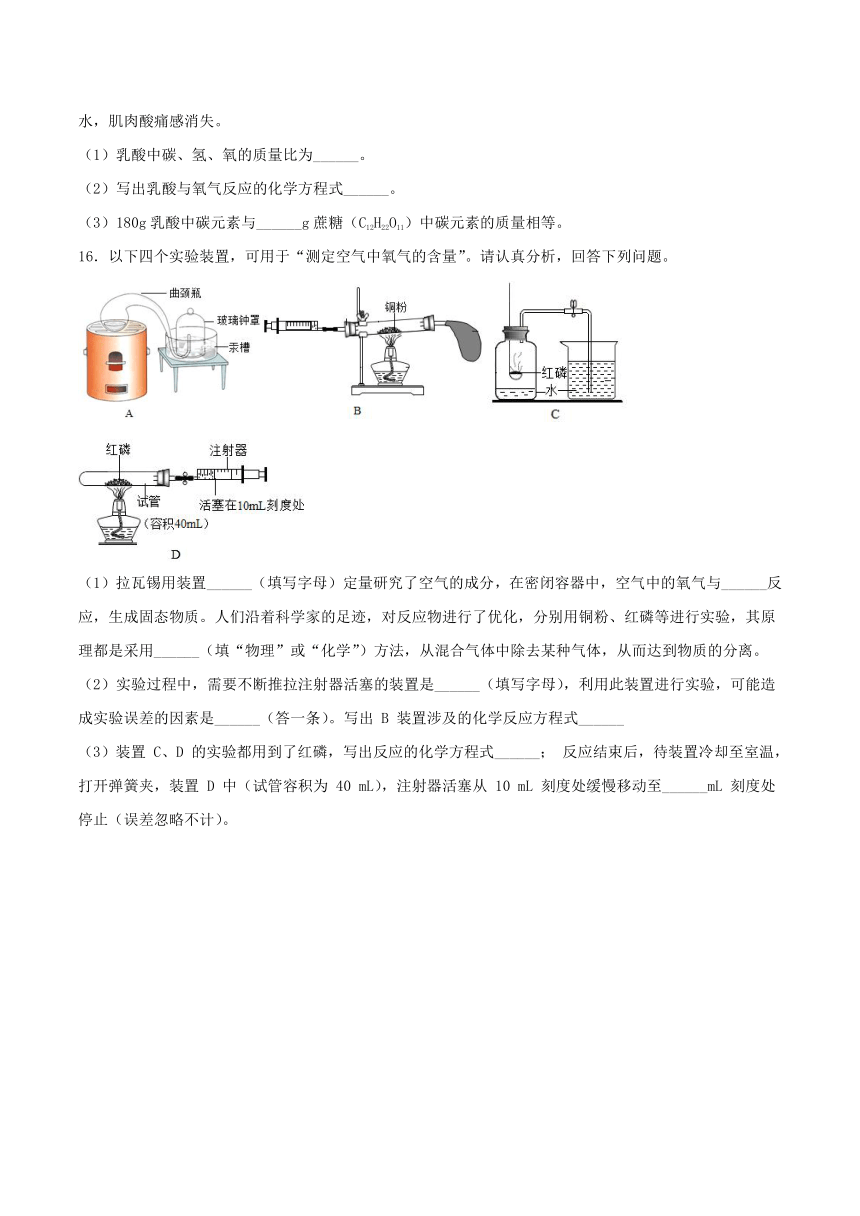
16.以下四个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
(1)拉瓦锡用装置______(填写字母)定量研究了空气的成分,在密闭容器中,空气中的氧气与______反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用______(填“物理”或“化学”)方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)实验过程中,需要不断推拉注射器活塞的装置是______(填写字母),利用此装置进行实验,可能造成实验误差的因素是______(答一条)。写出
B
装置涉及的化学反应方程式______
(3)装置
C、D
的实验都用到了红磷,写出反应的化学方程式______;
反应结束后,待装置冷却至室温,打开弹簧夹,装置
D
中(试管容积为
40
mL),注射器活塞从
10
mL
刻度处缓慢移动至______mL
刻度处停止(误差忽略不计)。
参考答案
1.C
【详解】
A、由化学方程式,可以确定“═”左边的是反应物,右边为生成物,故选项错误。
B、由化学方程式,根据化学式前的化学计量数可以确定反应中各物质间粒子个数比,故选项错误。
C、由化学方程式,无法确定化学反应的快慢,故选项正确。
D、由化学方程式,可以看出反应发生所需要的条件,故选项错误。
故选:C。
2.C
【详解】
根据质量守恒定律,反应前后原子的种类和数目不变,该方程式反应前后有4个钠原子,反应前有4个氧原子,反应后有8个氧原子,2个碳原子,故一个X分子中包含1个碳原子和2个氧原子,故X的化学式为CO2。
故选C。
3.A
【详解】
①由方程式可知,反应前后原子的种类和数目不变,选项正确;
②由方程式可知,每4个磷原子和5个氧分子在点燃条件下生成2个五氧化二磷分子,反应前后分子总数改变,选项错误;
③元素是具有相同质子数的同一类原子的总称,反应前后原子的种类和数目不变,可知反应前后元素的种类和质量不变,选项正确;
④单质中元素的化合价为零,化合物中元素的化合价代数和为零,反应前氧元素、磷元素的化合价都是0.反应后磷元素为+5价,氧元素为-2价,反应前后元素的化合价改变,选项错误;
⑤参加反应的各物质的质量总和等于反应后生成的各物质的质量总和,反应前后物质的总质量不变,选项正确;
⑥由方程式可知,每124份质量的磷和160份质量氧气在点燃的条件下恰好完全反应生成284份质量的五氧化二磷,选项错误。
故选A。
4.C
【详解】
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含As、O、S的个数分别是4、14、4,生成物中含As、O、S的个数分别是4、6、0,故生成物中还应含4个S、8个O,故X的化学式为:SO2。
故选C。
5.A
【详解】
A、红磷燃烧生产五氧化二磷,因只消耗空气中的氧气,生成物为固体可用于测定空气中氧气含量。化学方程式书写正确。正确。
B、实验室用过氧化氢溶液制氧气需要二氧化锰作催化剂。化学方程式应为:2H2O22H2O+O2↑。错误。
C、铁在氧气中燃烧生成四氧化三铁,化学方程式为3Fe
+2O2Fe3O4。错误。
D、高锰酸钾制取氧气化学方程式为2KMnO4K2MnO4+MnO2+
O2↑。锰酸钾化学式为K2MnO4。错误。
故选A。
6.A
【详解】
化学反应前后原子种类数目不变;反应物中钾原子、氧原子、氢原子的个数分别是2、6、4,生成物中钾原子、氧原子、氢原子的个数分别是2、4、2,故X中含有2个氢原子和2个氧原子,化学式为H2O2。
故选A。
7.B
【详解】
A、由质量守恒定律可知,反应后丙的质量=4g+10g+3g+4g?6g?4g?8g=3g,即X的值为3,选项错误;
B、由图和A可知,反应前后,物质丙的质量不变,则丙可能为该反应的催化剂,选项正确;
C、反应后乙减少的质量=10g?4g=6g,丁增加的质量=8g?4g=4g,则乙、丁两物质变化的质量比=6g:4g=3:2,选项错误;
D、反应后甲增加的质量=6g?4g=2g,丁增加的质量=8g?4g=4g,则甲、丁两物质变化的质量比=2g:4g=1:2,化学反应中,物质的质量比等于物质的相对分子质量与化学就计量数的乘积之比,题目中没有明确反应中甲和乙的化学计量数的关系,所以无法判断甲、乙的相对分子质量的关系,选项错误,故选B。
8.B
【详解】
A、由图可知,流程中二氧化碳被吸收,可以缓解温室效应,A正确。
B、转化①为:,B错误。
C、转化②中一变多,发生分解反应,C正确。
D、由流程图可知,每用一定量CO2制取C,须向体系中再添加一定量FeO,D正确。
故选:B。
9.D
【详解】
A、由图可知,每个甲分子由1个硅原子、4个氯原子构成,故甲的化学式为SiCl4,不符合题意;
B、根据质量守恒定律,化学反应前后,原子的种类和数目不变,不符合题意;
C、根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Si、Cl、H的个数分别是1、4、4,生成物中含Si、Cl、H的个数分别是1、0、0,故生成物中还应含4个H、4个Cl,故X的化学式为HCl,不符合题意;
D、由图可知,化学反应前后,分子的个数发生了改变,符合题意。
故选D。
10.B
【分析】
由反应的微观示意图可知,一氧化碳和氢气在一定条件下反应生成甲烷和水,反应的化学方程式为CO+3H2CH4+H2O;
【详解】
A、由质量守恒定律可知,化学反应前后原子的种类与数目不变,选项说法错误;
B、由分子结构模型可知,图中的单质是氢气,其化学式为H2,选项说法正确;
C、由微观反应示意图可知,反应前后分子种类发生了改变,选项说法错误;
D、由图示可知,该反应的反应物是一氧化碳和氢气,生成物是甲烷和水,反应的化学方程式为CO+3H2CH4+H2O,选项说法错误。
故选B。
11.B
【详解】
A、根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,因此该反应后4X的原子为8个氢原子、4个氧原子,所以X中有2个氢原子和一个氧原子,故X的化学式为,说法错误;
B、根据一种物质生成二种或二种以上物质的反应是分解反应,因此该反应属于分解反应,根据质量守恒定律,反应前后元素种类没有发生变化,说法正确;
C、高氯酸铵是由铵根离子和高氯酸根离子构成的,不含氯离子和氧离子,说法错误;
D、反应前后物质状态由固态变为气态和液态物质,但反应前后氢元素化合价没有改变,都是+1价,说法错误。
故选:B。
12.B
【分析】
从反应的微观示意图可推出此反应的表达式为3I+Ⅱ→2Ⅲ,三种物质的分子个数比为I:Ⅱ:Ⅲ=3:1:2,据此分析即可。
【详解】
A、根据微观示意图可知,该反应的反应物是两种,生成物是一种,属于化合反应,故A说法正确;
B、该反应中原子种类、数目、质量不变,元素种类、质量也不变,但两种元素的化合价都由单质的0价变成化合物中元素的化合价,因此都发生了改变,故B说法错误;
C、该反应中反应物是由同种原子构成的分子,属于单质,生成物是两种原子构成的分子,属于化合物,故C说法正确;
D、根据微观示意图可知,3I+Ⅱ→2Ⅲ,三种物质的分子个数比为I:Ⅱ:Ⅲ=3:1:2,因此每3n个物质I分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子,故D说法正确。
故选B。
【点睛】
本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答此类题的关键。
13.
动植物呼吸(炼钢、化工、航天、医疗急救等其他合理答案都给分)
防止燃烧时生成的熔融物溅落使瓶底炸裂
A、C(或A、E)
b
【详解】
(1)氧原子(核电荷数为8)核外电子数为8,分两层排布,第一层为2个电子,第二层为剩下的六个电子,其结构示意图为
;
(2)氧气的用途:动植物呼吸(炼钢、化工、航天、医疗急救等);
(3)实验室做铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是防止燃烧时生成的熔融物溅落使瓶底炸裂。
(4)①实验室加热氯酸钾和二氧化锰的混合物制取氧气,发生装置为固固加热型装置,收集装置可选用向上排空气法收集即装置C,或排水法收集即装置E,应选用一套装置组合是A、C(或A、E),反应的化学方程式为;
②B为固液反应型发生装置,用B作气体发生装置制氧气,反应药剂为过氧化氢溶液和二氧化锰(作催化剂)反应的化学方程式为;
③欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从短管进入,因为氧气的密度比水小;故答案为:b。
14.b
CO2
Ca(NO3)2+K2CO3=CaCO3↓+2KNO3
漏斗
硝酸钾的溶解度随着温度降低而显著减小,氯化钠溶解度受温度影响不大
NO
【详解】
(1)a.“黑火药”中不含有“黑火药分子”,该选项说法不正确;
b.“黑火药”中的KNO3属于复合肥料,是因为其中含有两种营养元素,即氮元素和钾元素,该选项说法正确
c.黑火药”中的C、S能够保持各自的化学性质,该选项说法不正确。故填:b。
(2)由质量守恒定律可知,反应前后硫原子都是1个,钾原子都是2个,氮原子都是2个,
反应前氧原子是6个,反应后应该是6个,包含在未知物质中,反应前碳原子是3个,反应后应该是3个,包含在未知物质中,因此依据质量守恒定律,空格上缺少的物质是
CO2
(3)①“反应”过程中,硝酸钙和碳酸钾反应生成碳酸钙沉淀和硝酸钾,反应的化学方程式为:Ca(NO3)2+K2CO3=CaCO3↓+2KNO3
②2“过滤”操作必须用到的玻璃仪器有烧杯玻璃棒和漏斗。
③其中“冷却到一定温度”能获得纯度较高的硝酸钾晶体的原因是KNO3的溶解度随着温度的降低而显著减小,氯化钠量少且溶解度受温度影响不大,难以析出晶体。
(4)该氧化物中氮为+2价,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,其化学式为NO。
15.
(1)6:1:8
(2)
(3)171
【分析】
(1)
乳酸中碳、氢、氧的质量比为(12×3):(1×6):(16×3)=6:1:8。
(2)
乳酸与吸入的氧气反应生成二氧化碳和水,乳酸与氧气反应的化学方程式。
(3)
设180g乳酸中碳元素与质量为x的蔗糖(C12H22O11)中碳元素的质量相等,则,解得x=171g。
16.A
汞
化学
B
铜粉量过少造成氧气未消耗完等
2
【详解】
(1)拉瓦锡用装置A定量研究了空气的成分,在密闭容器中,空气中的氧气与汞反应,生成固态物质氧化汞。用铜粉、红磷等进行实验,铜与氧气在加热条件下生成氧化铜,红磷与氧气在点燃条件下生成五氧化二磷,以上实验的原理都生成了新物质,是采用化学方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)实验过程中,需要不断推拉注射器活塞的装置是B,通过不断推拉注射器活塞保证氧气完全消耗;D装置有弹簧夹,红磷燃烧的过程中关闭弹簧夹,不需要不断推拉注射器活塞。利用B装置进行实验,可能造成实验误差的因素是铜粉量过少造成氧气未消耗完等。铜和氧气加热生成氧化铜,。
(3)装置C、D的实验都用到了红磷,红磷与氧气在点燃条件下生成五氧化二磷,反应的化学方程式为;氧气约占空气总体积的五分之一,40
mL的空气中氧气的体积是,反应结束后,待装置冷却至室温,打开弹簧夹,装置D中注射器活塞从10
mL刻度处缓慢移动至10mL-8mL=2mL刻度处停止(误差忽略不计)。
一、单选题(共12题)
1.根据化学方程式不能获得该反应的信息是(
)
A.反应物和生成物
B.反应中各物质间粒子个数比
C.化学反应的快慢
D.反应的条件
2.过氧化钠(Na2O2)是淡黄色粉末,常用于呼吸面具和潜水艇中,反应方程式:2Na2O2
+
2X
=
2Na2CO3+O2,则X
的化学式为(?
)
A.CO
B.NaHCO3
C.CO2
D.C
3.对于化学反应:4P+5O22P2O5,下列说法正确的是( )
①反应前后原子的种类和数目不变②反应前后分子总数不变③反应前后元素的种类和质量不变④反应前后元素的化合价不变.⑤反应前后物质的总质量不变⑥每4份质量的磷和5份质量氧气在点燃的条件下恰好完全反应生成2份质量的五氧化二磷
A.①③⑤
B.①③⑤⑥
C.①③④⑤
D.①②③⑤⑥
4.《本草纲目》记载:“雄黄,乃治疮杀毒要药也……”,雄黄主要成分为As4S4,在空气中加热到一定温度可以被氧化成剧毒物质三氧化二砷,其反应的化学方程式为:。则X的化学式为(
)
A.S
B.O2
C.SO2
D.SO3
5.下列化学方程式与事实相符且书写正确的是(
)
A.利用红磷测定空气中氧气含量:4P+5O22P2O5
B.实验室用过氧化氢溶液制氧气
2H2O2=2H2O+O2↑
C.铁在氧气中燃烧:4Fe
+3O22Fe2O3
D.用高锰酸钾制取氧气:2KMnO4K2MnO2+MnO2+
O2↑
6.超氧化钾(KO2)常备于急救器和消防队员背包中,能迅速与水反应放出氧气:,则X的化学式为(
)
A.H2O2
B.H2O
C.H2
D.CO2
7.容器内有甲、乙、丙、丁四种物质,一定条件下发生了化学反应,各物质的质量变化如图所示。下列说法正确的是(
)
A.X=0
B.丙可能为该反应的催化剂
C.乙、丁两物质变化的质量比为2:3
D.甲和丁的相对分子质量之比为1:2
8.由CO2制取C的太阳能工艺流程如图,利用铁的氧化物作催化剂,可提高效益。下列关于该原理说法错误的是(
)
A.该流程可以缓解温室效应
B.转化①为:
C.转化②中发生分解反应
D.每用一定量CO2制取C,须向体系中再添加一定量FeO
9.从陶瓷、玻璃、水泥到集成电路芯片,硅的用途非常广泛。工业制取高纯硅的部分反应原理的微观示意图如下图,有关判断错误的是(
)
A.甲的化学式是SiCl4
B.反应前后原子个数不变
C.X的化学式是HCl
D.反应前后分子个数不变
10.工业上将一氧化碳转化为甲烷的微观示意图如图所示。下列说法正确的是(
)
A.反应前后原子总数减少
B.图中单质的化学式为H2
C.反应前后分子种类不变
D.该反应的化学方程式为
11.神舟十二号载人飞船成功发射又一次振奋了国人的心。在航天飞船中常用铝粉与高氯酸铵(NH4ClO4)的混合物为固体然料。发射时,点燃的铝粉产生大量的热引发高氯酸铵发生下列反应:。有关该反应的说法正确的是(
)
A.X的化学式为H2
B.该反应属于分解反应,反应前后元素种类没有发生变化
C.高氯酸铵由、C1-、O2-构成
D.反应前后物质状态及所有元素的化合价都发生了变化
12.某化学反应的微观示意图如图。下列说法不正确的是(
)
A.该反应属于化合反应;
B.该反应中原子种类、数目、质量不变,元素种类、质量、化合价不变
C.该反应中反应物是单质,生成物是化合物
D.该反应中每3n个物质Ⅰ分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子
二、综合题(共4题)
13.氧气是生命活动的重要物质,在生活和生产中具有广泛应用。
(1)请画出氧原子(核电荷数为8)的结构示意图_____。
(2)请列举氧气的一种用途_____。
(3)实验室做铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是什么?_____。
(4)下图所示为实验室中常见的气体制备和收集装置。
①实验室加热氯酸钾和二氧化锰的混合物制取氧气,应选用一套装置组合是_____(填字母序号),反应的化学方程式为_____。
②用B作气体发生装置制氧气,反应的化学方程式为_____。
③欲使用如图装置用排水法收集氧气,先将瓶中装满水,再将氧气从_____(填“a”或“b”)端通入。
14.中国古代四大发明之一的“黑火药”是由木炭(C)、硫粉(S)和硝酸钾(KNO3)按一定比例混合而成。
(1)分类。下列关于“黑火药”说法正确的是____。
a.“黑火药”由“黑火药分子”构成
b.“黑火药”中的KNO3属于复合肥料
c.“黑火药”中的C、S不再保持各自的化学性质
(2)变化。“黑火药”爆炸时发生的主要反应是:S+2KNO3+3C=K2S+N2↑+3____↑。
(3)制备。古代曾用硝土(含有Ca(NO3)2、少量NaCl等)和草木灰(含有K2CO3)作原料
制取KNO3.某化学兴趣小组设计了如图实验流程:
①“反应”过程中的化学方程式为_______。
②“过滤”操作必须用到的玻璃仪器有烧杯、玻璃棒和_____。
③如图是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括“加热蒸发浓缩、再冷却到一定温度、过滤”等步骤。其中“冷却到一定温度”能获得纯度较高的硝酸钾晶体的原因是___。
(4)发展。现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C3H5O9N3)。硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。该氧化物中氮为+2价,其化学式为____。
15.2019长江三峡国际马拉松于12月1日在忠州鸣枪开赛,万余名跑友齐聚忠州跑完赛程。人剧烈运动后,血液中会产生较多的乳酸(C3H6O3),使肌肉酸痛。放松一段时间后,乳酸与吸入的氧气反应生成二氧化碳和水,肌肉酸痛感消失。
(1)乳酸中碳、氢、氧的质量比为______。
(2)写出乳酸与氧气反应的化学方程式______。
(3)180g乳酸中碳元素与______g蔗糖(C12H22O11)中碳元素的质量相等。
16.以下四个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
(1)拉瓦锡用装置______(填写字母)定量研究了空气的成分,在密闭容器中,空气中的氧气与______反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用______(填“物理”或“化学”)方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)实验过程中,需要不断推拉注射器活塞的装置是______(填写字母),利用此装置进行实验,可能造成实验误差的因素是______(答一条)。写出
B
装置涉及的化学反应方程式______
(3)装置
C、D
的实验都用到了红磷,写出反应的化学方程式______;
反应结束后,待装置冷却至室温,打开弹簧夹,装置
D
中(试管容积为
40
mL),注射器活塞从
10
mL
刻度处缓慢移动至______mL
刻度处停止(误差忽略不计)。
参考答案
1.C
【详解】
A、由化学方程式,可以确定“═”左边的是反应物,右边为生成物,故选项错误。
B、由化学方程式,根据化学式前的化学计量数可以确定反应中各物质间粒子个数比,故选项错误。
C、由化学方程式,无法确定化学反应的快慢,故选项正确。
D、由化学方程式,可以看出反应发生所需要的条件,故选项错误。
故选:C。
2.C
【详解】
根据质量守恒定律,反应前后原子的种类和数目不变,该方程式反应前后有4个钠原子,反应前有4个氧原子,反应后有8个氧原子,2个碳原子,故一个X分子中包含1个碳原子和2个氧原子,故X的化学式为CO2。
故选C。
3.A
【详解】
①由方程式可知,反应前后原子的种类和数目不变,选项正确;
②由方程式可知,每4个磷原子和5个氧分子在点燃条件下生成2个五氧化二磷分子,反应前后分子总数改变,选项错误;
③元素是具有相同质子数的同一类原子的总称,反应前后原子的种类和数目不变,可知反应前后元素的种类和质量不变,选项正确;
④单质中元素的化合价为零,化合物中元素的化合价代数和为零,反应前氧元素、磷元素的化合价都是0.反应后磷元素为+5价,氧元素为-2价,反应前后元素的化合价改变,选项错误;
⑤参加反应的各物质的质量总和等于反应后生成的各物质的质量总和,反应前后物质的总质量不变,选项正确;
⑥由方程式可知,每124份质量的磷和160份质量氧气在点燃的条件下恰好完全反应生成284份质量的五氧化二磷,选项错误。
故选A。
4.C
【详解】
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含As、O、S的个数分别是4、14、4,生成物中含As、O、S的个数分别是4、6、0,故生成物中还应含4个S、8个O,故X的化学式为:SO2。
故选C。
5.A
【详解】
A、红磷燃烧生产五氧化二磷,因只消耗空气中的氧气,生成物为固体可用于测定空气中氧气含量。化学方程式书写正确。正确。
B、实验室用过氧化氢溶液制氧气需要二氧化锰作催化剂。化学方程式应为:2H2O22H2O+O2↑。错误。
C、铁在氧气中燃烧生成四氧化三铁,化学方程式为3Fe
+2O2Fe3O4。错误。
D、高锰酸钾制取氧气化学方程式为2KMnO4K2MnO4+MnO2+
O2↑。锰酸钾化学式为K2MnO4。错误。
故选A。
6.A
【详解】
化学反应前后原子种类数目不变;反应物中钾原子、氧原子、氢原子的个数分别是2、6、4,生成物中钾原子、氧原子、氢原子的个数分别是2、4、2,故X中含有2个氢原子和2个氧原子,化学式为H2O2。
故选A。
7.B
【详解】
A、由质量守恒定律可知,反应后丙的质量=4g+10g+3g+4g?6g?4g?8g=3g,即X的值为3,选项错误;
B、由图和A可知,反应前后,物质丙的质量不变,则丙可能为该反应的催化剂,选项正确;
C、反应后乙减少的质量=10g?4g=6g,丁增加的质量=8g?4g=4g,则乙、丁两物质变化的质量比=6g:4g=3:2,选项错误;
D、反应后甲增加的质量=6g?4g=2g,丁增加的质量=8g?4g=4g,则甲、丁两物质变化的质量比=2g:4g=1:2,化学反应中,物质的质量比等于物质的相对分子质量与化学就计量数的乘积之比,题目中没有明确反应中甲和乙的化学计量数的关系,所以无法判断甲、乙的相对分子质量的关系,选项错误,故选B。
8.B
【详解】
A、由图可知,流程中二氧化碳被吸收,可以缓解温室效应,A正确。
B、转化①为:,B错误。
C、转化②中一变多,发生分解反应,C正确。
D、由流程图可知,每用一定量CO2制取C,须向体系中再添加一定量FeO,D正确。
故选:B。
9.D
【详解】
A、由图可知,每个甲分子由1个硅原子、4个氯原子构成,故甲的化学式为SiCl4,不符合题意;
B、根据质量守恒定律,化学反应前后,原子的种类和数目不变,不符合题意;
C、根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Si、Cl、H的个数分别是1、4、4,生成物中含Si、Cl、H的个数分别是1、0、0,故生成物中还应含4个H、4个Cl,故X的化学式为HCl,不符合题意;
D、由图可知,化学反应前后,分子的个数发生了改变,符合题意。
故选D。
10.B
【分析】
由反应的微观示意图可知,一氧化碳和氢气在一定条件下反应生成甲烷和水,反应的化学方程式为CO+3H2CH4+H2O;
【详解】
A、由质量守恒定律可知,化学反应前后原子的种类与数目不变,选项说法错误;
B、由分子结构模型可知,图中的单质是氢气,其化学式为H2,选项说法正确;
C、由微观反应示意图可知,反应前后分子种类发生了改变,选项说法错误;
D、由图示可知,该反应的反应物是一氧化碳和氢气,生成物是甲烷和水,反应的化学方程式为CO+3H2CH4+H2O,选项说法错误。
故选B。
11.B
【详解】
A、根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,因此该反应后4X的原子为8个氢原子、4个氧原子,所以X中有2个氢原子和一个氧原子,故X的化学式为,说法错误;
B、根据一种物质生成二种或二种以上物质的反应是分解反应,因此该反应属于分解反应,根据质量守恒定律,反应前后元素种类没有发生变化,说法正确;
C、高氯酸铵是由铵根离子和高氯酸根离子构成的,不含氯离子和氧离子,说法错误;
D、反应前后物质状态由固态变为气态和液态物质,但反应前后氢元素化合价没有改变,都是+1价,说法错误。
故选:B。
12.B
【分析】
从反应的微观示意图可推出此反应的表达式为3I+Ⅱ→2Ⅲ,三种物质的分子个数比为I:Ⅱ:Ⅲ=3:1:2,据此分析即可。
【详解】
A、根据微观示意图可知,该反应的反应物是两种,生成物是一种,属于化合反应,故A说法正确;
B、该反应中原子种类、数目、质量不变,元素种类、质量也不变,但两种元素的化合价都由单质的0价变成化合物中元素的化合价,因此都发生了改变,故B说法错误;
C、该反应中反应物是由同种原子构成的分子,属于单质,生成物是两种原子构成的分子,属于化合物,故C说法正确;
D、根据微观示意图可知,3I+Ⅱ→2Ⅲ,三种物质的分子个数比为I:Ⅱ:Ⅲ=3:1:2,因此每3n个物质I分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子,故D说法正确。
故选B。
【点睛】
本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答此类题的关键。
13.
动植物呼吸(炼钢、化工、航天、医疗急救等其他合理答案都给分)
防止燃烧时生成的熔融物溅落使瓶底炸裂
A、C(或A、E)
b
【详解】
(1)氧原子(核电荷数为8)核外电子数为8,分两层排布,第一层为2个电子,第二层为剩下的六个电子,其结构示意图为
;
(2)氧气的用途:动植物呼吸(炼钢、化工、航天、医疗急救等);
(3)实验室做铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是防止燃烧时生成的熔融物溅落使瓶底炸裂。
(4)①实验室加热氯酸钾和二氧化锰的混合物制取氧气,发生装置为固固加热型装置,收集装置可选用向上排空气法收集即装置C,或排水法收集即装置E,应选用一套装置组合是A、C(或A、E),反应的化学方程式为;
②B为固液反应型发生装置,用B作气体发生装置制氧气,反应药剂为过氧化氢溶液和二氧化锰(作催化剂)反应的化学方程式为;
③欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从短管进入,因为氧气的密度比水小;故答案为:b。
14.b
CO2
Ca(NO3)2+K2CO3=CaCO3↓+2KNO3
漏斗
硝酸钾的溶解度随着温度降低而显著减小,氯化钠溶解度受温度影响不大
NO
【详解】
(1)a.“黑火药”中不含有“黑火药分子”,该选项说法不正确;
b.“黑火药”中的KNO3属于复合肥料,是因为其中含有两种营养元素,即氮元素和钾元素,该选项说法正确
c.黑火药”中的C、S能够保持各自的化学性质,该选项说法不正确。故填:b。
(2)由质量守恒定律可知,反应前后硫原子都是1个,钾原子都是2个,氮原子都是2个,
反应前氧原子是6个,反应后应该是6个,包含在未知物质中,反应前碳原子是3个,反应后应该是3个,包含在未知物质中,因此依据质量守恒定律,空格上缺少的物质是
CO2
(3)①“反应”过程中,硝酸钙和碳酸钾反应生成碳酸钙沉淀和硝酸钾,反应的化学方程式为:Ca(NO3)2+K2CO3=CaCO3↓+2KNO3
②2“过滤”操作必须用到的玻璃仪器有烧杯玻璃棒和漏斗。
③其中“冷却到一定温度”能获得纯度较高的硝酸钾晶体的原因是KNO3的溶解度随着温度的降低而显著减小,氯化钠量少且溶解度受温度影响不大,难以析出晶体。
(4)该氧化物中氮为+2价,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,其化学式为NO。
15.
(1)6:1:8
(2)
(3)171
【分析】
(1)
乳酸中碳、氢、氧的质量比为(12×3):(1×6):(16×3)=6:1:8。
(2)
乳酸与吸入的氧气反应生成二氧化碳和水,乳酸与氧气反应的化学方程式。
(3)
设180g乳酸中碳元素与质量为x的蔗糖(C12H22O11)中碳元素的质量相等,则,解得x=171g。
16.A
汞
化学
B
铜粉量过少造成氧气未消耗完等
2
【详解】
(1)拉瓦锡用装置A定量研究了空气的成分,在密闭容器中,空气中的氧气与汞反应,生成固态物质氧化汞。用铜粉、红磷等进行实验,铜与氧气在加热条件下生成氧化铜,红磷与氧气在点燃条件下生成五氧化二磷,以上实验的原理都生成了新物质,是采用化学方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)实验过程中,需要不断推拉注射器活塞的装置是B,通过不断推拉注射器活塞保证氧气完全消耗;D装置有弹簧夹,红磷燃烧的过程中关闭弹簧夹,不需要不断推拉注射器活塞。利用B装置进行实验,可能造成实验误差的因素是铜粉量过少造成氧气未消耗完等。铜和氧气加热生成氧化铜,。
(3)装置C、D的实验都用到了红磷,红磷与氧气在点燃条件下生成五氧化二磷,反应的化学方程式为;氧气约占空气总体积的五分之一,40
mL的空气中氧气的体积是,反应结束后,待装置冷却至室温,打开弹簧夹,装置D中注射器活塞从10
mL刻度处缓慢移动至10mL-8mL=2mL刻度处停止(误差忽略不计)。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
