2.2.2 金属的化学性质 同步练习——溶液成分分析(含答案)
文档属性
| 名称 | 2.2.2 金属的化学性质 同步练习——溶液成分分析(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 302.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-10-03 00:00:00 | ||
图片预览


文档简介
2.2.2金属的化学性质——活动性验证
第1课时
比较金属的活动性
1.探究铁、铜、银的金属活泼性
①在盛有硫酸铜溶液的试管里浸入一段洁净的(经过除油、除锈)铁丝,过一会儿取出,发现铁丝的表面覆盖一层红色物质:Fe
+
CuSO4
=
FeSO4
+
Cu
②在盛有硫酸亚铁溶液的试管中,浸入一段洁净的铜丝,过一会儿取出,发现没有明显的现象:Cu+
FeSO4
-不反应
结论:金属活动性:铁比铜活泼
Fe>Cu
③在盛有硝酸银溶液的试管里浸入一段洁净的(经过除油、除锈)铜丝,过一会儿取出,观察到铜丝的表面覆盖一层银白色物质:Cu
+
2AgNO3
=
Cu(NO3)2
+
2Ag
④在盛有硝酸铜的试管中,浸入一段洁净的银丝,过一会儿取出,发现没有明显的现象:Ag
+
Cu(NO3)2
-
不反应
结论:铜、银的金属活动性比较:铜比银活泼
Cu>Ag
综合:铁比铜活泼,铜比银活泼。即Fe
>
Cu>Ag
拓展结论:活动性较强的金属能把另一种活动较弱的金属从它的盐的水溶液中置换出来。
但是K、Ca、Na三种金属的活动性太强,在与盐溶液反应时,会先与溶液中的水发生反应,生成对应的碱和氢气,碱再与盐发生复分解反应。如将钠金属放入硫酸铜溶液中
置换反应的应用
除去杂质FeCl2溶液中含有的少量CuCl2。
向溶液中加入足量的铁粉,充分反应后过滤。
Fe
+
CuCl2
=
Cu
+
FeCl2
1.现有X、Y、Z三种金属,如果把X、Y和Z分别投入到稀盐酸中,只有Y溶解并产生气泡,X、Z不反应;如果把X和Z分别放入硝酸银溶液中,过一会儿,在X表面有银析出,而Z没有变化,则X、Y、Z的金属活动性顺序为(
)
A.Y>X>Z
B.X>Y>Z
C.Z>Y>X
D.X>Z>Y
2.探究Mg、Fe、Cu三种金属的活动性顺序,下列试剂的选择方案不可行的是(
)
A.Mg、Cu、FeSO4溶液
B.Mg、Fe、Cu、稀硫酸
C.Fe、Cu、MgSO4溶液
D.Fe、MgSO4溶液、CuSO4溶液
3.把铁片分别放入下列各物质的溶液中,片刻后取出,溶液的质量增加的是
(
)
A.硫酸铝
B.硫酸铜
C.硫酸
D.硝酸银
4.可用金属活动性解释下列现象和事实的是(??
)
①镁和铝与稀盐酸反应的剧烈程度不同;
②不能用铜与稀硫酸反应制取氢气;
③用硫酸铜、石灰乳配置农药波尔多液时,不能用铁制容器;
④
铜能和浓硫酸反应。
A
.①③
B
.①②③
C
.①③④
D
.①②③④
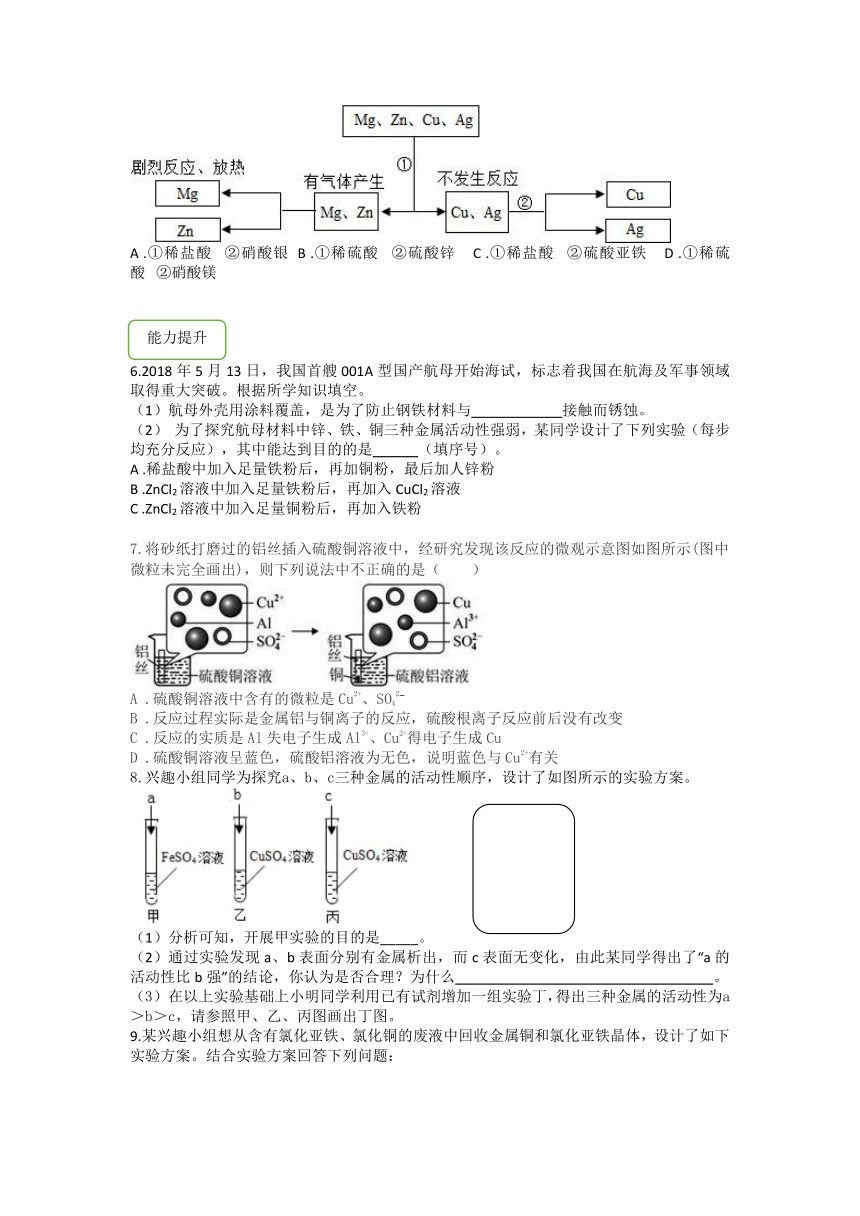
5.?(2021·金华模拟)?小明为探究镁、锌、铜、银的活动性顺序,设计如下实验流程,依据该流程设计,下面对物质①、②的选择合理的是(?
)
A
.①稀盐酸?
②硝酸银
B
.①稀硫酸?
②硫酸锌
C
.①稀盐酸?
②硫酸亚铁
D
.①稀硫酸?
②硝酸镁
6.2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)航母外壳用涂料覆盖,是为了防止钢铁材料与
接触而锈蚀。
(2)
为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是
(填序号)。
A
.稀盐酸中加入足量铁粉后,再加铜粉,最后加人锌粉
B
.ZnCl2?溶液中加入足量铁粉后,再加入CuCl2溶液
C
.ZnCl2溶液中加入足量铜粉后,再加入铁粉
7.将砂纸打磨过的铝丝插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示(图中微粒未完全画出),则下列说法中不正确的是(??)
A
.硫酸铜溶液中含有的微粒是Cu2+、SO42?
B
.反应过程实际是金属铝与铜离子的反应,硫酸根离子反应前后没有改变
C
.反应的实质是Al失电子生成Al3+、Cu2+得电子生成Cu
D
.硫酸铜溶液呈蓝色,硫酸铝溶液为无色,说明蓝色与Cu2+有关
8.兴趣小组同学为探究a、b、c三种金属的活动性顺序,设计了如图所示的实验方案。
分析可知,开展甲实验的目的是_____。
通过实验发现a、b表面分别有金属析出,而c表面无变化,由此某同学得出了“a的活动性比b强”的结论,你认为是否合理?为什么
。
在以上实验基础上小明同学利用已有试剂增加一组实验丁,得出三种金属的活动性为a>b>c,请参照甲、乙、丙图画出丁图。
9.某兴趣小组想从含有氯化亚铁、氯化铜的废液中回收金属铜和氯化亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
(1)
操作Ⅲ的名称是
,除去的物质是
(填化学式)。
(2)
操作Ⅱ中加入过来的试剂B的目的是
。
(3)
写出加入过量试剂A发生反应的化学方程式
。
第2课时
置换反应后溶液和固体成分分析
(1)金属与混合盐溶液的反应
【举例】将一定量的铁粉加入到硝酸铜和硝酸银的混合溶液中
先:Fe+2AgNO3===
Fe(NO3)2+2Ag
后:Fe+Cu(NO3)2===
Fe(NO3)2+Cu
反应后滤液、滤渣的成分分析
序号
加入铁粉的量
滤液成分
滤渣成分
①
少量
Fe(NO3)2、AgNO3、Cu(NO3)2
Ag
②
恰好与AgNO3完全反应
Fe(NO3)2、Cu(NO3)2
Ag
③
与Cu(NO3)2反应,没反应完
Fe(NO3)2、Cu(NO3)2
Ag、Cu
④
恰好与Cu(NO3)2完全反应
Fe(NO3)2
Ag、Cu
⑤
过量
Fe(NO3)2
Ag、Cu、Fe
(2)金属混合物与盐溶液的反应
【举例】将硝酸银溶液加入到铁和铜的混合物中
先:Fe+2AgNO3===
Fe(NO3)2+2Ag
后:Cu+2AgNO3===
Cu(NO3)2+2Ag
反应后滤液、滤渣的成分分析
序号
加入硝酸银溶液的量
滤液成分
滤渣成分
①
少量
Fe(NO3)2
Ag、Cu、Fe
②
恰好与Fe完全反应
Fe(NO3)2
Ag、Cu
③
与Cu
反应,没反应完
Fe(NO3)2、Cu(NO3)2
Ag、Cu
④
恰好与Cu
完全反应
Fe(NO3)2、Cu(NO3)2
Ag
⑤
过量
Fe(NO3)2、Cu(NO3)2、AgNO3
Ag
1.将一定量的铁粉加入到含有Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是( )
A.
滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2
B.
滤渣中一定不含Fe,滤液中一定含有Fe(NO3)2和Cu(NO3)2
C.
滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3
D.
滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO3
2.将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,将所得滤渣放入稀盐酸中,有气泡产生。下列说法错误的是( )
A.
滤液中最多含有两种溶质
B.
滤液中一定含有Zn(NO3)2,可能含有Fe(NO3)2
C.
滤渣里一定含有Fe和Ag,可能含有Zn
D.
若反应后所得滤液呈无色,则滤渣中一定含有Fe和Ag,一定没有Zn
3.为了探究金属与盐溶液的反应规律,将一定质量的锌粉和银粉加入
Cu(NO3)2
溶液中,充分反应,实验过程及实验现象如下图所示,则下列判断中正确的是(
)
A.滤液中可能含有
Ag+
B.滤渣中可能含有单质锌
C.滤液中一定含有
Cu2+
D.滤渣中一定含有单质铜
4.将一定量的锌粒投入到含溶质为Al(NO3)3、Cu(NO3)2、AgNO3的溶液中,充分反应后过滤,往滤液中滴加稀盐酸,无明显现象,则下列说法正确的是(
)
A.滤液中溶质为Al(NO3)3、Zn(NO3)3时,滤渣一定为Cu、Ag
B.锌粒先跟Al(NO3)3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象
C.锌粒先跟Cu(NO3)2反应无剩余,因此往滤液中滴加稀盐酸,无明显现象
D.锌粒先跟AgNO3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象
5.(2021·越城模拟)?烧杯中盛有等质量的锌粉和铁粉,向其中不断加入氯化铜溶液,测得烧杯中剩余固体的质量与加入氯化铜溶液质量的关系如图所示。下列相关说法正确的是(
??)
A
.ab段发生的是铁与氯化铜的反应
B
.向b点所得固体中加人稀盐酸,无气泡产生
C
.c点所得溶液呈浅绿色
D
.d点所得溶液中的溶质有2种
6.(2021·绍兴)?向一定质量的Mg(NO3)2和Cu(NO3)2混合溶液中加入a克锌粉和铁粉的混合物,充分反应后过滤,得到不饱和的滤液和滤渣,将滤渣洗涤、干燥后再称量,得到的固体质量仍为a克。下列分析合理的是(???
)
①滤渣中可能有铜??
???②向滤渣中加稀盐酸,可能有气泡产生??
③滤液中一定有Mg(NO3)2、Zn(NO3)2和Fe(NO3)2,可能有Cu(NO3)2?
④若忽略过滤操作中溶液损失,滤液中溶质的质量一定大于原混合溶液溶质的质量
A
.①②
B
.①③
C
.②③
D
.②④
7.某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:
①溶液甲中一定含有Al(NO3)3和Zn(NO3)2
②固体乙中一定含有Ag,可能含有Cu和Zn
③若溶液甲中插入洁净的铁丝,铁丝表面附着有固体,则溶液甲中一定有Cu(NO3)2
④向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有
AgNO3和Cu(NO3)2
上述四种说法正确的个数为(
)
A.1个
B.2个
C.3个
D.4个
8.为探究锌、铜、铁三种金属的活动性顺序,某学习小组做了如甲图所示实验,实验结束后,将试管①、试管②内的物质全部倒入同一只烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如乙图所示),下列说法正确的是(
)
A.反应后烧杯中的固体一定含有铁
B.甲图试管②中反应后固体一定含铁
C.反应后烧杯中的溶液一定不含有氯化铜
D.烧杯中最后所得固体的总质量一定大于2ag
9.向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示。下列说法正确的是(
)
A.a点所得溶液中的溶质是硝酸铜、硝酸锌
B.向b点所得固体中加入盐酸有气泡产生
C.c点所得固体为银和铜
D.d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜
10.某溶液含有
Cu(NO3)2和
AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是(?
)
A
.Cu
的活动性比
Ag
强,只用盐酸无法探究两者活动性强弱
B
.当溶质种类为1种时,金属单质种类可能为2种
C
.c~d
间(不含两点)的溶液中金属离子为
Zn2+、Cu2+
D
.从
m1?变化到
m2?时,溶液中硝酸铜的质量分数不变
11.现有一包由2.4g镁、6.5g锌、1.6g碳混合而成的粉末,把它加入到一定量的硝酸银溶液中,反应结束后,经过滤、洗涤、干燥,测得滤渣含有三种物质。则滤渣的质量可能是( )
A.10.5g
B.35.6g
C.44.8g
D.45.8g
12.为探究金属活动性顺序,学习小组设计并进行实验I和I1.实验结束,将两实验的废液全部倒入一洁净烧杯中,
反应后得到溶液A和固体B.实验过程及现象如图所示:
据此得出以下结论:
①通过实验I和II能验证Al、Ag.
Cu的金属活动性顺序;
②实验反应后固体中一定含有Cu;
③若A是无色溶液,A中可能含有AgNO3;
④若A呈蓝色,溶液A中至少有两种溶质⑤若A呈蓝色,固体B中定不含Cu;其中正确结论的个数有(
)
A.
1个
B.
2个
C.
3个
D.
4个
13金属材料在生产、生活中有着广泛的应用,人类的生产和生活都离不开金属。
(1)金属活动性顺序有重要的应用。铝、铜、铁为日常生活中常见的金属,某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如图的实验:
将A实验结束后①②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,其原因是_________________,一段时间后过滤,滤液中的溶质一定有________(填化学式)。
(2)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,他对反应过程进行了分析,得到了以下几个图像(横坐标表示加入铁的质量),其中错误的是_____(填字母序号)。
2.2.2金属的化学性质答案
1.A
2.C
3.C
4.B
5.?A
6.(1)氧气和水(2)
AB
7.A
8.
9.(1)
蒸发
HCl(2)
去除过量的铁粉(3)
1.C
2.D
3.D
4.D
5.C
6.C
7.D
8.D
9.C
10.D
11.C
12.B
13.
D
知识点分布
基础巩固
能力提升
重点掌握
基础巩固
能力提升
重点掌握
第1课时
比较金属的活动性
1.探究铁、铜、银的金属活泼性
①在盛有硫酸铜溶液的试管里浸入一段洁净的(经过除油、除锈)铁丝,过一会儿取出,发现铁丝的表面覆盖一层红色物质:Fe
+
CuSO4
=
FeSO4
+
Cu
②在盛有硫酸亚铁溶液的试管中,浸入一段洁净的铜丝,过一会儿取出,发现没有明显的现象:Cu+
FeSO4
-不反应
结论:金属活动性:铁比铜活泼
Fe>Cu
③在盛有硝酸银溶液的试管里浸入一段洁净的(经过除油、除锈)铜丝,过一会儿取出,观察到铜丝的表面覆盖一层银白色物质:Cu
+
2AgNO3
=
Cu(NO3)2
+
2Ag
④在盛有硝酸铜的试管中,浸入一段洁净的银丝,过一会儿取出,发现没有明显的现象:Ag
+
Cu(NO3)2
-
不反应
结论:铜、银的金属活动性比较:铜比银活泼
Cu>Ag
综合:铁比铜活泼,铜比银活泼。即Fe
>
Cu>Ag
拓展结论:活动性较强的金属能把另一种活动较弱的金属从它的盐的水溶液中置换出来。
但是K、Ca、Na三种金属的活动性太强,在与盐溶液反应时,会先与溶液中的水发生反应,生成对应的碱和氢气,碱再与盐发生复分解反应。如将钠金属放入硫酸铜溶液中
置换反应的应用
除去杂质FeCl2溶液中含有的少量CuCl2。
向溶液中加入足量的铁粉,充分反应后过滤。
Fe
+
CuCl2
=
Cu
+
FeCl2
1.现有X、Y、Z三种金属,如果把X、Y和Z分别投入到稀盐酸中,只有Y溶解并产生气泡,X、Z不反应;如果把X和Z分别放入硝酸银溶液中,过一会儿,在X表面有银析出,而Z没有变化,则X、Y、Z的金属活动性顺序为(
)
A.Y>X>Z
B.X>Y>Z
C.Z>Y>X
D.X>Z>Y
2.探究Mg、Fe、Cu三种金属的活动性顺序,下列试剂的选择方案不可行的是(
)
A.Mg、Cu、FeSO4溶液
B.Mg、Fe、Cu、稀硫酸
C.Fe、Cu、MgSO4溶液
D.Fe、MgSO4溶液、CuSO4溶液
3.把铁片分别放入下列各物质的溶液中,片刻后取出,溶液的质量增加的是
(
)
A.硫酸铝
B.硫酸铜
C.硫酸
D.硝酸银
4.可用金属活动性解释下列现象和事实的是(??
)
①镁和铝与稀盐酸反应的剧烈程度不同;
②不能用铜与稀硫酸反应制取氢气;
③用硫酸铜、石灰乳配置农药波尔多液时,不能用铁制容器;
④
铜能和浓硫酸反应。
A
.①③
B
.①②③
C
.①③④
D
.①②③④
5.?(2021·金华模拟)?小明为探究镁、锌、铜、银的活动性顺序,设计如下实验流程,依据该流程设计,下面对物质①、②的选择合理的是(?
)
A
.①稀盐酸?
②硝酸银
B
.①稀硫酸?
②硫酸锌
C
.①稀盐酸?
②硫酸亚铁
D
.①稀硫酸?
②硝酸镁
6.2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)航母外壳用涂料覆盖,是为了防止钢铁材料与
接触而锈蚀。
(2)
为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是
(填序号)。
A
.稀盐酸中加入足量铁粉后,再加铜粉,最后加人锌粉
B
.ZnCl2?溶液中加入足量铁粉后,再加入CuCl2溶液
C
.ZnCl2溶液中加入足量铜粉后,再加入铁粉
7.将砂纸打磨过的铝丝插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示(图中微粒未完全画出),则下列说法中不正确的是(??)
A
.硫酸铜溶液中含有的微粒是Cu2+、SO42?
B
.反应过程实际是金属铝与铜离子的反应,硫酸根离子反应前后没有改变
C
.反应的实质是Al失电子生成Al3+、Cu2+得电子生成Cu
D
.硫酸铜溶液呈蓝色,硫酸铝溶液为无色,说明蓝色与Cu2+有关
8.兴趣小组同学为探究a、b、c三种金属的活动性顺序,设计了如图所示的实验方案。
分析可知,开展甲实验的目的是_____。
通过实验发现a、b表面分别有金属析出,而c表面无变化,由此某同学得出了“a的活动性比b强”的结论,你认为是否合理?为什么
。
在以上实验基础上小明同学利用已有试剂增加一组实验丁,得出三种金属的活动性为a>b>c,请参照甲、乙、丙图画出丁图。
9.某兴趣小组想从含有氯化亚铁、氯化铜的废液中回收金属铜和氯化亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
(1)
操作Ⅲ的名称是
,除去的物质是
(填化学式)。
(2)
操作Ⅱ中加入过来的试剂B的目的是
。
(3)
写出加入过量试剂A发生反应的化学方程式
。
第2课时
置换反应后溶液和固体成分分析
(1)金属与混合盐溶液的反应
【举例】将一定量的铁粉加入到硝酸铜和硝酸银的混合溶液中
先:Fe+2AgNO3===
Fe(NO3)2+2Ag
后:Fe+Cu(NO3)2===
Fe(NO3)2+Cu
反应后滤液、滤渣的成分分析
序号
加入铁粉的量
滤液成分
滤渣成分
①
少量
Fe(NO3)2、AgNO3、Cu(NO3)2
Ag
②
恰好与AgNO3完全反应
Fe(NO3)2、Cu(NO3)2
Ag
③
与Cu(NO3)2反应,没反应完
Fe(NO3)2、Cu(NO3)2
Ag、Cu
④
恰好与Cu(NO3)2完全反应
Fe(NO3)2
Ag、Cu
⑤
过量
Fe(NO3)2
Ag、Cu、Fe
(2)金属混合物与盐溶液的反应
【举例】将硝酸银溶液加入到铁和铜的混合物中
先:Fe+2AgNO3===
Fe(NO3)2+2Ag
后:Cu+2AgNO3===
Cu(NO3)2+2Ag
反应后滤液、滤渣的成分分析
序号
加入硝酸银溶液的量
滤液成分
滤渣成分
①
少量
Fe(NO3)2
Ag、Cu、Fe
②
恰好与Fe完全反应
Fe(NO3)2
Ag、Cu
③
与Cu
反应,没反应完
Fe(NO3)2、Cu(NO3)2
Ag、Cu
④
恰好与Cu
完全反应
Fe(NO3)2、Cu(NO3)2
Ag
⑤
过量
Fe(NO3)2、Cu(NO3)2、AgNO3
Ag
1.将一定量的铁粉加入到含有Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是( )
A.
滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2
B.
滤渣中一定不含Fe,滤液中一定含有Fe(NO3)2和Cu(NO3)2
C.
滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3
D.
滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO3
2.将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,将所得滤渣放入稀盐酸中,有气泡产生。下列说法错误的是( )
A.
滤液中最多含有两种溶质
B.
滤液中一定含有Zn(NO3)2,可能含有Fe(NO3)2
C.
滤渣里一定含有Fe和Ag,可能含有Zn
D.
若反应后所得滤液呈无色,则滤渣中一定含有Fe和Ag,一定没有Zn
3.为了探究金属与盐溶液的反应规律,将一定质量的锌粉和银粉加入
Cu(NO3)2
溶液中,充分反应,实验过程及实验现象如下图所示,则下列判断中正确的是(
)
A.滤液中可能含有
Ag+
B.滤渣中可能含有单质锌
C.滤液中一定含有
Cu2+
D.滤渣中一定含有单质铜
4.将一定量的锌粒投入到含溶质为Al(NO3)3、Cu(NO3)2、AgNO3的溶液中,充分反应后过滤,往滤液中滴加稀盐酸,无明显现象,则下列说法正确的是(
)
A.滤液中溶质为Al(NO3)3、Zn(NO3)3时,滤渣一定为Cu、Ag
B.锌粒先跟Al(NO3)3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象
C.锌粒先跟Cu(NO3)2反应无剩余,因此往滤液中滴加稀盐酸,无明显现象
D.锌粒先跟AgNO3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象
5.(2021·越城模拟)?烧杯中盛有等质量的锌粉和铁粉,向其中不断加入氯化铜溶液,测得烧杯中剩余固体的质量与加入氯化铜溶液质量的关系如图所示。下列相关说法正确的是(
??)
A
.ab段发生的是铁与氯化铜的反应
B
.向b点所得固体中加人稀盐酸,无气泡产生
C
.c点所得溶液呈浅绿色
D
.d点所得溶液中的溶质有2种
6.(2021·绍兴)?向一定质量的Mg(NO3)2和Cu(NO3)2混合溶液中加入a克锌粉和铁粉的混合物,充分反应后过滤,得到不饱和的滤液和滤渣,将滤渣洗涤、干燥后再称量,得到的固体质量仍为a克。下列分析合理的是(???
)
①滤渣中可能有铜??
???②向滤渣中加稀盐酸,可能有气泡产生??
③滤液中一定有Mg(NO3)2、Zn(NO3)2和Fe(NO3)2,可能有Cu(NO3)2?
④若忽略过滤操作中溶液损失,滤液中溶质的质量一定大于原混合溶液溶质的质量
A
.①②
B
.①③
C
.②③
D
.②④
7.某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:
①溶液甲中一定含有Al(NO3)3和Zn(NO3)2
②固体乙中一定含有Ag,可能含有Cu和Zn
③若溶液甲中插入洁净的铁丝,铁丝表面附着有固体,则溶液甲中一定有Cu(NO3)2
④向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有
AgNO3和Cu(NO3)2
上述四种说法正确的个数为(
)
A.1个
B.2个
C.3个
D.4个
8.为探究锌、铜、铁三种金属的活动性顺序,某学习小组做了如甲图所示实验,实验结束后,将试管①、试管②内的物质全部倒入同一只烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如乙图所示),下列说法正确的是(
)
A.反应后烧杯中的固体一定含有铁
B.甲图试管②中反应后固体一定含铁
C.反应后烧杯中的溶液一定不含有氯化铜
D.烧杯中最后所得固体的总质量一定大于2ag
9.向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示。下列说法正确的是(
)
A.a点所得溶液中的溶质是硝酸铜、硝酸锌
B.向b点所得固体中加入盐酸有气泡产生
C.c点所得固体为银和铜
D.d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜
10.某溶液含有
Cu(NO3)2和
AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是(?
)
A
.Cu
的活动性比
Ag
强,只用盐酸无法探究两者活动性强弱
B
.当溶质种类为1种时,金属单质种类可能为2种
C
.c~d
间(不含两点)的溶液中金属离子为
Zn2+、Cu2+
D
.从
m1?变化到
m2?时,溶液中硝酸铜的质量分数不变
11.现有一包由2.4g镁、6.5g锌、1.6g碳混合而成的粉末,把它加入到一定量的硝酸银溶液中,反应结束后,经过滤、洗涤、干燥,测得滤渣含有三种物质。则滤渣的质量可能是( )
A.10.5g
B.35.6g
C.44.8g
D.45.8g
12.为探究金属活动性顺序,学习小组设计并进行实验I和I1.实验结束,将两实验的废液全部倒入一洁净烧杯中,
反应后得到溶液A和固体B.实验过程及现象如图所示:
据此得出以下结论:
①通过实验I和II能验证Al、Ag.
Cu的金属活动性顺序;
②实验反应后固体中一定含有Cu;
③若A是无色溶液,A中可能含有AgNO3;
④若A呈蓝色,溶液A中至少有两种溶质⑤若A呈蓝色,固体B中定不含Cu;其中正确结论的个数有(
)
A.
1个
B.
2个
C.
3个
D.
4个
13金属材料在生产、生活中有着广泛的应用,人类的生产和生活都离不开金属。
(1)金属活动性顺序有重要的应用。铝、铜、铁为日常生活中常见的金属,某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如图的实验:
将A实验结束后①②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,其原因是_________________,一段时间后过滤,滤液中的溶质一定有________(填化学式)。
(2)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,他对反应过程进行了分析,得到了以下几个图像(横坐标表示加入铁的质量),其中错误的是_____(填字母序号)。
2.2.2金属的化学性质答案
1.A
2.C
3.C
4.B
5.?A
6.(1)氧气和水(2)
AB
7.A
8.
9.(1)
蒸发
HCl(2)
去除过量的铁粉(3)
1.C
2.D
3.D
4.D
5.C
6.C
7.D
8.D
9.C
10.D
11.C
12.B
13.
D
知识点分布
基础巩固
能力提升
重点掌握
基础巩固
能力提升
重点掌握
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
