第三单元物质构成的奥秘练习(4)2020-2021学年人教版化学九年级(含解析)
文档属性
| 名称 | 第三单元物质构成的奥秘练习(4)2020-2021学年人教版化学九年级(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 96.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-28 00:00:00 | ||
图片预览



文档简介
第三单元物质构成的奥秘练习(4)2020-2021学年人教版化学九年级
姓名:___________班级:___________
一、单选题
1.对下列现象解释正确的是
A.酒精挥发——分子可分
B.花香四溢——分子不断运动
C.冰雪融化——分子很小
D.氧气液化——分子体积变小
2.下列对分子、原子和离子的认识正确的是
A.分子、原子和离子都能够直接构成物质
B.只有分子能保持物质的化学性质
C.原子的质量主要集中在质子上
D.氯化钠是由氯化钠离子构成的
3.关于钙原子(Ca)和钙离子(Ca2+)的判断中,不正确的是
A.核电荷数相等
B.核内质子数相等
C.核外电子数相等
D.质量几乎相等
4.下图是氩元素在元素周期表中的有关信息,下列说法错误的是
A.属于金属元素
B.氩的原子序数是18
C.氩原子具有稳定结构
D.相对原子质量是39.95
5.某微粒结构示意图见如图,下列说法错误的是:
A.x的数值为8
B.该元素的原子核外有3个电子层
C.该微粒属于金属元素
D.该微粒的符号可以表示为R1+
6.根据如图信息,下列说法正确的是
A.镁元素位于元素周期表第三周期
B.镁原子的相对原子质量为24.31g
C.镁离子的核外电子数为12
D.在化学反应中,镁原子容易失去电子形成Mg2-
7.北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。在元素周期表中锰元素的某些信息如图所示,下列有关锰的说法不正确的是
A.原子序数为25
B.属于金属元素
C.原子核内中子数为32
D.相对原子质量为54.94
8.用于核电工业的一种铀原子中含有92个质子和143个中子。有关该原子的说法不正确的是
A.质子数为92
B.电子数为143
C.核电荷数为92
D.相对原子质量为235
9.下列叙述完全符合事实的是
A.水结成冰后,体积变大是因为水分子变大
B.50mL水和50mL乙醇混合后总体积小于100mL
C.为了不影响实验时间,可以向燃着的酒精灯内添加酒精
D.高锰酸钾受热分解产生的二氧化锰是该反应中的催化剂
10.下列关于宏观事实的微观解释中,错误的是
A.自然界中水的天然循环——水分子不断运动
B.天然气经压缩储存在钢瓶中——压强增大,分子之间的间隔变大
C.电解水生成氢气和氧气——在化学反应中分子发生改变
D.通过气味辨别酒精和水——不同分子的性质不同
11.下列对宏观现象的微观解释中错误的是
A.不同的花儿有不同的香味,是因为不同的分子性质不同
B.氧气加压后变成液氧,是因为分子间间隔变小
C.非吸烟者受到被动吸烟的危害,是因为分子在不断地运动
D.变瘪的乒乓球放入热水中能鼓起来,是因为受热后分子体积变大
12.元素周期表是学习和研究化学的重要工具。如图是元素周期表中的一部分,据此判断以下与钾有关的叙述中不正确的是
A.钾元素是金属元素
B.钾元素的原子序数为19
C.钾元素、钠元素位于同一周期
D.钾元素的相对原子质量为39.10
13.分子、原子和离子都是构成物质的基本粒子,下列说法正确的是
A.分子由原子构成,分子比原子大
B.水遇冷凝结成冰,水分子停止了运动
C.在化学变化中,原子是最小的粒子,不可再分
D.氯化钠是由氯化钠分子构成的
14.日本福岛第一核电站发生严重的核泄漏,日本政府向福岛核电站附近居民发放碘片(I-127),以降低放射性碘对人体的伤害。已知核辐射中放射性碘(I-131)的核电荷数为53,则下列说法不正确的是
A.核裂变是一种化学变化
B.I-127原子和I-131原子的相对原子质量不相同
C.核能的利用证实原子的可分性
D.I-127原子与I-131原子属于同种元素
15.下列有关微观粒子的说法中,错误的是
A.美酒飘香,是因为分子在不停运动
B.大多数物体受热时体积增大,是因为受热时分子间空隙增大
C.该微粒属于阴离子,带一个单位的负电荷
D.在化学变化中,分子可以再分,原子不可再分
二、填空题
16.我们生活的世界由丰富多彩的物质组成,物质是由微小的粒子构成的。现有氯化钠、铁、二氧化碳三种物质,二氧化碳由______构成,铁由______构成,氯化钠由______、______构成。
17.逐梦航天,建设航天强国。中国九天云外揽月回。
(1)月球上有一种富含钛元素的月海玄武岩,如图是钛元素在元素周期表中的信息及部分原子结构示意图。
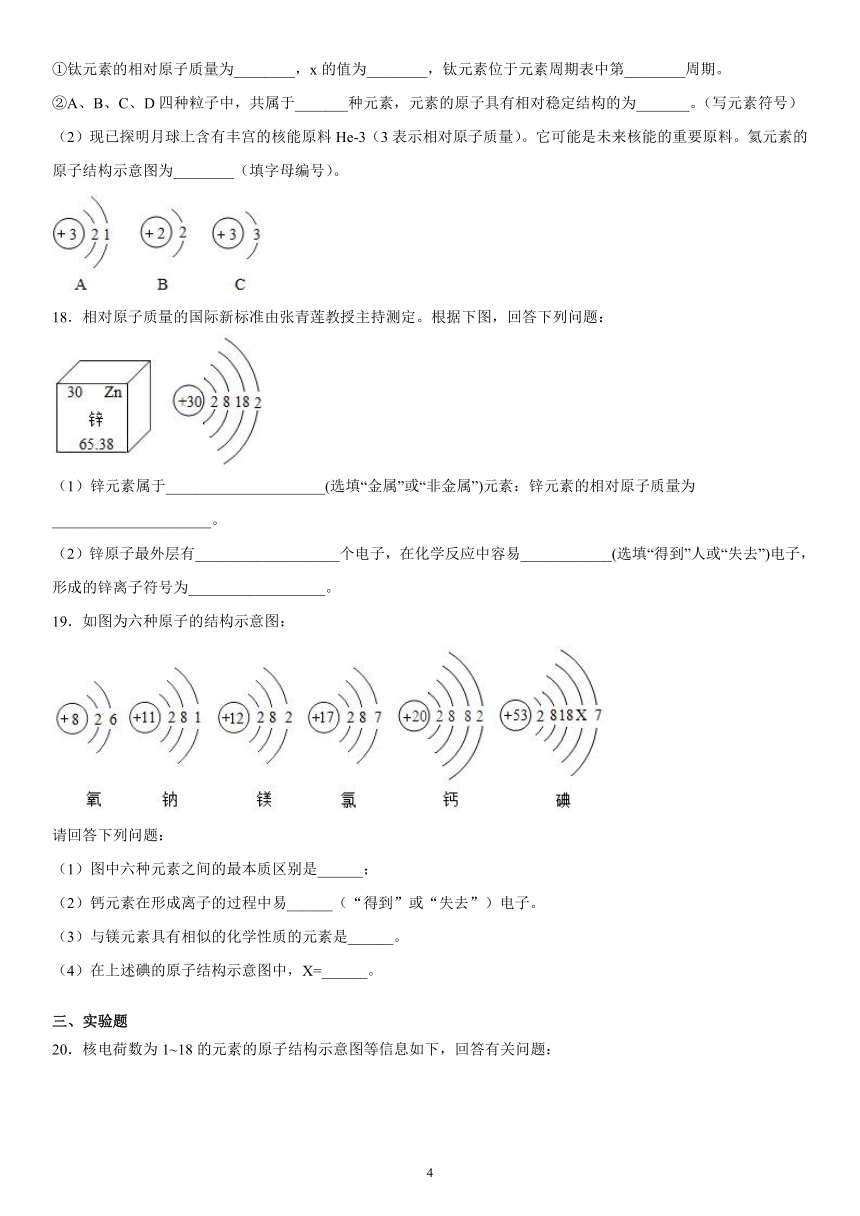
①钛元素的相对原子质量为________,x的值为________,钛元素位于元素周期表中第________周期。
②A、B、C、D四种粒子中,共属于_______种元素,元素的原子具有相对稳定结构的为_______。(写元素符号)
(2)现已探明月球上含有丰宫的核能原料He-3(3表示相对原子质量)。它可能是未来核能的重要原料。氦元素的原子结构示意图为________(填字母编号)。
18.相对原子质量的国际新标准由张青莲教授主持测定。根据下图,回答下列问题:
(1)锌元素属于_____________________(选填“金属”或“非金属”)元素:锌元素的相对原子质量为_____________________。
(2)锌原子最外层有___________________个电子,在化学反应中容易____________(选填“得到”人或“失去”)电子,形成的锌离子符号为__________________。
19.如图为六种原子的结构示意图:
请回答下列问题:
(1)图中六种元素之间的最本质区别是______;
(2)钙元素在形成离子的过程中易______(“得到”或“失去”)电子。
(3)与镁元素具有相似的化学性质的元素是______。
(4)在上述碘的原子结构示意图中,X=______。
三、实验题
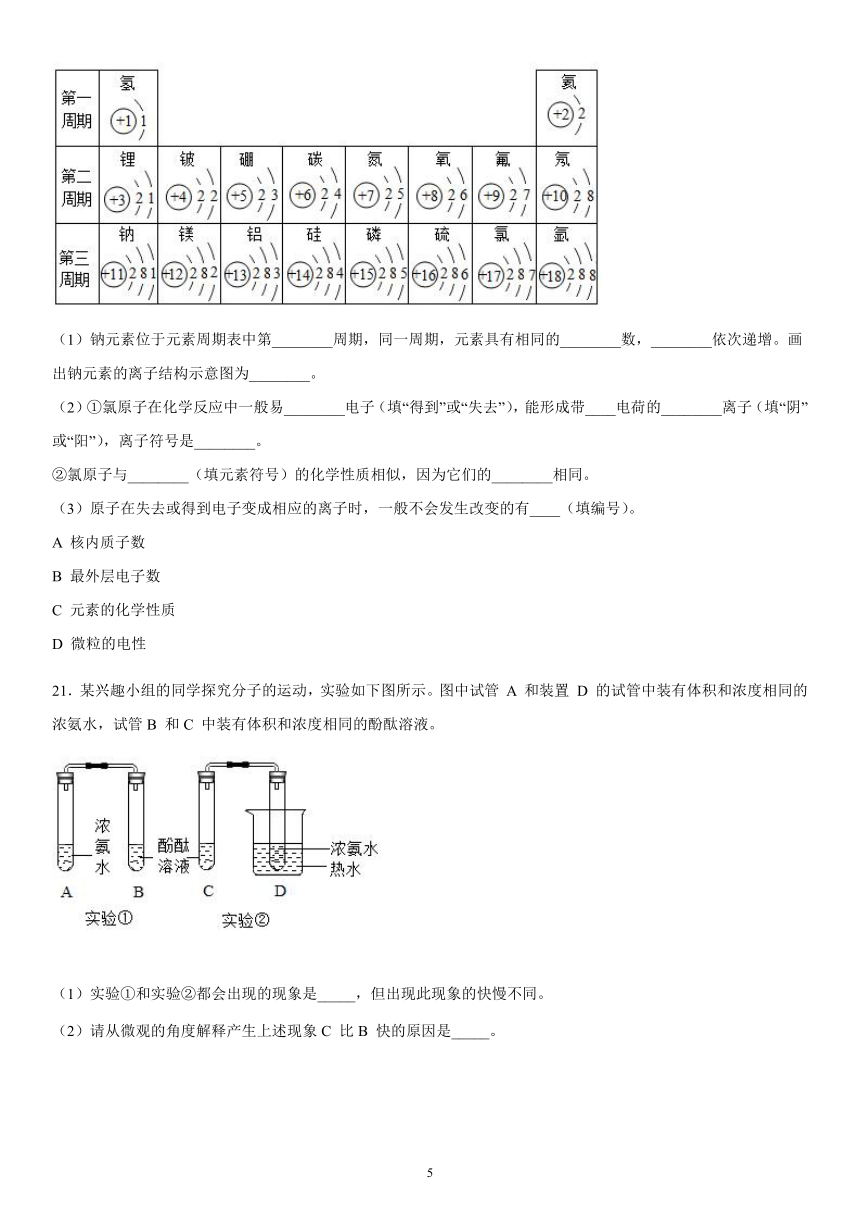
20.核电荷数为1~18的元素的原子结构示意图等信息如下,回答有关问题:
(1)钠元素位于元素周期表中第________周期,同一周期,元素具有相同的________数,________依次递增。画出钠元素的离子结构示意图为________。
(2)①氯原子在化学反应中一般易________电子(填“得到”或“失去”),能形成带____电荷的________离子(填“阴”或“阳”),离子符号是________。
②氯原子与________(填元素符号)的化学性质相似,因为它们的________相同。
(3)原子在失去或得到电子变成相应的离子时,一般不会发生改变的有____(填编号)。
A
核内质子数
B
最外层电子数
C
元素的化学性质
D
微粒的电性
21.某兴趣小组的同学探究分子的运动,实验如下图所示。图中试管
A
和装置
D
的试管中装有体积和浓度相同的浓氨水,试管B
和C
中装有体积和浓度相同的酚酞溶液。
(1)实验①和实验②都会出现的现象是_____,但出现此现象的快慢不同。
(2)请从微观的角度解释产生上述现象C
比B
快的原因是_____。
(
2
)
(
1
)
参考答案
1.B
【详解】
略
2.A
【详解】
A、分子、原子和离子都能够直接构成物质,正确;
B、由分子构成的物质,分子能保持物质的化学性质,由原子构成的物质由原子保持化学性质,错误;
C、原子的质量主要集中在原子核上,错误;
D、氯化钠是由氯离子、钠离子构成的,错误;
故选A。
3.C
【详解】
钙原子失去最外层的两个电子变成钙离子,故电子数不同,原子核不变,故核电荷数、核内质子数相同,原子的质量主要集中在原子核上,故质量几乎相等。故选C。
4.A
【详解】
A、由汉字结构可知,氩属于非金属元素,错误;
B、氩的原子序数是18,正确;
C、氩原子最外层有8个电子,具有稳定结构,正确;
D、相对原子质量是39.95,正确。
故选A。
【点睛】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
5.D
【详解】
A、如该微粒为原子,则11=2+x,x=9>8,违反第2层最多排8个电子的排布规律。如该微粒为离子,最外层排满,x=8,该微粒是钠离子。正确。
B、钠元素原子核外有3个电子层,第一层排2个,第二层排8个,第三层排1个,正确。
C、该微粒是钠离子,钠属于金属元素,正确。
D、钠离子符号为Na+,如果离子带1个单位的正电荷或负电荷,1省略不写。错误。
故选D。
6.A
【详解】
A、根据原子结构示意图,镁原子核外电子有三层,所以镁元素位于元素周期表第三周期,故选项正确;
B、相对原子质量单位是“1”,不是“克”,故选项错误;
C、核外电子数=原子序数,镁原子失去2个电子形成镁离子,则镁离子核外电子数为10,故选项错误;
D、在化学反应中,镁原子容易失去2个电子,带2个单位正电荷,镁离子表示为Mg2+,故选项错误。
故选A
7.C
【详解】
A、根据元素周期表中的一格可知,左上角的数字为25,该元素的原子序数为25,故选项说法正确。
B、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锰,带“钅”字旁,属于金属元素,故选项说法正确。
C、根据元素周期表中的一格可知,左上角的数字为25,表示原子序数为25;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为25,则中子数为55-25=30,故选项说法错误。
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为54.94,故选项说法正确。
故选:C。
8.B
【详解】
略
9.B
【详解】
A、水结成冰后,体积变大是因为水分子的间隙变大,不符合事实;
B、50mL水和50mL乙醇混合后总体积小于100mL,因为分子间有间隙,混合后水分子和乙醇分子跑到其中间隙中,符合事实;
C、不能向燃着的酒精等内添加酒精,否则会失火,不符合事实;
D、高锰酸钾受热分解产生的二氧化锰是该反应中的生成物,不符合事实。
故选:B。
10.B
【详解】
A、自然界中水的天然循环,是因为水分子不断运动的缘故,故选项解释正确。
B、天然气经压缩储存在钢瓶中,是因为分子间有间隔,气体受压后,分子间隔变小,气体的体积减小,故选项解释错误。
C、水通电生成氢气和氧气,是因为水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子,大量的氢分子、氧分子分别聚集成氢气、氧气,该事实说明在化学反应中,分子可分,在化学反应中分子发生改变,故选项解释正确。
D、通过气味辨别酒精和水,是因为分子是不断地运动的,且不同种的分子性质不同,故选项解释正确。
故选:B。
11.D
【详解】
A、不同的花儿有不同的香味,是因为不同的分子性质不同,不符合题意;
B、氧气加压后变成液氧,是因为受压后,分子间间隔变小,不符合题意;
C、非吸烟者受到被动吸烟的危害,是因为分子在不断地运动,不符合题意;
D、变瘪的乒乓球放入热水中能鼓起来,是因为受热后,分子之间的间隔变大,分子的体积不变,符合题意。
故选D。
12.C
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、由汉字结构可知,钾元素是金属元素,正确;
B、钾元素的原子序数为19,正确;
C、钾元素、钠元素位于同一族,不是同一周期,错误;
D、钾元素的相对原子质量为39.10,正确。
故选C。
13.C
【详解】
A、分子和原子不能比较大小,但由原子构成的分子,其分子比构成它的原子大;如果分子中不含该原子,则分子不一定比原子大,选项说法错误。
B、分子总是在不断运动的,选项说法错误;
C、原子是化学变化中的最小粒子,在化学变化中,原子是最小的粒子,不可再分,选项说法正确;
D、氯化钠是由钠离子与氯离子构成的,选项说法错误。
故选:C。
14.A
【详解】
A、核裂变是原子核发生裂变,原子发生了变化,属于核物理研究的范畴,而化学变化中原子核不发生变化,因此核裂变不是化学变化,符合题意;
B、因为“相对原子质量≈质子数+中子数”,虽然I-127原子和I-131原子质子数相同,但中子数不同,所以相对原子质量不相同,正确,不符合题意;
C、核能的利用证实了原子是可分的,正确,不符合题意;
D、I-127原子和I-131原子属于同种元素,因为它们是质子数相同的原子,所以属于同种元素,正确,不符合题意。
故选:A。
15.C
【详解】
A、美酒飘香,是因为分子在不断运动,带有酒香的分子四处扩散,不符合题意;
B、大多数物体受热时体积增大,是因为受热时分子间空隙增大,不符合题意;
C、该微粒中,质子数大于核外电子数,表示阳离子,带1个单位正电荷,符合题意;
D、原子是化学变化中的最小粒子,在化学变化中,分子可分为原子,原子不可再分,不符合题意。
故选C。
16.二氧化碳分子
铁原子
钠离子
氯离子
【详解】
二氧化碳是由二氧化碳分子构成的;铁属于金属单质,是由铁原子直接构成的;氯化钠是由钠离子和氯离子构成的。
【点睛】
17.47.87
2
四
三
Ne
B
【详解】
(1)①根据单元格信息,钛的相对原子质量为47.87;因为在原子中,质子数=核外电子数,所以x=22-2-8-10=2,元素所在的周期数等于原子的电子层数,故位于第四周期;
②据图可以看出,A、B、C、D四种粒子,有10、11、17三个数字,故共表示3种元素;B原子的质子数为10,是氦元素,最外层电子数为8,具有相对稳定结构;
(2)He原子是质子数为2的原子,其核外的电子数也是2,则该原子的原子结构示意图为。
18.
(1)
金属
65.38
(2)
2
失去
Zn2+
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
(1)
由汉字结构可知,锌元素属于金属元素;锌元素的相对原子质量为65.38。
(2)
原子结构示意图中弧线上的数字表示该层电子数;锌原子最外层有2个电子,小于4,在化学反应中容易失去2个电子,形成带两个单位正电荷的锌离子,由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,则符号为Zn2+。
19.
(1)质子数(核电荷数)不同
(2)失去
(3)钙
(4)18
【分析】
(1)
元素是质子数(核电荷数)相同的一类原子的总称,不同元素区别是质子数(核电荷数)不同,故填:质子数(核电荷数)不同。
(2)
钙原子最外层电子数是2小于4,在形成离子的过程中易失去电子数,故填:失去。
(3)
最外层电子数相同,化学性质相似,镁元素和钙元素最外层电子数相同,故填:钙。
(4)
原子中,核电荷数=核外电子数,故53=2+8+18+X+7,X=18,故填:18。
20.三
电子层数
质子数
得到
负
阴
Cl-
F
最外层电子数
A
【详解】
(1)由元素周期表可知,钠元素位于元素周期表中第三周期;根据核电荷数为1~18的元素的原子结构示意图可知,在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子质子数依次增加;钠元素的原子最外层电子数为1,在化学反应中易失去1个电子,形成稳定结构,其离子结构示意图为
,
故填:三;电子层数;质子数;
;
(2)由氯原子的结构示意图可知,氯原子的最外层电子数为7,多于4,在化学反应中易得到一个电子,形成带负电荷的阴离子,其离子符号为:Cl-,故填得到;负;阴;Cl-;
(3)A、原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,核内质子数不变,符合题意。
B、
原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,最外层电子数一定发生改变,不符合题意。
C、
原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,最外层电子数一定发生改变,元素的化学性质发生改变,不符合题意。
D、
原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,最外层电子数一定发生改变,微粒的电性发生改变,不符合题意。
故选A。
21.酚酞溶液变红
D中氨水的温度高于A中氨水的温度,D中的氨分子运动较快
【详解】
(1)氨水具有挥发性,挥发出来的氨气溶解到酚酞溶液中形成氨水,氨水显碱性,能够使酚酞溶液变红,即观察到的现象是实验①和实验②中的酚酞溶液变红,故填酚酞溶液变红。
(2)分子在不断地运动,且温度越高,分子的运动越快,D中氨水的温度高于A中氨水的温度,则D中的氨分子运动较快,使得C中的酚酞溶液比B中的酚酞溶液变红得快,故填D中氨水的温度高于A中氨水的温度,D中的氨分子运动较快。
(
2
)
(
1
)
姓名:___________班级:___________
一、单选题
1.对下列现象解释正确的是
A.酒精挥发——分子可分
B.花香四溢——分子不断运动
C.冰雪融化——分子很小
D.氧气液化——分子体积变小
2.下列对分子、原子和离子的认识正确的是
A.分子、原子和离子都能够直接构成物质
B.只有分子能保持物质的化学性质
C.原子的质量主要集中在质子上
D.氯化钠是由氯化钠离子构成的
3.关于钙原子(Ca)和钙离子(Ca2+)的判断中,不正确的是
A.核电荷数相等
B.核内质子数相等
C.核外电子数相等
D.质量几乎相等
4.下图是氩元素在元素周期表中的有关信息,下列说法错误的是
A.属于金属元素
B.氩的原子序数是18
C.氩原子具有稳定结构
D.相对原子质量是39.95
5.某微粒结构示意图见如图,下列说法错误的是:
A.x的数值为8
B.该元素的原子核外有3个电子层
C.该微粒属于金属元素
D.该微粒的符号可以表示为R1+
6.根据如图信息,下列说法正确的是
A.镁元素位于元素周期表第三周期
B.镁原子的相对原子质量为24.31g
C.镁离子的核外电子数为12
D.在化学反应中,镁原子容易失去电子形成Mg2-
7.北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。在元素周期表中锰元素的某些信息如图所示,下列有关锰的说法不正确的是
A.原子序数为25
B.属于金属元素
C.原子核内中子数为32
D.相对原子质量为54.94
8.用于核电工业的一种铀原子中含有92个质子和143个中子。有关该原子的说法不正确的是
A.质子数为92
B.电子数为143
C.核电荷数为92
D.相对原子质量为235
9.下列叙述完全符合事实的是
A.水结成冰后,体积变大是因为水分子变大
B.50mL水和50mL乙醇混合后总体积小于100mL
C.为了不影响实验时间,可以向燃着的酒精灯内添加酒精
D.高锰酸钾受热分解产生的二氧化锰是该反应中的催化剂
10.下列关于宏观事实的微观解释中,错误的是
A.自然界中水的天然循环——水分子不断运动
B.天然气经压缩储存在钢瓶中——压强增大,分子之间的间隔变大
C.电解水生成氢气和氧气——在化学反应中分子发生改变
D.通过气味辨别酒精和水——不同分子的性质不同
11.下列对宏观现象的微观解释中错误的是
A.不同的花儿有不同的香味,是因为不同的分子性质不同
B.氧气加压后变成液氧,是因为分子间间隔变小
C.非吸烟者受到被动吸烟的危害,是因为分子在不断地运动
D.变瘪的乒乓球放入热水中能鼓起来,是因为受热后分子体积变大
12.元素周期表是学习和研究化学的重要工具。如图是元素周期表中的一部分,据此判断以下与钾有关的叙述中不正确的是
A.钾元素是金属元素
B.钾元素的原子序数为19
C.钾元素、钠元素位于同一周期
D.钾元素的相对原子质量为39.10
13.分子、原子和离子都是构成物质的基本粒子,下列说法正确的是
A.分子由原子构成,分子比原子大
B.水遇冷凝结成冰,水分子停止了运动
C.在化学变化中,原子是最小的粒子,不可再分
D.氯化钠是由氯化钠分子构成的
14.日本福岛第一核电站发生严重的核泄漏,日本政府向福岛核电站附近居民发放碘片(I-127),以降低放射性碘对人体的伤害。已知核辐射中放射性碘(I-131)的核电荷数为53,则下列说法不正确的是
A.核裂变是一种化学变化
B.I-127原子和I-131原子的相对原子质量不相同
C.核能的利用证实原子的可分性
D.I-127原子与I-131原子属于同种元素
15.下列有关微观粒子的说法中,错误的是
A.美酒飘香,是因为分子在不停运动
B.大多数物体受热时体积增大,是因为受热时分子间空隙增大
C.该微粒属于阴离子,带一个单位的负电荷
D.在化学变化中,分子可以再分,原子不可再分
二、填空题
16.我们生活的世界由丰富多彩的物质组成,物质是由微小的粒子构成的。现有氯化钠、铁、二氧化碳三种物质,二氧化碳由______构成,铁由______构成,氯化钠由______、______构成。
17.逐梦航天,建设航天强国。中国九天云外揽月回。
(1)月球上有一种富含钛元素的月海玄武岩,如图是钛元素在元素周期表中的信息及部分原子结构示意图。
①钛元素的相对原子质量为________,x的值为________,钛元素位于元素周期表中第________周期。
②A、B、C、D四种粒子中,共属于_______种元素,元素的原子具有相对稳定结构的为_______。(写元素符号)
(2)现已探明月球上含有丰宫的核能原料He-3(3表示相对原子质量)。它可能是未来核能的重要原料。氦元素的原子结构示意图为________(填字母编号)。
18.相对原子质量的国际新标准由张青莲教授主持测定。根据下图,回答下列问题:
(1)锌元素属于_____________________(选填“金属”或“非金属”)元素:锌元素的相对原子质量为_____________________。
(2)锌原子最外层有___________________个电子,在化学反应中容易____________(选填“得到”人或“失去”)电子,形成的锌离子符号为__________________。
19.如图为六种原子的结构示意图:
请回答下列问题:
(1)图中六种元素之间的最本质区别是______;
(2)钙元素在形成离子的过程中易______(“得到”或“失去”)电子。
(3)与镁元素具有相似的化学性质的元素是______。
(4)在上述碘的原子结构示意图中,X=______。
三、实验题
20.核电荷数为1~18的元素的原子结构示意图等信息如下,回答有关问题:
(1)钠元素位于元素周期表中第________周期,同一周期,元素具有相同的________数,________依次递增。画出钠元素的离子结构示意图为________。
(2)①氯原子在化学反应中一般易________电子(填“得到”或“失去”),能形成带____电荷的________离子(填“阴”或“阳”),离子符号是________。
②氯原子与________(填元素符号)的化学性质相似,因为它们的________相同。
(3)原子在失去或得到电子变成相应的离子时,一般不会发生改变的有____(填编号)。
A
核内质子数
B
最外层电子数
C
元素的化学性质
D
微粒的电性
21.某兴趣小组的同学探究分子的运动,实验如下图所示。图中试管
A
和装置
D
的试管中装有体积和浓度相同的浓氨水,试管B
和C
中装有体积和浓度相同的酚酞溶液。
(1)实验①和实验②都会出现的现象是_____,但出现此现象的快慢不同。
(2)请从微观的角度解释产生上述现象C
比B
快的原因是_____。
(
2
)
(
1
)
参考答案
1.B
【详解】
略
2.A
【详解】
A、分子、原子和离子都能够直接构成物质,正确;
B、由分子构成的物质,分子能保持物质的化学性质,由原子构成的物质由原子保持化学性质,错误;
C、原子的质量主要集中在原子核上,错误;
D、氯化钠是由氯离子、钠离子构成的,错误;
故选A。
3.C
【详解】
钙原子失去最外层的两个电子变成钙离子,故电子数不同,原子核不变,故核电荷数、核内质子数相同,原子的质量主要集中在原子核上,故质量几乎相等。故选C。
4.A
【详解】
A、由汉字结构可知,氩属于非金属元素,错误;
B、氩的原子序数是18,正确;
C、氩原子最外层有8个电子,具有稳定结构,正确;
D、相对原子质量是39.95,正确。
故选A。
【点睛】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
5.D
【详解】
A、如该微粒为原子,则11=2+x,x=9>8,违反第2层最多排8个电子的排布规律。如该微粒为离子,最外层排满,x=8,该微粒是钠离子。正确。
B、钠元素原子核外有3个电子层,第一层排2个,第二层排8个,第三层排1个,正确。
C、该微粒是钠离子,钠属于金属元素,正确。
D、钠离子符号为Na+,如果离子带1个单位的正电荷或负电荷,1省略不写。错误。
故选D。
6.A
【详解】
A、根据原子结构示意图,镁原子核外电子有三层,所以镁元素位于元素周期表第三周期,故选项正确;
B、相对原子质量单位是“1”,不是“克”,故选项错误;
C、核外电子数=原子序数,镁原子失去2个电子形成镁离子,则镁离子核外电子数为10,故选项错误;
D、在化学反应中,镁原子容易失去2个电子,带2个单位正电荷,镁离子表示为Mg2+,故选项错误。
故选A
7.C
【详解】
A、根据元素周期表中的一格可知,左上角的数字为25,该元素的原子序数为25,故选项说法正确。
B、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锰,带“钅”字旁,属于金属元素,故选项说法正确。
C、根据元素周期表中的一格可知,左上角的数字为25,表示原子序数为25;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为25,则中子数为55-25=30,故选项说法错误。
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为54.94,故选项说法正确。
故选:C。
8.B
【详解】
略
9.B
【详解】
A、水结成冰后,体积变大是因为水分子的间隙变大,不符合事实;
B、50mL水和50mL乙醇混合后总体积小于100mL,因为分子间有间隙,混合后水分子和乙醇分子跑到其中间隙中,符合事实;
C、不能向燃着的酒精等内添加酒精,否则会失火,不符合事实;
D、高锰酸钾受热分解产生的二氧化锰是该反应中的生成物,不符合事实。
故选:B。
10.B
【详解】
A、自然界中水的天然循环,是因为水分子不断运动的缘故,故选项解释正确。
B、天然气经压缩储存在钢瓶中,是因为分子间有间隔,气体受压后,分子间隔变小,气体的体积减小,故选项解释错误。
C、水通电生成氢气和氧气,是因为水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子,大量的氢分子、氧分子分别聚集成氢气、氧气,该事实说明在化学反应中,分子可分,在化学反应中分子发生改变,故选项解释正确。
D、通过气味辨别酒精和水,是因为分子是不断地运动的,且不同种的分子性质不同,故选项解释正确。
故选:B。
11.D
【详解】
A、不同的花儿有不同的香味,是因为不同的分子性质不同,不符合题意;
B、氧气加压后变成液氧,是因为受压后,分子间间隔变小,不符合题意;
C、非吸烟者受到被动吸烟的危害,是因为分子在不断地运动,不符合题意;
D、变瘪的乒乓球放入热水中能鼓起来,是因为受热后,分子之间的间隔变大,分子的体积不变,符合题意。
故选D。
12.C
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、由汉字结构可知,钾元素是金属元素,正确;
B、钾元素的原子序数为19,正确;
C、钾元素、钠元素位于同一族,不是同一周期,错误;
D、钾元素的相对原子质量为39.10,正确。
故选C。
13.C
【详解】
A、分子和原子不能比较大小,但由原子构成的分子,其分子比构成它的原子大;如果分子中不含该原子,则分子不一定比原子大,选项说法错误。
B、分子总是在不断运动的,选项说法错误;
C、原子是化学变化中的最小粒子,在化学变化中,原子是最小的粒子,不可再分,选项说法正确;
D、氯化钠是由钠离子与氯离子构成的,选项说法错误。
故选:C。
14.A
【详解】
A、核裂变是原子核发生裂变,原子发生了变化,属于核物理研究的范畴,而化学变化中原子核不发生变化,因此核裂变不是化学变化,符合题意;
B、因为“相对原子质量≈质子数+中子数”,虽然I-127原子和I-131原子质子数相同,但中子数不同,所以相对原子质量不相同,正确,不符合题意;
C、核能的利用证实了原子是可分的,正确,不符合题意;
D、I-127原子和I-131原子属于同种元素,因为它们是质子数相同的原子,所以属于同种元素,正确,不符合题意。
故选:A。
15.C
【详解】
A、美酒飘香,是因为分子在不断运动,带有酒香的分子四处扩散,不符合题意;
B、大多数物体受热时体积增大,是因为受热时分子间空隙增大,不符合题意;
C、该微粒中,质子数大于核外电子数,表示阳离子,带1个单位正电荷,符合题意;
D、原子是化学变化中的最小粒子,在化学变化中,分子可分为原子,原子不可再分,不符合题意。
故选C。
16.二氧化碳分子
铁原子
钠离子
氯离子
【详解】
二氧化碳是由二氧化碳分子构成的;铁属于金属单质,是由铁原子直接构成的;氯化钠是由钠离子和氯离子构成的。
【点睛】
17.47.87
2
四
三
Ne
B
【详解】
(1)①根据单元格信息,钛的相对原子质量为47.87;因为在原子中,质子数=核外电子数,所以x=22-2-8-10=2,元素所在的周期数等于原子的电子层数,故位于第四周期;
②据图可以看出,A、B、C、D四种粒子,有10、11、17三个数字,故共表示3种元素;B原子的质子数为10,是氦元素,最外层电子数为8,具有相对稳定结构;
(2)He原子是质子数为2的原子,其核外的电子数也是2,则该原子的原子结构示意图为。
18.
(1)
金属
65.38
(2)
2
失去
Zn2+
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
(1)
由汉字结构可知,锌元素属于金属元素;锌元素的相对原子质量为65.38。
(2)
原子结构示意图中弧线上的数字表示该层电子数;锌原子最外层有2个电子,小于4,在化学反应中容易失去2个电子,形成带两个单位正电荷的锌离子,由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,则符号为Zn2+。
19.
(1)质子数(核电荷数)不同
(2)失去
(3)钙
(4)18
【分析】
(1)
元素是质子数(核电荷数)相同的一类原子的总称,不同元素区别是质子数(核电荷数)不同,故填:质子数(核电荷数)不同。
(2)
钙原子最外层电子数是2小于4,在形成离子的过程中易失去电子数,故填:失去。
(3)
最外层电子数相同,化学性质相似,镁元素和钙元素最外层电子数相同,故填:钙。
(4)
原子中,核电荷数=核外电子数,故53=2+8+18+X+7,X=18,故填:18。
20.三
电子层数
质子数
得到
负
阴
Cl-
F
最外层电子数
A
【详解】
(1)由元素周期表可知,钠元素位于元素周期表中第三周期;根据核电荷数为1~18的元素的原子结构示意图可知,在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子质子数依次增加;钠元素的原子最外层电子数为1,在化学反应中易失去1个电子,形成稳定结构,其离子结构示意图为
,
故填:三;电子层数;质子数;
;
(2)由氯原子的结构示意图可知,氯原子的最外层电子数为7,多于4,在化学反应中易得到一个电子,形成带负电荷的阴离子,其离子符号为:Cl-,故填得到;负;阴;Cl-;
(3)A、原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,核内质子数不变,符合题意。
B、
原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,最外层电子数一定发生改变,不符合题意。
C、
原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,最外层电子数一定发生改变,元素的化学性质发生改变,不符合题意。
D、
原子在失去或得到电子变成相应的离子时,通过核外电子的得失形成稳定结构,最外层电子数一定发生改变,微粒的电性发生改变,不符合题意。
故选A。
21.酚酞溶液变红
D中氨水的温度高于A中氨水的温度,D中的氨分子运动较快
【详解】
(1)氨水具有挥发性,挥发出来的氨气溶解到酚酞溶液中形成氨水,氨水显碱性,能够使酚酞溶液变红,即观察到的现象是实验①和实验②中的酚酞溶液变红,故填酚酞溶液变红。
(2)分子在不断地运动,且温度越高,分子的运动越快,D中氨水的温度高于A中氨水的温度,则D中的氨分子运动较快,使得C中的酚酞溶液比B中的酚酞溶液变红得快,故填D中氨水的温度高于A中氨水的温度,D中的氨分子运动较快。
(
2
)
(
1
)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
