3.3元素课后练习A--2021-2022学年九年级化学人教版上册(word版 含详细解答)
文档属性
| 名称 | 3.3元素课后练习A--2021-2022学年九年级化学人教版上册(word版 含详细解答) |  | |
| 格式 | zip | ||
| 文件大小 | 133.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-29 08:56:19 | ||
图片预览




文档简介
第三单元物质构成的奥秘课题三元素课后练习A九年级化学上学期(人教版)
练习
一、单选题,共12小题
1.下列符号既能表示某种元素,又能表示该元素的一个原子,还能表示一种物质的是
A.
B.
C.N
D.Cu
2.下列物质中,由地壳中含量最多的金属元素和非金属元素组成的是
A.水
B.二氧化碳
C.氧化铝
D.氧化铁
3.“富硒茶”是较好的保健饮品,这里的“硒”指的是
A.原子
B.分子
C.元素
D.离子
4.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是
A.①④的化学性质比较稳定
B.①④属于稀有气体元素
C.④是一种阳离子
D.③④属于同种元素
5.关于元素的叙述,错误的是
A.元素只讲种类,不讲个数
B.化学变化前后,元素种类一定不变
C.质子数相同的一类粒子属于同种元素
D.不同种元素的根本区别是核内质子数不同
6.地壳中,含量最多的元素是
A.硅元素
B.氧元素
C.铝元素
D.钙元素
7.2021年4月,日本政府计划将核废水排入海里,其中含有大量的氚。氚一旦进入人体可能从人体内部对人造成辐射损害,如果人类持续暴露在氚的辐射下,可能会导致细脑死亡,DNA遗传损伤。下列说法正确的是
A.氚原子与氢原子的最外层电子数相同
B.氚原子与氢原子都有中子,只是数目不同
C.氚与氢元素不属于同种元素
D.氚原子与氢原子相对原子质量相同
8.下图是某品牌燕麦片,其中包装袋上写着“加钙加铁”字样,这里的钙、铁指的是
A.离子
B.元素
C.分子
D.原子
9.下列符号中即表示一种元素,又表示一个原子,还表示一种物质的是
A.O
B.Cu
C.H2
D.Na+
10.如图为钟表式元素周期表,该钟表的整点时间小时数与该元素的质子数相等。对“时针”和“分针”所指时刻的两种元素,下列说法正确的是
A.1:00对应元素的单质均由分子构成
B.6:00对应的两种元素均为金属元素
C.8:00对应的两种元素易形成化合物
D.12:00对应元素的离子符号为M
11.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为
A.硒
B.硅
C.铝
D.锡
12.下列关于元素含量的说法正确的是
A.地壳中含量最多的金属元素是Fe
B.空气中含量最多的元素是N
C.人体中含量最多的元素是C
D.海水中含量最多的元素是Na
二、非选择题,共6小题
13.写出下列符号的意义或用化学符号表示。
(1)H:______,______。
(2)5Ag:______。
(3)2个氯原子:______。
(4)Mg2+中2的含义:______。
14.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
如图所示,X是______;Y是______。
15.地壳中含量前两位的元素形成的化合物是______;地中含最高的金属元形成的氧化物的化学式为______。
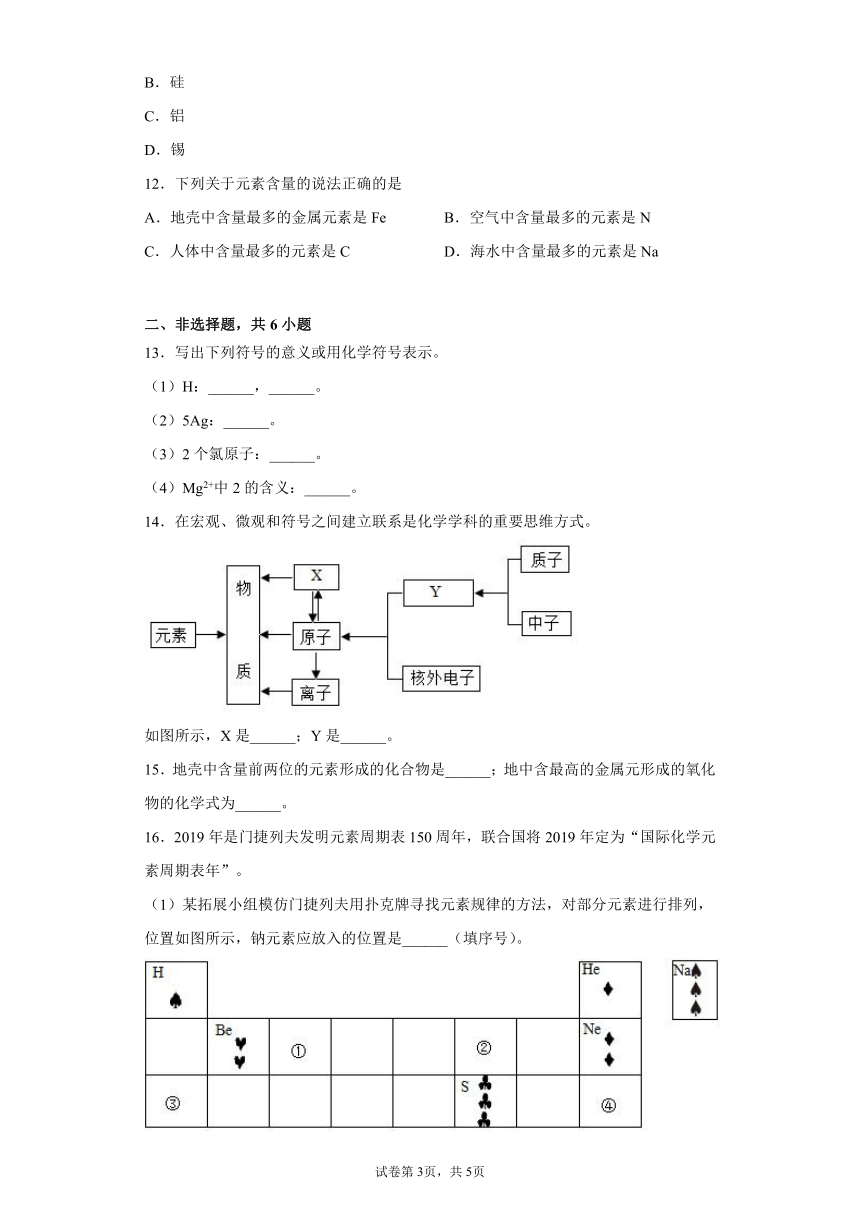
16.2019年是门捷列夫发明元素周期表150周年,联合国将2019年定为“国际化学元素周期表年”。
(1)某拓展小组模仿门捷列夫用扑克牌寻找元素规律的方法,对部分元素进行排列,位置如图所示,钠元素应放入的位置是______(填序号)。
(2)我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显等多个领域。氮原子和镓离子结钩示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是______(填序号)。
A.氮化镓的化学式为GaN
B.镓的相对原子质量是69.72g
C.镓原子核内有31个中子
D.镓元素位于第三周期,属于金属元素
(3)我国科学家最新研制出一种新型石墨烯—铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如图所示,
它们的化学性质______(填“相似”或“不相似”)。在化学反应中,铝原子容易______(填“得到”或“失去”)电子。
(4)下列几种粒子的结构示意图中共有______种元素,表示阳离子的离子符号是______。
17.用元素符号或化学式表示:
(1)2个铁原子______;
(2)4个氢分子______;
(3)5个碳酸根离子______;
(4)3个铁离子______。
18.元素锶形成的粒子结构示意图如图1所示,锶的元素符号为Sr。
(1)锶元素位于元素周期表中的第______周期。锶离子的化学符号是______。
(2)图2表示的微粒中,具有相对稳定结构的原子是______(填字母序号,下同),与锶元素化学性质相似的是______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.D
【详解】
略
2.C
【详解】
略
3.C
【详解】
略
4.B
【详解】
A、最外层电子排满,微粒化学性质稳定,①④最外层电子数都为8,已排满,化学性质稳定。正确;
B、质子数=原子序数,①是第8号元素氧元素,④是第11号元素钠元素。都不是稀有气体元素,错误;
C、④质子数>电子数,是阳离子。正确;
D、元素是具有相同质子数的一类原子的总称。③④质子数相同,属于同类元素。正确。
故选B。
5.C
【详解】
A、元素是具有相同核电荷数(或核内质子数)一类原子的总称,元素是宏观概念,只讲种类,不讲个数,选项说法正确;
B、根据质量守恒定律,化学变化前后,元素种类一定不变,选项说法正确;
C、质子数相同的一类粒子不一定属于同种元素,如氖原子和水分子质子数相同,不属于同种元素,选项说法不正确;
D、元素是具有相同核电荷数(或核内质子数)一类原子的总称,所以不同种元素的根本区别是核内质子数不同,选项说法正确。
故选C。
6.B
【详解】
地壳中含量最多的前四种元素分别是:氧、硅、铝、铁,故选B。
7.A
【详解】
A、氚原子与氢原子的最外层电子数均为1,最外层电子数相同,故选项说法正确。
B、氚原子中有中子,氢原子中没有中子,故选项说法错误。
C、氚与氢元素的核内质子数相同,属于同种元素,故选项说法错误。
D、相对原子质量=质子数+中子数,氚原子与氢原子的质子数相同,中子数不同,相对原子质量不同,故选项说法错误。
故选:A。
8.B
【详解】
包装袋上写的“加钙加铁”,这里的钙、铁指的是物质的组成,表示元素;故选B。
9.B
【分析】
元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义。
【详解】
A、O属于气态非金属元素,可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项错误;
B、Cu属于金属元素,可表示铜元素,表示一个铜原子,还能表示铜这一纯净物,故选项正确;
C、
该符号是氢气的化学式,不是元素符号,故选项错误;
D、该符号是钠离子的符号,不能表示一种元素,不能表示一个原子,也不能表示一种物质,故选项错误。
故选:B。
【点睛】
10.C
【详解】
A、1:00对应的元素是氢元素和镁元素,对应元素的单质氢气是由分子构成的,镁是由原子直接构成的,错误。
B、6:00对应的元素为碳元素和镁元素,镁是金属元素,碳属于非金属元素,错误。
C、8:00对应的两种元素为氧元素和镁元素,易形成化合物氧化镁,正确。
D、12:00对应元素是镁元素,对应元素的离子符号为Mg2+,错误。
故选:C。
11.B
【详解】
地壳中元素含量由多到少依次为:氧、硅、铝、铁,地壳中含量第二的元素是硅,翻译成“矽(xi)”,如今把这种“矽”元素命名为硅;
故选:B。
12.B
【详解】
A、地壳中含量最多的金属元素是铝元素,元素符号为Al,不符合题意;
B、空气中含量最多的物质是氮气,含量最多的元素是N,符合题意;
C、人体中含量最多的物质是水,含量最多的元素是O,不符合题意;
D、海水中含量最多的物质是水,含量最多的元素是O,不符合题意。
故选B。
13.
(1)
1个氢原子
氢元素
(2)5个银原子
(3)2Cl
(4)1个镁离子带有2个单位的正电荷
【详解】
(1)元素符号可表示一种元素、一个原子,H可表示氢元素、1个氢原子;
(2)当元素符号前面加上数字就只有微观意义,表示几个这样的原子,故5Ag表示5个银原子;
(3)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,2个氯原子可表示为:2Cl;
(4)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。离子符号右上角的数字表示每个离子所带电荷数,所以Mg2+中2的含义每个镁离子带2个单位的正电荷。
14.分子
原子核
【详解】
分子可分成原子,故X是分子;原子是由原子核和核外电子构成,故Y是原子核。
15.SiO2
Al2O3
【详解】
地壳中含量第一的元素是氧,第二位是硅,故填:SiO2;
地壳中含量最多的金属元素是铝,其氧化物为氧化铝,又称三氧化二铝,故填:Al2O3。
16.
(1)③
(2)A
(3)
不相似
失去
(4)
3
Mg2+
【分析】
(1)
钠原子的最外层电子数是1,和氢的最外层电子数相同,同一主族最外层电子数相同;则钠元素扑克牌应放入的位置是③。
(2)
A、根据镓离子结钩示意图,镓显+3价,氮最外层5个电子易得3个电子,显-3价,所以氮化镓表示GaN,故正确;
B、由元素周期表的信息可知,镓的相对原子质量为69.72,没有单位g,故错误;
C、元素周期表中,左上角是原子序数,原子序数=核内质子数=核电荷数,所以镓的核内质子数为31,不是中子数,故错误;
D、电子层数决定周期数,根据镓离子结钩示意图,得出镓原子核外电子层数有4层,位于第四周期,镓元素带有钅字旁,属于金属元素,故错误。
故选A。
(3)
根据信息图,碳原子的结钩示意图、铝原子的结钩示意图,可见最外层电子数不相等,化学性质不相似;铝原子最外层电子数是3,小于4,铝原子容易 失去电子。
(4)
质子数决定了元素的种类,图中质子数是:8、12、9,则有三种元素;阳离子的特点是质子数大于核外电子数,则B是阳离子,符号是:Mg2+。
17.
(1)2Fe
(2)4H2
(3)5
(4)3Fe3+
【分析】
(1)
由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个铁原子表示为:2Fe;
(2)
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则4个氢分子可表示为:4H2;
(3)
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故5个碳酸根离子可表示为:5;
(4)
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故3个铁离子可表示为:3Fe3+。
18.
(1)
五
(2)
AC
B
【分析】
(1)
锶元素的质子数是38可知,锶原子的核外有5个电子层,锶元素位于元素周期表中的第五周期;锶离子带两个单位的正电荷,化学符号是。
(2)
由粒子结构示意图可知,A的质子数等于电子数,最外层也是第一层,有2个电子,属于稳定结构的原子,在C中质子数等于电子数,最外层电子数是8,属于稳定结构的原子;由图1可知,锶原子最外层电子数为2,B的最外层电子数是2,与锶原子的最外层电子数相同,化学性质相似;A的最外层也是第一层,有2个电子,但其属于稳定结构,与锶原子的化学性质不相似。答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共12小题
1.下列符号既能表示某种元素,又能表示该元素的一个原子,还能表示一种物质的是
A.
B.
C.N
D.Cu
2.下列物质中,由地壳中含量最多的金属元素和非金属元素组成的是
A.水
B.二氧化碳
C.氧化铝
D.氧化铁
3.“富硒茶”是较好的保健饮品,这里的“硒”指的是
A.原子
B.分子
C.元素
D.离子
4.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是
A.①④的化学性质比较稳定
B.①④属于稀有气体元素
C.④是一种阳离子
D.③④属于同种元素
5.关于元素的叙述,错误的是
A.元素只讲种类,不讲个数
B.化学变化前后,元素种类一定不变
C.质子数相同的一类粒子属于同种元素
D.不同种元素的根本区别是核内质子数不同
6.地壳中,含量最多的元素是
A.硅元素
B.氧元素
C.铝元素
D.钙元素
7.2021年4月,日本政府计划将核废水排入海里,其中含有大量的氚。氚一旦进入人体可能从人体内部对人造成辐射损害,如果人类持续暴露在氚的辐射下,可能会导致细脑死亡,DNA遗传损伤。下列说法正确的是
A.氚原子与氢原子的最外层电子数相同
B.氚原子与氢原子都有中子,只是数目不同
C.氚与氢元素不属于同种元素
D.氚原子与氢原子相对原子质量相同
8.下图是某品牌燕麦片,其中包装袋上写着“加钙加铁”字样,这里的钙、铁指的是
A.离子
B.元素
C.分子
D.原子
9.下列符号中即表示一种元素,又表示一个原子,还表示一种物质的是
A.O
B.Cu
C.H2
D.Na+
10.如图为钟表式元素周期表,该钟表的整点时间小时数与该元素的质子数相等。对“时针”和“分针”所指时刻的两种元素,下列说法正确的是
A.1:00对应元素的单质均由分子构成
B.6:00对应的两种元素均为金属元素
C.8:00对应的两种元素易形成化合物
D.12:00对应元素的离子符号为M
11.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为
A.硒
B.硅
C.铝
D.锡
12.下列关于元素含量的说法正确的是
A.地壳中含量最多的金属元素是Fe
B.空气中含量最多的元素是N
C.人体中含量最多的元素是C
D.海水中含量最多的元素是Na
二、非选择题,共6小题
13.写出下列符号的意义或用化学符号表示。
(1)H:______,______。
(2)5Ag:______。
(3)2个氯原子:______。
(4)Mg2+中2的含义:______。
14.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
如图所示,X是______;Y是______。
15.地壳中含量前两位的元素形成的化合物是______;地中含最高的金属元形成的氧化物的化学式为______。
16.2019年是门捷列夫发明元素周期表150周年,联合国将2019年定为“国际化学元素周期表年”。
(1)某拓展小组模仿门捷列夫用扑克牌寻找元素规律的方法,对部分元素进行排列,位置如图所示,钠元素应放入的位置是______(填序号)。
(2)我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显等多个领域。氮原子和镓离子结钩示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是______(填序号)。
A.氮化镓的化学式为GaN
B.镓的相对原子质量是69.72g
C.镓原子核内有31个中子
D.镓元素位于第三周期,属于金属元素
(3)我国科学家最新研制出一种新型石墨烯—铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如图所示,
它们的化学性质______(填“相似”或“不相似”)。在化学反应中,铝原子容易______(填“得到”或“失去”)电子。
(4)下列几种粒子的结构示意图中共有______种元素,表示阳离子的离子符号是______。
17.用元素符号或化学式表示:
(1)2个铁原子______;
(2)4个氢分子______;
(3)5个碳酸根离子______;
(4)3个铁离子______。
18.元素锶形成的粒子结构示意图如图1所示,锶的元素符号为Sr。
(1)锶元素位于元素周期表中的第______周期。锶离子的化学符号是______。
(2)图2表示的微粒中,具有相对稳定结构的原子是______(填字母序号,下同),与锶元素化学性质相似的是______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.D
【详解】
略
2.C
【详解】
略
3.C
【详解】
略
4.B
【详解】
A、最外层电子排满,微粒化学性质稳定,①④最外层电子数都为8,已排满,化学性质稳定。正确;
B、质子数=原子序数,①是第8号元素氧元素,④是第11号元素钠元素。都不是稀有气体元素,错误;
C、④质子数>电子数,是阳离子。正确;
D、元素是具有相同质子数的一类原子的总称。③④质子数相同,属于同类元素。正确。
故选B。
5.C
【详解】
A、元素是具有相同核电荷数(或核内质子数)一类原子的总称,元素是宏观概念,只讲种类,不讲个数,选项说法正确;
B、根据质量守恒定律,化学变化前后,元素种类一定不变,选项说法正确;
C、质子数相同的一类粒子不一定属于同种元素,如氖原子和水分子质子数相同,不属于同种元素,选项说法不正确;
D、元素是具有相同核电荷数(或核内质子数)一类原子的总称,所以不同种元素的根本区别是核内质子数不同,选项说法正确。
故选C。
6.B
【详解】
地壳中含量最多的前四种元素分别是:氧、硅、铝、铁,故选B。
7.A
【详解】
A、氚原子与氢原子的最外层电子数均为1,最外层电子数相同,故选项说法正确。
B、氚原子中有中子,氢原子中没有中子,故选项说法错误。
C、氚与氢元素的核内质子数相同,属于同种元素,故选项说法错误。
D、相对原子质量=质子数+中子数,氚原子与氢原子的质子数相同,中子数不同,相对原子质量不同,故选项说法错误。
故选:A。
8.B
【详解】
包装袋上写的“加钙加铁”,这里的钙、铁指的是物质的组成,表示元素;故选B。
9.B
【分析】
元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义。
【详解】
A、O属于气态非金属元素,可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项错误;
B、Cu属于金属元素,可表示铜元素,表示一个铜原子,还能表示铜这一纯净物,故选项正确;
C、
该符号是氢气的化学式,不是元素符号,故选项错误;
D、该符号是钠离子的符号,不能表示一种元素,不能表示一个原子,也不能表示一种物质,故选项错误。
故选:B。
【点睛】
10.C
【详解】
A、1:00对应的元素是氢元素和镁元素,对应元素的单质氢气是由分子构成的,镁是由原子直接构成的,错误。
B、6:00对应的元素为碳元素和镁元素,镁是金属元素,碳属于非金属元素,错误。
C、8:00对应的两种元素为氧元素和镁元素,易形成化合物氧化镁,正确。
D、12:00对应元素是镁元素,对应元素的离子符号为Mg2+,错误。
故选:C。
11.B
【详解】
地壳中元素含量由多到少依次为:氧、硅、铝、铁,地壳中含量第二的元素是硅,翻译成“矽(xi)”,如今把这种“矽”元素命名为硅;
故选:B。
12.B
【详解】
A、地壳中含量最多的金属元素是铝元素,元素符号为Al,不符合题意;
B、空气中含量最多的物质是氮气,含量最多的元素是N,符合题意;
C、人体中含量最多的物质是水,含量最多的元素是O,不符合题意;
D、海水中含量最多的物质是水,含量最多的元素是O,不符合题意。
故选B。
13.
(1)
1个氢原子
氢元素
(2)5个银原子
(3)2Cl
(4)1个镁离子带有2个单位的正电荷
【详解】
(1)元素符号可表示一种元素、一个原子,H可表示氢元素、1个氢原子;
(2)当元素符号前面加上数字就只有微观意义,表示几个这样的原子,故5Ag表示5个银原子;
(3)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,2个氯原子可表示为:2Cl;
(4)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。离子符号右上角的数字表示每个离子所带电荷数,所以Mg2+中2的含义每个镁离子带2个单位的正电荷。
14.分子
原子核
【详解】
分子可分成原子,故X是分子;原子是由原子核和核外电子构成,故Y是原子核。
15.SiO2
Al2O3
【详解】
地壳中含量第一的元素是氧,第二位是硅,故填:SiO2;
地壳中含量最多的金属元素是铝,其氧化物为氧化铝,又称三氧化二铝,故填:Al2O3。
16.
(1)③
(2)A
(3)
不相似
失去
(4)
3
Mg2+
【分析】
(1)
钠原子的最外层电子数是1,和氢的最外层电子数相同,同一主族最外层电子数相同;则钠元素扑克牌应放入的位置是③。
(2)
A、根据镓离子结钩示意图,镓显+3价,氮最外层5个电子易得3个电子,显-3价,所以氮化镓表示GaN,故正确;
B、由元素周期表的信息可知,镓的相对原子质量为69.72,没有单位g,故错误;
C、元素周期表中,左上角是原子序数,原子序数=核内质子数=核电荷数,所以镓的核内质子数为31,不是中子数,故错误;
D、电子层数决定周期数,根据镓离子结钩示意图,得出镓原子核外电子层数有4层,位于第四周期,镓元素带有钅字旁,属于金属元素,故错误。
故选A。
(3)
根据信息图,碳原子的结钩示意图、铝原子的结钩示意图,可见最外层电子数不相等,化学性质不相似;铝原子最外层电子数是3,小于4,铝原子容易 失去电子。
(4)
质子数决定了元素的种类,图中质子数是:8、12、9,则有三种元素;阳离子的特点是质子数大于核外电子数,则B是阳离子,符号是:Mg2+。
17.
(1)2Fe
(2)4H2
(3)5
(4)3Fe3+
【分析】
(1)
由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个铁原子表示为:2Fe;
(2)
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则4个氢分子可表示为:4H2;
(3)
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故5个碳酸根离子可表示为:5;
(4)
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故3个铁离子可表示为:3Fe3+。
18.
(1)
五
(2)
AC
B
【分析】
(1)
锶元素的质子数是38可知,锶原子的核外有5个电子层,锶元素位于元素周期表中的第五周期;锶离子带两个单位的正电荷,化学符号是。
(2)
由粒子结构示意图可知,A的质子数等于电子数,最外层也是第一层,有2个电子,属于稳定结构的原子,在C中质子数等于电子数,最外层电子数是8,属于稳定结构的原子;由图1可知,锶原子最外层电子数为2,B的最外层电子数是2,与锶原子的最外层电子数相同,化学性质相似;A的最外层也是第一层,有2个电子,但其属于稳定结构,与锶原子的化学性质不相似。答案第1页,共2页
答案第1页,共2页
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
