第三单元 海水中的化单元练习—2021-2022学年九年级化学鲁教版(五四制)全一册(含解析)
文档属性
| 名称 | 第三单元 海水中的化单元练习—2021-2022学年九年级化学鲁教版(五四制)全一册(含解析) |  | |
| 格式 | zip | ||
| 文件大小 | 292.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-29 22:46:16 | ||
图片预览


文档简介
第三单元
海水中的化学
——2021-2022学年化学鲁教版(五四制)九年级全一册单元练习
1.利用蒸发、冷凝的方法可以从海水中获取淡水,下列叙述正确的是(
)
A.蒸发时,水分子的运动速率加快
B.蒸发时,海水的质量变大
C.冷凝时,水分子之间的间隔不变
D.冷凝时,淡水的体积不变
2.物质的性质与用途密切相关,下列做法不合理的是(
)
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、造纸、洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁)用食盐水清洗
3.海洋是人类的资源宝库。下列有关叙述中错误的是(
)
A.海水晒盐的基本原理是蒸发结晶
B.海水淡化的常用方法是多级闪急蒸馏法
C.海底蕴藏的可燃冰的主要成分是干冰
D.利用海水涨落推动水轮机转动,从而可以发电
4.下列有关海洋资源及其综合利用的说法错误的是(
)
A.海水制镁应用了富集提纯的思想
B.蒸馏法淡化海水是利用了海水中各组分的颗粒大小不同
C.海底的可燃冰大量燃烧后,也会造成温室效应
D.侯氏制碱法生产过程需要同合成氨厂联合,故称联合制碱法
5.在教材粗盐提纯实验中,有以下操作:
①用量筒取水时俯视读数
②第一次称量时右盘忘记放纸片
③加热过程中有液体溅出
④滤液浑浊就蒸发
⑤转移固体不完整
⑥提前撤离酒精灯
导致氯化钠产率偏低的可能原因是( )
A.②③④⑤
B.①②④⑤
C.①②③
D.②③⑤
6.欲除去粗盐中的可溶性杂质(氯化钙、氯化镁、硫酸钠)得到精盐,不能选用的试剂是(
)
A.碳酸钠溶液
B.氢氧化钾溶液
C.稀盐酸
D.氢氧化钡溶液
7.下列物质的名称、俗称、化学式和分类对应完全正确的一组是(
)
A.氧化钙、熟石灰、CaO、氧化物
B.氯化氢、盐酸、HCl、酸
C.氢氧化钠、火碱、NaOH、碱
D.碳酸氢钠、苏打、、盐
8.在“粗盐中难溶性杂质的去除”实验中,玻璃棒的用途不正确的是(
)
A.称取粗盐后,把粗盐研磨细
B.溶解时搅拌,加速粗盐溶解
C.称量精盐前,把精盐固体转移到纸上
D.蒸发时搅拌,防止局部温度过高,造成液滴飞溅
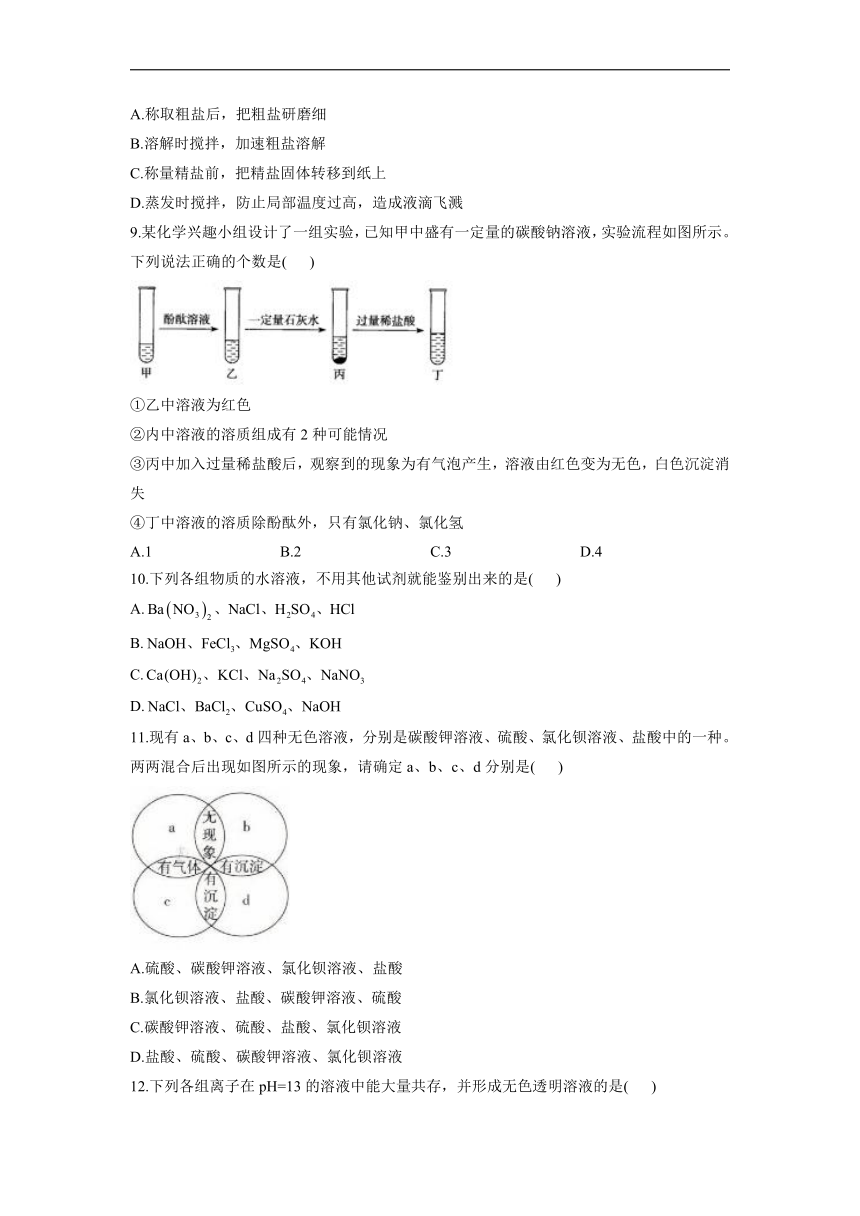
9.某化学兴趣小组设计了一组实验,已知甲中盛有一定量的碳酸钠溶液,实验流程如图所示。
下列说法正确的个数是(
)
①乙中溶液为红色
②内中溶液的溶质组成有2种可能情况
③丙中加入过量稀盐酸后,观察到的现象为有气泡产生,溶液由红色变为无色,白色沉淀消失
④丁中溶液的溶质除酚酞外,只有氯化钠、氯化氢
A.1
B.2
C.3
D.4
10.下列各组物质的水溶液,不用其他试剂就能鉴别出来的是(
)
A.
B.
C.
D.
11.现有a、b、c、d四种无色溶液,分别是碳酸钾溶液、硫酸、氯化钡溶液、盐酸中的一种。两两混合后出现如图所示的现象,请确定a、b、c、d分别是(
)
A.硫酸、碳酸钾溶液、氯化钡溶液、盐酸
B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸
C.碳酸钾溶液、硫酸、盐酸、氯化钡溶液
D.盐酸、硫酸、碳酸钾溶液、氯化钡溶液
12.下列各组离子在pH=13的溶液中能大量共存,并形成无色透明溶液的是(
)
A.
B.
C.
D.
13.下列框图中的物质均为初中化学常见的物质,已知D在农业生产中常用于改良酸性土壤,下图是它们之间的相互转化关系(部分生成物未标出)。请回答:
(1)请写出下列物质的化学式:D_________,G_________,H_________。
(2)气体C的用途是_________(写一条),固体B的俗称是_________。
(3)请写出反应G+EH的化学方程式:_________。
(4)该转化关系中涉及的基本反应类型有_________种。
14.氯化钠是必不可少的生活用品,更是重要的化工原料。
(1)“烧干海水变银山”是郭沫若对海南鸴歌海盐场的赞美诗作。海水“晒盐”是通过______________(填“蒸发结晶”或“降温结晶”)的方法获取食盐。
(2)抗日战争期间,我国著名制碱专家侯德榜打破西方国家对制碱技术的垄断,创立
“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如下:
①制碱过程中,可以循环利用的物质是______________,产物中可作氮肥的是______________;
②产物中
比先结晶析出。请结合生产原理及图解释其原因:______________。
15.重庆多地曾出现过盐井,从天然盐井中获取粗盐(含泥沙、等杂质)为了除去以上杂质得到精盐,小明设计如下实验。
【提示】杂质含量较少,不考虑微溶物形成沉淀
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和______。
(2)沉淀b所含物质为
和______。
(3)物质X是______。
(4)滤液c中加入稀盐酸后发生中和反应的化学方程式为______。
(5)为了证明滴加的溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有______。
A.B.
C、
D.KCl
答案以及解析
1.答案:A
解析:分子是不断运动的,温度升高,分子的运动速率加快;蒸发时,由于水分子不断运动到空气中,因此海水的质量会减小;冷凝时,水分子之间的间隔会变小,淡水的体积缩小。
2.答案:D
解析:碳酸钙和氢氧化镁均不与食盐水发生反应,食盐水不能除去水垢,D错误。
3.答案:C
解析:NaCl的溶解度受温度变化的影响小,从海水中获得粗盐主要利用阳光和自然风蒸发水分,使氯化钠结晶出来,基本原理是蒸发结晶,A正确。海水淡化的常用方法是多级闪急蒸馏法,是利用减压时水的沸点降低,使热盐水依次流经若干个压力逐渐降低的闪蒸室,逐渐蒸发降温,再将水蒸气冷凝成水,B正确。海底蕴藏的可燃冰的主要成分是甲烷的水合物,不是干冰,C错误。海水涨落的过程中伴随着巨大的能量,利用海水涨落推动水轮机转动,可以发电,D正确。
4.答案:B
解析:海水制镁应用了富集提纯的思想,A正确。蒸馏法淡化海水是利用海水中各成份的沸点不同进行分离的,B错误。可燃冰主要成分是甲烷,大量燃烧后会生成二氧化碳,也会造成温室效应,C正确。侯氏制碱法生产过程中需要通入氨气,需要同合成氨厂联合,故称联合制碱法,D正确。
5.答案:D
6.答案:B
7.答案:C
解析:氧化钙俗称生石灰,A错误;盐酸是氯化氢气体的水溶液,B错误;氢氧化钠俗称火碱、烧碱、苛性钠,其化学式为NaOH,属于碱,C正确;碳酸氢钠俗称小苏打,其化学式为,苏打是碳酸钠的俗称,D错误。
8.答案:A
解析:称取粗盐后,把粗盐硏磨细,应用研钵和研杵进行,A错误。溶解时玻璃棒的作用是搅拌,加速粗盐溶解,B正确。称量精盐前,可用玻璃棒把精盐固体转移到纸上,C正确。蒸发时搅拌,防止因局部温度过高,造成液滴飞溅,D正确。
9.答案:B
解析:①碳酸钠溶液显碱性,能使酚酞溶液变红色,故乙中溶液为红色,正确。②碳酸钠能与石灰水反应生成碳酸钙沉淀和氢氧化钠,丙中溶液的溶质组成有氢氧化钠、氢氧化钠和碳酸钠、氢氧化钠和氢氧化钙3种可能情况,错误。③丙中加入过量稀盐酸后,碳酸钙沉淀能与稀盐酸反应生成二氧化碳气体,观察到的现象为有气泡产生,白色沉淀消失;稀盐酸过量,最终溶液显酸性,溶液由红色变为无色,正确。④丁中溶液的溶质除酚酞外,还有氯化钠、氯化氢、氯化钙,错误。故选B。
10.答案:D
解析:A项组内四种物质的溶液两两混合时,与反应能产生白色沉淀,但其余两两混合均没有明显现象,故A不符合题意;B项中溶液是黄色的,能与溶液反应产生红褐色沉淀的是NaOH、KOH溶液,无法鉴别NaOH、KOH溶液,故B不符合题意;C项组内四种物质的溶液两两混合时,均没有明显现象,故C不符合题意;D项中溶液是蓝色的,能与溶液反应产生蓝色沉淀的是NaOH溶液,能与溶液反应产生白色沉淀的是溶液,与溶液混合无明显现象的是氯化钠溶液,故D符合题意。
11.答案:D
解析:观察题图可知:d能够和c、b都产生沉淀,且c能够和a反应产生气体,依据氯化钡溶液和碳酸钾溶液、硫酸反应都能产生沉淀,其中碳酸钾溶液能够和盐酸反应产生气体,可知d是氯化钡溶液、c是碳酸钾溶液、a是盐酸,则b是硫酸,代入验证,符合转化关系,D符合题意。
12.答案:A
解析:pH=13的溶液显碱性,溶液中含有大量的,A项中离子在碱性条件下均不反应,且溶液为无色,正确;B项中与结合生成水和二氧化碳,与结合生成水,因此不能大量共存,错误;C项中和结合生成氨气和水,不能大量共存,错误;D项中和结合生成氢氧化铜沉淀,不能大量共存,错误。
13.答案:(1);;(2)作气体肥料(或灭火,合理即可);生石灰
(3)(4)三
解析:已知D在农业生产中常用于改良酸性土壤,则D是,B和水反应能生成,则B为CaO。A高温下生成气体C和固体B,可推知A是碳酸钙,C是二氧化碳。D与碳酸钠溶液反应得到E溶液,则E是氢氧化钠。H是蓝色沉淀,则H是氢氧化铜,E与G反应生成H,由于F与稀硫酸反应生成G,则G是硫酸铜。(1)D是氢氧化钙,其化学式为;G是硫酸铜,其化学式为;H是氢氧化铜,其化学式为。
(2)气体C是二氧化碳,可作气体肥料、灭火剂等;B是氧化钙,其俗称是生石灰。
(3)G+EH是硫酸铜与氢氧化钠的反应,化学方程式为。
(4)AB+C属于分解反应;B+水D属于化合反应;其余反应均为复分解反应,涉及的基本反应类型有三种。
14.答案:(1)蒸发结晶(2)①;
②同温下碳酸氢钠的溶解度比氯化铵小,且反应时生成碳酸氢钠的质量比氯化铵大。
解析:(2)①由生产原理示意图可以看出,碳酸氢钠分解生成的二氧化碳能再作为原料,故二氧化碳可循环利用。氯化铵中含有N、P、K中的氮元素,可供植物生长所需,可作氮肥。②由化学方程式可知,每生成84g碳酸氢钠,会有53.5g氯化铵生成,且同温度下氯化铵的溶解度比碳酸氢钠大,故碳酸氢钠先达到饱和,先结晶析出。
15.答案:(1).
漏斗
(2).
(3).
(4).
(5).
C
解析:
(2)加入氢氧化钡溶液发生的反应是:、
、,沉淀b中含有和。
(3)X溶液的作用是除去和过量的,所以是碳酸钠溶液。
(4)滤液c中含有杂质氢氧化钠和碳酸钠,加入过量稀盐酸可以将它们除去,氢氧化钠与盐酸的反应是中和反应。
(5)氢氧化钡溶液过量时,上层清液中含有,碳酸钾、硫酸钠都能与反应生成白色沉淀,但碳酸钾也能与反应生成白色沉淀,故选C。
海水中的化学
——2021-2022学年化学鲁教版(五四制)九年级全一册单元练习
1.利用蒸发、冷凝的方法可以从海水中获取淡水,下列叙述正确的是(
)
A.蒸发时,水分子的运动速率加快
B.蒸发时,海水的质量变大
C.冷凝时,水分子之间的间隔不变
D.冷凝时,淡水的体积不变
2.物质的性质与用途密切相关,下列做法不合理的是(
)
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、造纸、洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁)用食盐水清洗
3.海洋是人类的资源宝库。下列有关叙述中错误的是(
)
A.海水晒盐的基本原理是蒸发结晶
B.海水淡化的常用方法是多级闪急蒸馏法
C.海底蕴藏的可燃冰的主要成分是干冰
D.利用海水涨落推动水轮机转动,从而可以发电
4.下列有关海洋资源及其综合利用的说法错误的是(
)
A.海水制镁应用了富集提纯的思想
B.蒸馏法淡化海水是利用了海水中各组分的颗粒大小不同
C.海底的可燃冰大量燃烧后,也会造成温室效应
D.侯氏制碱法生产过程需要同合成氨厂联合,故称联合制碱法
5.在教材粗盐提纯实验中,有以下操作:
①用量筒取水时俯视读数
②第一次称量时右盘忘记放纸片
③加热过程中有液体溅出
④滤液浑浊就蒸发
⑤转移固体不完整
⑥提前撤离酒精灯
导致氯化钠产率偏低的可能原因是( )
A.②③④⑤
B.①②④⑤
C.①②③
D.②③⑤
6.欲除去粗盐中的可溶性杂质(氯化钙、氯化镁、硫酸钠)得到精盐,不能选用的试剂是(
)
A.碳酸钠溶液
B.氢氧化钾溶液
C.稀盐酸
D.氢氧化钡溶液
7.下列物质的名称、俗称、化学式和分类对应完全正确的一组是(
)
A.氧化钙、熟石灰、CaO、氧化物
B.氯化氢、盐酸、HCl、酸
C.氢氧化钠、火碱、NaOH、碱
D.碳酸氢钠、苏打、、盐
8.在“粗盐中难溶性杂质的去除”实验中,玻璃棒的用途不正确的是(
)
A.称取粗盐后,把粗盐研磨细
B.溶解时搅拌,加速粗盐溶解
C.称量精盐前,把精盐固体转移到纸上
D.蒸发时搅拌,防止局部温度过高,造成液滴飞溅
9.某化学兴趣小组设计了一组实验,已知甲中盛有一定量的碳酸钠溶液,实验流程如图所示。
下列说法正确的个数是(
)
①乙中溶液为红色
②内中溶液的溶质组成有2种可能情况
③丙中加入过量稀盐酸后,观察到的现象为有气泡产生,溶液由红色变为无色,白色沉淀消失
④丁中溶液的溶质除酚酞外,只有氯化钠、氯化氢
A.1
B.2
C.3
D.4
10.下列各组物质的水溶液,不用其他试剂就能鉴别出来的是(
)
A.
B.
C.
D.
11.现有a、b、c、d四种无色溶液,分别是碳酸钾溶液、硫酸、氯化钡溶液、盐酸中的一种。两两混合后出现如图所示的现象,请确定a、b、c、d分别是(
)
A.硫酸、碳酸钾溶液、氯化钡溶液、盐酸
B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸
C.碳酸钾溶液、硫酸、盐酸、氯化钡溶液
D.盐酸、硫酸、碳酸钾溶液、氯化钡溶液
12.下列各组离子在pH=13的溶液中能大量共存,并形成无色透明溶液的是(
)
A.
B.
C.
D.
13.下列框图中的物质均为初中化学常见的物质,已知D在农业生产中常用于改良酸性土壤,下图是它们之间的相互转化关系(部分生成物未标出)。请回答:
(1)请写出下列物质的化学式:D_________,G_________,H_________。
(2)气体C的用途是_________(写一条),固体B的俗称是_________。
(3)请写出反应G+EH的化学方程式:_________。
(4)该转化关系中涉及的基本反应类型有_________种。
14.氯化钠是必不可少的生活用品,更是重要的化工原料。
(1)“烧干海水变银山”是郭沫若对海南鸴歌海盐场的赞美诗作。海水“晒盐”是通过______________(填“蒸发结晶”或“降温结晶”)的方法获取食盐。
(2)抗日战争期间,我国著名制碱专家侯德榜打破西方国家对制碱技术的垄断,创立
“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如下:
①制碱过程中,可以循环利用的物质是______________,产物中可作氮肥的是______________;
②产物中
比先结晶析出。请结合生产原理及图解释其原因:______________。
15.重庆多地曾出现过盐井,从天然盐井中获取粗盐(含泥沙、等杂质)为了除去以上杂质得到精盐,小明设计如下实验。
【提示】杂质含量较少,不考虑微溶物形成沉淀
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和______。
(2)沉淀b所含物质为
和______。
(3)物质X是______。
(4)滤液c中加入稀盐酸后发生中和反应的化学方程式为______。
(5)为了证明滴加的溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有______。
A.B.
C、
D.KCl
答案以及解析
1.答案:A
解析:分子是不断运动的,温度升高,分子的运动速率加快;蒸发时,由于水分子不断运动到空气中,因此海水的质量会减小;冷凝时,水分子之间的间隔会变小,淡水的体积缩小。
2.答案:D
解析:碳酸钙和氢氧化镁均不与食盐水发生反应,食盐水不能除去水垢,D错误。
3.答案:C
解析:NaCl的溶解度受温度变化的影响小,从海水中获得粗盐主要利用阳光和自然风蒸发水分,使氯化钠结晶出来,基本原理是蒸发结晶,A正确。海水淡化的常用方法是多级闪急蒸馏法,是利用减压时水的沸点降低,使热盐水依次流经若干个压力逐渐降低的闪蒸室,逐渐蒸发降温,再将水蒸气冷凝成水,B正确。海底蕴藏的可燃冰的主要成分是甲烷的水合物,不是干冰,C错误。海水涨落的过程中伴随着巨大的能量,利用海水涨落推动水轮机转动,可以发电,D正确。
4.答案:B
解析:海水制镁应用了富集提纯的思想,A正确。蒸馏法淡化海水是利用海水中各成份的沸点不同进行分离的,B错误。可燃冰主要成分是甲烷,大量燃烧后会生成二氧化碳,也会造成温室效应,C正确。侯氏制碱法生产过程中需要通入氨气,需要同合成氨厂联合,故称联合制碱法,D正确。
5.答案:D
6.答案:B
7.答案:C
解析:氧化钙俗称生石灰,A错误;盐酸是氯化氢气体的水溶液,B错误;氢氧化钠俗称火碱、烧碱、苛性钠,其化学式为NaOH,属于碱,C正确;碳酸氢钠俗称小苏打,其化学式为,苏打是碳酸钠的俗称,D错误。
8.答案:A
解析:称取粗盐后,把粗盐硏磨细,应用研钵和研杵进行,A错误。溶解时玻璃棒的作用是搅拌,加速粗盐溶解,B正确。称量精盐前,可用玻璃棒把精盐固体转移到纸上,C正确。蒸发时搅拌,防止因局部温度过高,造成液滴飞溅,D正确。
9.答案:B
解析:①碳酸钠溶液显碱性,能使酚酞溶液变红色,故乙中溶液为红色,正确。②碳酸钠能与石灰水反应生成碳酸钙沉淀和氢氧化钠,丙中溶液的溶质组成有氢氧化钠、氢氧化钠和碳酸钠、氢氧化钠和氢氧化钙3种可能情况,错误。③丙中加入过量稀盐酸后,碳酸钙沉淀能与稀盐酸反应生成二氧化碳气体,观察到的现象为有气泡产生,白色沉淀消失;稀盐酸过量,最终溶液显酸性,溶液由红色变为无色,正确。④丁中溶液的溶质除酚酞外,还有氯化钠、氯化氢、氯化钙,错误。故选B。
10.答案:D
解析:A项组内四种物质的溶液两两混合时,与反应能产生白色沉淀,但其余两两混合均没有明显现象,故A不符合题意;B项中溶液是黄色的,能与溶液反应产生红褐色沉淀的是NaOH、KOH溶液,无法鉴别NaOH、KOH溶液,故B不符合题意;C项组内四种物质的溶液两两混合时,均没有明显现象,故C不符合题意;D项中溶液是蓝色的,能与溶液反应产生蓝色沉淀的是NaOH溶液,能与溶液反应产生白色沉淀的是溶液,与溶液混合无明显现象的是氯化钠溶液,故D符合题意。
11.答案:D
解析:观察题图可知:d能够和c、b都产生沉淀,且c能够和a反应产生气体,依据氯化钡溶液和碳酸钾溶液、硫酸反应都能产生沉淀,其中碳酸钾溶液能够和盐酸反应产生气体,可知d是氯化钡溶液、c是碳酸钾溶液、a是盐酸,则b是硫酸,代入验证,符合转化关系,D符合题意。
12.答案:A
解析:pH=13的溶液显碱性,溶液中含有大量的,A项中离子在碱性条件下均不反应,且溶液为无色,正确;B项中与结合生成水和二氧化碳,与结合生成水,因此不能大量共存,错误;C项中和结合生成氨气和水,不能大量共存,错误;D项中和结合生成氢氧化铜沉淀,不能大量共存,错误。
13.答案:(1);;(2)作气体肥料(或灭火,合理即可);生石灰
(3)(4)三
解析:已知D在农业生产中常用于改良酸性土壤,则D是,B和水反应能生成,则B为CaO。A高温下生成气体C和固体B,可推知A是碳酸钙,C是二氧化碳。D与碳酸钠溶液反应得到E溶液,则E是氢氧化钠。H是蓝色沉淀,则H是氢氧化铜,E与G反应生成H,由于F与稀硫酸反应生成G,则G是硫酸铜。(1)D是氢氧化钙,其化学式为;G是硫酸铜,其化学式为;H是氢氧化铜,其化学式为。
(2)气体C是二氧化碳,可作气体肥料、灭火剂等;B是氧化钙,其俗称是生石灰。
(3)G+EH是硫酸铜与氢氧化钠的反应,化学方程式为。
(4)AB+C属于分解反应;B+水D属于化合反应;其余反应均为复分解反应,涉及的基本反应类型有三种。
14.答案:(1)蒸发结晶(2)①;
②同温下碳酸氢钠的溶解度比氯化铵小,且反应时生成碳酸氢钠的质量比氯化铵大。
解析:(2)①由生产原理示意图可以看出,碳酸氢钠分解生成的二氧化碳能再作为原料,故二氧化碳可循环利用。氯化铵中含有N、P、K中的氮元素,可供植物生长所需,可作氮肥。②由化学方程式可知,每生成84g碳酸氢钠,会有53.5g氯化铵生成,且同温度下氯化铵的溶解度比碳酸氢钠大,故碳酸氢钠先达到饱和,先结晶析出。
15.答案:(1).
漏斗
(2).
(3).
(4).
(5).
C
解析:
(2)加入氢氧化钡溶液发生的反应是:、
、,沉淀b中含有和。
(3)X溶液的作用是除去和过量的,所以是碳酸钠溶液。
(4)滤液c中含有杂质氢氧化钠和碳酸钠,加入过量稀盐酸可以将它们除去,氢氧化钠与盐酸的反应是中和反应。
(5)氢氧化钡溶液过量时,上层清液中含有,碳酸钾、硫酸钠都能与反应生成白色沉淀,但碳酸钾也能与反应生成白色沉淀,故选C。
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
