5.2化学反应的表示课时练习--2021-2022学年九年级化学鲁教版上册(word版 含解析)
文档属性
| 名称 | 5.2化学反应的表示课时练习--2021-2022学年九年级化学鲁教版上册(word版 含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 155.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-30 00:00:00 | ||
图片预览



文档简介
第五单元定量研究化学反应第二节化学反应的表示课时练习鲁教版初中化学九年级上册
一、单选题(共12题)
1.下列化学方程式中,书写正确的是( )
A.H2OH2↑+O↑
B.S+O2SO2
C.Fe+CuSO4=FeSO4+Cu↓
D.NH4HCO3NH3↑+H2O+CO2↑
2.根据化学方程式不能获得该反应的信息是(
)
A.反应物和生成物
B.反应中各物质间粒子个数比
C.化学反应的快慢
D.反应的条件
3.化学方程式不能提供的信息是(
)
A.哪些物质参加化学反应,生成物是什么
B.化学反应的是在什么条件下进行的
C.各物质之间的质量关系是多少
D.化学反应速度的快慢
4.下列化学方程式书写正确的是(
)
A.S
+O2↑SO2
B.HgO=Hg
+
O2
C.Fe
+
CuSO4
=Cu
+
FeSO4
D.2P
+
5O2P2O5
5.通过化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,不能得出的结论是(
)
A.该反应中的反应物和生成物
B.化学反应的快慢
C.反应发生所需的条件
D.各反应物和生成物的质量比
6.下列化学方程式书写完全正确的是(
)
A.铁在氧气中燃烧的化学方程式为:4Fe+3O2
2
Fe2O3
B.用双氧水和二氧化锰制氧气:2H2O22H2↑+
O2↑
C.用氯酸钾和二氧化锰为原料制氧气:2KClO32KCl
+3
O2↑
D.镁条燃烧
2Mg
+
O22MgO
7.化学是在原子、分子水平上研究物质组成、结构、性质以及变化规律的一门基础自然学科。下列有关说法中,错误的是(
)
A.组成:由两种或两种以上元素组成的物质属于化合物
B.结构:分子、原子、离子是构成物质的三种基本微粒
C.性质:水在三态变化过程中,其化学性质保持不变
D.变化,则R中一定含碳、氢、氧三种元素
8.如图是某反应前后分子种类变化的微观示意图。下列说法正确的是(
)
A.反应前后分子个数不变
B.反应中涉及到3种氧化物
C.反应中甲、乙分子个数比为1:1
D.丙的相对分子质量为64
9.下列化学方程式书写正确的是(
)
A.S+O2↑═SO2↑
B.CaO+Na2CO3=CaCO3↓+Na2O
C.Zn+H2SO4═ZnSO4+H2↑
D.CaCl2+H2O+CO2=CaCO3↓+2HCl
10.已知常温下铜与稀硝酸反应:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2X↑。下列说法不正确的是(
)
A.物质X属于氧化物
B.铜的化合价由0变为+2
C.物质X的化学式为NO
D.该实验要在通风橱内完成
11.如图是一种处理汽车尾气的微观示意图,下列说法错误的是(
)
A.分子在化学变化中不可再分
B.反应前后分子的数目发生改变
C.参加反应的甲和乙的分子个数比为1:1
D.每个丁分子由2个氧原子和1个碳原子构成
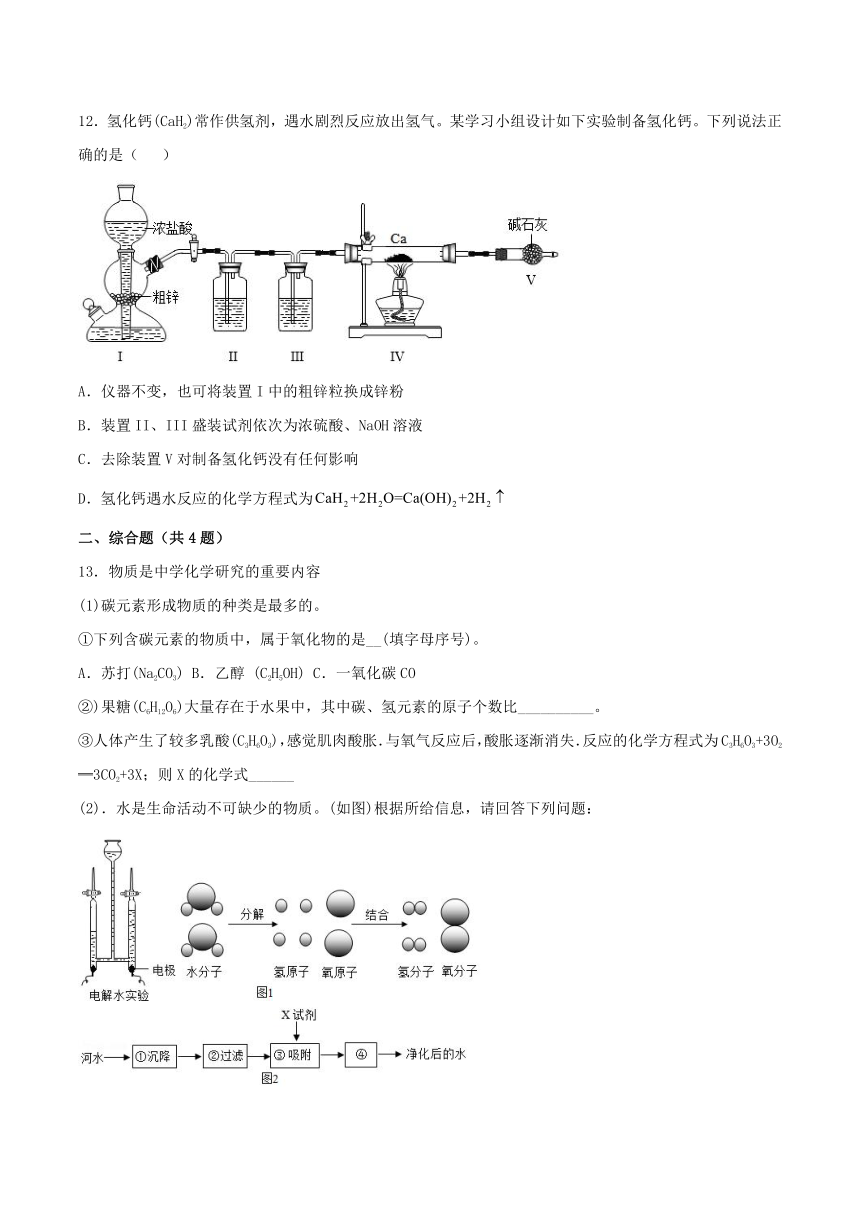
12.氢化钙(CaH2)常作供氢剂,遇水剧烈反应放出氢气。某学习小组设计如下实验制备氢化钙。下列说法正确的是(
)
A.仪器不变,也可将装置I中的粗锌粒换成锌粉
B.装置II、III盛装试剂依次为浓硫酸、NaOH溶液
C.去除装置V对制备氢化钙没有任何影响
D.氢化钙遇水反应的化学方程式为
二、综合题(共4题)
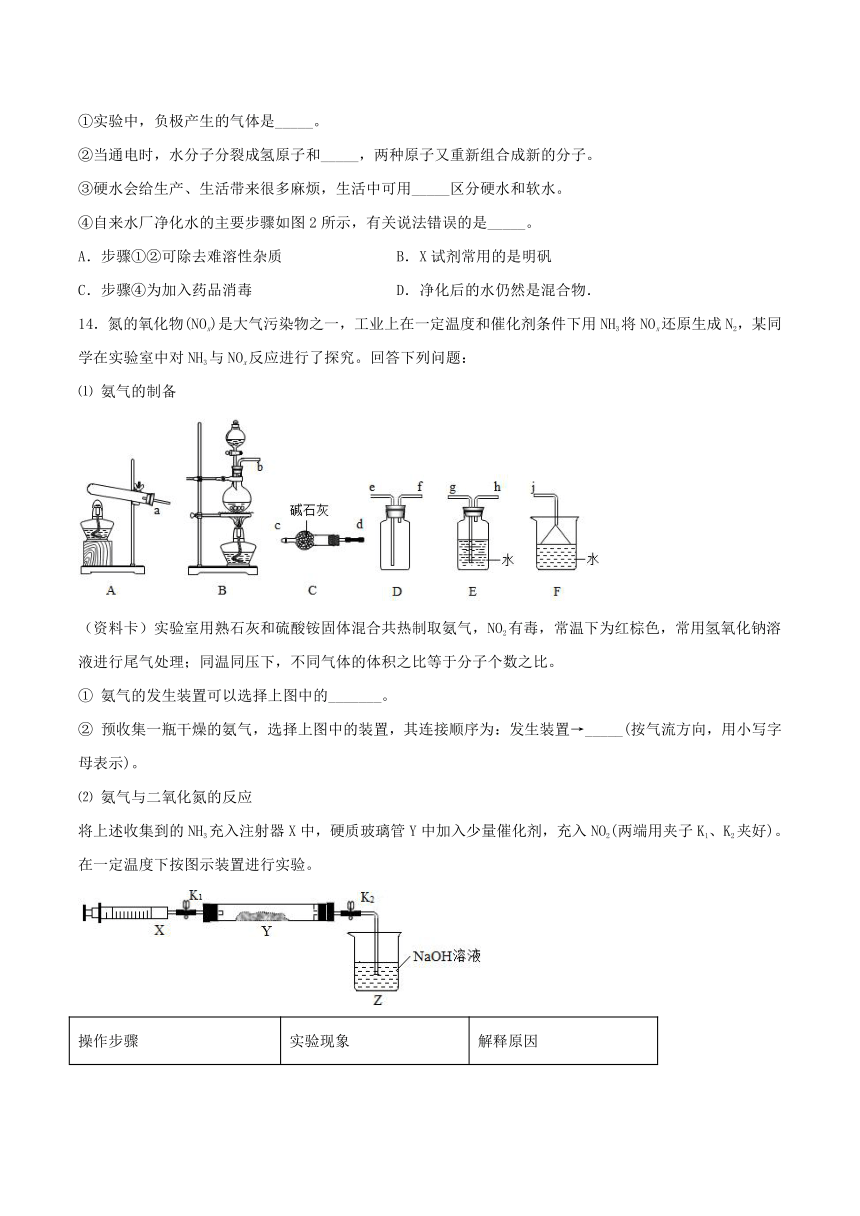
13.物质是中学化学研究的重要内容
(1)碳元素形成物质的种类是最多的。
①下列含碳元素的物质中,属于氧化物的是__(填字母序号)。
A.苏打(Na2CO3)
B.乙醇
(C2H5OH)
C.一氧化碳CO
②)果糖(C6H12O6)大量存在于水果中,其中碳、氢元素的原子个数比__________。
③人体产生了较多乳酸(C3H6O3),感觉肌肉酸胀.与氧气反应后,酸胀逐渐消失.反应的化学方程式为C3H6O3+3O2═3CO2+3X;则X的化学式______
(2).水是生命活动不可缺少的物质。(如图)根据所给信息,请回答下列问题:
①实验中,负极产生的气体是_____。
②当通电时,水分子分裂成氢原子和_____,两种原子又重新组合成新的分子。
③硬水会给生产、生活带来很多麻烦,生活中可用_____区分硬水和软水。
④自来水厂净化水的主要步骤如图2所示,有关说法错误的是_____。
A.步骤①②可除去难溶性杂质
B.X试剂常用的是明矾
C.步骤④为加入药品消毒
D.净化后的水仍然是混合物.
14.氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
⑴
氨气的制备
(资料卡)实验室用熟石灰和硫酸铵固体混合共热制取氨气,NO2有毒,常温下为红棕色,常用氢氧化钠溶液进行尾气处理;同温同压下,不同气体的体积之比等于分子个数之比。
①
氨气的发生装置可以选择上图中的_______。
②
预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→_____(按气流方向,用小写字母表示)。
⑵
氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
操作步骤
实验现象
解释原因
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中
①
Y管中______________
②
反应的化学方程式:
__________________
将注射器活塞退回原处并固定,待装置恢复到室温
Y管中有少量水珠
生成的气态水凝集
打开K2
③
_________________
④
_________________
15.阅读下面的资料,回答有关问题
新型灭菌消毒剂——ClO2
目前,新冠肺炎依然疫情肆虐全球。为抑制新冠病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂——ClO2.在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,熔点-59℃,沸点11°C.在常温下,1L水中大约能溶解2.9gClO2.ClO2受热或者见光易分解,具有强氧化性和很强的腐蚀性。含有2%的ClO2和0.085%Na2CO3的水溶液无色、无臭、无腐蚀性,常温下稳定,不易分解;该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良,高效安全的消毒剂。我国从2000年起就逐渐用ClO2取代氯气(Cl2)对饮用水进行消毒。
(1)ClO2的名称是_____,分子中氯元素的化合价是_____。
(2)下列消毒剂中,不属于“含氯消毒剂”的是_____(填字母序号)。
A
84消毒液(含NaClO)
B
双氧水
C
氯气
D
过氧乙酸(C2H4O3)
(3)ClO2的化学性质有_____(写出两点即可)。
(4)下列有关ClO2的说法正确的是_____(填字母序号)。
A
0℃时,ClO2
为黄绿色气体
B
常温下,100g
水中大约能溶解
0.29gClO2
C
用棕色试剂瓶盛装
ClO2
并置于冷暗处保存
D
ClO2
溶液浓度越小杀菌效果越差
(5)ClO2
遇热水生成次氯酸(HClO)和两种气态单质。写出该反应的化学方程式:_____(ClO2
与水的化学计量数之比为
4:1)。
16.某同学对催化剂产生了兴趣,通过查资料了解到氧化铜、氧化铁等都能加速氯酸钾的分解。为了证明氧化铜能加快氯酸钾的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关记录见下表:
实验序号
KClO3质量
加入其它的物质
待测数据
1
1.2g
无其它物质
2
1.2g
加入少量的CuO
(1)上述实验中的“待测数据”指_____。
(2)从如图仪器中选择合适的并加以组装_____。
(3)为探究CuO在实验2中是否起催化作用,还需探究的氧化铜的_____在化学反应前后不变。其反应的文字表达式为_____。
参考答案
1.D
【详解】
A、该化学方程式中氧气的化学式书写错误,正确的化学方程式应为2H2O2H2↑+O2↑;
B、该化学方程式的反应条件应为点燃,正确的化学方程式为:S+O2SO2;
C、该化学方程式反应物中铁是固体,铜的后面不需标注↓,正确的化学方程式应为:Fe+CuSO4=FeSO4+Cu;
D、该化学方程式书写完全正确;
故选D。
2.C
【详解】
A、由化学方程式,可以确定“═”左边的是反应物,右边为生成物,故选项错误。
B、由化学方程式,根据化学式前的化学计量数可以确定反应中各物质间粒子个数比,故选项错误。
C、由化学方程式,无法确定化学反应的快慢,故选项正确。
D、由化学方程式,可以看出反应发生所需要的条件,故选项错误。
故选:C。
3.D
【详解】
A、化学方程式等号前是反应物,等号后是生成物,能提供哪些物质参加化学反应,生成物是什么,不符合题意。
B、等号上方和下方表示反应条件,能提供化学反应是在什么条件下进行的,不符合题意。
C、化学方程式能反映参加反应各物质质量比例关系,不符合题意。
D、化学方程式不能体现化学反应速度的快慢,符合题意。
故选:D。
4.C
【详解】
A、化学方程式中氧气是反应物,氧气后面不需要标注气体符号↑,正确的化学方程式为:,书写不正确,不符合题意;
B、化学方程式没有配平,缺少反应条件,正确的化学方程式:,书写不正确,不符合题意;
C、铁和硫酸铜反应生成铜和硫酸亚铁,Fe
+
CuSO4
=Cu
+
FeSO4,该反应化学方程式书写正确,符合题意;
D、化学方程式没有配平,正确的化学方程式为:,书写不正确,不符合题意;
答案:C。
5.B
【详解】
A、化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,可得出反应物是铁和稀盐酸,生成物是氯化亚铁和氢气,说法正确,不符合题意;
B、化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,无法确定化学反应的快慢,说法错误,不符合题意;
C、化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,可得出反应所需的条件是常温常压,说法正确,不符合题意;
D、通过化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,可得出每有56份质量的铁和73份质量的盐酸完全反应生成127份质量的氯化亚铁和2份质量的氢气,说法正确,不符合题意;
故选:B。
6.D
【详解】
A、铁在氧气中燃烧生成四氧化三铁,该反应的化学方程式为:,A错误;
B、过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学方程式为:,B错误;
C、用氯酸钾和二氧化锰为原料制氧气,氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气,该反应的化学方程式为:,C错误;
D、镁条燃烧生成氧化镁,该反应的化学方程式为:,D正确。
故选D
7.A
【详解】
A、由两种或两种以上元素组成的物质不一定是化合物,例如氧气和氮气放在一块属于混合物,故错误;
B、分子、原子、离子是构成物质的三种基本微粒,故正确;
C、水在三态变化过程中,其化学性质保持不变,因为只是水的状态变化,水分子未发生改变,故正确;
D、由,根据质量守恒定律,反应前后原子种类、个数不变,反应前碳原子为6个,氧原子为18个,氢原子为12个,反应后氧原子为12个,则一个R分子中含6个碳原子、12个氢原子、6个氧原子,则R中一定含碳、氢、氧三种元素,故正确;
故选:A。
8.D
【分析】
由反应的微观示意图可知,硫化氢在氧气中燃烧生成二氧化硫和水,反应的化学方程式为2H2S+3O22SO2+2H2O;
【详解】
A、由反应的化学方程式可知,反应前后分子个数发生改变,选项说法不正确;
B、氧化物是由两种元素组成的化合物中,其中一种元素是氧元素,H2S中不含氧元素,不属于氧化物,O2是一种单质,不属于氧化物;SO2、H2O属于氧化物,选项说法不正确;
C、由反应的化学方程式可知,反应中甲、乙分子个数比为2:3,选项说法不正确;
D、丙为二氧化硫,其相对分子质量为32+16×2=64,选项说法正确。
故选D。
9.C
【分析】
根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;个和↓的标注是否正确。
【详解】
A、该化学方程式缺少反应条件,氧气是反应物,氧气、二氧化硫后面不需要标注↑,正确的化学方程式应为:,故选项错误;
B、氧化钙不与碳酸钠反应,故选项错误;
C、该化学方程式书写完全正确;
D、氯化钙与水、二氧化碳不反应,故选项错误。
故选C。
10.C
【分析】
根据化学反应前后,元素种类不变,原子个数不变,可得出X为NO2。
【详解】
A、二氧化氮属于氧化物,故选项正确;
B、铜在反应物中是单质,化合价为0,在生成物硝酸铜中显+2,故选项正确;
C、物质X的化学式为NO2,故选项错误;
D、二氧化氮有毒,所以该实验要在通风橱内完成,故选项正确。
故选C
11.A
【详解】
由处理汽车尾气的微观示意图可写出方程式为:;
A、由微粒的变化可知,分子的种类发生了变化,说明了分子在化学变化中可再分,故A说法错误;
B、由方程式的意义可知,每4个分子变化成了3个分子,反应前后分子的数目发生改变,故B说法正确;
C、由方程式的意义可知,参加反应的甲和乙的分子个数比为2:2=1:1,故C说法正确;
D、由分子的模型图可知,每个丁分子由2个氧原子和1个碳原子构成,故D说法正确。
故选:A。
12.D
【详解】
A、仪器不变,不能将装置I中的粗锌粒换成锌粉,锌粉颗粒直径太小,无法控制实验的开始和结束,说法错误;
B、装置II应盛装氢氧化钠溶液,出去氢气中混有的氯化氢,装置III应盛放浓硫酸,干燥氢气,说法错误;
C、若去除装置V,空气中的水进入装置IV,会和新制得的CaH2反应,说法错误;
D、氢化钙与水反应生成氢氧化钙和水,该反应的化学方程式:;
答案:D。
13.C
1:2
H2O
氢气
氧原子
肥皂水
B
【解析】
(1)
①根据氧化物是由两种元素组成,且其中一种元素是氧元素的化合物解答;②根据化学式的意义分析解答;③根据反应原理解答;(2)
①根据电解水实验结论分析解答;②根据化学变化的实质分析解答;③根据用肥皂水区分硬水和软水解答;④根据活性炭有吸附作用分析解答。(1)
①氧化物是由两种元素组成,且其中一种元素是氧元素的化合物,由此可知,属于氧化物的是一氧化碳,故选C;②果糖(C6H12O6)大量存在于水果中,其中碳、氢元素的原子个数比6:12=1:2,③乳酸和氧气反应生成二氧化碳和水,写出反应物、生成物的化学式,然后以乳酸为起点,利用最小公倍数法配平,方程式是C3H6O3+3O2═3CO2+3H20,故x为H2O;(2)
①由电解水实验结论“负氢正氧,氧一氢二”可知,实验中,负极产生的气体是氢气;②当通电时,水分子分裂成氢原子和氧原子,两种原子又重新组合成新的分子;③生活中可用肥皂水区分硬水和软水;④A、步骤①是沉降,步骤②是过滤,可除去难溶性杂质,正确;B、活性炭有吸附性,故X试剂常用的是活性炭,错误;C、步骤④为加入药品消毒,正确;D、净化后的水含有一些可溶性杂质,仍然是混合物,正确。故选B。
14.A
d→c→f→e→i
红棕色气体颜色慢慢变浅
8NH3+6NO2
7N2
+12H2O
Z中NaOH溶液产生倒吸现象
反应后气体分子数减少,Y管内压强小于外界大气压
【详解】
(1)①实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,反应物状态为固体与固体,反应条件为加热,所以选择A为发生装置;②实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,制备的气体中含有水蒸气,氨气为碱性气体,应选择盛有碱石灰干燥管干燥气体,氨气极易溶于水,密度小于空气密度所以应选择向下排空气法收集气体,氨气极易溶于水,尾气可以用水吸收,注意防止倒吸的发生,所以正确的连接顺序为:发生装置→d→c→f→e→j;
(2)打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中,则氨气与二氧化氮发生归中反应
生成无色氮气,所以看到现象为:红棕色气体慢慢变浅;根据反应8NH3+6NO2
7N2+12H2O,以及装置恢复至室温后气态水凝聚可判断反应后气体分子数减少,装置内压强降低,所以打开K2在大气压的作用下发生倒吸。
15.二氧化氯
+4
BD
受热或者见光易分解,具有强氧化性(或很强的腐蚀性)
BC
8ClO2+2H2O4HClO+2Cl2+7O2
【详解】
(1)ClO2属于氧化物,根据氧化物的命名方法,ClO2的名称是二氧化氯,故填二氧化氯;
化合物中氧元素的化合价为-2价,设氯元素的化合价为x,根据化合物中各元素的化合价的代数和为零,则x+(-2)×2=0,x=+4,故填+4。
(2)A
84消毒液的主要成分是NaClO,其中含有氯元素,属于含氯消毒剂,选项错误;
B
双氧水的主要成分是H2O2,其中不含氯元素,不属于含氯消毒剂,选项正确;
C
氯气是氯元素组成的单质,其中含有氯元素,属于含氯消毒剂,选项错误;
D
过氧乙酸的主要成分是C2H4O3,其中不含氯元素,不属于含氯消毒剂,选项正确,故填BD。
(3)由题文可知,二氧化氯受热或者见光易分解,具有强氧化性和很强的腐蚀性,这些性质均需在化学变化中表现出来,属于化学性质,故填受热或者见光易分解,具有强氧化性(或很强的腐蚀性)。
(4)A
在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,选项错误;
B
由题文可知,在常温下,1L水中大约能溶解2.9gClO2,选项正确;
C
ClO2受热或者见光易分解,所以用棕色试剂瓶盛装
ClO2
并置于冷暗处保存,选项正确;
D
含有2%的ClO2和0.085%Na2CO3的水溶液常温下稳定,不易分解,该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良,高效安全的消毒剂,所以并不是ClO2
溶液浓度越小杀菌效果越差,选项错误,故填BC。
(5)二氧化氯与水在加热的条件下反应生成次氯酸和两种气态单质,一定有氧气,不可能是吃没有杀菌主要的氢气,则另一种单质气体一定为氯气,故反应的化学方程式写为:8ClO2+2H2O4HClO+2Cl2+7O2。
16.收集40mL氧气所需时间
DBE
质量和化学性质
氯酸钾氯化钾+氧气
【详解】
(1)本题的实验目的证明氧化铜能加快氯酸钾的分解,能够缩短制取等量氧气的反应时间,所以“待测数据”为收集40mL氧气所需时间,故填收集40mL氧气所需时间。
(2)加热氯酸钾制取氧气是固体受热生成气体的反应,应选择固体受热发生装置,即装置D,收集的气体的同时要测量制取的气体的体积,需要装置BE,故填DBE。
(3)催化剂反应前后质量和化学性质保持不变,验证氧化铜是否为氯酸钾分解反应的催化剂,还需要探究的氧化铜的氯酸钾在氧化铜的质量和化学性质在化学反应前后不变,故填质量和化学性质;
氯酸钾在氧化铜作催化剂和加热的条件下分解生成氯化钾和氧气,故反应的文字表达式写为:氯酸钾氯化钾+氧气。
一、单选题(共12题)
1.下列化学方程式中,书写正确的是( )
A.H2OH2↑+O↑
B.S+O2SO2
C.Fe+CuSO4=FeSO4+Cu↓
D.NH4HCO3NH3↑+H2O+CO2↑
2.根据化学方程式不能获得该反应的信息是(
)
A.反应物和生成物
B.反应中各物质间粒子个数比
C.化学反应的快慢
D.反应的条件
3.化学方程式不能提供的信息是(
)
A.哪些物质参加化学反应,生成物是什么
B.化学反应的是在什么条件下进行的
C.各物质之间的质量关系是多少
D.化学反应速度的快慢
4.下列化学方程式书写正确的是(
)
A.S
+O2↑SO2
B.HgO=Hg
+
O2
C.Fe
+
CuSO4
=Cu
+
FeSO4
D.2P
+
5O2P2O5
5.通过化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,不能得出的结论是(
)
A.该反应中的反应物和生成物
B.化学反应的快慢
C.反应发生所需的条件
D.各反应物和生成物的质量比
6.下列化学方程式书写完全正确的是(
)
A.铁在氧气中燃烧的化学方程式为:4Fe+3O2
2
Fe2O3
B.用双氧水和二氧化锰制氧气:2H2O22H2↑+
O2↑
C.用氯酸钾和二氧化锰为原料制氧气:2KClO32KCl
+3
O2↑
D.镁条燃烧
2Mg
+
O22MgO
7.化学是在原子、分子水平上研究物质组成、结构、性质以及变化规律的一门基础自然学科。下列有关说法中,错误的是(
)
A.组成:由两种或两种以上元素组成的物质属于化合物
B.结构:分子、原子、离子是构成物质的三种基本微粒
C.性质:水在三态变化过程中,其化学性质保持不变
D.变化,则R中一定含碳、氢、氧三种元素
8.如图是某反应前后分子种类变化的微观示意图。下列说法正确的是(
)
A.反应前后分子个数不变
B.反应中涉及到3种氧化物
C.反应中甲、乙分子个数比为1:1
D.丙的相对分子质量为64
9.下列化学方程式书写正确的是(
)
A.S+O2↑═SO2↑
B.CaO+Na2CO3=CaCO3↓+Na2O
C.Zn+H2SO4═ZnSO4+H2↑
D.CaCl2+H2O+CO2=CaCO3↓+2HCl
10.已知常温下铜与稀硝酸反应:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2X↑。下列说法不正确的是(
)
A.物质X属于氧化物
B.铜的化合价由0变为+2
C.物质X的化学式为NO
D.该实验要在通风橱内完成
11.如图是一种处理汽车尾气的微观示意图,下列说法错误的是(
)
A.分子在化学变化中不可再分
B.反应前后分子的数目发生改变
C.参加反应的甲和乙的分子个数比为1:1
D.每个丁分子由2个氧原子和1个碳原子构成
12.氢化钙(CaH2)常作供氢剂,遇水剧烈反应放出氢气。某学习小组设计如下实验制备氢化钙。下列说法正确的是(
)
A.仪器不变,也可将装置I中的粗锌粒换成锌粉
B.装置II、III盛装试剂依次为浓硫酸、NaOH溶液
C.去除装置V对制备氢化钙没有任何影响
D.氢化钙遇水反应的化学方程式为
二、综合题(共4题)
13.物质是中学化学研究的重要内容
(1)碳元素形成物质的种类是最多的。
①下列含碳元素的物质中,属于氧化物的是__(填字母序号)。
A.苏打(Na2CO3)
B.乙醇
(C2H5OH)
C.一氧化碳CO
②)果糖(C6H12O6)大量存在于水果中,其中碳、氢元素的原子个数比__________。
③人体产生了较多乳酸(C3H6O3),感觉肌肉酸胀.与氧气反应后,酸胀逐渐消失.反应的化学方程式为C3H6O3+3O2═3CO2+3X;则X的化学式______
(2).水是生命活动不可缺少的物质。(如图)根据所给信息,请回答下列问题:
①实验中,负极产生的气体是_____。
②当通电时,水分子分裂成氢原子和_____,两种原子又重新组合成新的分子。
③硬水会给生产、生活带来很多麻烦,生活中可用_____区分硬水和软水。
④自来水厂净化水的主要步骤如图2所示,有关说法错误的是_____。
A.步骤①②可除去难溶性杂质
B.X试剂常用的是明矾
C.步骤④为加入药品消毒
D.净化后的水仍然是混合物.
14.氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
⑴
氨气的制备
(资料卡)实验室用熟石灰和硫酸铵固体混合共热制取氨气,NO2有毒,常温下为红棕色,常用氢氧化钠溶液进行尾气处理;同温同压下,不同气体的体积之比等于分子个数之比。
①
氨气的发生装置可以选择上图中的_______。
②
预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→_____(按气流方向,用小写字母表示)。
⑵
氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
操作步骤
实验现象
解释原因
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中
①
Y管中______________
②
反应的化学方程式:
__________________
将注射器活塞退回原处并固定,待装置恢复到室温
Y管中有少量水珠
生成的气态水凝集
打开K2
③
_________________
④
_________________
15.阅读下面的资料,回答有关问题
新型灭菌消毒剂——ClO2
目前,新冠肺炎依然疫情肆虐全球。为抑制新冠病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂——ClO2.在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,熔点-59℃,沸点11°C.在常温下,1L水中大约能溶解2.9gClO2.ClO2受热或者见光易分解,具有强氧化性和很强的腐蚀性。含有2%的ClO2和0.085%Na2CO3的水溶液无色、无臭、无腐蚀性,常温下稳定,不易分解;该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良,高效安全的消毒剂。我国从2000年起就逐渐用ClO2取代氯气(Cl2)对饮用水进行消毒。
(1)ClO2的名称是_____,分子中氯元素的化合价是_____。
(2)下列消毒剂中,不属于“含氯消毒剂”的是_____(填字母序号)。
A
84消毒液(含NaClO)
B
双氧水
C
氯气
D
过氧乙酸(C2H4O3)
(3)ClO2的化学性质有_____(写出两点即可)。
(4)下列有关ClO2的说法正确的是_____(填字母序号)。
A
0℃时,ClO2
为黄绿色气体
B
常温下,100g
水中大约能溶解
0.29gClO2
C
用棕色试剂瓶盛装
ClO2
并置于冷暗处保存
D
ClO2
溶液浓度越小杀菌效果越差
(5)ClO2
遇热水生成次氯酸(HClO)和两种气态单质。写出该反应的化学方程式:_____(ClO2
与水的化学计量数之比为
4:1)。
16.某同学对催化剂产生了兴趣,通过查资料了解到氧化铜、氧化铁等都能加速氯酸钾的分解。为了证明氧化铜能加快氯酸钾的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关记录见下表:
实验序号
KClO3质量
加入其它的物质
待测数据
1
1.2g
无其它物质
2
1.2g
加入少量的CuO
(1)上述实验中的“待测数据”指_____。
(2)从如图仪器中选择合适的并加以组装_____。
(3)为探究CuO在实验2中是否起催化作用,还需探究的氧化铜的_____在化学反应前后不变。其反应的文字表达式为_____。
参考答案
1.D
【详解】
A、该化学方程式中氧气的化学式书写错误,正确的化学方程式应为2H2O2H2↑+O2↑;
B、该化学方程式的反应条件应为点燃,正确的化学方程式为:S+O2SO2;
C、该化学方程式反应物中铁是固体,铜的后面不需标注↓,正确的化学方程式应为:Fe+CuSO4=FeSO4+Cu;
D、该化学方程式书写完全正确;
故选D。
2.C
【详解】
A、由化学方程式,可以确定“═”左边的是反应物,右边为生成物,故选项错误。
B、由化学方程式,根据化学式前的化学计量数可以确定反应中各物质间粒子个数比,故选项错误。
C、由化学方程式,无法确定化学反应的快慢,故选项正确。
D、由化学方程式,可以看出反应发生所需要的条件,故选项错误。
故选:C。
3.D
【详解】
A、化学方程式等号前是反应物,等号后是生成物,能提供哪些物质参加化学反应,生成物是什么,不符合题意。
B、等号上方和下方表示反应条件,能提供化学反应是在什么条件下进行的,不符合题意。
C、化学方程式能反映参加反应各物质质量比例关系,不符合题意。
D、化学方程式不能体现化学反应速度的快慢,符合题意。
故选:D。
4.C
【详解】
A、化学方程式中氧气是反应物,氧气后面不需要标注气体符号↑,正确的化学方程式为:,书写不正确,不符合题意;
B、化学方程式没有配平,缺少反应条件,正确的化学方程式:,书写不正确,不符合题意;
C、铁和硫酸铜反应生成铜和硫酸亚铁,Fe
+
CuSO4
=Cu
+
FeSO4,该反应化学方程式书写正确,符合题意;
D、化学方程式没有配平,正确的化学方程式为:,书写不正确,不符合题意;
答案:C。
5.B
【详解】
A、化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,可得出反应物是铁和稀盐酸,生成物是氯化亚铁和氢气,说法正确,不符合题意;
B、化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,无法确定化学反应的快慢,说法错误,不符合题意;
C、化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,可得出反应所需的条件是常温常压,说法正确,不符合题意;
D、通过化学方程式Fe
+
2HCl
=
FeCl2
+
H2↑,可得出每有56份质量的铁和73份质量的盐酸完全反应生成127份质量的氯化亚铁和2份质量的氢气,说法正确,不符合题意;
故选:B。
6.D
【详解】
A、铁在氧气中燃烧生成四氧化三铁,该反应的化学方程式为:,A错误;
B、过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学方程式为:,B错误;
C、用氯酸钾和二氧化锰为原料制氧气,氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气,该反应的化学方程式为:,C错误;
D、镁条燃烧生成氧化镁,该反应的化学方程式为:,D正确。
故选D
7.A
【详解】
A、由两种或两种以上元素组成的物质不一定是化合物,例如氧气和氮气放在一块属于混合物,故错误;
B、分子、原子、离子是构成物质的三种基本微粒,故正确;
C、水在三态变化过程中,其化学性质保持不变,因为只是水的状态变化,水分子未发生改变,故正确;
D、由,根据质量守恒定律,反应前后原子种类、个数不变,反应前碳原子为6个,氧原子为18个,氢原子为12个,反应后氧原子为12个,则一个R分子中含6个碳原子、12个氢原子、6个氧原子,则R中一定含碳、氢、氧三种元素,故正确;
故选:A。
8.D
【分析】
由反应的微观示意图可知,硫化氢在氧气中燃烧生成二氧化硫和水,反应的化学方程式为2H2S+3O22SO2+2H2O;
【详解】
A、由反应的化学方程式可知,反应前后分子个数发生改变,选项说法不正确;
B、氧化物是由两种元素组成的化合物中,其中一种元素是氧元素,H2S中不含氧元素,不属于氧化物,O2是一种单质,不属于氧化物;SO2、H2O属于氧化物,选项说法不正确;
C、由反应的化学方程式可知,反应中甲、乙分子个数比为2:3,选项说法不正确;
D、丙为二氧化硫,其相对分子质量为32+16×2=64,选项说法正确。
故选D。
9.C
【分析】
根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;个和↓的标注是否正确。
【详解】
A、该化学方程式缺少反应条件,氧气是反应物,氧气、二氧化硫后面不需要标注↑,正确的化学方程式应为:,故选项错误;
B、氧化钙不与碳酸钠反应,故选项错误;
C、该化学方程式书写完全正确;
D、氯化钙与水、二氧化碳不反应,故选项错误。
故选C。
10.C
【分析】
根据化学反应前后,元素种类不变,原子个数不变,可得出X为NO2。
【详解】
A、二氧化氮属于氧化物,故选项正确;
B、铜在反应物中是单质,化合价为0,在生成物硝酸铜中显+2,故选项正确;
C、物质X的化学式为NO2,故选项错误;
D、二氧化氮有毒,所以该实验要在通风橱内完成,故选项正确。
故选C
11.A
【详解】
由处理汽车尾气的微观示意图可写出方程式为:;
A、由微粒的变化可知,分子的种类发生了变化,说明了分子在化学变化中可再分,故A说法错误;
B、由方程式的意义可知,每4个分子变化成了3个分子,反应前后分子的数目发生改变,故B说法正确;
C、由方程式的意义可知,参加反应的甲和乙的分子个数比为2:2=1:1,故C说法正确;
D、由分子的模型图可知,每个丁分子由2个氧原子和1个碳原子构成,故D说法正确。
故选:A。
12.D
【详解】
A、仪器不变,不能将装置I中的粗锌粒换成锌粉,锌粉颗粒直径太小,无法控制实验的开始和结束,说法错误;
B、装置II应盛装氢氧化钠溶液,出去氢气中混有的氯化氢,装置III应盛放浓硫酸,干燥氢气,说法错误;
C、若去除装置V,空气中的水进入装置IV,会和新制得的CaH2反应,说法错误;
D、氢化钙与水反应生成氢氧化钙和水,该反应的化学方程式:;
答案:D。
13.C
1:2
H2O
氢气
氧原子
肥皂水
B
【解析】
(1)
①根据氧化物是由两种元素组成,且其中一种元素是氧元素的化合物解答;②根据化学式的意义分析解答;③根据反应原理解答;(2)
①根据电解水实验结论分析解答;②根据化学变化的实质分析解答;③根据用肥皂水区分硬水和软水解答;④根据活性炭有吸附作用分析解答。(1)
①氧化物是由两种元素组成,且其中一种元素是氧元素的化合物,由此可知,属于氧化物的是一氧化碳,故选C;②果糖(C6H12O6)大量存在于水果中,其中碳、氢元素的原子个数比6:12=1:2,③乳酸和氧气反应生成二氧化碳和水,写出反应物、生成物的化学式,然后以乳酸为起点,利用最小公倍数法配平,方程式是C3H6O3+3O2═3CO2+3H20,故x为H2O;(2)
①由电解水实验结论“负氢正氧,氧一氢二”可知,实验中,负极产生的气体是氢气;②当通电时,水分子分裂成氢原子和氧原子,两种原子又重新组合成新的分子;③生活中可用肥皂水区分硬水和软水;④A、步骤①是沉降,步骤②是过滤,可除去难溶性杂质,正确;B、活性炭有吸附性,故X试剂常用的是活性炭,错误;C、步骤④为加入药品消毒,正确;D、净化后的水含有一些可溶性杂质,仍然是混合物,正确。故选B。
14.A
d→c→f→e→i
红棕色气体颜色慢慢变浅
8NH3+6NO2
7N2
+12H2O
Z中NaOH溶液产生倒吸现象
反应后气体分子数减少,Y管内压强小于外界大气压
【详解】
(1)①实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,反应物状态为固体与固体,反应条件为加热,所以选择A为发生装置;②实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,制备的气体中含有水蒸气,氨气为碱性气体,应选择盛有碱石灰干燥管干燥气体,氨气极易溶于水,密度小于空气密度所以应选择向下排空气法收集气体,氨气极易溶于水,尾气可以用水吸收,注意防止倒吸的发生,所以正确的连接顺序为:发生装置→d→c→f→e→j;
(2)打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中,则氨气与二氧化氮发生归中反应
生成无色氮气,所以看到现象为:红棕色气体慢慢变浅;根据反应8NH3+6NO2
7N2+12H2O,以及装置恢复至室温后气态水凝聚可判断反应后气体分子数减少,装置内压强降低,所以打开K2在大气压的作用下发生倒吸。
15.二氧化氯
+4
BD
受热或者见光易分解,具有强氧化性(或很强的腐蚀性)
BC
8ClO2+2H2O4HClO+2Cl2+7O2
【详解】
(1)ClO2属于氧化物,根据氧化物的命名方法,ClO2的名称是二氧化氯,故填二氧化氯;
化合物中氧元素的化合价为-2价,设氯元素的化合价为x,根据化合物中各元素的化合价的代数和为零,则x+(-2)×2=0,x=+4,故填+4。
(2)A
84消毒液的主要成分是NaClO,其中含有氯元素,属于含氯消毒剂,选项错误;
B
双氧水的主要成分是H2O2,其中不含氯元素,不属于含氯消毒剂,选项正确;
C
氯气是氯元素组成的单质,其中含有氯元素,属于含氯消毒剂,选项错误;
D
过氧乙酸的主要成分是C2H4O3,其中不含氯元素,不属于含氯消毒剂,选项正确,故填BD。
(3)由题文可知,二氧化氯受热或者见光易分解,具有强氧化性和很强的腐蚀性,这些性质均需在化学变化中表现出来,属于化学性质,故填受热或者见光易分解,具有强氧化性(或很强的腐蚀性)。
(4)A
在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,选项错误;
B
由题文可知,在常温下,1L水中大约能溶解2.9gClO2,选项正确;
C
ClO2受热或者见光易分解,所以用棕色试剂瓶盛装
ClO2
并置于冷暗处保存,选项正确;
D
含有2%的ClO2和0.085%Na2CO3的水溶液常温下稳定,不易分解,该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良,高效安全的消毒剂,所以并不是ClO2
溶液浓度越小杀菌效果越差,选项错误,故填BC。
(5)二氧化氯与水在加热的条件下反应生成次氯酸和两种气态单质,一定有氧气,不可能是吃没有杀菌主要的氢气,则另一种单质气体一定为氯气,故反应的化学方程式写为:8ClO2+2H2O4HClO+2Cl2+7O2。
16.收集40mL氧气所需时间
DBE
质量和化学性质
氯酸钾氯化钾+氧气
【详解】
(1)本题的实验目的证明氧化铜能加快氯酸钾的分解,能够缩短制取等量氧气的反应时间,所以“待测数据”为收集40mL氧气所需时间,故填收集40mL氧气所需时间。
(2)加热氯酸钾制取氧气是固体受热生成气体的反应,应选择固体受热发生装置,即装置D,收集的气体的同时要测量制取的气体的体积,需要装置BE,故填DBE。
(3)催化剂反应前后质量和化学性质保持不变,验证氧化铜是否为氯酸钾分解反应的催化剂,还需要探究的氧化铜的氯酸钾在氧化铜的质量和化学性质在化学反应前后不变,故填质量和化学性质;
氯酸钾在氧化铜作催化剂和加热的条件下分解生成氯化钾和氧气,故反应的文字表达式写为:氯酸钾氯化钾+氧气。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
