第六单元第二节化石燃料的利用课时练习-2021-2022学年九年级化学鲁教版上册(word版 含解析)
文档属性
| 名称 | 第六单元第二节化石燃料的利用课时练习-2021-2022学年九年级化学鲁教版上册(word版 含解析) |  | |
| 格式 | zip | ||
| 文件大小 | 76.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-30 10:18:52 | ||
图片预览




文档简介
第六单元燃烧与燃料第二节化石燃料的利用课时练习鲁教版初中化学九年级上册
一、单选题(共12题)
1.下列关于煤、石油、天然气的说法中正确的是(
)
A.都是可再生能源
B.都是复杂的固态混合物
C.完全燃烧都有二氧化碳生成
D.在地球上的蕴藏都是无限的
2.关于能量和能源的利用,下列说法不正确的是(
)
A.人类大量使用煤会导致酸雨效应
B.三大化石燃料中相对污染较小的是天然气
C.家中由于天然气使用不当引起的火灾,可以用二氧化碳灭火器灭火
D.根据能量守恒定律可知能量是守恒的,所以不会存在能源危机
3.燃料及其燃烧被广泛应用于生活和生产中、下列有关燃料和燃烧的说法不正确的是(
)
A.氢气是理想的清洁、高能燃料
B.石油通过炼制可以得到液化石油气、汽油、煤油等
C.物质与氧气反应时都会发生燃烧
D.燃放鞭炮就是使火药在极小的空间燃烧而引起爆炸
4.分析下列反应,所得结论不正确的是(
)
①
②
③
A.可燃物燃烧不一定要有氧气参与反应
B.上述反应都是化合反应
C.反应中均发生了能量变化
D.②、③说明化学变化中分子种类发生了变化
5.2019年科学家合成出一种新物质C18,关于C18的叙述中错误的是(
)
A.该物质由碳元素组成
B.该物质由C18分子构成
C.该物质常温下化学性质非常活泼
D.1个C18分子由18个碳原子构成
6.推理是一种常用的学习方法。下列推理正确的是(
)
A.溶液都是均一、稳定的,所以均一、稳定的物质一定是溶液
B.化合物是由不同种元素组成的,所以由不同种元素组成组成的纯净物都是化合物
C.化学变化都伴有能量变化,所以有能量变化的一定是化学变化
D.同种元素的原子质子数相同,则质子数相同的微粒一定是同种元素
7.某研究小组进行空气中氧气含量的验证实验。试管中加入足量的白磷,按图1装置连接好。数据采集开始后,将试管放入热水中恒温加热,引燃白磷;待火星熄灭后,将试管放入冷水中冷却至室温。压强传感器测定的压强变化如图2所示,通过初始压强(P1)与反应结束后的压强(P2),可以计算出氧气的体积分数:O2%=(P1-P2)/P1×100%。下列说法错误的是(
)
A.a-b段,压强增大是因为气体受热膨胀
B.b-c段,压强增大是因为白磷燃烧放热,气体急速膨胀
C.c-e段,压强减小是因为试管放入冷水中,气体冷却体积变小
D.P1和P2的压强分别为a和e所对应的压强
8.对下列事实的解释合理的是(
)
A.活性炭净水——降低水中Ca2+、Mg2+的含量
B.CO能燃烧,CO2不能燃烧——构成物质分子的原子种类不同
C.金刚石和石墨的物理性质存在明显差异——碳原子排列方式不同
D.6000L氧气在加压的情况下装入容积为40L钢瓶中——氧分子变小
9.2019年我国正式进入5G元年,5G是最新一代蜂窝移动通信技术,石墨烯被列为5G交换机唯一有效的散热方案。石墨烯为单层石墨,这种“只有一个碳原子厚的碳薄片”被公认为是目前世界上最薄、最坚硬、传导电子速度最快的材料,下列有关石墨烯的说法中正确的是(
)
A.石墨烯是一种新型化合物
B.常温下化学性质活泼
C.在充足的氧气中燃烧生成二氧化碳
D.石墨烯的硬度小于金刚石
10.关于煤、一氧化碳、酒精这三种燃料的叙述,正确的是(
)
A.燃烧后都放出热量
B.都是化合物
C.都属于化石燃料
D.都具有氧化性
11.对下列事实的微观解释错误的是(
)
选项
事实
解释
A
向汤中加入少量的NaCl整锅汤变咸
氯化钠分子是不断运动的
B
工业上用空气制取氧气的过程属于物理变化
分子的种类没有发生变化
C
金刚石。石墨性质存在明显差异
碳原子的排列方式不同
D
一氧化碳和二氧化碳化学性质不同
分子构成不同
A.A
B.B
C.C
D.D
12.1839年6月我国民族英雄林则徐在虎门利用化学反应CaO+H2O
=Ca(OH)2销毁了荼害中国人民的鸦片。从变化观念和平衡思想认识此反应,下列说法不正确的是(
)
A.10g生石灰与5g水反应生成15g熟石灰
B.反应前后,原子种类不变,原子个数也不变
C.生石灰和水反应放出大量的热
D.此反应不是氧化反应
二、综合题(共4题)
13.多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
①单质碳在常温下具有稳定性,属于___________性质。(填物理性质或化学性质)
②木炭具有还原性,可以冶炼金属。请在□内填入配平后的系数。
□Fe3O4+□C□Fe+□CO2↑____________
③近期浙江大学实验室里诞生了世界上最轻的材料——“碳海绵”。由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。关于碳海绵的说法正确的是_______(填字母序号)。
A.具有吸附性
B.可重复利用
C.可以处理海上石油泄漏
④自然界中石灰岩逐渐变成碳酸氢钙(Ca(HCO3)2)形成溶洞。碳酸氢钙由_______种元素组成,其中氢元素与氧元素的物质的量之比是________,0.5mol该物质中钙元素的质量是_____g,0.5mol该物质中约含有________个氢原子。
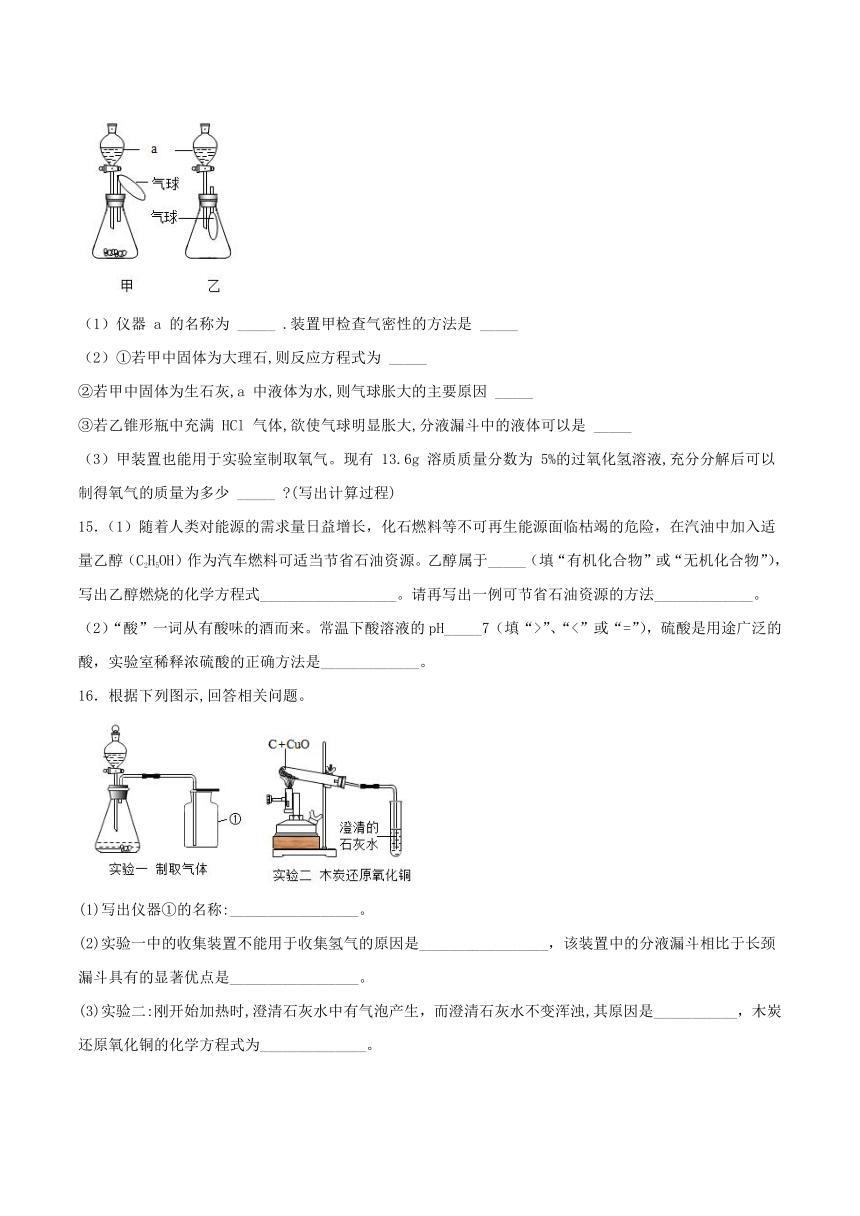
14.如图是一组“吹气球”实验,请回答:
(1)仪器
a
的名称为
_____
.装置甲检查气密性的方法是
_____
(2)①若甲中固体为大理石,则反应方程式为
_____
②若甲中固体为生石灰,a
中液体为水,则气球胀大的主要原因
_____
③若乙锥形瓶中充满
HCl
气体,欲使气球明显胀大,分液漏斗中的液体可以是
_____
(3)甲装置也能用于实验室制取氧气。现有
13.6g
溶质质量分数为
5%的过氧化氢溶液,充分分解后可以制得氧气的质量为多少
_____
(写出计算过程)
15.(1)随着人类对能源的需求量日益增长,化石燃料等不可再生能源面临枯竭的危险,在汽油中加入适量乙醇(C2H5OH)作为汽车燃料可适当节省石油资源。乙醇属于_____(填“有机化合物”或“无机化合物”),写出乙醇燃烧的化学方程式__________________。请再写出一例可节省石油资源的方法_____________。
(2)“酸”一词从有酸味的酒而来。常温下酸溶液的pH_____7(填“>”、“<”或“=”),硫酸是用途广泛的酸,实验室稀释浓硫酸的正确方法是_____________。
16.根据下列图示,回答相关问题。
(1)写出仪器①的名称:_________________。
(2)实验一中的收集装置不能用于收集氢气的原因是_________________,该装置中的分液漏斗相比于长颈漏斗具有的显著优点是_________________。
(3)实验二:刚开始加热时,澄清石灰水中有气泡产生,而澄清石灰水不变浑浊,其原因是___________,木炭还原氧化铜的化学方程式为______________。
参考答案
1.C
【详解】
A、煤、石油、天然气都是不可再生能源,错误;
B、石油是液态、天然气是气态,不都是固态混合物,错误;
C、煤、石油、天然气都含有碳元素,完全燃烧都有二氧化碳生成,正确;
D、煤、石油、天然气在地球上的蕴藏都是有限的,错误。
故选C。
2.D
【详解】
A、煤中含有硫、氮元素,大量使用煤会生成二氧化硫、氮的氧化物,会导致酸雨,说法正确;
B、煤和石油中含有硫、氮元素、燃烧后会生成二氧化硫、氮的氧化物,会导致酸雨,天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,都不是空气污染物,三大化石燃料中相对污染较小的是天然气,说法正确;
C、二氧化碳不能燃烧,也不支持燃烧,密度比空气大,常用于灭火,家中由于天然气使用不当引起的火灾,可以用二氧化碳灭火器灭火,说法正确;
D、地球上化石燃料能源的存储量是有限的,如果过量开采这些能源,会存在能源危机,说法错误;
答案:D。
3.C
【详解】
A、氢气燃烧只生成水,不污染空气且发热量高,是最理想的清洁、高能燃料,故正确;
B、石油通过炼制可以得到液化石油气、汽油、煤油等,故正确;
C、物质与氧气反应不一定燃烧,像物质的缓慢氧化:食物腐烂、铁生锈等就没岀现燃烧,故错误;
D、燃放鞭炮就是使火药在极小的空间燃烧而引起爆炸,故正确。
故选C。
4.B
【详解】
A、
氢气可以在氯气中燃烧,由此可知可燃物燃烧不一定要有氧气参与反应,故选项说法正确;
B、反应①②符合“多变一”的特点,是化合反应,②的生成物是两种,不是化合反应,故选项说法错误;
C、三个反应都是物质的燃烧,燃烧过程中都会放出热量,故选项说法正确;
D、反应物乙醇、氧气、氢气、氯气都是由分子构成的,反应后变成了二氧化碳分子、水分子、氯化氢分子,所以②、③说明化学变化中分子种类发生了变化,故选项说法正确。
故选:B。
5.C
【详解】
A、物质由元素组成,C18由碳元素组成,正确。
B、从化学式可知该物质是由分子构成的,该物质由C18分子构成,正确。
C、碳单质常温下化学性质稳定,该物质常温下化学性质稳定,错误。
D、微观上分子由原子构成,从化学式可知1个C18分子由18个碳原子构成,正确。
故选C。
【点睛】
6.B
【详解】
A、溶液都是均一、稳定的,但均一、稳定的物质不一定是溶液,如水、酒精是纯净物,不是溶液,推理不正确,不符合题意;
B、化合物是由不同种元素组成的,所以由不同种元素组成组成的纯净物都是化合物,推理正确,符合题意;
C、
化学变化都伴有能量变化,但有能量变化的不一定是化学变化,如灯泡发光是物理变化,推理不正确,不符合题意;
D、同种元素的原子质子数相同,但质子数相同的微粒不一定是同种元素,如氖原子和水分子质子数均为10,不属于同种元素,推理不正确,不符合题意。
故选B。
7.C
【分析】
在装有空气的密闭容器中,欲用燃烧法测定空气中氧气含量,该实验一般要注意以下几点:①装置的气密性好;②所用药品必须是足量;③读数时一定要冷却到原温度;据此进行分析判断。
【详解】
A、a-b段,压强增大是因为将试管放入热水中恒温加热,气体受热膨胀,此选项说法正确;
B、b-c段,白磷燃烧放出大量的热,压强增大是因为白磷燃烧放热,气体急速膨胀,此选项说法正确;
C、c-e段,压强减小,主要是因为白磷燃烧消耗氧气,使装置内气压减小,此选项说法错误;
D、P1表示初始压强,P2表示反应结束后的压强,则P1和P2的压强分别为a和e所对应的压强,此选项说法正确;
故选:C。
【点睛】
本题难度不大,掌握用燃烧法测定空气中氧气含量的实验原理、注意事项等是正确解答本题的关键。
8.C
【详解】
A、活性炭具有吸附性,能吸附异味和色素,但不能降低水中Ca2+、Mg2+的的含量,故选项说法错误。
B、CO能燃烧,CO2不能燃烧,是因为它们分子的构成不同,化学性质不同,故选项说法错误。
C、金刚石和石墨的物理性质存在明显差异,是因为它们中碳原子排列方式不同,故选项说法正确。
D、6000L氧气在加压的情况下装入容积为40L钢瓶中,是因为分子间有间隔,气体受压后,分子间的间隔变小,故选项说法错误。
故选:C。
9.C
【详解】
A、石墨烯为单层石墨,石墨是碳单质,所以石墨烯也是单质,错误;
B、石墨烯是碳单质,常温下化学性质稳定,错误;
C、碳单质在充足的氧气中燃烧生成二氧化碳,正确;
D、石墨烯被公认为是目前世界上最薄、最坚硬、传导电子速度最快的材料,所以硬度大于金刚石,错误。
故选:C。
10.A
【详解】
A、煤、一氧化碳、酒精均具有可燃性,燃烧后都放出热量,符合题意;
B、煤的主要成分是碳,还含有其它杂质,属于混合物,一氧化碳是由C、O元素组成的纯净物,属于化合物,酒精是由C、H、O元素组成的纯净物,属于化合物,不符合题意;
C、煤属于化石燃料,一氧化碳、酒精不属于化石燃料,不符合题意;
D、煤的主要成分是碳,碳具有还原性,一氧化碳具有还原性,酒精具有还原性,不符合题意。
故选A。
11.A
【详解】
A、向汤中加入少量的NaCl整锅汤变咸,是因为钠离子和氯离子是不断运动的,符合题意;
B、工业上用空气制取氧气的过程,是利用液氮和液氧沸点的不同,将其分离,分子的种类没有发生变化,属于物理变化,不符合题意;
C、金刚石、石墨碳原子的排列方式不同,物理性质存在明显差异,不符合题意;
D、一氧化碳和二氧化碳化学性质不同,是因为分子构成不同,一氧化碳由一氧化碳分子构成,二氧化碳由二氧化碳分子构成,不符合题意。
故选A。
12.A
【详解】
A、由可知10g生石灰与3.2g水反应生成13.2g熟石灰,错误;
B、根据质量守恒定律可知反应前后,原子种类不变,原子个数也不变,正确;
C、生石灰和水反应放出大量的热,正确;
D、反应前后各元素的化合价未发生变化,因此此反应不是氧化反应,正确;
故选A。
13.化学性质
1,2,3,2
ABC
4
1:3
20
6.02×1023
【详解】
①①单质碳在常温下具有稳定性,属于化学性质;②化学方程式配平为:2C+
Fe3O43Fe+2CO2↑;③A、碳海绵,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),正确;B、由于碳海绵将吸入的石油挤出后仍可恢复原状,可重复使用,正确;C、由于碳海绵有吸附性,对石油有很强的吸附能力,可处理海上石油泄漏,正确;④碳酸氢钙的一个分子中共有11个原子,其中氢元素与氧元素的物质的量之比是2:6=1:3,0.5mol该物质中钙元素的质量是40g/mol×0.5mol=20g,0.5mol该物质中约含有0.5mol×2×6.02×1023=6.02×1023个碳原子。
14.分液漏斗
旋转分液漏斗活塞,向锥形瓶中加水会看到气球胀大,一段时间后气球大小没有变化,说明气密性良好
CaCO3
+
2HCl
==
CaCl2
+
H2O
+
CO2↑
生石灰与水反应放热,使瓶内压强增大
氢氧化钠溶液
0.32g
【详解】
(1)仪器a的名称是:分液漏斗;装置甲检查气密性的方法是:旋转分液漏斗活塞,向锥形瓶中加水会看到气球胀大,一段时间后气球大小没有变化,说明气密性良好。
(2)①大理石和稀盐酸反应生成二氧化碳气体,故若甲中固体为大理石,则反应方程式为:CaCO3
+
2HCl
==
CaCl2
+
H2O
+
CO2↑;
②生石灰与水反应放热,使瓶内压强增大,则气球胀大;
③乙锥形瓶中HCl气体被吸收时,装置内压强减小,内部的气球胀大,氢氧化钠溶液可以吸收氯化氢气体;
(3)设制得氧气的质量为x,
x=0.32g
【点睛】
本题难度不大,使气球胀大的原理是改变装置的压强,造成压强差。除气体的变化外,通过反应放热或吸热也能改变装置的压强。
15.有机化合物
C2H5OH+3O22CO2+3H2O
开发新能源,石油制品回收再利用,或多坐公共交通工具,距离近的步行和骑自行车等等
<
把浓硫酸缓缓地沿器壁注入水中,并用玻璃棒不断搅拌
【详解】
(1)乙醇属于有机化合物;乙醇与氧气在点燃的条件下反应生成二氧化碳和水,反应方程式为C2H5OH+3O22CO2+3H2O;减少化石燃料可以减少环境的污染,减少方法有开发新能源,石油制品回收再利用,或多坐公共交通工具,距离近的步行和骑自行车等等;
(2)酸溶液的瓶pH小于7;稀释浓硫酸的方法是把浓硫酸缓缓地沿器壁注入水中,并用玻璃棒不断搅拌
16.集气瓶
氢气密度比空气密度小,不能用向上排空气法收集
可以控制反应速率
加热时空气体积膨胀,先排出了空气
【详解】
(1)仪器①是集气瓶;故填:集气瓶;
(2)氢气密度比空气密度小,不能用向上排空气法收集,所以实验一中的收集装置不能用于收集氢气;该装置中的分液漏斗可以通过控制液体的滴加速率来控制反应的速率。故填:氢气密度比空气密度小,不能用向上排空气法收集;可以控制反应速率;
(3)实验二:刚开始加热时,空气体积受热膨胀,先排出空气,澄清石灰水中有气泡产生,而澄清石灰水不变浑浊;木炭和氧化铜在高温条件下反应生成铜和二氧化碳,反应的化学方程式为。故填:加热时空气体积膨胀,先排出了空气;。
一、单选题(共12题)
1.下列关于煤、石油、天然气的说法中正确的是(
)
A.都是可再生能源
B.都是复杂的固态混合物
C.完全燃烧都有二氧化碳生成
D.在地球上的蕴藏都是无限的
2.关于能量和能源的利用,下列说法不正确的是(
)
A.人类大量使用煤会导致酸雨效应
B.三大化石燃料中相对污染较小的是天然气
C.家中由于天然气使用不当引起的火灾,可以用二氧化碳灭火器灭火
D.根据能量守恒定律可知能量是守恒的,所以不会存在能源危机
3.燃料及其燃烧被广泛应用于生活和生产中、下列有关燃料和燃烧的说法不正确的是(
)
A.氢气是理想的清洁、高能燃料
B.石油通过炼制可以得到液化石油气、汽油、煤油等
C.物质与氧气反应时都会发生燃烧
D.燃放鞭炮就是使火药在极小的空间燃烧而引起爆炸
4.分析下列反应,所得结论不正确的是(
)
①
②
③
A.可燃物燃烧不一定要有氧气参与反应
B.上述反应都是化合反应
C.反应中均发生了能量变化
D.②、③说明化学变化中分子种类发生了变化
5.2019年科学家合成出一种新物质C18,关于C18的叙述中错误的是(
)
A.该物质由碳元素组成
B.该物质由C18分子构成
C.该物质常温下化学性质非常活泼
D.1个C18分子由18个碳原子构成
6.推理是一种常用的学习方法。下列推理正确的是(
)
A.溶液都是均一、稳定的,所以均一、稳定的物质一定是溶液
B.化合物是由不同种元素组成的,所以由不同种元素组成组成的纯净物都是化合物
C.化学变化都伴有能量变化,所以有能量变化的一定是化学变化
D.同种元素的原子质子数相同,则质子数相同的微粒一定是同种元素
7.某研究小组进行空气中氧气含量的验证实验。试管中加入足量的白磷,按图1装置连接好。数据采集开始后,将试管放入热水中恒温加热,引燃白磷;待火星熄灭后,将试管放入冷水中冷却至室温。压强传感器测定的压强变化如图2所示,通过初始压强(P1)与反应结束后的压强(P2),可以计算出氧气的体积分数:O2%=(P1-P2)/P1×100%。下列说法错误的是(
)
A.a-b段,压强增大是因为气体受热膨胀
B.b-c段,压强增大是因为白磷燃烧放热,气体急速膨胀
C.c-e段,压强减小是因为试管放入冷水中,气体冷却体积变小
D.P1和P2的压强分别为a和e所对应的压强
8.对下列事实的解释合理的是(
)
A.活性炭净水——降低水中Ca2+、Mg2+的含量
B.CO能燃烧,CO2不能燃烧——构成物质分子的原子种类不同
C.金刚石和石墨的物理性质存在明显差异——碳原子排列方式不同
D.6000L氧气在加压的情况下装入容积为40L钢瓶中——氧分子变小
9.2019年我国正式进入5G元年,5G是最新一代蜂窝移动通信技术,石墨烯被列为5G交换机唯一有效的散热方案。石墨烯为单层石墨,这种“只有一个碳原子厚的碳薄片”被公认为是目前世界上最薄、最坚硬、传导电子速度最快的材料,下列有关石墨烯的说法中正确的是(
)
A.石墨烯是一种新型化合物
B.常温下化学性质活泼
C.在充足的氧气中燃烧生成二氧化碳
D.石墨烯的硬度小于金刚石
10.关于煤、一氧化碳、酒精这三种燃料的叙述,正确的是(
)
A.燃烧后都放出热量
B.都是化合物
C.都属于化石燃料
D.都具有氧化性
11.对下列事实的微观解释错误的是(
)
选项
事实
解释
A
向汤中加入少量的NaCl整锅汤变咸
氯化钠分子是不断运动的
B
工业上用空气制取氧气的过程属于物理变化
分子的种类没有发生变化
C
金刚石。石墨性质存在明显差异
碳原子的排列方式不同
D
一氧化碳和二氧化碳化学性质不同
分子构成不同
A.A
B.B
C.C
D.D
12.1839年6月我国民族英雄林则徐在虎门利用化学反应CaO+H2O
=Ca(OH)2销毁了荼害中国人民的鸦片。从变化观念和平衡思想认识此反应,下列说法不正确的是(
)
A.10g生石灰与5g水反应生成15g熟石灰
B.反应前后,原子种类不变,原子个数也不变
C.生石灰和水反应放出大量的热
D.此反应不是氧化反应
二、综合题(共4题)
13.多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
①单质碳在常温下具有稳定性,属于___________性质。(填物理性质或化学性质)
②木炭具有还原性,可以冶炼金属。请在□内填入配平后的系数。
□Fe3O4+□C□Fe+□CO2↑____________
③近期浙江大学实验室里诞生了世界上最轻的材料——“碳海绵”。由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。关于碳海绵的说法正确的是_______(填字母序号)。
A.具有吸附性
B.可重复利用
C.可以处理海上石油泄漏
④自然界中石灰岩逐渐变成碳酸氢钙(Ca(HCO3)2)形成溶洞。碳酸氢钙由_______种元素组成,其中氢元素与氧元素的物质的量之比是________,0.5mol该物质中钙元素的质量是_____g,0.5mol该物质中约含有________个氢原子。
14.如图是一组“吹气球”实验,请回答:
(1)仪器
a
的名称为
_____
.装置甲检查气密性的方法是
_____
(2)①若甲中固体为大理石,则反应方程式为
_____
②若甲中固体为生石灰,a
中液体为水,则气球胀大的主要原因
_____
③若乙锥形瓶中充满
HCl
气体,欲使气球明显胀大,分液漏斗中的液体可以是
_____
(3)甲装置也能用于实验室制取氧气。现有
13.6g
溶质质量分数为
5%的过氧化氢溶液,充分分解后可以制得氧气的质量为多少
_____
(写出计算过程)
15.(1)随着人类对能源的需求量日益增长,化石燃料等不可再生能源面临枯竭的危险,在汽油中加入适量乙醇(C2H5OH)作为汽车燃料可适当节省石油资源。乙醇属于_____(填“有机化合物”或“无机化合物”),写出乙醇燃烧的化学方程式__________________。请再写出一例可节省石油资源的方法_____________。
(2)“酸”一词从有酸味的酒而来。常温下酸溶液的pH_____7(填“>”、“<”或“=”),硫酸是用途广泛的酸,实验室稀释浓硫酸的正确方法是_____________。
16.根据下列图示,回答相关问题。
(1)写出仪器①的名称:_________________。
(2)实验一中的收集装置不能用于收集氢气的原因是_________________,该装置中的分液漏斗相比于长颈漏斗具有的显著优点是_________________。
(3)实验二:刚开始加热时,澄清石灰水中有气泡产生,而澄清石灰水不变浑浊,其原因是___________,木炭还原氧化铜的化学方程式为______________。
参考答案
1.C
【详解】
A、煤、石油、天然气都是不可再生能源,错误;
B、石油是液态、天然气是气态,不都是固态混合物,错误;
C、煤、石油、天然气都含有碳元素,完全燃烧都有二氧化碳生成,正确;
D、煤、石油、天然气在地球上的蕴藏都是有限的,错误。
故选C。
2.D
【详解】
A、煤中含有硫、氮元素,大量使用煤会生成二氧化硫、氮的氧化物,会导致酸雨,说法正确;
B、煤和石油中含有硫、氮元素、燃烧后会生成二氧化硫、氮的氧化物,会导致酸雨,天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,都不是空气污染物,三大化石燃料中相对污染较小的是天然气,说法正确;
C、二氧化碳不能燃烧,也不支持燃烧,密度比空气大,常用于灭火,家中由于天然气使用不当引起的火灾,可以用二氧化碳灭火器灭火,说法正确;
D、地球上化石燃料能源的存储量是有限的,如果过量开采这些能源,会存在能源危机,说法错误;
答案:D。
3.C
【详解】
A、氢气燃烧只生成水,不污染空气且发热量高,是最理想的清洁、高能燃料,故正确;
B、石油通过炼制可以得到液化石油气、汽油、煤油等,故正确;
C、物质与氧气反应不一定燃烧,像物质的缓慢氧化:食物腐烂、铁生锈等就没岀现燃烧,故错误;
D、燃放鞭炮就是使火药在极小的空间燃烧而引起爆炸,故正确。
故选C。
4.B
【详解】
A、
氢气可以在氯气中燃烧,由此可知可燃物燃烧不一定要有氧气参与反应,故选项说法正确;
B、反应①②符合“多变一”的特点,是化合反应,②的生成物是两种,不是化合反应,故选项说法错误;
C、三个反应都是物质的燃烧,燃烧过程中都会放出热量,故选项说法正确;
D、反应物乙醇、氧气、氢气、氯气都是由分子构成的,反应后变成了二氧化碳分子、水分子、氯化氢分子,所以②、③说明化学变化中分子种类发生了变化,故选项说法正确。
故选:B。
5.C
【详解】
A、物质由元素组成,C18由碳元素组成,正确。
B、从化学式可知该物质是由分子构成的,该物质由C18分子构成,正确。
C、碳单质常温下化学性质稳定,该物质常温下化学性质稳定,错误。
D、微观上分子由原子构成,从化学式可知1个C18分子由18个碳原子构成,正确。
故选C。
【点睛】
6.B
【详解】
A、溶液都是均一、稳定的,但均一、稳定的物质不一定是溶液,如水、酒精是纯净物,不是溶液,推理不正确,不符合题意;
B、化合物是由不同种元素组成的,所以由不同种元素组成组成的纯净物都是化合物,推理正确,符合题意;
C、
化学变化都伴有能量变化,但有能量变化的不一定是化学变化,如灯泡发光是物理变化,推理不正确,不符合题意;
D、同种元素的原子质子数相同,但质子数相同的微粒不一定是同种元素,如氖原子和水分子质子数均为10,不属于同种元素,推理不正确,不符合题意。
故选B。
7.C
【分析】
在装有空气的密闭容器中,欲用燃烧法测定空气中氧气含量,该实验一般要注意以下几点:①装置的气密性好;②所用药品必须是足量;③读数时一定要冷却到原温度;据此进行分析判断。
【详解】
A、a-b段,压强增大是因为将试管放入热水中恒温加热,气体受热膨胀,此选项说法正确;
B、b-c段,白磷燃烧放出大量的热,压强增大是因为白磷燃烧放热,气体急速膨胀,此选项说法正确;
C、c-e段,压强减小,主要是因为白磷燃烧消耗氧气,使装置内气压减小,此选项说法错误;
D、P1表示初始压强,P2表示反应结束后的压强,则P1和P2的压强分别为a和e所对应的压强,此选项说法正确;
故选:C。
【点睛】
本题难度不大,掌握用燃烧法测定空气中氧气含量的实验原理、注意事项等是正确解答本题的关键。
8.C
【详解】
A、活性炭具有吸附性,能吸附异味和色素,但不能降低水中Ca2+、Mg2+的的含量,故选项说法错误。
B、CO能燃烧,CO2不能燃烧,是因为它们分子的构成不同,化学性质不同,故选项说法错误。
C、金刚石和石墨的物理性质存在明显差异,是因为它们中碳原子排列方式不同,故选项说法正确。
D、6000L氧气在加压的情况下装入容积为40L钢瓶中,是因为分子间有间隔,气体受压后,分子间的间隔变小,故选项说法错误。
故选:C。
9.C
【详解】
A、石墨烯为单层石墨,石墨是碳单质,所以石墨烯也是单质,错误;
B、石墨烯是碳单质,常温下化学性质稳定,错误;
C、碳单质在充足的氧气中燃烧生成二氧化碳,正确;
D、石墨烯被公认为是目前世界上最薄、最坚硬、传导电子速度最快的材料,所以硬度大于金刚石,错误。
故选:C。
10.A
【详解】
A、煤、一氧化碳、酒精均具有可燃性,燃烧后都放出热量,符合题意;
B、煤的主要成分是碳,还含有其它杂质,属于混合物,一氧化碳是由C、O元素组成的纯净物,属于化合物,酒精是由C、H、O元素组成的纯净物,属于化合物,不符合题意;
C、煤属于化石燃料,一氧化碳、酒精不属于化石燃料,不符合题意;
D、煤的主要成分是碳,碳具有还原性,一氧化碳具有还原性,酒精具有还原性,不符合题意。
故选A。
11.A
【详解】
A、向汤中加入少量的NaCl整锅汤变咸,是因为钠离子和氯离子是不断运动的,符合题意;
B、工业上用空气制取氧气的过程,是利用液氮和液氧沸点的不同,将其分离,分子的种类没有发生变化,属于物理变化,不符合题意;
C、金刚石、石墨碳原子的排列方式不同,物理性质存在明显差异,不符合题意;
D、一氧化碳和二氧化碳化学性质不同,是因为分子构成不同,一氧化碳由一氧化碳分子构成,二氧化碳由二氧化碳分子构成,不符合题意。
故选A。
12.A
【详解】
A、由可知10g生石灰与3.2g水反应生成13.2g熟石灰,错误;
B、根据质量守恒定律可知反应前后,原子种类不变,原子个数也不变,正确;
C、生石灰和水反应放出大量的热,正确;
D、反应前后各元素的化合价未发生变化,因此此反应不是氧化反应,正确;
故选A。
13.化学性质
1,2,3,2
ABC
4
1:3
20
6.02×1023
【详解】
①①单质碳在常温下具有稳定性,属于化学性质;②化学方程式配平为:2C+
Fe3O43Fe+2CO2↑;③A、碳海绵,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),正确;B、由于碳海绵将吸入的石油挤出后仍可恢复原状,可重复使用,正确;C、由于碳海绵有吸附性,对石油有很强的吸附能力,可处理海上石油泄漏,正确;④碳酸氢钙的一个分子中共有11个原子,其中氢元素与氧元素的物质的量之比是2:6=1:3,0.5mol该物质中钙元素的质量是40g/mol×0.5mol=20g,0.5mol该物质中约含有0.5mol×2×6.02×1023=6.02×1023个碳原子。
14.分液漏斗
旋转分液漏斗活塞,向锥形瓶中加水会看到气球胀大,一段时间后气球大小没有变化,说明气密性良好
CaCO3
+
2HCl
==
CaCl2
+
H2O
+
CO2↑
生石灰与水反应放热,使瓶内压强增大
氢氧化钠溶液
0.32g
【详解】
(1)仪器a的名称是:分液漏斗;装置甲检查气密性的方法是:旋转分液漏斗活塞,向锥形瓶中加水会看到气球胀大,一段时间后气球大小没有变化,说明气密性良好。
(2)①大理石和稀盐酸反应生成二氧化碳气体,故若甲中固体为大理石,则反应方程式为:CaCO3
+
2HCl
==
CaCl2
+
H2O
+
CO2↑;
②生石灰与水反应放热,使瓶内压强增大,则气球胀大;
③乙锥形瓶中HCl气体被吸收时,装置内压强减小,内部的气球胀大,氢氧化钠溶液可以吸收氯化氢气体;
(3)设制得氧气的质量为x,
x=0.32g
【点睛】
本题难度不大,使气球胀大的原理是改变装置的压强,造成压强差。除气体的变化外,通过反应放热或吸热也能改变装置的压强。
15.有机化合物
C2H5OH+3O22CO2+3H2O
开发新能源,石油制品回收再利用,或多坐公共交通工具,距离近的步行和骑自行车等等
<
把浓硫酸缓缓地沿器壁注入水中,并用玻璃棒不断搅拌
【详解】
(1)乙醇属于有机化合物;乙醇与氧气在点燃的条件下反应生成二氧化碳和水,反应方程式为C2H5OH+3O22CO2+3H2O;减少化石燃料可以减少环境的污染,减少方法有开发新能源,石油制品回收再利用,或多坐公共交通工具,距离近的步行和骑自行车等等;
(2)酸溶液的瓶pH小于7;稀释浓硫酸的方法是把浓硫酸缓缓地沿器壁注入水中,并用玻璃棒不断搅拌
16.集气瓶
氢气密度比空气密度小,不能用向上排空气法收集
可以控制反应速率
加热时空气体积膨胀,先排出了空气
【详解】
(1)仪器①是集气瓶;故填:集气瓶;
(2)氢气密度比空气密度小,不能用向上排空气法收集,所以实验一中的收集装置不能用于收集氢气;该装置中的分液漏斗可以通过控制液体的滴加速率来控制反应的速率。故填:氢气密度比空气密度小,不能用向上排空气法收集;可以控制反应速率;
(3)实验二:刚开始加热时,空气体积受热膨胀,先排出空气,澄清石灰水中有气泡产生,而澄清石灰水不变浑浊;木炭和氧化铜在高温条件下反应生成铜和二氧化碳,反应的化学方程式为。故填:加热时空气体积膨胀,先排出了空气;。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
