第七单元 燃料及其利用 单元测试题—2021-2022学年九年级化学人教版上册(word版 含答案)
文档属性
| 名称 | 第七单元 燃料及其利用 单元测试题—2021-2022学年九年级化学人教版上册(word版 含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 180.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-02 00:00:00 | ||
图片预览



文档简介
第七单元《燃料及其利用》测试题
一、单选题
1.山西云岗石窟有很多佛像雕刻,原本栩栩如生的雕像已经变得模糊不清,有的表面还出现了斑点,造成这种现象的原因之一是酸雨.下列气体中能形成酸雨的是
A.O2
B.CO
C.SO2
D.N2
2.2021年6月5日世界环境日主题为“改善环境质量推动绿色发展”。下列做法不符合这一主题的是
A.大力发展燃煤发电
B.关停重污染企业
C.推广使用新能源汽车
D.限制燃放烟花爆竹
3.危险化学品泄漏或爆炸事件常给我们敲响安全警钟,操作不当就会存在安全隐患。下列做法错误的是
A.点燃氢气前先验纯
B.发现室内燃气泄漏,应立即打开排气扇通气
C.矿井作业要注意通风
D.油库、面粉厂、纺织厂等场所要严禁烟火
4.逻辑推理是一种重要的化学思维方法,以下推理合理的是
A.燃烧需要同时满足三个条件才能发生,所以灭火也一定同时控制这三个条件
B.因为CO、CO2的组成元素相同,所以它们的化学性质也相同
C.点燃H2与O2的混合气体可能爆炸,则点燃CH4和O2的混合气体也可能爆炸
D.把燃着的木条伸入某瓶无色气体中,木条熄灭,证明瓶中的气体一定是二氧化碳
5.如图是有关燃烧条件的探究(已知白磷的着火点为40℃,红磷的着火点是240℃)。下列说法正确的是
A.热水的作用只是为了提供热量
B.铜片上的白磷燃烧而红磷不燃烧说明温度是可燃物燃烧的条件之一
C.向水中的白磷通氧气,白磷也不会发生燃烧
D.该实验只能探究可燃物发生燃烧的一个条件
6.下列做法中,不正确的是
A.炒菜时油锅着火,立即盖上锅盖
B.家用电器着火时,立即用泡沫灭火器灭火
C.天然气泄漏时,立即关闭阀门并开窗
D.燃放烟花爆竹时,要远离人群和可燃物
7.下面是人们对化学科学的各种常见认识,其中错误的是
A.化学面对现代日益严重的环境问题显得无能为力
B.化学在能源、资源的合理开发和安全应用方面大显身手
C.化学是一门具有极强实用性的科学
D.化学的发展极大满足了人们对新物质的需求
8.下列关于“碳循环”和“氧循环”的说法错误的是
A.碳循环和氧循环过程中均发生了化学变化
B.碳循环和氧循环分别是指二氧化碳和氧气的循环
C.绿色植物通过光合作用,将太阳能转化成化学能
D.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
9.今年春天我国多地发生火灾,造成巨大生命财产损失,警示我们,消防安全是保障我们人身财产安全的一项重要工程,下列有关说法正确的是
A.发现天然气泄漏,点火检查泄漏处
B.电器着火应先切断电源,再用二氧化碳灭火器扑灭
C.所有的爆炸都是由剧烈燃烧引起的
D.消防员用高压水枪灭火的原理是降低了可燃物的着火点
10.下列有关燃烧与灭火的说法正确的是
A.电烤炉着火时,用水浇灭
B.用扇子可以扇灭蜡烛,是因为可以降低着火点
C.煤炉的火焰呈现黄色时,调小进风口可使燃烧更充分
D.液态氧和气态氧都能助燃,是因为同种分子其化学性质相同
11.下列关于石油的说法,错误的是
A.石油是混合物
B.石油产品可用于发电
C.石油是一种化工产品
D.石油是不可再生资源
12.充分燃烧1kg天然气和煤所产生的CO2和SO2气体的质量如图所示,请利用所学知识,并结合图像判断下列叙述正确的是
①煤和天然气均属于化石燃料
②等量的煤和天然气充分燃烧,煤更容易导致酸雨
③使用天然气有助于缓解温室效应加剧的环境问题
④有煤存在的地方,都有天然气存在
A.①②
B.①④
C.②③
D.③④
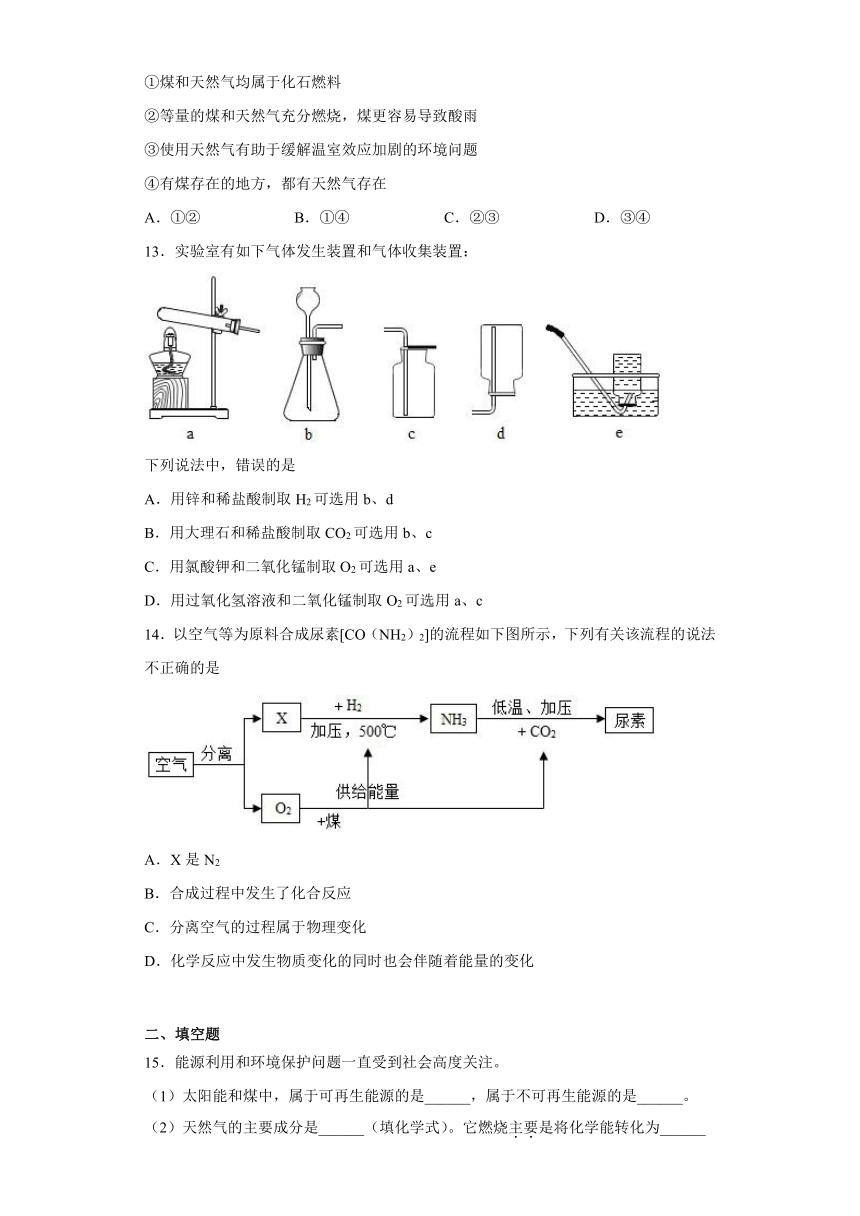
13.实验室有如下气体发生装置和气体收集装置:
下列说法中,错误的是
A.用锌和稀盐酸制取H2可选用b、d
B.用大理石和稀盐酸制取CO2可选用b、c
C.用氯酸钾和二氧化锰制取O2可选用a、e
D.用过氧化氢溶液和二氧化锰制取O2可选用a、c
14.以空气等为原料合成尿素[CO(NH2)2]的流程如下图所示,下列有关该流程的说法不正确的是
A.X是N2
B.合成过程中发生了化合反应
C.分离空气的过程属于物理变化
D.化学反应中发生物质变化的同时也会伴随着能量的变化
二、填空题
15.能源利用和环境保护问题一直受到社会高度关注。
(1)太阳能和煤中,属于可再生能源的是______,属于不可再生能源的是______。
(2)天然气的主要成分是______(填化学式)。它燃烧主要是将化学能转化为______能。
(3)从环境保护的角度考虑,最理想的燃料是______(填物质名称)。
(4)煤在不充分燃烧的情况下,会产生某些有毒气体。其中______(填化学式)极易与血液中的血红蛋白结合,引起中毒。
16.2020年9月,习近平在联大针对气候变化表示:“中国将力争碳排放2030年前达到峰值,争取在2060年前实现碳中和”。由所学知识回答:
(1)以上说的“碳排放和碳中和”中的“碳”指的是______(填化学式),降低碳排放会减缓______。现阶段,下列措施合理的是______(填序号)。
A.禁止烧煤
B.研发汽车新能源
C.鼓励乘坐公交出行
D.随手关灯
(2)氢燃料电池把氢能转化为电能,氢燃料电池的优点是______(填序号)。
A.产物是水,不污染空气
B.制取氢气成本较低
(3)甲醇(CH3OH)也是一种新型燃料,试写出甲醇完全燃烧的化学方程式:______。
17.燃料的利用与生产生活密切相关。
(1)酒精完全燃烧的化学方程式为______;
(2)氢气作为最理想的新型能源,其优点是______(写出一条即可)。
18.2017年我国研制出一种新型多功能复合催化剂,首次实现了二氧化碳直接加氢制取高辛烷值汽油。
(1)对“CO2变汽油”的研究成果,下列说法正确的是_______(填序号)。
①可有效缓解全球温室效应
②可减少对化石燃料的依赖
③该转化过程中发生化学变化
④该催化剂在该反应中可以重复使用
(2)通过如图I、II、III三个环节,可将CO2成功转化为汽油。一定条件下,环节I除生成CO外,还生成了一种化合物,反应的化学方程式为_______,该反应中CO2发生了_______(填“氧化或还原”)反应。
(3)氧化铟是复合催化剂的成分之一、元素周期表中,铟(In)元素与铝元素位于同一族,写出氧化铟的化学式_______。
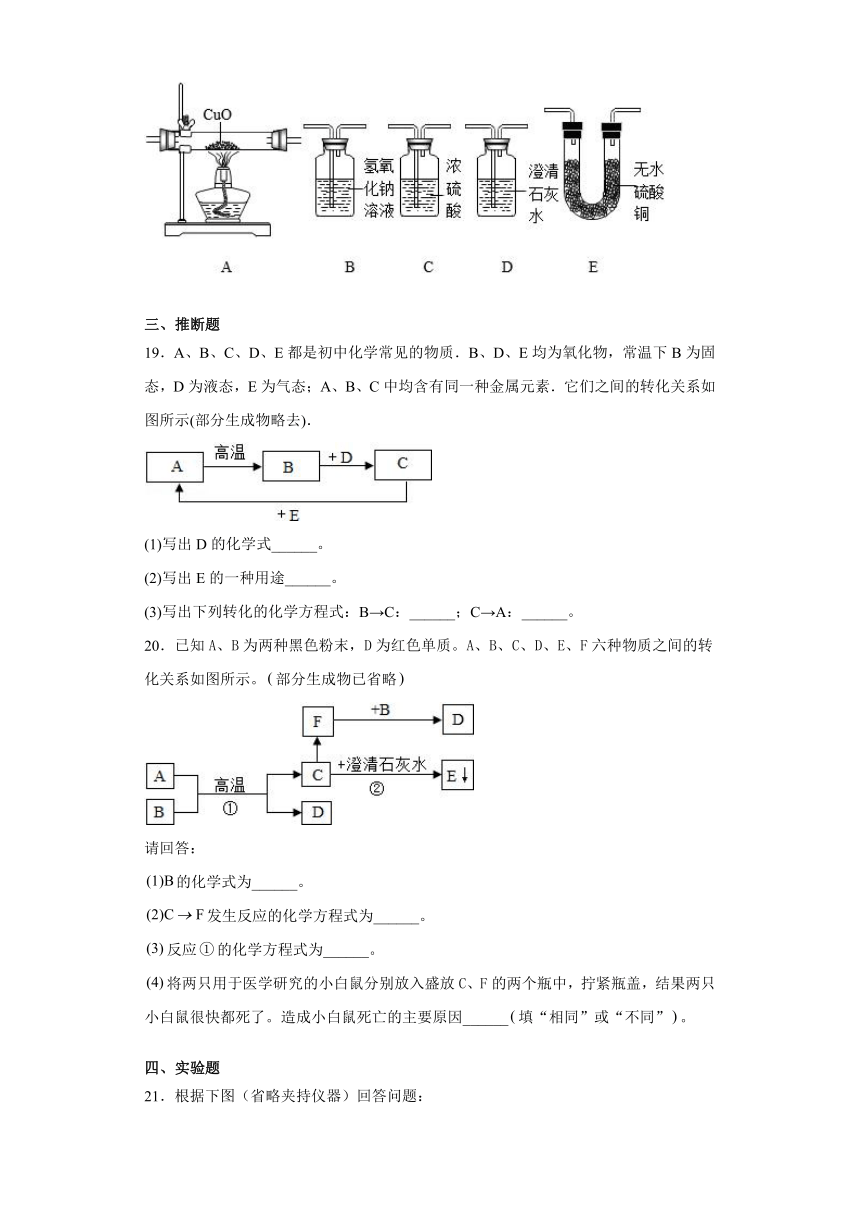
(4)欲用如图所示装置验证该高辛烷值汽油的燃烧尾气中含有CO2、CO和H2O,则装置正确的连接顺序是(用最少的装置,假设每步均完全反应)尾气→_______。
三、推断题
19.A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).
(1)写出D的化学式______。
(2)写出E的一种用途______。
(3)写出下列转化的化学方程式:B→C:______;C→A:______。
20.已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E、F六种物质之间的转化关系如图所示。部分生成物已省略
请回答:
的化学式为______。
发生反应的化学方程式为______。
反应的化学方程式为______。
将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了。造成小白鼠死亡的主要原因______填“相同”或“不同”。
四、实验题
21.根据下图(省略夹持仪器)回答问题:
(1)仪器e的名称是________。
(2)用高锰酸钾分解制取氧气的化学方程式为____________________________,制备并导出氧气的装置应选取仪器是c、h、________(填序号),收集氧气(用于做铁丝燃烧实验)应选取的仪器是________(填序号)。
(3)用锌粒和稀盐酸制备H2(可随时使反应发生或终止)应选取的仪器是________(填序号)。
(4)氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。课外小组同学利用(3)中产生的H2与金属钙反应制取CaH2(如图)。请回答:
①洗气瓶中m、n应选下列试剂的________、________(填序号)。
I.NaHCO3溶液、II.NaOH溶液、III.浓硫酸。
②为防止钙被氧化,在加热钙之前必须进行的操作是____。
③CaH2与水反应的化学方程式为_________。
22.实验是研究化学的重要方法。
实验一、气体制取和性质实验
(1)实验室常选用过氧化氢溶液制O2,则发生装置应选择图中的_______(填字母),请写出该反应的化学方程式_______。检验该装置气密性的方法是_______。
(2)制得的O2可选择E装置进行收集,可知O2具有_____性质。若选择F装置进行收集,则气体从____(填“a”或“b”)端通入。
(3)实验室制CO2的原理是_______(用化学方程式表示)。用G装置制备CO2,锥形瓶内的反应进行较长时间后,用燃着的火柴放在集气瓶口,火焰仍不熄灭的原因是_______。
实验二、探究H2O2质量分数、溶液pH、温度对H2O2分解速率的影响,设计下表实验方案:
实验序号
H2O2质量分数/%
pH
温度/℃
每分钟内产生气体体积
1
30
5
20
2
30
6
20
3
30
11
20
4
15
11
30
5
a
11
30
(4)实验1~3的实验目的是_______。
(5)实验3、5可探究温度对过氧化氢分解速率的影响,则a=_______。
实验三、探究制取氧气的适宜催化剂,实验方案如下:
步骤Ⅰ.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小完全相同的海藻酸钠微球,备用。
步骤Ⅱ.取m粒含MnO2的海藻酸钠微球,采用如图所示装置进行实验。改用其他三种微球,分别重复上述实验,得到如图所示的锥形瓶内压强随时间变化的曲线图。
(6)每次实验时,海藻酸钠微球数应相同的原因是_______。
(7)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其可能原因是_______。
(8)从实验曲线看,催化效果较好、反应温和的催化剂是_______。
五、计算题
23.为测定某金属锌样品中锌单质的质量分数,称取该样品进行如图所示实验。多次实验后,所得数据(平均值)如下表:
反应前质量
充分反应后质量
装置+稀硫酸(足量)
锌样品
装置+剩余物质
若锌样品中杂质不参加反应,且不考虑容器中水分蒸发。求:
(1)生成氢气的质量为________;
(2)该锌样品中锌单质的质量分数(要求写出计算过程)。
24.某市冬天取暖主要以煤为燃料。已知原煤中含硫1%,若燃烧1000
t这样的原煤可以产生二氧化硫________t,这些原煤中的硫元素全部转化成硫酸(
S→H2SO4),可生产0.05%的硫酸溶液_________t,通过以上信息你得到哪些启示?(答出两点即可)________
参考答案
1.C
2.A
3.B
4.C
5.B
6.B
7.A
8.B
9.B
10.D
11.C
12.A
13.D
14.B
15.(1)
太阳能
煤
(2)
CH4
热
(3)氢气
(4)CO
16.CO2
温室效应
BCD
A
17.
燃烧产热量高(燃烧产物无污染等)
18.①②③④
还原
In2O3
EDBDAD
19.H2O
灭火等
CaO+H2O=Ca(OH)2
CaCO3CaO+CO2↑
20.CuO
CO2+C2CO
C+
2CuO2Cu
+
CO2↑
不同
21.量筒
a、i
b、o、l、g
c、j、f、n(或d、f、i、n)
II
III
先通一段时间H2,排尽装置内空气
22.B
用止水夹夹住导管处的橡皮管,关闭分液漏斗活塞,往漏斗里注水,盖上漏斗盖,打开分液漏斗活塞,水不能顺利流下,表明气密性良好
不易溶于水,且与水不反应
a
长颈漏斗下端未在液面以下,反应生成的二氧化碳气体从长颈漏斗下端逸出
探究pH值对过氧化氢分解速率的影响
30
确保变量上只有催化剂的种类不同
反应速率过快,内部压强迅速增大,橡皮塞被弹开,压强瞬间回落
氧化铜
23.(1)根据质量守恒定律可知,生成的氢气的质量为342.10g+20.00g-361.70g=0.40g;
答:生成氢气的质量为0.40g。
(2)设锌单质的质量为x。
解得:x=13.00g
样品中锌单质的质量分数为
答:该锌样品中锌单质的质量分数为65%。
24.(1)20
(2)6.125×105(3)酸雨会给人类生活和生态带来严重危窖(如酸雨腐蚀大理石雕像、金属建筑物、破坏森林、酸化土壤等);使用脱硫煤;开发新能源代替现有的化石燃料等。
一、单选题
1.山西云岗石窟有很多佛像雕刻,原本栩栩如生的雕像已经变得模糊不清,有的表面还出现了斑点,造成这种现象的原因之一是酸雨.下列气体中能形成酸雨的是
A.O2
B.CO
C.SO2
D.N2
2.2021年6月5日世界环境日主题为“改善环境质量推动绿色发展”。下列做法不符合这一主题的是
A.大力发展燃煤发电
B.关停重污染企业
C.推广使用新能源汽车
D.限制燃放烟花爆竹
3.危险化学品泄漏或爆炸事件常给我们敲响安全警钟,操作不当就会存在安全隐患。下列做法错误的是
A.点燃氢气前先验纯
B.发现室内燃气泄漏,应立即打开排气扇通气
C.矿井作业要注意通风
D.油库、面粉厂、纺织厂等场所要严禁烟火
4.逻辑推理是一种重要的化学思维方法,以下推理合理的是
A.燃烧需要同时满足三个条件才能发生,所以灭火也一定同时控制这三个条件
B.因为CO、CO2的组成元素相同,所以它们的化学性质也相同
C.点燃H2与O2的混合气体可能爆炸,则点燃CH4和O2的混合气体也可能爆炸
D.把燃着的木条伸入某瓶无色气体中,木条熄灭,证明瓶中的气体一定是二氧化碳
5.如图是有关燃烧条件的探究(已知白磷的着火点为40℃,红磷的着火点是240℃)。下列说法正确的是
A.热水的作用只是为了提供热量
B.铜片上的白磷燃烧而红磷不燃烧说明温度是可燃物燃烧的条件之一
C.向水中的白磷通氧气,白磷也不会发生燃烧
D.该实验只能探究可燃物发生燃烧的一个条件
6.下列做法中,不正确的是
A.炒菜时油锅着火,立即盖上锅盖
B.家用电器着火时,立即用泡沫灭火器灭火
C.天然气泄漏时,立即关闭阀门并开窗
D.燃放烟花爆竹时,要远离人群和可燃物
7.下面是人们对化学科学的各种常见认识,其中错误的是
A.化学面对现代日益严重的环境问题显得无能为力
B.化学在能源、资源的合理开发和安全应用方面大显身手
C.化学是一门具有极强实用性的科学
D.化学的发展极大满足了人们对新物质的需求
8.下列关于“碳循环”和“氧循环”的说法错误的是
A.碳循环和氧循环过程中均发生了化学变化
B.碳循环和氧循环分别是指二氧化碳和氧气的循环
C.绿色植物通过光合作用,将太阳能转化成化学能
D.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
9.今年春天我国多地发生火灾,造成巨大生命财产损失,警示我们,消防安全是保障我们人身财产安全的一项重要工程,下列有关说法正确的是
A.发现天然气泄漏,点火检查泄漏处
B.电器着火应先切断电源,再用二氧化碳灭火器扑灭
C.所有的爆炸都是由剧烈燃烧引起的
D.消防员用高压水枪灭火的原理是降低了可燃物的着火点
10.下列有关燃烧与灭火的说法正确的是
A.电烤炉着火时,用水浇灭
B.用扇子可以扇灭蜡烛,是因为可以降低着火点
C.煤炉的火焰呈现黄色时,调小进风口可使燃烧更充分
D.液态氧和气态氧都能助燃,是因为同种分子其化学性质相同
11.下列关于石油的说法,错误的是
A.石油是混合物
B.石油产品可用于发电
C.石油是一种化工产品
D.石油是不可再生资源
12.充分燃烧1kg天然气和煤所产生的CO2和SO2气体的质量如图所示,请利用所学知识,并结合图像判断下列叙述正确的是
①煤和天然气均属于化石燃料
②等量的煤和天然气充分燃烧,煤更容易导致酸雨
③使用天然气有助于缓解温室效应加剧的环境问题
④有煤存在的地方,都有天然气存在
A.①②
B.①④
C.②③
D.③④
13.实验室有如下气体发生装置和气体收集装置:
下列说法中,错误的是
A.用锌和稀盐酸制取H2可选用b、d
B.用大理石和稀盐酸制取CO2可选用b、c
C.用氯酸钾和二氧化锰制取O2可选用a、e
D.用过氧化氢溶液和二氧化锰制取O2可选用a、c
14.以空气等为原料合成尿素[CO(NH2)2]的流程如下图所示,下列有关该流程的说法不正确的是
A.X是N2
B.合成过程中发生了化合反应
C.分离空气的过程属于物理变化
D.化学反应中发生物质变化的同时也会伴随着能量的变化
二、填空题
15.能源利用和环境保护问题一直受到社会高度关注。
(1)太阳能和煤中,属于可再生能源的是______,属于不可再生能源的是______。
(2)天然气的主要成分是______(填化学式)。它燃烧主要是将化学能转化为______能。
(3)从环境保护的角度考虑,最理想的燃料是______(填物质名称)。
(4)煤在不充分燃烧的情况下,会产生某些有毒气体。其中______(填化学式)极易与血液中的血红蛋白结合,引起中毒。
16.2020年9月,习近平在联大针对气候变化表示:“中国将力争碳排放2030年前达到峰值,争取在2060年前实现碳中和”。由所学知识回答:
(1)以上说的“碳排放和碳中和”中的“碳”指的是______(填化学式),降低碳排放会减缓______。现阶段,下列措施合理的是______(填序号)。
A.禁止烧煤
B.研发汽车新能源
C.鼓励乘坐公交出行
D.随手关灯
(2)氢燃料电池把氢能转化为电能,氢燃料电池的优点是______(填序号)。
A.产物是水,不污染空气
B.制取氢气成本较低
(3)甲醇(CH3OH)也是一种新型燃料,试写出甲醇完全燃烧的化学方程式:______。
17.燃料的利用与生产生活密切相关。
(1)酒精完全燃烧的化学方程式为______;
(2)氢气作为最理想的新型能源,其优点是______(写出一条即可)。
18.2017年我国研制出一种新型多功能复合催化剂,首次实现了二氧化碳直接加氢制取高辛烷值汽油。
(1)对“CO2变汽油”的研究成果,下列说法正确的是_______(填序号)。
①可有效缓解全球温室效应
②可减少对化石燃料的依赖
③该转化过程中发生化学变化
④该催化剂在该反应中可以重复使用
(2)通过如图I、II、III三个环节,可将CO2成功转化为汽油。一定条件下,环节I除生成CO外,还生成了一种化合物,反应的化学方程式为_______,该反应中CO2发生了_______(填“氧化或还原”)反应。
(3)氧化铟是复合催化剂的成分之一、元素周期表中,铟(In)元素与铝元素位于同一族,写出氧化铟的化学式_______。
(4)欲用如图所示装置验证该高辛烷值汽油的燃烧尾气中含有CO2、CO和H2O,则装置正确的连接顺序是(用最少的装置,假设每步均完全反应)尾气→_______。
三、推断题
19.A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).
(1)写出D的化学式______。
(2)写出E的一种用途______。
(3)写出下列转化的化学方程式:B→C:______;C→A:______。
20.已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E、F六种物质之间的转化关系如图所示。部分生成物已省略
请回答:
的化学式为______。
发生反应的化学方程式为______。
反应的化学方程式为______。
将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了。造成小白鼠死亡的主要原因______填“相同”或“不同”。
四、实验题
21.根据下图(省略夹持仪器)回答问题:
(1)仪器e的名称是________。
(2)用高锰酸钾分解制取氧气的化学方程式为____________________________,制备并导出氧气的装置应选取仪器是c、h、________(填序号),收集氧气(用于做铁丝燃烧实验)应选取的仪器是________(填序号)。
(3)用锌粒和稀盐酸制备H2(可随时使反应发生或终止)应选取的仪器是________(填序号)。
(4)氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。课外小组同学利用(3)中产生的H2与金属钙反应制取CaH2(如图)。请回答:
①洗气瓶中m、n应选下列试剂的________、________(填序号)。
I.NaHCO3溶液、II.NaOH溶液、III.浓硫酸。
②为防止钙被氧化,在加热钙之前必须进行的操作是____。
③CaH2与水反应的化学方程式为_________。
22.实验是研究化学的重要方法。
实验一、气体制取和性质实验
(1)实验室常选用过氧化氢溶液制O2,则发生装置应选择图中的_______(填字母),请写出该反应的化学方程式_______。检验该装置气密性的方法是_______。
(2)制得的O2可选择E装置进行收集,可知O2具有_____性质。若选择F装置进行收集,则气体从____(填“a”或“b”)端通入。
(3)实验室制CO2的原理是_______(用化学方程式表示)。用G装置制备CO2,锥形瓶内的反应进行较长时间后,用燃着的火柴放在集气瓶口,火焰仍不熄灭的原因是_______。
实验二、探究H2O2质量分数、溶液pH、温度对H2O2分解速率的影响,设计下表实验方案:
实验序号
H2O2质量分数/%
pH
温度/℃
每分钟内产生气体体积
1
30
5
20
2
30
6
20
3
30
11
20
4
15
11
30
5
a
11
30
(4)实验1~3的实验目的是_______。
(5)实验3、5可探究温度对过氧化氢分解速率的影响,则a=_______。
实验三、探究制取氧气的适宜催化剂,实验方案如下:
步骤Ⅰ.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小完全相同的海藻酸钠微球,备用。
步骤Ⅱ.取m粒含MnO2的海藻酸钠微球,采用如图所示装置进行实验。改用其他三种微球,分别重复上述实验,得到如图所示的锥形瓶内压强随时间变化的曲线图。
(6)每次实验时,海藻酸钠微球数应相同的原因是_______。
(7)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其可能原因是_______。
(8)从实验曲线看,催化效果较好、反应温和的催化剂是_______。
五、计算题
23.为测定某金属锌样品中锌单质的质量分数,称取该样品进行如图所示实验。多次实验后,所得数据(平均值)如下表:
反应前质量
充分反应后质量
装置+稀硫酸(足量)
锌样品
装置+剩余物质
若锌样品中杂质不参加反应,且不考虑容器中水分蒸发。求:
(1)生成氢气的质量为________;
(2)该锌样品中锌单质的质量分数(要求写出计算过程)。
24.某市冬天取暖主要以煤为燃料。已知原煤中含硫1%,若燃烧1000
t这样的原煤可以产生二氧化硫________t,这些原煤中的硫元素全部转化成硫酸(
S→H2SO4),可生产0.05%的硫酸溶液_________t,通过以上信息你得到哪些启示?(答出两点即可)________
参考答案
1.C
2.A
3.B
4.C
5.B
6.B
7.A
8.B
9.B
10.D
11.C
12.A
13.D
14.B
15.(1)
太阳能
煤
(2)
CH4
热
(3)氢气
(4)CO
16.CO2
温室效应
BCD
A
17.
燃烧产热量高(燃烧产物无污染等)
18.①②③④
还原
In2O3
EDBDAD
19.H2O
灭火等
CaO+H2O=Ca(OH)2
CaCO3CaO+CO2↑
20.CuO
CO2+C2CO
C+
2CuO2Cu
+
CO2↑
不同
21.量筒
a、i
b、o、l、g
c、j、f、n(或d、f、i、n)
II
III
先通一段时间H2,排尽装置内空气
22.B
用止水夹夹住导管处的橡皮管,关闭分液漏斗活塞,往漏斗里注水,盖上漏斗盖,打开分液漏斗活塞,水不能顺利流下,表明气密性良好
不易溶于水,且与水不反应
a
长颈漏斗下端未在液面以下,反应生成的二氧化碳气体从长颈漏斗下端逸出
探究pH值对过氧化氢分解速率的影响
30
确保变量上只有催化剂的种类不同
反应速率过快,内部压强迅速增大,橡皮塞被弹开,压强瞬间回落
氧化铜
23.(1)根据质量守恒定律可知,生成的氢气的质量为342.10g+20.00g-361.70g=0.40g;
答:生成氢气的质量为0.40g。
(2)设锌单质的质量为x。
解得:x=13.00g
样品中锌单质的质量分数为
答:该锌样品中锌单质的质量分数为65%。
24.(1)20
(2)6.125×105(3)酸雨会给人类生活和生态带来严重危窖(如酸雨腐蚀大理石雕像、金属建筑物、破坏森林、酸化土壤等);使用脱硫煤;开发新能源代替现有的化石燃料等。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
