第2章 身边的化学物质 期末达标测试卷——2021-2022学年沪教版九年级上册化学(word版 含答案)
文档属性
| 名称 | 第2章 身边的化学物质 期末达标测试卷——2021-2022学年沪教版九年级上册化学(word版 含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 420.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-04 00:00:00 | ||
图片预览



文档简介
第二章达标测试卷
可能用到的相对原子质量:H:1 B:11 C:12 O:16
第Ⅰ卷 选择题
本卷共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一个选项符合题目要求。
1.材料与人类生活密切相关。下列物品的主要成分属于有机合成材料的是( )
2.“庄稼一枝花,全靠肥当家。”下列属于复合肥料的是( )
A.NH4HCO3
B.KCl
C.(NH4)2HPO4
D.CO(NH2)2
3.“中国绿都·最氧三明”是三明市名片。下列做法不利于保护三明市“绿水青山”的是( )
A.全面推广垃圾分类回收
B.生活污水直接排入河流中
C.用新能源公交车代替老旧公交车
D.购物时使用布袋等代替塑料袋
4.下列实验基本操作中,正确的是( )
5.石油古称“洧水”,《汉书》中“高奴县有洧水可燃”,《梦溪笔谈》中“予知其烟可用,试扫其烟为墨,黑光如漆”,下列关于“洧水”的说法错误的是( )
A.具有可燃性
B.是一种黏稠状液体
C.是可再生能源
D.“其烟”的主要成分为炭黑
6.
维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法中错误的是( )
A.维生素C是有机物
B.维生素C中氢元素的质量分数约是4.5%
C.维生素C中含氢分子和氧分子的个数比是4∶3
D.维生素C中C、H、O三种元素的质量比是9∶1∶12
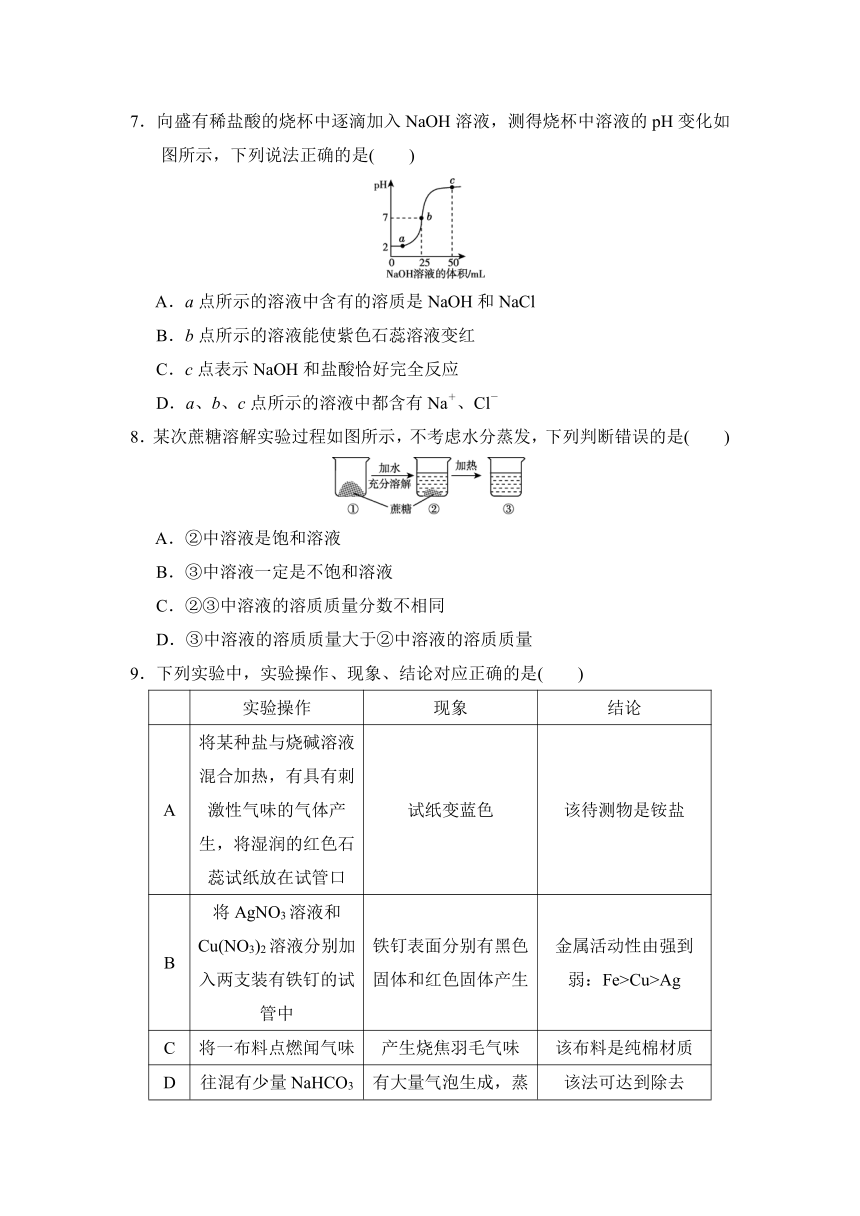
7.向盛有稀盐酸的烧杯中逐滴加入NaOH溶液,测得烧杯中溶液的pH变化如图所示,下列说法正确的是( )
A.a点所示的溶液中含有的溶质是NaOH和NaCl
B.b点所示的溶液能使紫色石蕊溶液变红
C.c点表示NaOH和盐酸恰好完全反应
D.a、b、c点所示的溶液中都含有Na+、Cl-
8.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
9.下列实验中,实验操作、现象、结论对应正确的是( )
实验操作
现象
结论
A
将某种盐与烧碱溶液混合加热,有具有刺激性气味的气体产生,将湿润的红色石蕊试纸放在试管口
试纸变蓝色
该待测物是铵盐
B
将AgNO3溶液和Cu(NO3)2溶液分别加入两支装有铁钉的试管中
铁钉表面分别有黑色固体和红色固体产生
金属活动性由强到弱:Fe>Cu>Ag
C
将一布料点燃闻气味
产生烧焦羽毛气味
该布料是纯棉材质
D
往混有少量NaHCO3的Na2CO3固体中加入稀盐酸,并蒸发结晶
有大量气泡生成,蒸发后得到白色晶体
该法可达到除去NaHCO3的目的
10.往石灰水中先滴加稀盐酸,然后滴加碳酸钠溶液,溶液pH的部分变化如图所示。下列分析正确的是( )
A.ab段的反应现象是产生沉淀
B.b点时,溶液中可能有HCl或Na2CO3,但不可能两种都有
C.c点时,溶液中没有发生化学反应
D.d点时,溶液中的溶质为Na2CO3、NaCl、CaCO3
第Ⅱ卷 非选择题
本卷共8题,共70分。
11.(6分)化学与我们的生产、生活息息相关,现有以下物质:
①食醋 ②Na2CO3 ③葡萄糖 ④CH4 ⑤熟石灰 ⑥维生素A
请选择合适物质的序号填空:
(1)用来制造洗涤剂、洗衣粉的是________。
(2)能为人体提供能量的物质是________。
(3)常用作厨房调味品的是________。
(4)常用于改良酸性土壤的是________。
(5)最简单的有机化合物是________。
(6)人体缺乏后能导致夜盲症的是________。
12.(10分)用化学知识解释生活中的问题。
(1)某学校学生的午餐为米饭、炖牛肉、炒芹菜、油炸花生米等,其中富含蛋白质的是________。
(2)在治疗胃酸过多症的药物成分中,含有的物质不可能是________(填字母)。
A.碳酸氢钠
B.氢氧化铝
C.氢氧化钠
D.碳酸钙
(3)生活中常用作食品干燥剂的是________,其干燥原理是_____________________________________________________________(用化学方程式表示)。
(4)用汽油或加了洗涤剂的水都能除去衣服上的油污,其中洗涤剂清洗油污原理是______________________________________________________。
(5)汽车方便了人们的出行,氢能源汽车备受人们关注。氢能源汽车在行驶过程中的能量转化是从________能开始,最终转化为________能。氢能源有本身无毒、原料来源广、可再生、_________________________________________(填一点)等优点。
13.(7分)右表是某同学自制盐汽水的配料用量表。已知:20
℃时,氯化钠的溶解度为36.0
g。
(1)盐汽水的能量很低,能量主要由________提供。
(2)20
℃时,该盐汽水____________(填“能”或“不能”)继续溶解氯化钠固体。氯化钠固体溶于水形成溶液的过程中,溶液的温度________________(填“降低”“升高”或“基本不变”)。
(3)柠檬酸(C6H8O7)中碳、氢元素的质量比为________。
(4)盐汽水中的“汽”是由柠檬酸与小苏打反应生成二氧化碳、水和柠檬酸钠(C6H5O7Na3)形成的,该反应的化学方程式为___________________________________。
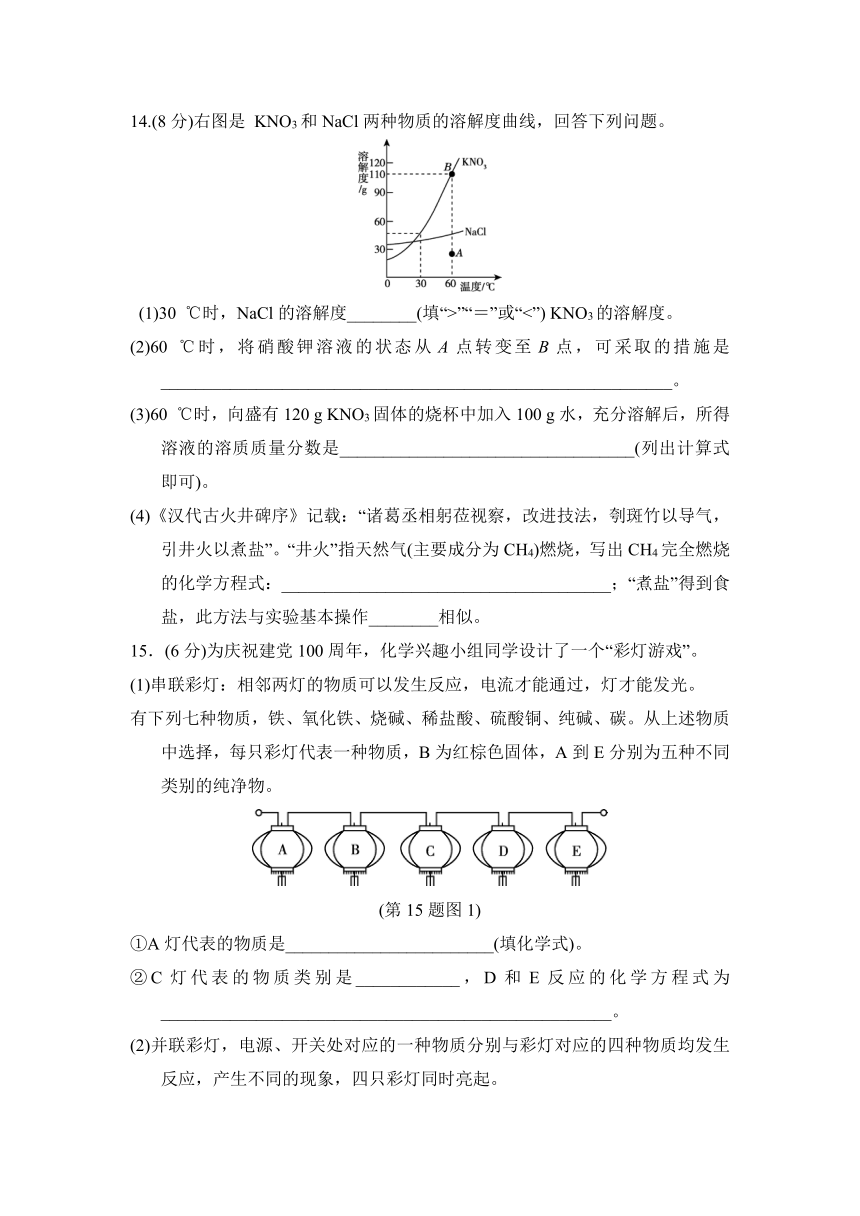
14.(8分)右图是
KNO3和NaCl两种物质的溶解度曲线,回答下列问题。
(1)30
℃时,NaCl的溶解度________(填“>”“=”或“<”)
KNO3的溶解度。
(2)60
℃时,将硝酸钾溶液的状态从A点转变至B点,可采取的措施是___________________________________________________________。
(3)60
℃时,向盛有120
g
KNO3固体的烧杯中加入100
g水,充分溶解后,所得溶液的溶质质量分数是__________________________________(列出计算式即可)。
(4)《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气,引井火以煮盐”。“井火”指天然气(主要成分为CH4)燃烧,写出CH4完全燃烧的化学方程式:______________________________________;“煮盐”得到食盐,此方法与实验基本操作________相似。
15.(6分)为庆祝建党100周年,化学兴趣小组同学设计了一个“彩灯游戏”。
(1)串联彩灯:相邻两灯的物质可以发生反应,电流才能通过,灯才能发光。
有下列七种物质,铁、氧化铁、烧碱、稀盐酸、硫酸铜、纯碱、碳。从上述物质中选择,每只彩灯代表一种物质,B为红棕色固体,A到E分别为五种不同类别的纯净物。
(第15题图1)
①A灯代表的物质是________________________(填化学式)。
②C灯代表的物质类别是____________,D和E反应的化学方程式为____________________________________________________。
(2)并联彩灯,电源、开关处对应的一种物质分别与彩灯对应的四种物质均发生反应,产生不同的现象,四只彩灯同时亮起。
(第15题图2)
①电源、开关处的物质是________________________(填化学式)。
②Cu(NO3)2处对应的现象是____________________________________________。
16.(7分)请你参与实验室配制一定溶质质量分数的硝酸钾溶液的实验,并进行实验过程的探究:
(1)计算:配制50
g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为________g,所需蒸馏水的体积为________mL(水的密度约为1
g/cm3)。
(2)称量:分别在天平左右两盘放上纸片,调节平衡后,应________(填序号)。
A.先在托盘上放置所需的砝码,再添加硝酸钾直至天平平衡
B.先添加所需的硝酸钾,再添加砝码直至天平平衡
【探究】在称量过程中,某同学的称量操作如图1所示,你认为该操作对本次实验的数据处理的正确性________(填“有”或“没有”)影响,理由是__________________________________。
(3)量取:准确量取所需蒸馏水要用到的仪器是________(填图2中的序号)。
(4)溶解:将称量好的硝酸钾和蒸馏水混合溶解。
17.(20分)为验证氢氧化钠与盐酸反应,化学小组同学用各自实验台上提供的药品做了实验探究和微观探析。
(第17题图1)
(1)甲组同学向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后溶液仍为无色,此现象________(填“能”或“不能”)证明氢氧化钠与盐酸发生了反应。
(2)乙组同学进行实验时,发现试管中出现了“怪现象”:有气泡产生。同学们通过讨论一致认为乙组同学所用的NaOH溶液已变质,写出产生气泡的反应的化学方程式:___________________________________________。
【提出问题】变质的NaOH溶液中含有哪些溶质?
【作出猜想】猜想一:________;猜想二:NaOH、Na2CO3
【查阅资料】1.CaCl2溶液显中性。
2.稀盐酸和氢氧化钠溶液反应的微观变化如图2所示。
(第17题图2)
【进行实验】
(第17题图3)
①操作Ⅰ所得固体物质是________(填名称)。
②滴加酚酞溶液后的现象为___________________________________________,证明猜想二成立。
③小丹同学用CuSO4溶液代替酚酞溶液也证明了猜想二成立,写出此反应的化学方程式:______________________________________。
【反思交流】实验室的化学药品应____________保存。
【微观探析】分析图中反应前后没有发生变化的微粒是钠离子和氯离子,反应的实质是______________和____________结合生成水。
18.(6分)“7150灭火剂”(C3H9B3O6,相对分子质量为174)以雾状形式喷射到燃着的金属时,立即发生燃烧反应:2C3H9B3O6+9O23B2O3+9H2O+6CO2。反应能很快耗尽金属物质附近的氧气,生成的玻璃状物质B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348
g“7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4
g·L-1,结果保留一位小数)
答案
第Ⅰ卷
1.B 2.C 3.B 4.D 5.C 6.C
7.D 点拨:a点时溶液的pH小于7,溶液显酸性,说明稀盐酸过量,所得溶液中的溶质为HCl和NaCl;b点溶液的pH等于7,呈中性,不能使紫色石蕊溶液变红;c点溶液的pH大于7,呈碱性,氢氧化钠溶液过量;氢氧化钠与盐酸反应生成氯化钠和水,a、b、c点所示的溶液中均含有氯化钠,都含有Na+、Cl-。
8.B 点拨:①→②充分溶解后固体有剩余,②中溶液是饱和溶液,②加热得到溶液③,③中没有固体剩余,③中溶液有可能是饱和溶液,也有可能是不饱和溶液。
9.A 点拨:A.铵盐与碱反应生成氨气,氨气有刺激性气味,氨气与湿润的红色石蕊试纸接触,氨气与水结合生成氨水,氨水显碱性能使红色石蕊试纸变蓝,故A正确;B.将AgNO3溶液和Cu(NO3)2溶液分别加入两支装有铁钉的试管中,铁钉表面分别有黑色固体和红色固体产生,这两个实验能判断出金属活动性顺序:Fe>Ag和Fe>Cu,但无法判断Cu和Ag的金属活动性强弱,故B不正确;C.灼烧纯棉布料,不会闻到烧焦羽毛气味,故C不正确;D.NaHCO3和Na2CO3都能与盐酸反应,不仅能除掉NaHCO3,而且将主要物质Na2CO3也反应了,无法达到实验目的,故D不正确。
故选A。
10.C
第Ⅱ卷
11.(1)② (2)③ (3)①
(4)⑤ (5)④ (6)⑥
12.(1)炖牛肉
(2)C
(3)CaO;CaO+H2O===Ca(OH)2
(4)乳化作用
(5)化学(或氢);机械;燃烧产物是水,不污染空气(或热值高)
13.(1)蔗糖
(2)能;基本不变
(3)9∶1
(4)3NaHCO3+C6H8O7===C6H5O7Na3+3H2O+3CO2↑
14.(1)<
(2)加入适量的硝酸钾(或恒温蒸发一部分水)
(3)×100%
(4)CH4+2O2CO2+2H2O;蒸发结晶
点拨:(1)由图可知,30
℃时,NaCl的溶解度(2)60
℃时,将硝酸钾溶液的状态从A点(不饱和溶液),转变至B点(饱和溶液),可采取的措施是加入适量的硝酸钾或恒温蒸发一部分水。
(3)60
℃时,硝酸钾溶解度为110
g,向盛有120
g
KNO3固体的烧杯中加入100
g水,充分溶解后,所得溶液的溶质质量分数是×100%。
(4)CH4完全燃烧生成二氧化碳和水,化学方程式为CH4+2O2CO2+2H2O,“煮盐”得到食盐,此方法与实验基本操作蒸发结晶相似。
15.(1)①C
②酸;2NaOH+CuSO4
===Na2SO4+Cu(OH)2↓
(2)①Ba(OH)2 ②产生蓝色沉淀
16.(1)5;45
(2)A
【探究】没有;称量过程中没有使用游码
(3)B、C
17.(1)能
(2)Na2CO3+2HCl===2NaCl+H2O+CO2↑
【作出猜想】Na2CO3
【进行实验】①碳酸钙 ②溶液B变成红色
③CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
【反思交流】密封
【微观探析】氢离子(或H+);氢氧根离子(或OH-)
点拨:(1)碱性溶液能使酚酞变红色,所以甲组同学向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后溶液仍为无色,此现象能证明氢氧化钠与盐酸发生了反应;
(2)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为Na2CO3+2HCl
===2NaCl+H2O+CO2↑;
【作出猜想】氢氧化钠可能部分变质,可能全部变质,全部变质生成Na2CO3;
①变质氢氧化钠中含有碳酸钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
②酚酞遇碱性溶液变红色,所以滴加酚酞溶液后的现象为溶液B变成红色,证明猜想二成立;
③氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为CuSO4+2NaOH
===Cu(OH)2↓+Na2SO4;
【反思交流】为防止变质,实验室的化学药品应密封保存;
【微观探析】图中反应前后没有发生变化的微粒是钠离子和氯离子,反应的实质是氢离子和氢氧根离子结合生成水。
18.解:设消耗氧气的质量为x。
2C3H9B3O6+9O23B2O3+9H2O+6CO2
348
288
348
g
x
=
x=288
g
氧气的体积=≈205.7
L。
答:消耗常温下205.7
L的氧气。
可能用到的相对原子质量:H:1 B:11 C:12 O:16
第Ⅰ卷 选择题
本卷共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一个选项符合题目要求。
1.材料与人类生活密切相关。下列物品的主要成分属于有机合成材料的是( )
2.“庄稼一枝花,全靠肥当家。”下列属于复合肥料的是( )
A.NH4HCO3
B.KCl
C.(NH4)2HPO4
D.CO(NH2)2
3.“中国绿都·最氧三明”是三明市名片。下列做法不利于保护三明市“绿水青山”的是( )
A.全面推广垃圾分类回收
B.生活污水直接排入河流中
C.用新能源公交车代替老旧公交车
D.购物时使用布袋等代替塑料袋
4.下列实验基本操作中,正确的是( )
5.石油古称“洧水”,《汉书》中“高奴县有洧水可燃”,《梦溪笔谈》中“予知其烟可用,试扫其烟为墨,黑光如漆”,下列关于“洧水”的说法错误的是( )
A.具有可燃性
B.是一种黏稠状液体
C.是可再生能源
D.“其烟”的主要成分为炭黑
6.
维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法中错误的是( )
A.维生素C是有机物
B.维生素C中氢元素的质量分数约是4.5%
C.维生素C中含氢分子和氧分子的个数比是4∶3
D.维生素C中C、H、O三种元素的质量比是9∶1∶12
7.向盛有稀盐酸的烧杯中逐滴加入NaOH溶液,测得烧杯中溶液的pH变化如图所示,下列说法正确的是( )
A.a点所示的溶液中含有的溶质是NaOH和NaCl
B.b点所示的溶液能使紫色石蕊溶液变红
C.c点表示NaOH和盐酸恰好完全反应
D.a、b、c点所示的溶液中都含有Na+、Cl-
8.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
9.下列实验中,实验操作、现象、结论对应正确的是( )
实验操作
现象
结论
A
将某种盐与烧碱溶液混合加热,有具有刺激性气味的气体产生,将湿润的红色石蕊试纸放在试管口
试纸变蓝色
该待测物是铵盐
B
将AgNO3溶液和Cu(NO3)2溶液分别加入两支装有铁钉的试管中
铁钉表面分别有黑色固体和红色固体产生
金属活动性由强到弱:Fe>Cu>Ag
C
将一布料点燃闻气味
产生烧焦羽毛气味
该布料是纯棉材质
D
往混有少量NaHCO3的Na2CO3固体中加入稀盐酸,并蒸发结晶
有大量气泡生成,蒸发后得到白色晶体
该法可达到除去NaHCO3的目的
10.往石灰水中先滴加稀盐酸,然后滴加碳酸钠溶液,溶液pH的部分变化如图所示。下列分析正确的是( )
A.ab段的反应现象是产生沉淀
B.b点时,溶液中可能有HCl或Na2CO3,但不可能两种都有
C.c点时,溶液中没有发生化学反应
D.d点时,溶液中的溶质为Na2CO3、NaCl、CaCO3
第Ⅱ卷 非选择题
本卷共8题,共70分。
11.(6分)化学与我们的生产、生活息息相关,现有以下物质:
①食醋 ②Na2CO3 ③葡萄糖 ④CH4 ⑤熟石灰 ⑥维生素A
请选择合适物质的序号填空:
(1)用来制造洗涤剂、洗衣粉的是________。
(2)能为人体提供能量的物质是________。
(3)常用作厨房调味品的是________。
(4)常用于改良酸性土壤的是________。
(5)最简单的有机化合物是________。
(6)人体缺乏后能导致夜盲症的是________。
12.(10分)用化学知识解释生活中的问题。
(1)某学校学生的午餐为米饭、炖牛肉、炒芹菜、油炸花生米等,其中富含蛋白质的是________。
(2)在治疗胃酸过多症的药物成分中,含有的物质不可能是________(填字母)。
A.碳酸氢钠
B.氢氧化铝
C.氢氧化钠
D.碳酸钙
(3)生活中常用作食品干燥剂的是________,其干燥原理是_____________________________________________________________(用化学方程式表示)。
(4)用汽油或加了洗涤剂的水都能除去衣服上的油污,其中洗涤剂清洗油污原理是______________________________________________________。
(5)汽车方便了人们的出行,氢能源汽车备受人们关注。氢能源汽车在行驶过程中的能量转化是从________能开始,最终转化为________能。氢能源有本身无毒、原料来源广、可再生、_________________________________________(填一点)等优点。
13.(7分)右表是某同学自制盐汽水的配料用量表。已知:20
℃时,氯化钠的溶解度为36.0
g。
(1)盐汽水的能量很低,能量主要由________提供。
(2)20
℃时,该盐汽水____________(填“能”或“不能”)继续溶解氯化钠固体。氯化钠固体溶于水形成溶液的过程中,溶液的温度________________(填“降低”“升高”或“基本不变”)。
(3)柠檬酸(C6H8O7)中碳、氢元素的质量比为________。
(4)盐汽水中的“汽”是由柠檬酸与小苏打反应生成二氧化碳、水和柠檬酸钠(C6H5O7Na3)形成的,该反应的化学方程式为___________________________________。
14.(8分)右图是
KNO3和NaCl两种物质的溶解度曲线,回答下列问题。
(1)30
℃时,NaCl的溶解度________(填“>”“=”或“<”)
KNO3的溶解度。
(2)60
℃时,将硝酸钾溶液的状态从A点转变至B点,可采取的措施是___________________________________________________________。
(3)60
℃时,向盛有120
g
KNO3固体的烧杯中加入100
g水,充分溶解后,所得溶液的溶质质量分数是__________________________________(列出计算式即可)。
(4)《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气,引井火以煮盐”。“井火”指天然气(主要成分为CH4)燃烧,写出CH4完全燃烧的化学方程式:______________________________________;“煮盐”得到食盐,此方法与实验基本操作________相似。
15.(6分)为庆祝建党100周年,化学兴趣小组同学设计了一个“彩灯游戏”。
(1)串联彩灯:相邻两灯的物质可以发生反应,电流才能通过,灯才能发光。
有下列七种物质,铁、氧化铁、烧碱、稀盐酸、硫酸铜、纯碱、碳。从上述物质中选择,每只彩灯代表一种物质,B为红棕色固体,A到E分别为五种不同类别的纯净物。
(第15题图1)
①A灯代表的物质是________________________(填化学式)。
②C灯代表的物质类别是____________,D和E反应的化学方程式为____________________________________________________。
(2)并联彩灯,电源、开关处对应的一种物质分别与彩灯对应的四种物质均发生反应,产生不同的现象,四只彩灯同时亮起。
(第15题图2)
①电源、开关处的物质是________________________(填化学式)。
②Cu(NO3)2处对应的现象是____________________________________________。
16.(7分)请你参与实验室配制一定溶质质量分数的硝酸钾溶液的实验,并进行实验过程的探究:
(1)计算:配制50
g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为________g,所需蒸馏水的体积为________mL(水的密度约为1
g/cm3)。
(2)称量:分别在天平左右两盘放上纸片,调节平衡后,应________(填序号)。
A.先在托盘上放置所需的砝码,再添加硝酸钾直至天平平衡
B.先添加所需的硝酸钾,再添加砝码直至天平平衡
【探究】在称量过程中,某同学的称量操作如图1所示,你认为该操作对本次实验的数据处理的正确性________(填“有”或“没有”)影响,理由是__________________________________。
(3)量取:准确量取所需蒸馏水要用到的仪器是________(填图2中的序号)。
(4)溶解:将称量好的硝酸钾和蒸馏水混合溶解。
17.(20分)为验证氢氧化钠与盐酸反应,化学小组同学用各自实验台上提供的药品做了实验探究和微观探析。
(第17题图1)
(1)甲组同学向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后溶液仍为无色,此现象________(填“能”或“不能”)证明氢氧化钠与盐酸发生了反应。
(2)乙组同学进行实验时,发现试管中出现了“怪现象”:有气泡产生。同学们通过讨论一致认为乙组同学所用的NaOH溶液已变质,写出产生气泡的反应的化学方程式:___________________________________________。
【提出问题】变质的NaOH溶液中含有哪些溶质?
【作出猜想】猜想一:________;猜想二:NaOH、Na2CO3
【查阅资料】1.CaCl2溶液显中性。
2.稀盐酸和氢氧化钠溶液反应的微观变化如图2所示。
(第17题图2)
【进行实验】
(第17题图3)
①操作Ⅰ所得固体物质是________(填名称)。
②滴加酚酞溶液后的现象为___________________________________________,证明猜想二成立。
③小丹同学用CuSO4溶液代替酚酞溶液也证明了猜想二成立,写出此反应的化学方程式:______________________________________。
【反思交流】实验室的化学药品应____________保存。
【微观探析】分析图中反应前后没有发生变化的微粒是钠离子和氯离子,反应的实质是______________和____________结合生成水。
18.(6分)“7150灭火剂”(C3H9B3O6,相对分子质量为174)以雾状形式喷射到燃着的金属时,立即发生燃烧反应:2C3H9B3O6+9O23B2O3+9H2O+6CO2。反应能很快耗尽金属物质附近的氧气,生成的玻璃状物质B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348
g“7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4
g·L-1,结果保留一位小数)
答案
第Ⅰ卷
1.B 2.C 3.B 4.D 5.C 6.C
7.D 点拨:a点时溶液的pH小于7,溶液显酸性,说明稀盐酸过量,所得溶液中的溶质为HCl和NaCl;b点溶液的pH等于7,呈中性,不能使紫色石蕊溶液变红;c点溶液的pH大于7,呈碱性,氢氧化钠溶液过量;氢氧化钠与盐酸反应生成氯化钠和水,a、b、c点所示的溶液中均含有氯化钠,都含有Na+、Cl-。
8.B 点拨:①→②充分溶解后固体有剩余,②中溶液是饱和溶液,②加热得到溶液③,③中没有固体剩余,③中溶液有可能是饱和溶液,也有可能是不饱和溶液。
9.A 点拨:A.铵盐与碱反应生成氨气,氨气有刺激性气味,氨气与湿润的红色石蕊试纸接触,氨气与水结合生成氨水,氨水显碱性能使红色石蕊试纸变蓝,故A正确;B.将AgNO3溶液和Cu(NO3)2溶液分别加入两支装有铁钉的试管中,铁钉表面分别有黑色固体和红色固体产生,这两个实验能判断出金属活动性顺序:Fe>Ag和Fe>Cu,但无法判断Cu和Ag的金属活动性强弱,故B不正确;C.灼烧纯棉布料,不会闻到烧焦羽毛气味,故C不正确;D.NaHCO3和Na2CO3都能与盐酸反应,不仅能除掉NaHCO3,而且将主要物质Na2CO3也反应了,无法达到实验目的,故D不正确。
故选A。
10.C
第Ⅱ卷
11.(1)② (2)③ (3)①
(4)⑤ (5)④ (6)⑥
12.(1)炖牛肉
(2)C
(3)CaO;CaO+H2O===Ca(OH)2
(4)乳化作用
(5)化学(或氢);机械;燃烧产物是水,不污染空气(或热值高)
13.(1)蔗糖
(2)能;基本不变
(3)9∶1
(4)3NaHCO3+C6H8O7===C6H5O7Na3+3H2O+3CO2↑
14.(1)<
(2)加入适量的硝酸钾(或恒温蒸发一部分水)
(3)×100%
(4)CH4+2O2CO2+2H2O;蒸发结晶
点拨:(1)由图可知,30
℃时,NaCl的溶解度
℃时,将硝酸钾溶液的状态从A点(不饱和溶液),转变至B点(饱和溶液),可采取的措施是加入适量的硝酸钾或恒温蒸发一部分水。
(3)60
℃时,硝酸钾溶解度为110
g,向盛有120
g
KNO3固体的烧杯中加入100
g水,充分溶解后,所得溶液的溶质质量分数是×100%。
(4)CH4完全燃烧生成二氧化碳和水,化学方程式为CH4+2O2CO2+2H2O,“煮盐”得到食盐,此方法与实验基本操作蒸发结晶相似。
15.(1)①C
②酸;2NaOH+CuSO4
===Na2SO4+Cu(OH)2↓
(2)①Ba(OH)2 ②产生蓝色沉淀
16.(1)5;45
(2)A
【探究】没有;称量过程中没有使用游码
(3)B、C
17.(1)能
(2)Na2CO3+2HCl===2NaCl+H2O+CO2↑
【作出猜想】Na2CO3
【进行实验】①碳酸钙 ②溶液B变成红色
③CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
【反思交流】密封
【微观探析】氢离子(或H+);氢氧根离子(或OH-)
点拨:(1)碱性溶液能使酚酞变红色,所以甲组同学向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后溶液仍为无色,此现象能证明氢氧化钠与盐酸发生了反应;
(2)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为Na2CO3+2HCl
===2NaCl+H2O+CO2↑;
【作出猜想】氢氧化钠可能部分变质,可能全部变质,全部变质生成Na2CO3;
①变质氢氧化钠中含有碳酸钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
②酚酞遇碱性溶液变红色,所以滴加酚酞溶液后的现象为溶液B变成红色,证明猜想二成立;
③氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为CuSO4+2NaOH
===Cu(OH)2↓+Na2SO4;
【反思交流】为防止变质,实验室的化学药品应密封保存;
【微观探析】图中反应前后没有发生变化的微粒是钠离子和氯离子,反应的实质是氢离子和氢氧根离子结合生成水。
18.解:设消耗氧气的质量为x。
2C3H9B3O6+9O23B2O3+9H2O+6CO2
348
288
348
g
x
=
x=288
g
氧气的体积=≈205.7
L。
答:消耗常温下205.7
L的氧气。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
