2.2 重要的酸 同步练习(含答案)
文档属性
| 名称 | 2.2 重要的酸 同步练习(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 154.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-10-04 00:00:00 | ||
图片预览



文档简介
第2节
重要的酸
易错点拨
易错点1
硫酸的化学性质
例1
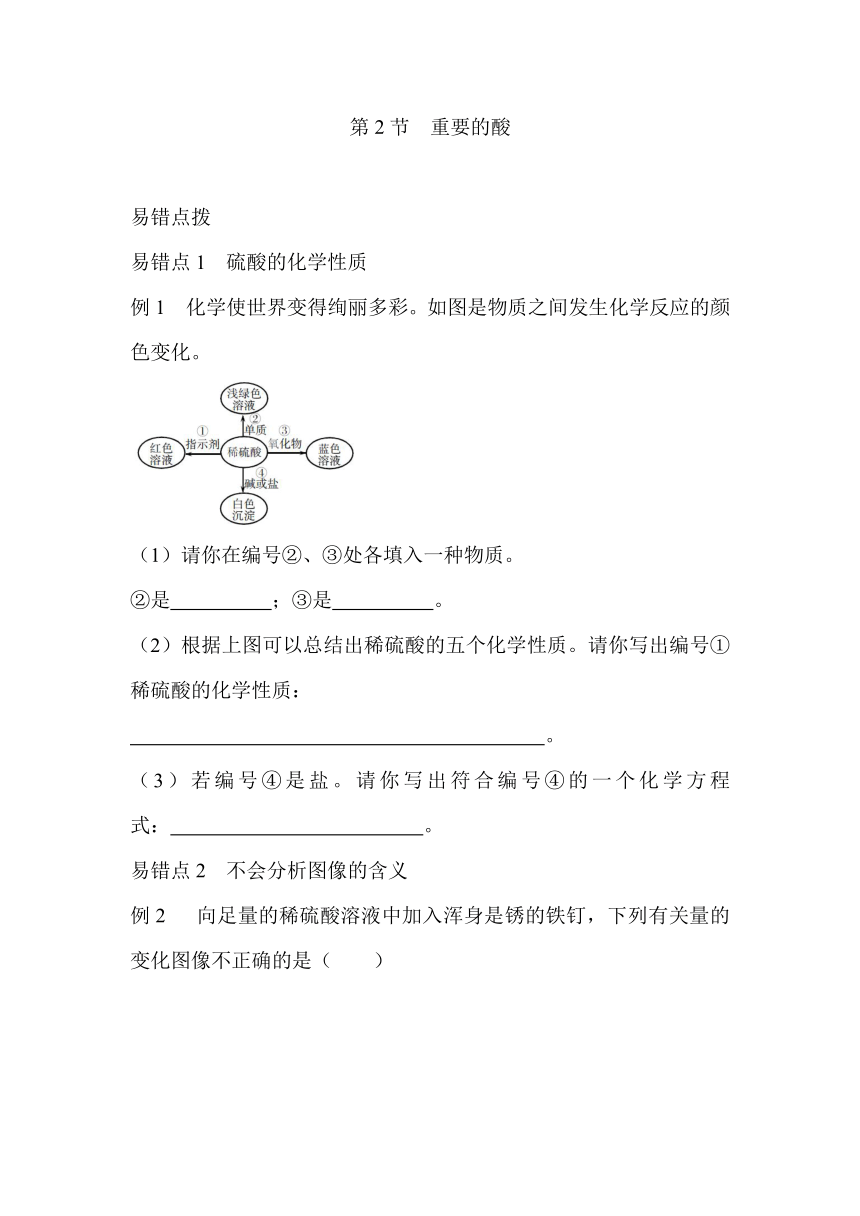
化学使世界变得绚丽多彩。如图是物质之间发生化学反应的颜色变化。
(1)请你在编号②、③处各填入一种物质。
②是
;③是
。
(2)根据上图可以总结出稀硫酸的五个化学性质。请你写出编号①稀硫酸的化学性质:
。
(3)若编号④是盐。请你写出符合编号④的一个化学方程式:
。
易错点2
不会分析图像的含义
例2
向足量的稀硫酸溶液中加入浑身是锈的铁钉,下列有关量的变化图像不正确的是(
)
综合应用
例3
李兴同学将BaCl2溶液与H2SO4溶液混合,得到一种浊液,该反应的化学方程式为
。李兴又将浊液过滤,并探究滤液的成分。
【提出猜想】
猜想1:滤液里的溶质只有HCl;
猜想2:滤液里的溶质有HCl和H2SO4;
猜想3:滤液里的溶质有HCl和
。
【设计验证实验】
操作Ⅰ:滤液验证猜想2
操作Ⅱ:滤液验证猜想3
其中操作
不能达到实验目的,应该将药品更换成
(填序号)。
A.
AgNO3溶液
B.
BaCl2溶液
C.
NaHCO3固体
D.
金属铝
巩固提升
1.
酸溶液中都含有大量H+,因此不同酸表现出一些共同性质。下列关于盐酸性质的描述中,不属于酸的共同性质的是(
)
A.
能使紫色石蕊试液变为红色
B.
能与氢氧化钠溶液反应生成水
C.
能与硝酸银溶液反应生成白色沉淀
D.
能与锌反应生成氢气
2.
(舟山中考)往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量Y随加入锌粒的质量变化的关系,则Y不可能表示(
)
A.
硫酸的质量分数
B.
生成的硫酸锌的质量
C.
溶液的pH
D.
生成氢气的质量
3.
“盐酸化性乌龟壳,一头一尾四只脚”——如图是小王归纳的稀盐酸的化学性质,X的物质类别与图中其他物质不同,则物质X是下列物质中的(
)
A.
硝酸钾
B.
氧化铜
C.
碳酸钾
D.
氢氧化钾
4.
下列各物质中加入适量的稀盐酸,不能将杂质除去的是(
)
A.
氯化钠中混有少量碳酸钠
B.
硫酸钠中混有少量碳酸钙
C.
铜粉中混有少量铁屑
D.
氯化钾中混有少量氢氧化钾
5.
回答下列与酸有关的问题。
(1)胃液中可以帮助消化的酸的化学式为
。
(2)浓硫酸敞口放置在空气中溶质的质量分数变小,是因为浓硫酸具有
。
(3)将浓盐酸敞口放置在空气中,由于溶质
,溶质的质量分数
,溶液pH会
。
6.
如图1所示是氢氧化钠溶液与盐酸反应的实验研究。
(1)未滴加盐酸时,烧杯中溶液呈
色。
(2)随着盐酸不断滴入,烧杯中溶液的pH逐渐
(填“增大”“减小”或“不变”),该反应的化学方程式是
。
(3)随着盐酸不断滴入,烧杯中溶液温度变化如坐标图2所示。某时刻测得溶液的温度是32℃,请判断b点时溶液的酸碱性并说明理由:
。
(4)当溶液的温度为38℃时,可证明溶液不含氢氧化钠的实验方法是
(填选项)。
A.品尝烧杯中溶液的味道
B.用手蘸取烧杯中溶液并体验是否有滑腻感
C.往烧杯中再滴加少量氢氧化钠溶液并观察溶液颜色
7.小明打扫卫生时发现地砖上的铁锈(主要成分为Fe2O3)用水很难清洗,决定运用所学知识解决这一难题,他进行了如下活动:
①通过测试pH,寻找除锈剂,结果如下表:
物品
食用醋
洗洁精
油污净
洁厕灵
pH
3
10
13
1
②将少量洁厕灵倒在地砖的锈斑上,进行擦拭冲洗,铁锈很快被清除;
③查阅资料得知“洁厕灵”的主要成分是一些酸和多种其他物质组成的混合物。根据上述材料,请回答:
(1)铁锈在水中的溶解性为
(填“易溶”“可溶”或“难溶”)。
(2)上述物品中,酸性最强的是
。
(3)如果洁厕灵中某酸的化学式为HR,该酸与铁锈反应的化学方程式为
。
参考答案
第2节
重要的酸
【易错点拨】例1
(1)铁(或Fe)
氧化铜(或CuO)
(2)稀硫酸可使紫色石蕊试液变红
(3)BaCl2+H2SO4BaSO4↓+2HCl(合理均可)
例2
C
【综合应用】例3
BaCl2+H2SO42HCl+BaSO4↓
BaCl2
Ⅰ
B
【巩固提升】1.
C
2.
A
3.
C
4.
B
5.
(1)HCl
(2)吸水性
(3)挥发
变小
增大
6.
(1)红
(2)减小
NaOH+HClNaCl+H2O
(3)酸性,因为溶液的温度降低,盐酸已过量
(4)C
7.
(1)难溶
(2)洁厕灵
(3)6HR+Fe2O32FeR3+3H2O
重要的酸
易错点拨
易错点1
硫酸的化学性质
例1
化学使世界变得绚丽多彩。如图是物质之间发生化学反应的颜色变化。
(1)请你在编号②、③处各填入一种物质。
②是
;③是
。
(2)根据上图可以总结出稀硫酸的五个化学性质。请你写出编号①稀硫酸的化学性质:
。
(3)若编号④是盐。请你写出符合编号④的一个化学方程式:
。
易错点2
不会分析图像的含义
例2
向足量的稀硫酸溶液中加入浑身是锈的铁钉,下列有关量的变化图像不正确的是(
)
综合应用
例3
李兴同学将BaCl2溶液与H2SO4溶液混合,得到一种浊液,该反应的化学方程式为
。李兴又将浊液过滤,并探究滤液的成分。
【提出猜想】
猜想1:滤液里的溶质只有HCl;
猜想2:滤液里的溶质有HCl和H2SO4;
猜想3:滤液里的溶质有HCl和
。
【设计验证实验】
操作Ⅰ:滤液验证猜想2
操作Ⅱ:滤液验证猜想3
其中操作
不能达到实验目的,应该将药品更换成
(填序号)。
A.
AgNO3溶液
B.
BaCl2溶液
C.
NaHCO3固体
D.
金属铝
巩固提升
1.
酸溶液中都含有大量H+,因此不同酸表现出一些共同性质。下列关于盐酸性质的描述中,不属于酸的共同性质的是(
)
A.
能使紫色石蕊试液变为红色
B.
能与氢氧化钠溶液反应生成水
C.
能与硝酸银溶液反应生成白色沉淀
D.
能与锌反应生成氢气
2.
(舟山中考)往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量Y随加入锌粒的质量变化的关系,则Y不可能表示(
)
A.
硫酸的质量分数
B.
生成的硫酸锌的质量
C.
溶液的pH
D.
生成氢气的质量
3.
“盐酸化性乌龟壳,一头一尾四只脚”——如图是小王归纳的稀盐酸的化学性质,X的物质类别与图中其他物质不同,则物质X是下列物质中的(
)
A.
硝酸钾
B.
氧化铜
C.
碳酸钾
D.
氢氧化钾
4.
下列各物质中加入适量的稀盐酸,不能将杂质除去的是(
)
A.
氯化钠中混有少量碳酸钠
B.
硫酸钠中混有少量碳酸钙
C.
铜粉中混有少量铁屑
D.
氯化钾中混有少量氢氧化钾
5.
回答下列与酸有关的问题。
(1)胃液中可以帮助消化的酸的化学式为
。
(2)浓硫酸敞口放置在空气中溶质的质量分数变小,是因为浓硫酸具有
。
(3)将浓盐酸敞口放置在空气中,由于溶质
,溶质的质量分数
,溶液pH会
。
6.
如图1所示是氢氧化钠溶液与盐酸反应的实验研究。
(1)未滴加盐酸时,烧杯中溶液呈
色。
(2)随着盐酸不断滴入,烧杯中溶液的pH逐渐
(填“增大”“减小”或“不变”),该反应的化学方程式是
。
(3)随着盐酸不断滴入,烧杯中溶液温度变化如坐标图2所示。某时刻测得溶液的温度是32℃,请判断b点时溶液的酸碱性并说明理由:
。
(4)当溶液的温度为38℃时,可证明溶液不含氢氧化钠的实验方法是
(填选项)。
A.品尝烧杯中溶液的味道
B.用手蘸取烧杯中溶液并体验是否有滑腻感
C.往烧杯中再滴加少量氢氧化钠溶液并观察溶液颜色
7.小明打扫卫生时发现地砖上的铁锈(主要成分为Fe2O3)用水很难清洗,决定运用所学知识解决这一难题,他进行了如下活动:
①通过测试pH,寻找除锈剂,结果如下表:
物品
食用醋
洗洁精
油污净
洁厕灵
pH
3
10
13
1
②将少量洁厕灵倒在地砖的锈斑上,进行擦拭冲洗,铁锈很快被清除;
③查阅资料得知“洁厕灵”的主要成分是一些酸和多种其他物质组成的混合物。根据上述材料,请回答:
(1)铁锈在水中的溶解性为
(填“易溶”“可溶”或“难溶”)。
(2)上述物品中,酸性最强的是
。
(3)如果洁厕灵中某酸的化学式为HR,该酸与铁锈反应的化学方程式为
。
参考答案
第2节
重要的酸
【易错点拨】例1
(1)铁(或Fe)
氧化铜(或CuO)
(2)稀硫酸可使紫色石蕊试液变红
(3)BaCl2+H2SO4BaSO4↓+2HCl(合理均可)
例2
C
【综合应用】例3
BaCl2+H2SO42HCl+BaSO4↓
BaCl2
Ⅰ
B
【巩固提升】1.
C
2.
A
3.
C
4.
B
5.
(1)HCl
(2)吸水性
(3)挥发
变小
增大
6.
(1)红
(2)减小
NaOH+HClNaCl+H2O
(3)酸性,因为溶液的温度降低,盐酸已过量
(4)C
7.
(1)难溶
(2)洁厕灵
(3)6HR+Fe2O32FeR3+3H2O
