2021-2022学年高一上学期化学鲁科版(2019)必修第一册1.2.2 氯气的性质和制备 课件 (39张ppt)
文档属性
| 名称 | 2021-2022学年高一上学期化学鲁科版(2019)必修第一册1.2.2 氯气的性质和制备 课件 (39张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-06 10:19:27 | ||
图片预览











文档简介
(共39张PPT)
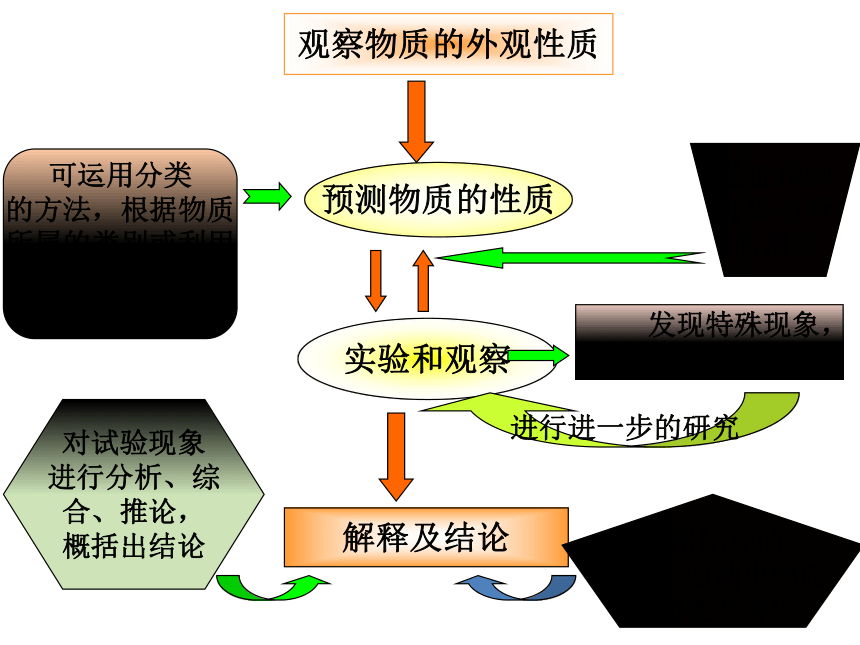
研究物质性质的基本程序
良好的方法能使我们更好的发挥天赋和才能,而拙劣的方法则可能妨碍才能的发挥。
——贝尔纳
1、能说出研究物质性质的一般程序。
2、能初步运用研究物质性质的基本方法和程序研究氯气的性质。
3、了解氯气的物理性质,掌握氯气的化学性质,了解次氯酸盐的漂白原理。
观察物质的外观性质
预测物质的性质
实验和观察
解释及结论
可运用分类
的方法,根据物质
所属的类别或利用
有关反应规律预测
物质的性质
对试验现象
进行分析、综
合、推论,
概括出结论
验证预测
并做出新
的预测
运用比较的
方法,归纳出物质
的通性及特性
发现特殊现象,
提出新问题。
进行进一步的研究
本节将带给我们许多实用的知识。
氯气泄漏事件
某高速公路一辆满载液氯的液罐车发生车祸,大量液氯外泄,据目击者描述:“一股
的气体溢出,并有刺激性气味。
事故发生后消防员不断地用水枪喷射,但因气体扩散,造成多人中毒死亡的特大事故,附近居民采取应急措施,疏散到一高坡上。
黄绿色
稀释有毒气体
消防官兵紧急排险
紧急疏散的群众
通过该氯气泄漏事故,你能总结出氯气的物理性质吗?
1.黄绿色气体。
2.有刺激性气味
3.有毒(怎么闻?)
4.能溶于水(1:2),形成氯水。
5.密度大于空气。
6.易液化得到液氯。
一、氯气的物理性质
氯气
液氯
固态氯
-101℃
-34.6℃
不能用排水法收集氯气
但能用排饱和食盐水法
能用向上排空气法收集氯气
如何收集Cl2
思考与交流
有人用软管将氯气导入鼠洞来杀灭老鼠,效果很好,这样做,利用氯气的什么性质?
毒性和密度大于空气
二、预测氯气的化学性质
1、Cl2与O2、
H2氢气都是非金属单质,应该
具有某些类似性质。
与Na、Fe、Cu等
金属单质反应。
与H2、S、P等
非金属单质反应。
与酸、盐等反应。
但从原子结构看,氯元
素与氧元素更相似,它
们的原子的最外层电子
数都比较多,容易得到
电子成为8电子的稳定结
构,所以都是较活泼的
非金属元素。氧气与氯
气都是活泼的非金属单质
预测
Cl2
Na
Cu
Fe
现象:
反应方程式:
现象:
反应方程式:
现象:
反应方程式:
燃烧、黄色火焰、白烟
燃烧、棕黄色的烟
燃烧、红棕色的烟
1、与金属单质反应
三、化学性质
点燃
2Fe+3Cl2
2FeCl3
点燃
Cu+Cl2
CuCl2
2Na+C12
2NaC1
点燃
Cl2与绝大多数金属能反应(除极少数不活泼金属),且与变价金属(如Fe、
Cu)反应生成最高价化合物.
2、氯气与某些非金属的反应
点燃
H2+Cl2
2HCl
a、纯净的氢气在氯气中的燃烧
光照
H2+Cl2
2HCl
氢气和氯气混合气体光照时发生爆炸
生成刺激性气体,溶于水得盐酸
(利用该反应工业制盐酸)
实验现象:
产生苍白色火焰,
瓶口有白雾产生,
安静的燃烧,
爆炸,瓶口有白雾
(解释?)
思考:1、烟和雾有什么区别
烟:是固体小颗粒形成的;
雾:是小液滴形成的
。
思考:
2、初中课本对燃烧的定义:
可燃物与空气中的氧气发生的一种发光发热的剧烈的氧化反应。现在你认为科学吗?
燃烧不一定有氧气参加,任何发光发热的剧烈的化学反应都称为燃烧。
氯气的检验:
用湿润的淀粉碘化钾试纸检验
现象:
试纸变蓝
原理:
Cl2
+
2KI
=
I2
+
2KCl,淀粉遇I2变蓝
Cl2与O2的性质相似,但氧气不易溶于水,而氯气能溶于水。
思考
那么,氯气溶于水的过程只是一个纯物理过程吗?能否设计实验证明?
思考与假设
思考一、如果氯气溶于水仅仅是纯物理过程,则氯水成分是什么
思考二、氯水的颜色:黄绿色——说明氯水中含有什么分子?能否由此说明氯气与水没反应
思考三、若Cl2与H2O发生了反应,可能会生成什么?
如何设计实验检验?
Cl2、H2O
说明含有Cl2分子。
不能,因为也许氯气只是没反应完全。
可能是:Cl2、H2O、HCl(Cl-
、
H+)
实验探究
装置设计:
干燥氯气
干燥红纸片
湿润红纸片
NaOH溶液
不褪色
褪色
吸收余氯
实验探究
氯气能否与水反应探究
气体(H2)
现象
结论
有H+
镁粉
氯水
探究一:氯水与镁粉反应
氯气能否与水反应
实验探究
探究二:氯水与硝酸银(酸化)溶液反应
氯水
HNO3酸化的AgNO3溶液
白色沉淀
现象
结论
有Cl-
实验探究
氯气能否与水反应探究
探究四:氯水与紫色纸条反应
纸条先变红后褪色
现象
结论
氯水中有漂白性物质
紫色纸条
氯水
实验探究
氯气能否与水反应探究
现在,能否写出氯气与水反应的化学方程式?
依据:质量守恒定律
HCl
Cl2
+
H2O
+
HClO
实验探究
实验结论:
1、氯气不仅能溶于水,还能与水发生化学反应,
生成HCl和HClO,反应的化学方程式为:
2、干燥的Cl2不具有漂白性,湿润的Cl2有漂白性。
3、HClO具有漂白性。
原因:它遇到有色物质时,能破坏其中的有机色质,
使有色物质褪色。
补充:HClO不稳定,见光分解:2HClO
=
HCl
+O2
↑
Cl2+H2O
HCl+HClO
新制氯水中含有的微粒:
久置氯水中含有微粒:
三分子:Cl2
、
H2O
、
HClO
四离子:H+
、Cl
―
、
ClO
―
、
OH
―(极少量)
H2O、Cl
―
、
H+
、
OH
―
(极少量)
实际变为盐酸,溶液酸性
.
光
2HClO
2
HCl+O2
增强
总结:
思考:氯水长期放置最终变成什么?
Cl2+H2O
HCl+HClO
【总结】新制氯水与久置氯水的性质区别
新制
久置
成分
性质
分子:
离子:
Cl2、HClO、H2O
H+,Cl-,ClO-
,OH-
分子:H2O
离子:H+,Cl-
有酸性,强氧化性,能漂白,消毒,光照时HClO分解
只有酸性
结论:氯水久置会发生变质,只能现配现用。
氯水保存:棕色瓶中,阴凉、避光处保存。
氯水与液氯的区别
液
氯
氯
水
所含微粒
物质类别
化学性质
Cl2分子
H2O、Cl2、HClO、
H
+、
ClO
-
、
Cl-
、
OH-
纯净物
混合物
具有氯气的化学性质
具有所含微粒的性质
氯气能与碱反应吗?
Cl2
+
H2O
=
HCl
+
HClO
分步进行:
HCl
+
NaOH
=
NaCl
+
H2O
HClO+
NaOH
=
NaClO
+
H2O
Cl2
+
2
NaOH
=
NaCl
+
NaClO
+
H2O
次氯酸钠
总反应
Cl2与NaOH溶液
应用:①实验室常用NaOH溶液吸收多余的Cl2
,以消除污染。②制“84消毒液”
知识拓展
2Cl2+2Ca(OH)
2
=
CaCl
2
+Ca(ClO)
2+2H2O
【思考】Cl2与熟石灰反应有何应用?
漂白粉制备原理:
漂白粉漂白原理:
CO2+Ca(ClO)
2+
H2O
=
CaCO
3
↓+
2HClO
漂白粉主要成分:
CaCl
2
+Ca(ClO)
2
漂白粉有效成分:
Ca(ClO)
2
漂白粉保存方法:
漂白粉露置在空气中失效原理:
CO2+Ca(ClO)
2+
H2O
=
CaCO
3
+
2HClO
【思考】漂白粉能否长期露置在空气中?
密封保存(隔绝H2O和CO2
)
漂白粉长期露置在空气中最终会变为:
CaCO
3
Cl2
颜色
气味
溶解性
毒性
状态
物理性质
化学性质
(1)与铁反应
.
与铜反应
.
与钠反应
.
(2)与氢气反应
.
(3)与水反应
.
(4)与某些酸或盐溶液反应
.
小结
(5)与碱反应
.
Cl2的实验室制法
实验室如何制得纯净的氯气?
瑞典化学家舍勒
舍勒
【瑞典】
公元1742一1786
他测定过软锰矿(二氧化锰)的性质。证明软锰矿是一种强氧化剂。他用盐酸与软锰矿首次实现了下述反应:
MnO2
+
4HCl(浓)
=
MnCl2
+
Cl2
↑
+
2H2O
2、实验装置:
1、实验原理:
MnO2
+
4HCl(浓)
=
MnCl2
+
Cl2
↑
+
2H2O
发生装置
收集装置
尾气吸收装置
净化装置
NaOH溶液
干燥装置
除HCl
除水蒸气
无水CaCl2
实验室还能选用其他试剂反应制取氯气:
用高锰酸钾(氯酸钾)和浓盐酸反应:
【知识拓展】
2KMnO4
+
16HCl
=2KCl
+2MnCl2
+5Cl2
↑+
8H2O
KClO3+6HCl
=
KCl+3H2O+3Cl2
↑
1.重要的化工原料;
2.用于杀毒消菌;
3.用于漂白粉;
4.制药生产中等
氯气的用途
1、氯气有毒,曾被德国制成毒气弹用于侵略战争。当这
种毒气弹顺风爆炸时,可选用的防御办法是(
)
①人躲到低洼的地方去
②人躲到较高的地方去
③用沾有氢氧化钠溶液的软布蒙面
④用沾有肥皂水或尿液的软布蒙面
A、①④
B、②③
C、②④
D、②③④
C
2、下列关于氯水的叙述中正确的是(
)
A、新制氯水中只含有Cl2和H2O
B、新制氯水可以使紫色石蕊试液先变红后退色
C、光照氯水有气泡冒出,该气体是氯气
D、氯水放置数天后,溶液的酸性减弱
B
3、下列关于氯气和含氯化合物的叙述不正确的是(
)
A、干燥的氯气和新制氯水都能使鲜艳的红花退色
B、用排水法可以收集到纯净的氯气
C、氯气和氯化氢通入硝酸银溶液中均能生成白色沉淀
D、氯气能用于杀菌、消毒和漂白
B
4、下列氯化物中,既能由金属和氯气直接化合生成,
又能由金属和盐酸反应制得的是(
)
A、CuCl2
B、FeCl2
C、FeCl3
D、AlCl3
5、下列物质中既含氯气分子,又含氯离子的是(
)
A、氯化钠溶液
B、新制氯水
C、
漂白粉
D、液氯
D
B
6、如图:A处通入氯气,C中是干燥的红色布条。
关闭
B阀时,C处红布条无变化;打开B阀时,C处红布条褪色。
下述不正确的是(
)
A.D中可能是浓硫酸
B.通入的氯气含有水蒸气
C.D中可以是NaOH溶液
D.D中可以是饱和食盐水
A
D
Cl2被D吸收,
或被D干燥。
研究物质性质的基本程序
良好的方法能使我们更好的发挥天赋和才能,而拙劣的方法则可能妨碍才能的发挥。
——贝尔纳
1、能说出研究物质性质的一般程序。
2、能初步运用研究物质性质的基本方法和程序研究氯气的性质。
3、了解氯气的物理性质,掌握氯气的化学性质,了解次氯酸盐的漂白原理。
观察物质的外观性质
预测物质的性质
实验和观察
解释及结论
可运用分类
的方法,根据物质
所属的类别或利用
有关反应规律预测
物质的性质
对试验现象
进行分析、综
合、推论,
概括出结论
验证预测
并做出新
的预测
运用比较的
方法,归纳出物质
的通性及特性
发现特殊现象,
提出新问题。
进行进一步的研究
本节将带给我们许多实用的知识。
氯气泄漏事件
某高速公路一辆满载液氯的液罐车发生车祸,大量液氯外泄,据目击者描述:“一股
的气体溢出,并有刺激性气味。
事故发生后消防员不断地用水枪喷射,但因气体扩散,造成多人中毒死亡的特大事故,附近居民采取应急措施,疏散到一高坡上。
黄绿色
稀释有毒气体
消防官兵紧急排险
紧急疏散的群众
通过该氯气泄漏事故,你能总结出氯气的物理性质吗?
1.黄绿色气体。
2.有刺激性气味
3.有毒(怎么闻?)
4.能溶于水(1:2),形成氯水。
5.密度大于空气。
6.易液化得到液氯。
一、氯气的物理性质
氯气
液氯
固态氯
-101℃
-34.6℃
不能用排水法收集氯气
但能用排饱和食盐水法
能用向上排空气法收集氯气
如何收集Cl2
思考与交流
有人用软管将氯气导入鼠洞来杀灭老鼠,效果很好,这样做,利用氯气的什么性质?
毒性和密度大于空气
二、预测氯气的化学性质
1、Cl2与O2、
H2氢气都是非金属单质,应该
具有某些类似性质。
与Na、Fe、Cu等
金属单质反应。
与H2、S、P等
非金属单质反应。
与酸、盐等反应。
但从原子结构看,氯元
素与氧元素更相似,它
们的原子的最外层电子
数都比较多,容易得到
电子成为8电子的稳定结
构,所以都是较活泼的
非金属元素。氧气与氯
气都是活泼的非金属单质
预测
Cl2
Na
Cu
Fe
现象:
反应方程式:
现象:
反应方程式:
现象:
反应方程式:
燃烧、黄色火焰、白烟
燃烧、棕黄色的烟
燃烧、红棕色的烟
1、与金属单质反应
三、化学性质
点燃
2Fe+3Cl2
2FeCl3
点燃
Cu+Cl2
CuCl2
2Na+C12
2NaC1
点燃
Cl2与绝大多数金属能反应(除极少数不活泼金属),且与变价金属(如Fe、
Cu)反应生成最高价化合物.
2、氯气与某些非金属的反应
点燃
H2+Cl2
2HCl
a、纯净的氢气在氯气中的燃烧
光照
H2+Cl2
2HCl
氢气和氯气混合气体光照时发生爆炸
生成刺激性气体,溶于水得盐酸
(利用该反应工业制盐酸)
实验现象:
产生苍白色火焰,
瓶口有白雾产生,
安静的燃烧,
爆炸,瓶口有白雾
(解释?)
思考:1、烟和雾有什么区别
烟:是固体小颗粒形成的;
雾:是小液滴形成的
。
思考:
2、初中课本对燃烧的定义:
可燃物与空气中的氧气发生的一种发光发热的剧烈的氧化反应。现在你认为科学吗?
燃烧不一定有氧气参加,任何发光发热的剧烈的化学反应都称为燃烧。
氯气的检验:
用湿润的淀粉碘化钾试纸检验
现象:
试纸变蓝
原理:
Cl2
+
2KI
=
I2
+
2KCl,淀粉遇I2变蓝
Cl2与O2的性质相似,但氧气不易溶于水,而氯气能溶于水。
思考
那么,氯气溶于水的过程只是一个纯物理过程吗?能否设计实验证明?
思考与假设
思考一、如果氯气溶于水仅仅是纯物理过程,则氯水成分是什么
思考二、氯水的颜色:黄绿色——说明氯水中含有什么分子?能否由此说明氯气与水没反应
思考三、若Cl2与H2O发生了反应,可能会生成什么?
如何设计实验检验?
Cl2、H2O
说明含有Cl2分子。
不能,因为也许氯气只是没反应完全。
可能是:Cl2、H2O、HCl(Cl-
、
H+)
实验探究
装置设计:
干燥氯气
干燥红纸片
湿润红纸片
NaOH溶液
不褪色
褪色
吸收余氯
实验探究
氯气能否与水反应探究
气体(H2)
现象
结论
有H+
镁粉
氯水
探究一:氯水与镁粉反应
氯气能否与水反应
实验探究
探究二:氯水与硝酸银(酸化)溶液反应
氯水
HNO3酸化的AgNO3溶液
白色沉淀
现象
结论
有Cl-
实验探究
氯气能否与水反应探究
探究四:氯水与紫色纸条反应
纸条先变红后褪色
现象
结论
氯水中有漂白性物质
紫色纸条
氯水
实验探究
氯气能否与水反应探究
现在,能否写出氯气与水反应的化学方程式?
依据:质量守恒定律
HCl
Cl2
+
H2O
+
HClO
实验探究
实验结论:
1、氯气不仅能溶于水,还能与水发生化学反应,
生成HCl和HClO,反应的化学方程式为:
2、干燥的Cl2不具有漂白性,湿润的Cl2有漂白性。
3、HClO具有漂白性。
原因:它遇到有色物质时,能破坏其中的有机色质,
使有色物质褪色。
补充:HClO不稳定,见光分解:2HClO
=
HCl
+O2
↑
Cl2+H2O
HCl+HClO
新制氯水中含有的微粒:
久置氯水中含有微粒:
三分子:Cl2
、
H2O
、
HClO
四离子:H+
、Cl
―
、
ClO
―
、
OH
―(极少量)
H2O、Cl
―
、
H+
、
OH
―
(极少量)
实际变为盐酸,溶液酸性
.
光
2HClO
2
HCl+O2
增强
总结:
思考:氯水长期放置最终变成什么?
Cl2+H2O
HCl+HClO
【总结】新制氯水与久置氯水的性质区别
新制
久置
成分
性质
分子:
离子:
Cl2、HClO、H2O
H+,Cl-,ClO-
,OH-
分子:H2O
离子:H+,Cl-
有酸性,强氧化性,能漂白,消毒,光照时HClO分解
只有酸性
结论:氯水久置会发生变质,只能现配现用。
氯水保存:棕色瓶中,阴凉、避光处保存。
氯水与液氯的区别
液
氯
氯
水
所含微粒
物质类别
化学性质
Cl2分子
H2O、Cl2、HClO、
H
+、
ClO
-
、
Cl-
、
OH-
纯净物
混合物
具有氯气的化学性质
具有所含微粒的性质
氯气能与碱反应吗?
Cl2
+
H2O
=
HCl
+
HClO
分步进行:
HCl
+
NaOH
=
NaCl
+
H2O
HClO+
NaOH
=
NaClO
+
H2O
Cl2
+
2
NaOH
=
NaCl
+
NaClO
+
H2O
次氯酸钠
总反应
Cl2与NaOH溶液
应用:①实验室常用NaOH溶液吸收多余的Cl2
,以消除污染。②制“84消毒液”
知识拓展
2Cl2+2Ca(OH)
2
=
CaCl
2
+Ca(ClO)
2+2H2O
【思考】Cl2与熟石灰反应有何应用?
漂白粉制备原理:
漂白粉漂白原理:
CO2+Ca(ClO)
2+
H2O
=
CaCO
3
↓+
2HClO
漂白粉主要成分:
CaCl
2
+Ca(ClO)
2
漂白粉有效成分:
Ca(ClO)
2
漂白粉保存方法:
漂白粉露置在空气中失效原理:
CO2+Ca(ClO)
2+
H2O
=
CaCO
3
+
2HClO
【思考】漂白粉能否长期露置在空气中?
密封保存(隔绝H2O和CO2
)
漂白粉长期露置在空气中最终会变为:
CaCO
3
Cl2
颜色
气味
溶解性
毒性
状态
物理性质
化学性质
(1)与铁反应
.
与铜反应
.
与钠反应
.
(2)与氢气反应
.
(3)与水反应
.
(4)与某些酸或盐溶液反应
.
小结
(5)与碱反应
.
Cl2的实验室制法
实验室如何制得纯净的氯气?
瑞典化学家舍勒
舍勒
【瑞典】
公元1742一1786
他测定过软锰矿(二氧化锰)的性质。证明软锰矿是一种强氧化剂。他用盐酸与软锰矿首次实现了下述反应:
MnO2
+
4HCl(浓)
=
MnCl2
+
Cl2
↑
+
2H2O
2、实验装置:
1、实验原理:
MnO2
+
4HCl(浓)
=
MnCl2
+
Cl2
↑
+
2H2O
发生装置
收集装置
尾气吸收装置
净化装置
NaOH溶液
干燥装置
除HCl
除水蒸气
无水CaCl2
实验室还能选用其他试剂反应制取氯气:
用高锰酸钾(氯酸钾)和浓盐酸反应:
【知识拓展】
2KMnO4
+
16HCl
=2KCl
+2MnCl2
+5Cl2
↑+
8H2O
KClO3+6HCl
=
KCl+3H2O+3Cl2
↑
1.重要的化工原料;
2.用于杀毒消菌;
3.用于漂白粉;
4.制药生产中等
氯气的用途
1、氯气有毒,曾被德国制成毒气弹用于侵略战争。当这
种毒气弹顺风爆炸时,可选用的防御办法是(
)
①人躲到低洼的地方去
②人躲到较高的地方去
③用沾有氢氧化钠溶液的软布蒙面
④用沾有肥皂水或尿液的软布蒙面
A、①④
B、②③
C、②④
D、②③④
C
2、下列关于氯水的叙述中正确的是(
)
A、新制氯水中只含有Cl2和H2O
B、新制氯水可以使紫色石蕊试液先变红后退色
C、光照氯水有气泡冒出,该气体是氯气
D、氯水放置数天后,溶液的酸性减弱
B
3、下列关于氯气和含氯化合物的叙述不正确的是(
)
A、干燥的氯气和新制氯水都能使鲜艳的红花退色
B、用排水法可以收集到纯净的氯气
C、氯气和氯化氢通入硝酸银溶液中均能生成白色沉淀
D、氯气能用于杀菌、消毒和漂白
B
4、下列氯化物中,既能由金属和氯气直接化合生成,
又能由金属和盐酸反应制得的是(
)
A、CuCl2
B、FeCl2
C、FeCl3
D、AlCl3
5、下列物质中既含氯气分子,又含氯离子的是(
)
A、氯化钠溶液
B、新制氯水
C、
漂白粉
D、液氯
D
B
6、如图:A处通入氯气,C中是干燥的红色布条。
关闭
B阀时,C处红布条无变化;打开B阀时,C处红布条褪色。
下述不正确的是(
)
A.D中可能是浓硫酸
B.通入的氯气含有水蒸气
C.D中可以是NaOH溶液
D.D中可以是饱和食盐水
A
D
Cl2被D吸收,
或被D干燥。
