上海市上交大附高2021-2022学年高二上学期9月摸底测试化学试题(Word版含答案)
文档属性
| 名称 | 上海市上交大附高2021-2022学年高二上学期9月摸底测试化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 680.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-08 00:00:00 | ||
图片预览



文档简介
上海交通大学附属中学2021-2022学年度第一学期
高二化学摸底测试
可能用到的相对原子质量:-1
-14
-16
-32
-56
-64
一、选择题
1.
化学与生活、环境、科技等密切相关,下列说法不正确的是(
)
A.
葡萄酒中通常添加微量起到灭菌和抗氧化的作用
B.
受热易分解,因此可用于制胃酸中和剂
C.
高压钠灯可用于道路照明
D.
二氧化硫和氮氧化物的超量排放是形成酸雨的主要原因
2.
下列过程中属于人工固氮的是(
)
A.
用氨气和二氧化碳合成尿素
B.
工业合成氨
C.
闪电时,氮气转移为一氧化氮
D.
分离液态空气制氮气
3.
常温下,能鉴别浓和稀,且与浓强氧化性有关的是(
)
A.
铝片
B.
纸
C.
铜片
D.
焦炭
4.
下列叙述正确的是(
)
A.
切开的金属钠暴露在空气中,表面会生成淡黄色的粉末
B.
钠与硫酸铜溶液反应时,有大量红色固体铜出现
C.
钠在空气中受热时,先熔化,产生黄色的火焰,生成白色粉末
D.
钠在空气中长期放置,最终主要产物为碳酸钠
5.
室温时,在由水电离出的的无色溶液中,一定能大量共存的离子组是(
)
A.
、、、
B.
、、、
C.
、、、
D.
、、、
6.
设为阿伏加德罗常数的值,下列叙述正确的是(
)
A.
密闭容器中,和充分催化反应后分子总数为
B.
溶液中,的数量为
C.
与足量反应生成和的混合物,转移的电子数为
D.
时,的溶液中,含有的数目为
7.
检验铵根离子的实验所依据的是(
)
①铵根离子水解显酸性;②与间发生反应加热后产生氨气;③能电离出和;④石蕊在碱性条件下变为蓝色
A.
②④
B.
①②③④
C.
①②③
D.
②③④
8.
铁粉投入到足量的的稀硫酸的烧杯中,时铁粉刚好全部溶解(假设反应后溶液体积不变),下列表示这个反应的速率正确的是(
)
A.
B.
C.
D.
9.
反应在一密闭容器中进行,下列条件的改变对其化学反应速率几乎无影响的是(
)
A.
保持容积不变,增加的物质的量
B.
将容器的容积缩小一半
C.
保持容积不变,充入
D.
保持压强不变,充入
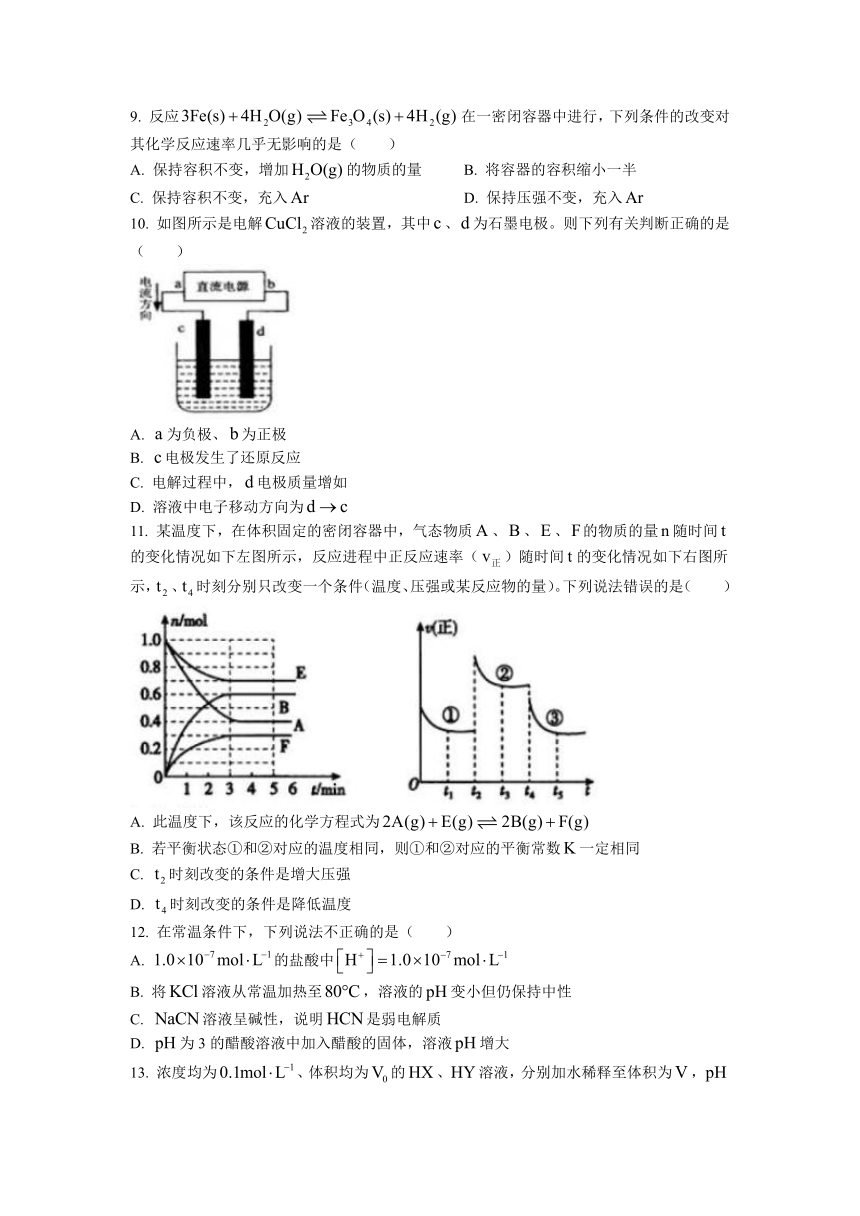
10.
如图所示是电解溶液的装置,其中、为石墨电极。则下列有关判断正确的是(
)
A.
为负极、为正极
B.
电极发生了还原反应
C.
电解过程中,电极质量增如
D.
溶液中电子移动方向为
11.
某温度下,在体积固定的密闭容器中,气态物质、、、的物质的量随时间的变化情况如下左图所示,反应进程中正反应速率()随时间的变化情况如下右图所示,、时刻分别只改变一个条件(温度、压强或某反应物的量)。下列说法错误的是(
)
A.
此温度下,该反应的化学方程式为
B.
若平衡状态①和②对应的温度相同,则①和②对应的平衡常数一定相同
C.
时刻改变的条件是增大压强
D.
时刻改变的条件是降低温度
12.
在常温条件下,下列说法不正确的是(
)
A.
的盐酸中
B.
将溶液从常温加热至,溶液的变小但仍保持中性
C.
溶液呈碱性,说明是弱电解质
D.
为3的醋酸溶液中加入醋酸的固体,溶液增大
13.
浓度均为、体积均为的、溶液,分别加水稀释至体积为,随的变化关系如图所示。下列叙述正确的是(
)
A.
比易电离
B.
常温下,由水电离出的:
C.
相同温度下,电离常数:
D.
未稀释时两溶液的导电能力相同
14.
下列离子方程式书写正确的是(
)
A.
钠与水反应:
B.
硫化氢气体通入氯水中:
C.
硫酸和氢氧化钡溶液混合:
D.
铁与稀硫酸反应:
15.
下列工业生产所采取的措施和其对应目的不一致的是(
)
A.
合成氨工业采用高压条件,目的是加大反应速率并促进平衡向合成氨的方向移动
B.
接触法制硫酸中,使用热交换器的目的是充分利用能源
C.
氧化为时需使用催化剂,这样是为了提高的转化率
D.
用氨水吸收硫酸的尾气,目的是保护环境且能够得到化肥
16.
下列事实不能用勒夏特列原理解释的是(
)
A.
配制氯化铁溶液时,一般将氯化铁固体加入盐酸中,然后加水稀释
B.
平衡体系,加压时颜色变深
C.
温度升高,纯水的减小
D.
打开汽水瓶盖,即有大量气泡逸出
17.
已知,某无色溶液中可能含有、、、,向该溶液中加入少量溴水,溶液仍呈无色,则下列判断正确的是(
)
A.
可能含有
B.
肯定不含
C.
可能含有
D.
可能含有
18.
下列溶液中,操作和现象对应正确的是(
)
选项
溶液
操作
现象
A
滴有酚酞的明矾溶液
加热
颜色变深
B
滴有酚酞的氨水
加入少量固体
颜色变浅
C
滴有酚酞的溶液
加入少量的固体
颜色变浅
D
氯化铁溶液
加热
颜色变浅
19.
常温下,下列溶液中的微粒浓度关系正确的是(
)
A.
新制氯水中加入适量固体:
B.
的溶液:
C.
的氨水与的盐酸等体积混合:
D.
溶液与溶液等体积混合:
20.
将完全溶于适量浓硝酸中,收集到氮的氧化物(含、、)的混合物,这些气体恰好能被溶液完全吸收,生成含和的盐溶液,其中的物质的量是(
)
A.
B.
C.
D.
二、综合分析题
(一)下图图1为氮元素及其化合物的转化关系,图2为实验室制取某气体的装置。
完成下列填空:
21.
图1中的化学式为__________。从化合价上看,具有___________(填“氧化”或“还原”)性。
22.
实验室常用图2中的发生装置制备氨气,该反应化学方程式为_____________________。若要收集一瓶氨气,图2虚框中的连接图应为___________(选填编号,气体均从左面导管进入)。
下列试剂不能用于干燥的是___________(选填字母)。
a.
浓硫酸
b.
碱石灰
c.
固体
d.
无水
23.
已知(磷化氢)与的分子结构相似,试写出的结构式__________。
24.
汽车排气管上装有催化转换器可减少尾气对环境的污染,汽车尾气中的有害气体和在催化下可相互反应转化为无毒无害气体排放,写出该反应的化学方程式____________________。工业尾气中氮的氧化物常采用碱液吸收法处理。与按物质的量之比被足量溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_____________________。
(二)、、等钠盐在生活、生产中都有着较广的应用。
完成下列填空:
25.
硫通常是一种淡黄色的晶体,高温下其蒸气有橙色、无色、红棕色等颜色,化学式分别为、、等,它们互为_____________________。
26.
纺织工业中常用氯气作漂白剂,可以作为漂白后布匹的“脱氧剂”,试配平该化学方程式并标出电子转移的方向和数目:
若消耗标准状况下的气体,则转移电子数目是__________。
27.
向溶液中加入少许固体,忽略溶液体积变化,溶液中的的变化是__________(选填“增大”、“减小”或“不变”)。
28.
的水溶液中存在如下等式,在横线处填上适当的微粒补充完整下列等式:
。
向溶液中滴加酚酞,溶液变为红色,若在该溶液中再滴加过量的溶液,现象为_____________________。
(三)有科研工作者研究利用废气制取,反应原理。
在的恒容密闭容器中,的起始物质的量均为,控制不同温度进行此反应。实验过程中测得的转化率如图所示。
【注】曲线表示的平衡转化率与温度的关系;
曲线表示不同温度下反应经过相同时间时的转化率。
完成下列填空:
29.
写出该反应的平衡常数表达式:__________。下列能作为判断其达到平衡状态的标志是___________(选填编号)。
①
②
③、、各自不再变化
④容器内气体密度不再变化
⑤容器内气体平均摩尔质量不再变化
30.
下列关于正反应方向反应热效应的推断合理的是__________(选填字母)。
a.
根据曲线可知为吸热反应
b.
根据曲线可知为放热反应
c.
根据曲线可知为吸热反应
d.
根据曲线可知为放热反应
31.
时,反应经过达到平衡状态,此时的转化率为,则内反应速率__________。
32.
随着温度升高,曲线向逐渐靠近,说明对于该反应,不改变其他条件的情况下,升温能够___________(选填字母)。
a.
仅加快正反应速率
b.
仅加快逆反应速率
c.
提高的分解率
d.
缩短达到平衡所需的时间
33.
尾气可用硫酸铜溶液吸收,写出反应的离子方程式____________________。
(四)某化学社团小组设计了如图所示装置,验证跟反应时需要与水接触。完成下列填空:
【装置分析】
34.
装置①中反应的离子方程式是_______________________________。
35.
装置②中的试剂是___________,装置③中的试剂是__________(均选填字母)。
a.
饱和溶液
b.
饱和溶液
c.
浓
d.
水
【进行实验】
步骤1,打开,关闭,打开分液漏斗活塞加入盐酸,将带火星的木条放在处;
步骤2:打开,关闭,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
36.
步骤1和步骤2中,处带火星的木条产生的实验现象分别是__________、__________。
37.
的电子式是_____________,与反应的化学方程式是____________________。关于该反应,下列叙述中正确的有____________(选填字母)。
A.
有离子键、共价键的断裂与生成
B.
是氧化剂,是还原剂
C.
反应物和生成物中都含离子化合物
D.
转移电子,生成气体体积为
【实验反思】
38.
有同学提出质疑:上述实验不足以证明有水存在时与发生了化学反应。其理由是______________________________。
参考答案
一、选择题
1
2
3
4
5
6
7
8
9
10
B
B
A
D
C
C
D
D
C
B
11
12
13
14
15
16
17
18
19
20
C
A
B
B
C
B
D
B
D
A
二、综合分析题
(一)21.
;氧化
22.
;②:ad
23.
24.
;
(二)25.
同素异形体
26.
;
电子转移方向和数目略;
27.
增大
28.
;产生白色沉淀,且红色褪去
(三)29.
;③⑤
30.
a
31.
0.02
33.
(四)34.
;
35.
a;
36.
步骤1中木条不复燃,步骤2
中木条复燃;
37.
;
38.
气体中有水,水也可与反应产生使木条复燃
高二化学摸底测试
可能用到的相对原子质量:-1
-14
-16
-32
-56
-64
一、选择题
1.
化学与生活、环境、科技等密切相关,下列说法不正确的是(
)
A.
葡萄酒中通常添加微量起到灭菌和抗氧化的作用
B.
受热易分解,因此可用于制胃酸中和剂
C.
高压钠灯可用于道路照明
D.
二氧化硫和氮氧化物的超量排放是形成酸雨的主要原因
2.
下列过程中属于人工固氮的是(
)
A.
用氨气和二氧化碳合成尿素
B.
工业合成氨
C.
闪电时,氮气转移为一氧化氮
D.
分离液态空气制氮气
3.
常温下,能鉴别浓和稀,且与浓强氧化性有关的是(
)
A.
铝片
B.
纸
C.
铜片
D.
焦炭
4.
下列叙述正确的是(
)
A.
切开的金属钠暴露在空气中,表面会生成淡黄色的粉末
B.
钠与硫酸铜溶液反应时,有大量红色固体铜出现
C.
钠在空气中受热时,先熔化,产生黄色的火焰,生成白色粉末
D.
钠在空气中长期放置,最终主要产物为碳酸钠
5.
室温时,在由水电离出的的无色溶液中,一定能大量共存的离子组是(
)
A.
、、、
B.
、、、
C.
、、、
D.
、、、
6.
设为阿伏加德罗常数的值,下列叙述正确的是(
)
A.
密闭容器中,和充分催化反应后分子总数为
B.
溶液中,的数量为
C.
与足量反应生成和的混合物,转移的电子数为
D.
时,的溶液中,含有的数目为
7.
检验铵根离子的实验所依据的是(
)
①铵根离子水解显酸性;②与间发生反应加热后产生氨气;③能电离出和;④石蕊在碱性条件下变为蓝色
A.
②④
B.
①②③④
C.
①②③
D.
②③④
8.
铁粉投入到足量的的稀硫酸的烧杯中,时铁粉刚好全部溶解(假设反应后溶液体积不变),下列表示这个反应的速率正确的是(
)
A.
B.
C.
D.
9.
反应在一密闭容器中进行,下列条件的改变对其化学反应速率几乎无影响的是(
)
A.
保持容积不变,增加的物质的量
B.
将容器的容积缩小一半
C.
保持容积不变,充入
D.
保持压强不变,充入
10.
如图所示是电解溶液的装置,其中、为石墨电极。则下列有关判断正确的是(
)
A.
为负极、为正极
B.
电极发生了还原反应
C.
电解过程中,电极质量增如
D.
溶液中电子移动方向为
11.
某温度下,在体积固定的密闭容器中,气态物质、、、的物质的量随时间的变化情况如下左图所示,反应进程中正反应速率()随时间的变化情况如下右图所示,、时刻分别只改变一个条件(温度、压强或某反应物的量)。下列说法错误的是(
)
A.
此温度下,该反应的化学方程式为
B.
若平衡状态①和②对应的温度相同,则①和②对应的平衡常数一定相同
C.
时刻改变的条件是增大压强
D.
时刻改变的条件是降低温度
12.
在常温条件下,下列说法不正确的是(
)
A.
的盐酸中
B.
将溶液从常温加热至,溶液的变小但仍保持中性
C.
溶液呈碱性,说明是弱电解质
D.
为3的醋酸溶液中加入醋酸的固体,溶液增大
13.
浓度均为、体积均为的、溶液,分别加水稀释至体积为,随的变化关系如图所示。下列叙述正确的是(
)
A.
比易电离
B.
常温下,由水电离出的:
C.
相同温度下,电离常数:
D.
未稀释时两溶液的导电能力相同
14.
下列离子方程式书写正确的是(
)
A.
钠与水反应:
B.
硫化氢气体通入氯水中:
C.
硫酸和氢氧化钡溶液混合:
D.
铁与稀硫酸反应:
15.
下列工业生产所采取的措施和其对应目的不一致的是(
)
A.
合成氨工业采用高压条件,目的是加大反应速率并促进平衡向合成氨的方向移动
B.
接触法制硫酸中,使用热交换器的目的是充分利用能源
C.
氧化为时需使用催化剂,这样是为了提高的转化率
D.
用氨水吸收硫酸的尾气,目的是保护环境且能够得到化肥
16.
下列事实不能用勒夏特列原理解释的是(
)
A.
配制氯化铁溶液时,一般将氯化铁固体加入盐酸中,然后加水稀释
B.
平衡体系,加压时颜色变深
C.
温度升高,纯水的减小
D.
打开汽水瓶盖,即有大量气泡逸出
17.
已知,某无色溶液中可能含有、、、,向该溶液中加入少量溴水,溶液仍呈无色,则下列判断正确的是(
)
A.
可能含有
B.
肯定不含
C.
可能含有
D.
可能含有
18.
下列溶液中,操作和现象对应正确的是(
)
选项
溶液
操作
现象
A
滴有酚酞的明矾溶液
加热
颜色变深
B
滴有酚酞的氨水
加入少量固体
颜色变浅
C
滴有酚酞的溶液
加入少量的固体
颜色变浅
D
氯化铁溶液
加热
颜色变浅
19.
常温下,下列溶液中的微粒浓度关系正确的是(
)
A.
新制氯水中加入适量固体:
B.
的溶液:
C.
的氨水与的盐酸等体积混合:
D.
溶液与溶液等体积混合:
20.
将完全溶于适量浓硝酸中,收集到氮的氧化物(含、、)的混合物,这些气体恰好能被溶液完全吸收,生成含和的盐溶液,其中的物质的量是(
)
A.
B.
C.
D.
二、综合分析题
(一)下图图1为氮元素及其化合物的转化关系,图2为实验室制取某气体的装置。
完成下列填空:
21.
图1中的化学式为__________。从化合价上看,具有___________(填“氧化”或“还原”)性。
22.
实验室常用图2中的发生装置制备氨气,该反应化学方程式为_____________________。若要收集一瓶氨气,图2虚框中的连接图应为___________(选填编号,气体均从左面导管进入)。
下列试剂不能用于干燥的是___________(选填字母)。
a.
浓硫酸
b.
碱石灰
c.
固体
d.
无水
23.
已知(磷化氢)与的分子结构相似,试写出的结构式__________。
24.
汽车排气管上装有催化转换器可减少尾气对环境的污染,汽车尾气中的有害气体和在催化下可相互反应转化为无毒无害气体排放,写出该反应的化学方程式____________________。工业尾气中氮的氧化物常采用碱液吸收法处理。与按物质的量之比被足量溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_____________________。
(二)、、等钠盐在生活、生产中都有着较广的应用。
完成下列填空:
25.
硫通常是一种淡黄色的晶体,高温下其蒸气有橙色、无色、红棕色等颜色,化学式分别为、、等,它们互为_____________________。
26.
纺织工业中常用氯气作漂白剂,可以作为漂白后布匹的“脱氧剂”,试配平该化学方程式并标出电子转移的方向和数目:
若消耗标准状况下的气体,则转移电子数目是__________。
27.
向溶液中加入少许固体,忽略溶液体积变化,溶液中的的变化是__________(选填“增大”、“减小”或“不变”)。
28.
的水溶液中存在如下等式,在横线处填上适当的微粒补充完整下列等式:
。
向溶液中滴加酚酞,溶液变为红色,若在该溶液中再滴加过量的溶液,现象为_____________________。
(三)有科研工作者研究利用废气制取,反应原理。
在的恒容密闭容器中,的起始物质的量均为,控制不同温度进行此反应。实验过程中测得的转化率如图所示。
【注】曲线表示的平衡转化率与温度的关系;
曲线表示不同温度下反应经过相同时间时的转化率。
完成下列填空:
29.
写出该反应的平衡常数表达式:__________。下列能作为判断其达到平衡状态的标志是___________(选填编号)。
①
②
③、、各自不再变化
④容器内气体密度不再变化
⑤容器内气体平均摩尔质量不再变化
30.
下列关于正反应方向反应热效应的推断合理的是__________(选填字母)。
a.
根据曲线可知为吸热反应
b.
根据曲线可知为放热反应
c.
根据曲线可知为吸热反应
d.
根据曲线可知为放热反应
31.
时,反应经过达到平衡状态,此时的转化率为,则内反应速率__________。
32.
随着温度升高,曲线向逐渐靠近,说明对于该反应,不改变其他条件的情况下,升温能够___________(选填字母)。
a.
仅加快正反应速率
b.
仅加快逆反应速率
c.
提高的分解率
d.
缩短达到平衡所需的时间
33.
尾气可用硫酸铜溶液吸收,写出反应的离子方程式____________________。
(四)某化学社团小组设计了如图所示装置,验证跟反应时需要与水接触。完成下列填空:
【装置分析】
34.
装置①中反应的离子方程式是_______________________________。
35.
装置②中的试剂是___________,装置③中的试剂是__________(均选填字母)。
a.
饱和溶液
b.
饱和溶液
c.
浓
d.
水
【进行实验】
步骤1,打开,关闭,打开分液漏斗活塞加入盐酸,将带火星的木条放在处;
步骤2:打开,关闭,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
36.
步骤1和步骤2中,处带火星的木条产生的实验现象分别是__________、__________。
37.
的电子式是_____________,与反应的化学方程式是____________________。关于该反应,下列叙述中正确的有____________(选填字母)。
A.
有离子键、共价键的断裂与生成
B.
是氧化剂,是还原剂
C.
反应物和生成物中都含离子化合物
D.
转移电子,生成气体体积为
【实验反思】
38.
有同学提出质疑:上述实验不足以证明有水存在时与发生了化学反应。其理由是______________________________。
参考答案
一、选择题
1
2
3
4
5
6
7
8
9
10
B
B
A
D
C
C
D
D
C
B
11
12
13
14
15
16
17
18
19
20
C
A
B
B
C
B
D
B
D
A
二、综合分析题
(一)21.
;氧化
22.
;②:ad
23.
24.
;
(二)25.
同素异形体
26.
;
电子转移方向和数目略;
27.
增大
28.
;产生白色沉淀,且红色褪去
(三)29.
;③⑤
30.
a
31.
0.02
33.
(四)34.
;
35.
a;
36.
步骤1中木条不复燃,步骤2
中木条复燃;
37.
;
38.
气体中有水,水也可与反应产生使木条复燃
同课章节目录
