5.1 质量守恒定律(第二课时)课件--2021-2022学年九年级化学人教版上册(22张PPT)
文档属性
| 名称 | 5.1 质量守恒定律(第二课时)课件--2021-2022学年九年级化学人教版上册(22张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1008.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-08 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
课题1
质量守恒定律
(第二课时)
化学方程式
(一)表示化学反应的方法:
1、文字表达式
2、化学方程式
用化学式来表示化学反应的式子
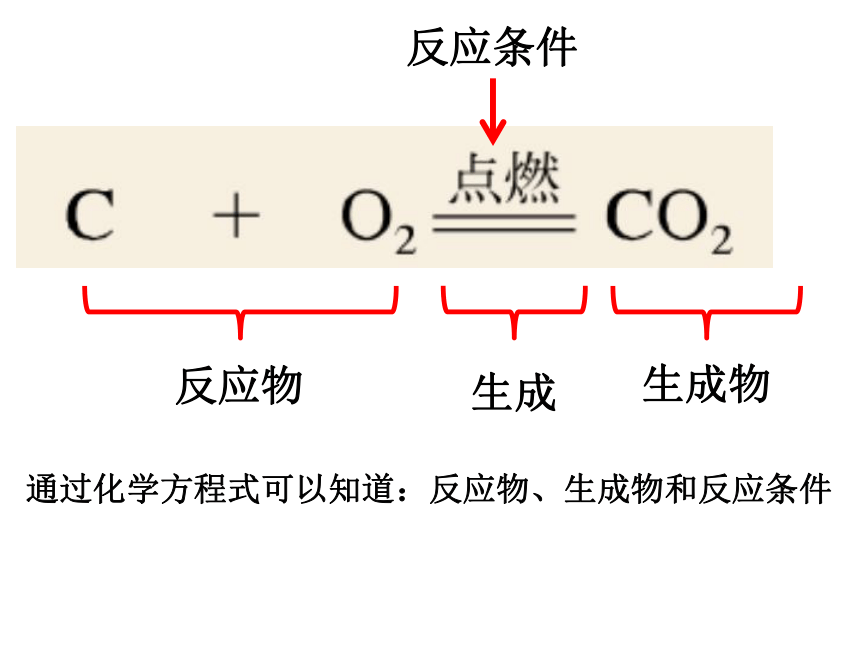
反应物
生成物
反应条件
生成
通过化学方程式可以知道:反应物、生成物和反应条件
反应物:
生成物:
反应条件:
高锰酸钾
锰酸钾、二氧化锰和氧气
加热
化学方程式除了可以获得反应物、生成物和反应条件,还能计算出两个比
通过相对分子质量(或相对原子质量)还可以表示各物质之间的质量关系,即各物质之间的质量比
12
:
32
:
44
这个比例就是说:碳与氧气在点燃的条件下反应生成二氧化碳;每12份质量的碳与32份质量的氧气完全反应,生成44份质量的二氧化碳。
(二)质量比
思考:
1、现在有24kg的碳和64kg的氧气反应,最多会生成
kg的二氧化碳
2、要生成132kg的二氧化碳,至少要
kg碳和
kg的氧气
3、现有12kg的碳和76kg的氧气反应,最多会生成
kg的二氧化碳
12
:
32
:
44
36
96
44
88
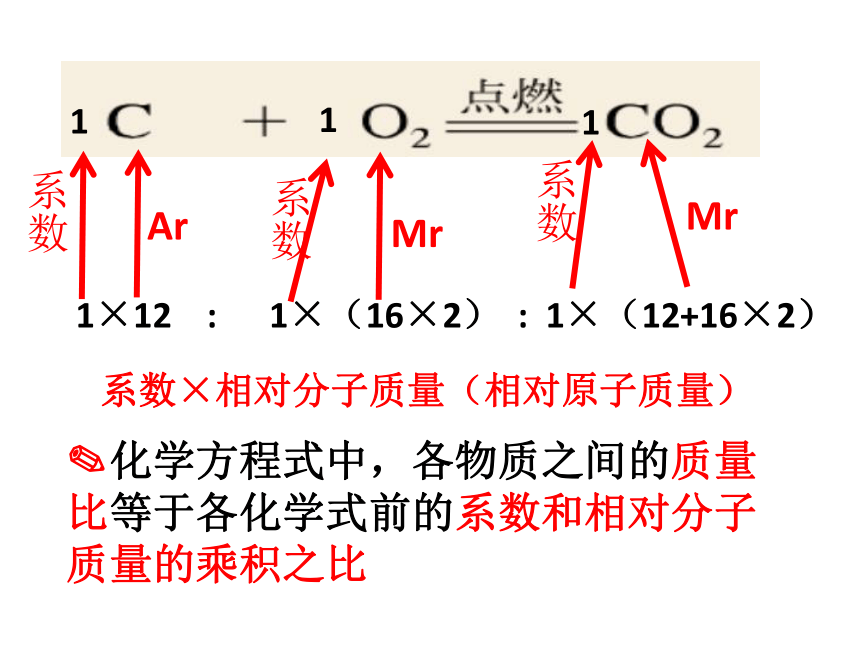
1×12
:
1×(16×2)
:
1×(12+16×2)
系数×相对分子质量(相对原子质量)
1
系数
Ar
1
系数
Mr
1
系数
Mr
化学方程式中,各物质之间的质量比等于各化学式前的系数和相对分子质量的乘积之比
2H2O2
2H2O
+
O2↑
MnO2
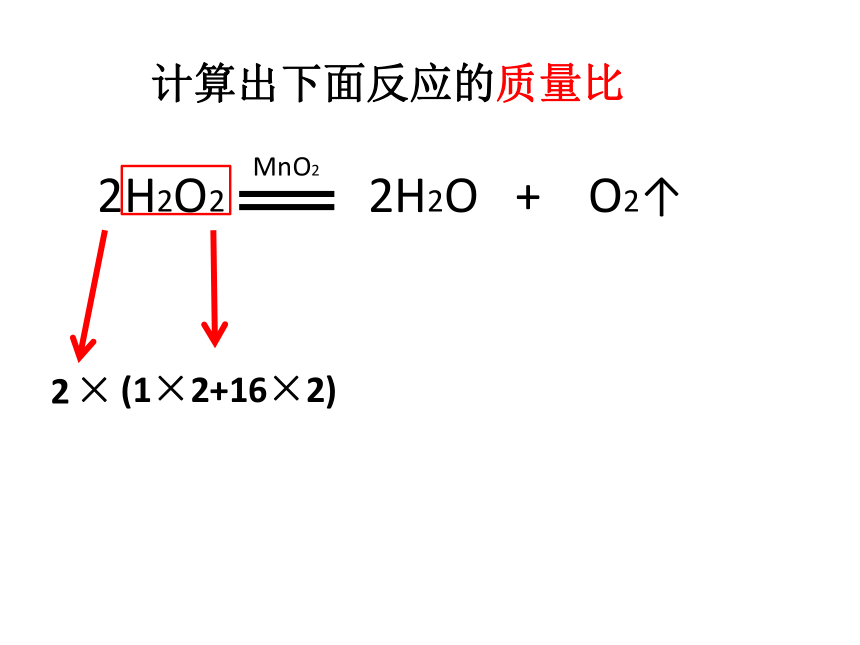
计算出下面反应的质量比
2
(1×2+16×2)
×
2H2O2
2H2O
+
O2↑
MnO2
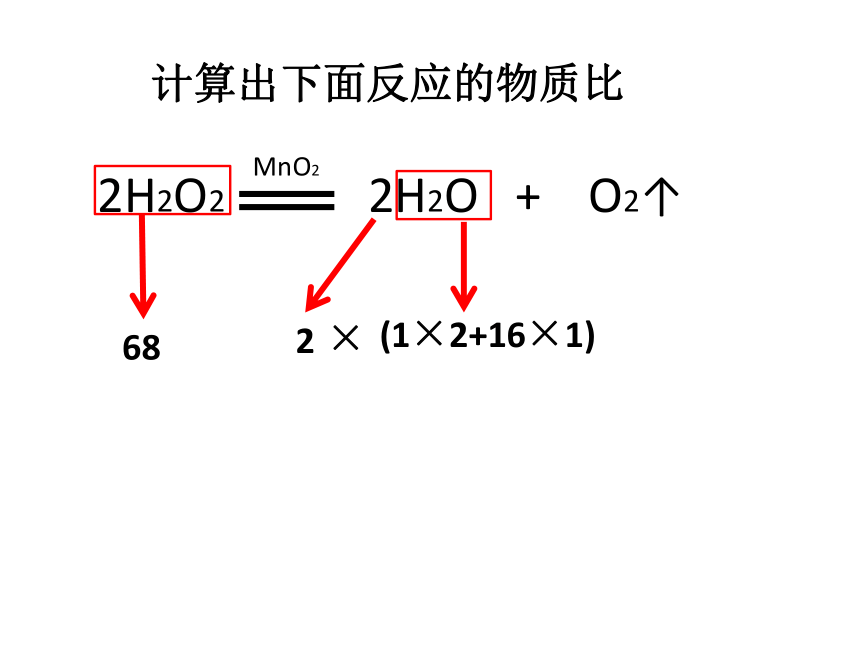
计算出下面反应的物质比
68
2
(1×2+16×1)
×
2H2O2
2H2O
+
O2
↑
MnO2
计算出下面反应的物质比
68
36
1
1
(16×2)
×
2H2O2
2H2O
+
O2
↑
MnO2
计算出下面反应的物质比
68
36
32
:
:
过氧化氢在二氧化锰的催化作用下,生成水和氧气;每______份质量的过氧化氢完全反应,生成_____份质量的水和_____份质量的氧气。
68
36
32
算一算
要生成64g的氧气,至少需要过氧化氢多少克?
解:设过氧化氢的质量为
m
反应中氧气和过氧化氢的质量比为
32
:
68
所以,64g
:m
=
32
:
68
所以,m
=
136g
答:要生成64g的氧气,至少需要过氧化氢136g。
化学方程式还能表示出反应中的反应物、生成物各种粒子的相对数量关系,即各物质间的粒子比
1
:
1
:
1
1
:1
:1是表示在这个反应中,每1个碳原子和1个氧分子反应生成1个二氧化碳分子
(三)粒子比
1
:
1
:
1
1
系数
1
系数
1
系数
化学方程式中,各物质之间的粒子比等于各化学式前的系数之比
2KClO3
2KCl
+
3O2
↑
△
MnO2
现要生成600个氧分子,那需要
个氯酸钾分子,同时会生成
个
氯化钾分子
400
400
2
:
2
:
3
在这个反应中,每______________反应生成_____________和_____________。
2个氯酸钾分子
2个氯化钾分子
3个氧分子
4P
+
5O2
2P2O5
点燃
2H2O
O2↑+
2H2↑
通电
计算下列化学方程式中各物质的粒子比和质量比
4
:
5
:
2
2
:
1
:
2
4P
+
5O2
2P2O5
点燃
(4×31)
(5×32)
(2×142)
:
:
(2×18)
(1×32)
(2×2)
:
:
2H2O
O2↑+
2H2↑
通电
1、化学方程式中“
”的意义包括(
)
①反应物、生成物的元素种类相同
②反应物、生成物的质量总和相等
③反应物、生成物的原子种类相同
④反应物、生成物的原子数目相等
⑤反应物、生成物的体积相等
⑥反应物、生成物的分子数目相同
⑦“生成”的意思
A.①③⑤⑦
B.②④⑥⑦
C.①②③④⑦
D.②⑦
C
2.红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的关系的图像正确的是(
)
A
B
C
D
时间
元素种类
时间
原子数目
时间
物质的总质量
时间
原子种类
D
3.将25g氯酸钾和6g二氧化锰的混合物加热一段时间后,
得到残余固体的质量为22
g,则产生氧气____g。
4.煤的汽化是提高煤的利用率、减少环境污染的有效措
施之一。煤的汽化过程中发生了化学反应C+H2O====CO+X。
请你写出X的化学式
。
9
H2
5、在一个密闭容器内有四种物质,在一定条件下完全反应后,测得反应前后各物质的质量如下表,下列推理正确的是
A.反应后生成15gZ
B.反应后Q的质量为9g
C.该反应是化合反应
D.该反应是分解反应
物质
X
Y
Z
Q
反应前质量/g
4
10
1
21
反应后质量/g
0
12
15
待测
①反应前后总质量相等;
②反应后质量增加为生成物,质量减少为反应物,质量不变为催化剂或不参与反应。
物质
X
Y
Z
Q
反应前质量/g
4
10
1
21
反应后质量/g
0
12
15
待测
4+10+1+21
=
0+12+15+待测
=9
反应后质量减少的为反应物,质量增加的为生成物
X
+
Q
→
Y
+
Z
A.反应后生成15gZ
B.反应后Q的质量为9g
C.该反应是化合反应
D.该反应是分解反应
课题1
质量守恒定律
(第二课时)
化学方程式
(一)表示化学反应的方法:
1、文字表达式
2、化学方程式
用化学式来表示化学反应的式子
反应物
生成物
反应条件
生成
通过化学方程式可以知道:反应物、生成物和反应条件
反应物:
生成物:
反应条件:
高锰酸钾
锰酸钾、二氧化锰和氧气
加热
化学方程式除了可以获得反应物、生成物和反应条件,还能计算出两个比
通过相对分子质量(或相对原子质量)还可以表示各物质之间的质量关系,即各物质之间的质量比
12
:
32
:
44
这个比例就是说:碳与氧气在点燃的条件下反应生成二氧化碳;每12份质量的碳与32份质量的氧气完全反应,生成44份质量的二氧化碳。
(二)质量比
思考:
1、现在有24kg的碳和64kg的氧气反应,最多会生成
kg的二氧化碳
2、要生成132kg的二氧化碳,至少要
kg碳和
kg的氧气
3、现有12kg的碳和76kg的氧气反应,最多会生成
kg的二氧化碳
12
:
32
:
44
36
96
44
88
1×12
:
1×(16×2)
:
1×(12+16×2)
系数×相对分子质量(相对原子质量)
1
系数
Ar
1
系数
Mr
1
系数
Mr
化学方程式中,各物质之间的质量比等于各化学式前的系数和相对分子质量的乘积之比
2H2O2
2H2O
+
O2↑
MnO2
计算出下面反应的质量比
2
(1×2+16×2)
×
2H2O2
2H2O
+
O2↑
MnO2
计算出下面反应的物质比
68
2
(1×2+16×1)
×
2H2O2
2H2O
+
O2
↑
MnO2
计算出下面反应的物质比
68
36
1
1
(16×2)
×
2H2O2
2H2O
+
O2
↑
MnO2
计算出下面反应的物质比
68
36
32
:
:
过氧化氢在二氧化锰的催化作用下,生成水和氧气;每______份质量的过氧化氢完全反应,生成_____份质量的水和_____份质量的氧气。
68
36
32
算一算
要生成64g的氧气,至少需要过氧化氢多少克?
解:设过氧化氢的质量为
m
反应中氧气和过氧化氢的质量比为
32
:
68
所以,64g
:m
=
32
:
68
所以,m
=
136g
答:要生成64g的氧气,至少需要过氧化氢136g。
化学方程式还能表示出反应中的反应物、生成物各种粒子的相对数量关系,即各物质间的粒子比
1
:
1
:
1
1
:1
:1是表示在这个反应中,每1个碳原子和1个氧分子反应生成1个二氧化碳分子
(三)粒子比
1
:
1
:
1
1
系数
1
系数
1
系数
化学方程式中,各物质之间的粒子比等于各化学式前的系数之比
2KClO3
2KCl
+
3O2
↑
△
MnO2
现要生成600个氧分子,那需要
个氯酸钾分子,同时会生成
个
氯化钾分子
400
400
2
:
2
:
3
在这个反应中,每______________反应生成_____________和_____________。
2个氯酸钾分子
2个氯化钾分子
3个氧分子
4P
+
5O2
2P2O5
点燃
2H2O
O2↑+
2H2↑
通电
计算下列化学方程式中各物质的粒子比和质量比
4
:
5
:
2
2
:
1
:
2
4P
+
5O2
2P2O5
点燃
(4×31)
(5×32)
(2×142)
:
:
(2×18)
(1×32)
(2×2)
:
:
2H2O
O2↑+
2H2↑
通电
1、化学方程式中“
”的意义包括(
)
①反应物、生成物的元素种类相同
②反应物、生成物的质量总和相等
③反应物、生成物的原子种类相同
④反应物、生成物的原子数目相等
⑤反应物、生成物的体积相等
⑥反应物、生成物的分子数目相同
⑦“生成”的意思
A.①③⑤⑦
B.②④⑥⑦
C.①②③④⑦
D.②⑦
C
2.红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的关系的图像正确的是(
)
A
B
C
D
时间
元素种类
时间
原子数目
时间
物质的总质量
时间
原子种类
D
3.将25g氯酸钾和6g二氧化锰的混合物加热一段时间后,
得到残余固体的质量为22
g,则产生氧气____g。
4.煤的汽化是提高煤的利用率、减少环境污染的有效措
施之一。煤的汽化过程中发生了化学反应C+H2O====CO+X。
请你写出X的化学式
。
9
H2
5、在一个密闭容器内有四种物质,在一定条件下完全反应后,测得反应前后各物质的质量如下表,下列推理正确的是
A.反应后生成15gZ
B.反应后Q的质量为9g
C.该反应是化合反应
D.该反应是分解反应
物质
X
Y
Z
Q
反应前质量/g
4
10
1
21
反应后质量/g
0
12
15
待测
①反应前后总质量相等;
②反应后质量增加为生成物,质量减少为反应物,质量不变为催化剂或不参与反应。
物质
X
Y
Z
Q
反应前质量/g
4
10
1
21
反应后质量/g
0
12
15
待测
4+10+1+21
=
0+12+15+待测
=9
反应后质量减少的为反应物,质量增加的为生成物
X
+
Q
→
Y
+
Z
A.反应后生成15gZ
B.反应后Q的质量为9g
C.该反应是化合反应
D.该反应是分解反应
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
