2021-2022学年高二化学鲁科版(2019)选择性必修3第二章《官能团与有机化学反应 烃的衍生物》测试题(含答案)
文档属性
| 名称 | 2021-2022学年高二化学鲁科版(2019)选择性必修3第二章《官能团与有机化学反应 烃的衍生物》测试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 423.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-11 00:00:00 | ||
图片预览




文档简介
第二章《官能团与有机化学反应 烃的衍生物》测试题
一、单选题(共15题)
1.我们的生活和科技领域很多与化学密切相关。下列说法正确的是
A.煤的液化、气化主要是为了减少的排放
B.北斗三号全球卫星导航系统正式开通,其导航芯片的主要成分是二氧化硅
C.缺铁性贫血患者服用补铁剂时,与维生素同时服用效果更好
D.新冠病毒可用酒精或双氧水消毒,其消毒原理相同
2.化学反应经常伴随着颜色变化,下列有关反应显示的颜色正确的有
①蛋白质遇浓硝酸一黄色; ②淀粉溶液遇单质碘一蓝色;
③溴化银见光分解一银白色; ④热的氧化铜遇乙醇一绿色;
⑤新制氯水久置后一无色; ⑥苯酚在空气中氧化一粉红色。
A.2个 B.3个 C.4个 D.5个
3.下列说法不正确的是
A.糯米中的1mol淀粉能完全水解生成2mol葡萄糖
B.葡萄糖能发生银镜反应,说明其含有醛基,具有还原性
C.环式核糖与碱基、磷酸基团共同组成核糖核苷酸
D.蛋白质是含肽键的生物大分子
4.随着科学的发展,学科间的交叉和综合越来越多,学科之间的界限越来越不明显。下列研究或变化不属于化学研究范畴的是
A.MERS病毒疫苗的研制 B.近期出现雾霾的原因探究
C.朝鲜的原子弹爆炸实验 D.济南钢铁集团冶炼特种钢
5.可用于鉴别乙醇、乙醛、乙酸三种无色液体的一种试剂是
A.水 B.新制Cu(OH)2悬浊液
C.NaOH溶液 D.酚酞溶液
6.下列说法不正确的是
A.用稀盐酸清洗铜器表面
B.明矾可以对自来水消毒杀菌
C.KMnO4具有氧化性,其稀溶液可用于消毒
D.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
7.对以下古诗文中的现象,分析正确的是
A.“以硫黄、雄黄合硝石并蜜烧之,焰起烧手、面及屋舍”,指的是黑火药爆炸,其主要反应的方程式为:S+2KNO3+3C=K2S+N2↑+3CO2↑
B.“司南之杓(勺),投之于地,其杓指南”,司南中“杓”的主要成分为Fe2O3
C.“试玉要烧三日满,辨才须待七年期”,此文中“玉”的主要成分为硅酸盐,该诗句表明玉的硬度很大
D.“自古书契多编以竹简,其用缣帛者(丝织品)谓之为纸”,文中“纸”的主要成分是纤维素
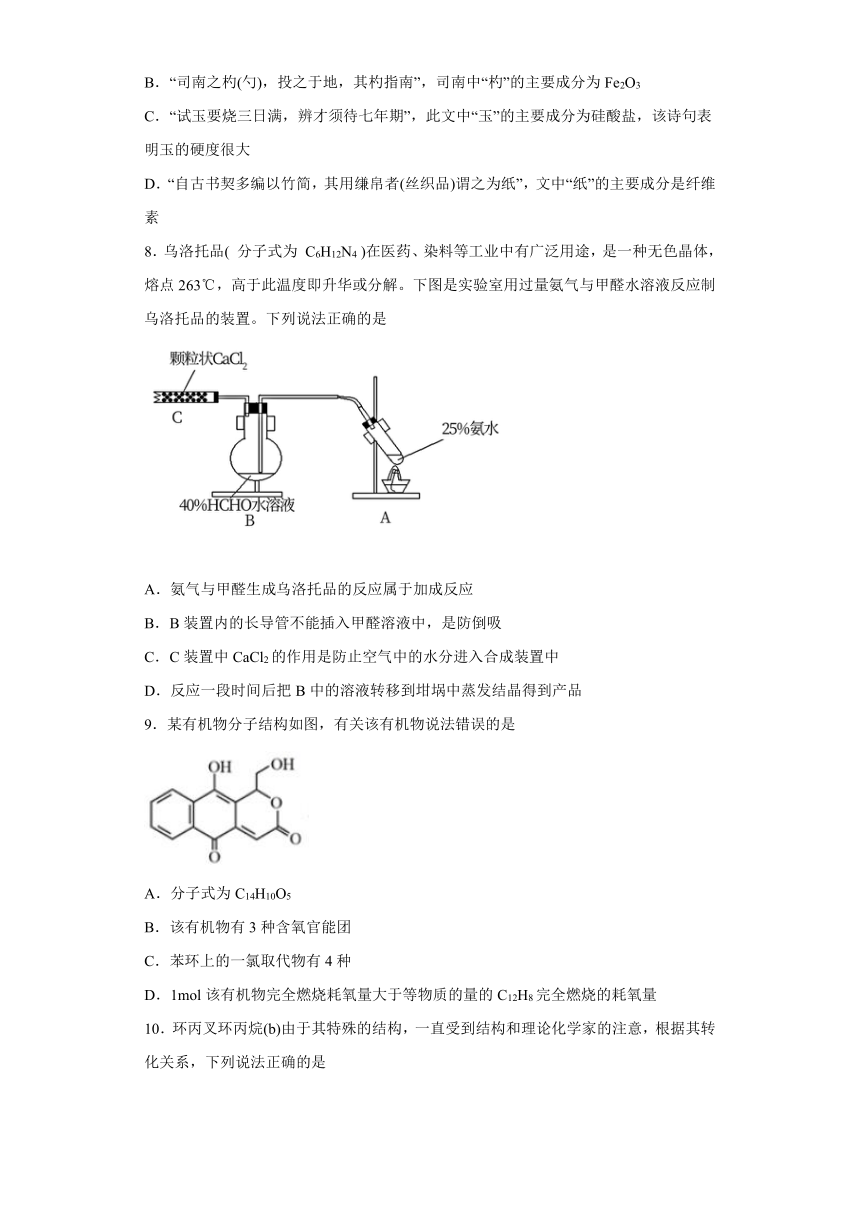
8.乌洛托品( 分子式为 C6H12N4 )在医药、染料等工业中有广泛用途,是一种无色晶体,熔点263℃,高于此温度即升华或分解。下图是实验室用过量氨气与甲醛水溶液反应制乌洛托品的装置。下列说法正确的是
A.氨气与甲醛生成乌洛托品的反应属于加成反应
B.B装置内的长导管不能插入甲醛溶液中,是防倒吸
C.C装置中CaCl2的作用是防止空气中的水分进入合成装置中
D.反应一段时间后把B中的溶液转移到坩埚中蒸发结晶得到产品
9.某有机物分子结构如图,有关该有机物说法错误的是
A.分子式为C14H10O5
B.该有机物有3种含氧官能团
C.苯环上的一氯取代物有4种
D.1mol该有机物完全燃烧耗氧量大于等物质的量的C12H8完全燃烧的耗氧量
10.环丙叉环丙烷(b)由于其特殊的结构,一直受到结构和理论化学家的注意,根据其转化关系,下列说法正确的是
A.b的所有原子都在一个平面内
B.m的同分异构体中属于芳香族化合物的共有5种
C.p在氢氧化钠的乙醇溶液中加热生成烯烃
D.反应①是加成反应,反应②是消去反应
11.下列有关实验装置及用途叙述完全正确的是
A.a装置检验消去反应的产物丙烯 B.b装置检验酸性:盐酸>碳酸>硅酸
C.c装置用于实验室制取并收集乙烯 D.d装置用于实验室制硝基苯
12.下列说法不正确的是
A.固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,难溶于有机溶剂
B.盐析作用析出的蛋白质仍具有原来的活性,因此盐析可用于分离、提纯蛋白质
C.葵花籽油不能使酸性高锰酸钾溶液紫色褪去
D.石油减压分馏可得到重柴油、润滑油、石蜡等馏分,未被汽化的剩余物质是沥青
13.用括号中的试剂除去各组中的杂质,不正确的是
A.苯中的甲苯(溴水) B.乙醇中的水(新制CaO)
C.乙醛中的乙酸(NaOH) D.苯中的苯酚(NaOH)
14.足量的金属钠分别与甲醇、乙二醇、丙三醇反应,放出等体积的氢气,消耗这三种醇的物质的量之比是
A.6:3:2 B.2:3:6 C.3:2:1 D.1:2:3
15.下列实验能达到目的的是
A.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中含有乙烯
B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡
C.淀粉溶液和稀H2SO4混合加热,加入新制的Cu(OH)2悬浊液加热至沸腾,检验淀粉水解产物有还原性
D.利用图示装置并根据有关实验现象能推知酸性: CH3COOH> H2CO3>C6H5OH
二、填空题(共8题)
16.在① ② ③ ④ ⑤ (过氧乙酸),五种有机物中:
(1)能制成防疫口罩主要材料聚丙烯无纺布的是______(写名称,下同);能发生消法反应的是______;能发生银镜反应的是______;能与溶液显紫色的是______。
(2)可以由轻质油通过______(填“分馏”或“裂解”)制得。由在一定条件下合成聚丙烯的化学方程式是______。
(3)因具有强氧化性可作消毒剂的是______(填序号)。
17.(1)乙二酸、苯甲酸、硬脂酸、石炭酸都属于羧酸类有机物_____
(2)酯的官能团是酯基_____
(3)乙酸乙酯分子中含有甲基、乙基和酯基_____
(4)用CH3CH218OH与CH3COOH发生酯化反应,生成H218O_____
(5)用碳酸钠溶液可鉴别乙醇、乙酸和乙酸乙酯____
(6)在酸性条件下,的水解产物是CH3CO18OH和C2H5OH_____
(7)羧基和酯基中的均能与H2加成____
(8)C4H8O2同分异构体的类型有羧酸、酯、羟基醛等_____
18.已知下面两个反应,其中A为氯代烃,B为烯烃(其相对分子质量为42)。
反应①:
反应②:
请回答下列问题:
(1)化合物B的分子式为_____________.
(2)假设A分子中有两种等效氢且比例为6∶1,则反应①的化学方程式为_______;
(3)写出B在有机过氧化物()中与反应的化学方程式:_____;
(4)下列有关实验室检验A中是否有氯元素的方法或试剂正确的是______(填字母)。
a.燃烧法 b.溶液
c.溶液+稀硝酸溶液 d.醇溶液溶液
19.短周期元素A、B、C、D、E ,A为原子半径最小的元素,A、D同主族,D、E同周期,C、E同主族且E的原子序数为C的原子序数的2倍,B为组成物质种类最多的元素。
(1)E离子的原子结构示意图_______。
(2)分别由A、C、D、E四种元素组成的两种盐可相互反应得到气体,写出这个反应的离子方程式_______。
(3)由A、B、C三种元素组成的物质X,式量为46,在一定条件下与C、D两种元素的单质均可反应。写出X与C单质在红热的铜丝存在时反应的化学方程式_______。
(4)A、C、D三种元素组成的化合物Y中含有的化学键为_______,B的最高价氧化物与等物质的量的Y溶液反应后,溶液显_______(“酸”“碱”或“中”)性,原因是:_______。
20.I.X由四种常见元素组成的化合物,其中一种是氢元素,其摩尔质量小于200g·mol-1。某学习小组进行了如下实验:
已知:气体A在标况下的密度为0.714g·L-1,A完全燃烧的气体产物E能使澄清石灰水变浑浊,沉淀D是混合物。
请回答:
(1)气体E的结构式_______,沉淀D是______(写化学式),X的化学式______。
(2)写出化合物X与足量盐酸反应的化学方程式________。
II.纯净的氮化镁(Mg3N2)是淡黄色固体,热稳定性较好,遇水极易发生反应。某同学初步设计了如图实验装置制备氮化镁(夹持及加热仪器没有画出)。
已知:Mg+2NH3Mg(NH2)2+H2↑。
请回答:
(1)写出A中反应的化学方程式________。
(2)下列说法不正确的是________。
A.为了得到纯净的氮化镁,实验前需要排除装置中的空气
B.装置B起到了缓冲、安全的作用
C.装置C只吸收水,避免镁和水反应产生副产物
D.将装置B、C简化成装有碱石灰的U形管,也能达到实验目的
E.实验后,取D中固体加少量水,能生成使湿润的蓝色石蕊试纸变红的气体
21.下面的实验可以帮助我们认识乙醇与氢卤酸的反应,组装如图装置。在试管I中依次加入2mL蒸馏水,4mL浓硫酸,2mL 95%的乙醇和3g溴化钠粉末,在试管II中注入蒸馏水,烧杯中注入自来水。加热试管I至微沸状态数分钟,冷却。
(1)该反应中,加入蒸馏水,浓硫酸,溴化钠固体的目的是_______。
(2)判断有溴乙烷生成的现象是_______。
(3)试管I中反应除了生成溴乙烷,还可能生成的有机物有_______(任写一种结构简式)。
(4)为检验溴乙烷与NaOH乙醇溶液发生消去反应后生成的气体中是否含乙烯,设计出实验装置图(如图)。其中洗气瓶中水的作用是_______。
22.实验室制备乙酸乙酯的实验装置如图所示,回答下列问题:
(1)该实验中混合乙醇和浓硫酸的方法是_____。
(2)该装置与教材上的相比做了一些改进,其中仪器a的名称_____,改进后的装置仍然存在一定的不足,请指出其中的一点_____。
(3)试管②中溶液呈红色的原因是_____。(用离子方程式表示)。
(4)某实验小组在分离操作中,摇晃了试管②,发现上下两层溶液均变为无色,该小组对褪色原因进行探究。
Ⅰ.经过讨论猜想褪色原因是挥发的乙酸中和碳酸钠。
编号 操作 现象
实验1 用pH计测量饱和碳酸钠溶液pH pH=12.23
实验2 分离出试管②下层液体,用pH计测定pH pH=12.21
由实验1、2得出的结论是_____。
Ⅱ.查阅资料:酚酞是一种白色晶状粉末,不溶于水,1g酚酞可溶于13mL乙醇或70mL乙醚中。
编号 操作 现象
实验3 取5mL饱和碳酸钠溶液,滴入几滴酚酞溶液,再加入3mL纯净的乙酸乙酯,振荡 碳酸钠溶液先变红,加入乙酸乙酯振荡后褪色
实验4 分离出试管②上层液体,加入饱和碳酸钠溶液,振荡 溶液变成浅红色,静置分层后红色消失
由实验3、4得出的结论是_____。
23.某兴趣小组在实验室用乙醇、浓硫酸、溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。有关数据见下表:
乙醇 溴乙烷 液溴
相对分子质量 46 109 160
状态 无色液体 无色液体 深红色液体
密度/(g·cm-3) 0.79 1.44 3.1
沸点/℃ 78.5 38.4 59
I.溴乙烷的制备:
反应原理如下:
H2SO4+NaBrNaHSO4+HBr↑
CH3CH2OH+HBrCH3CH2Br+H2O
实验装置如图(加热装置夹持装置均省略):
(1)图甲中B仪器的名称_______,作用为_______。
(2)若图甲中A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应生成了_______;F连接导管通入稀NaOH溶液中,其目的主要是吸收_______等尾气防止污染空气。
II.溴乙烷性质的探究。用如图实验装置验证溴乙烷的性质:
(3)在乙中试管内加入10 mL 6 mol·L-1 NaOH溶液和2 mL溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______。
(4)若将乙中试管里的NaOH溶液换成NaOH乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a试管中的水的作用是_______;若无a试管,将生成的气体直接通入b试管中,则b中的试剂可以为_______。
参考答案
1.C 2.C 3.A 4.C 5.B 6.B 7.A 8.B 9.D 10.B 11.D 12.C 13.A 14.A 15.B
16.丙烯 溴乙烷 乙醛 苯酚 裂解 ⑤
17.错误 正确 正确 错误 正确 错误 错误 正确
18. c
19. H++HSO=H2O+SO2↑ 2C2H5OH+O22CH3CHO+2H2O 共价键和离子键 碱 反应后所得溶液为NaHCO3,HCO发生水解和电离:HCO+H2O H2CO3+OH- ,HCO CO+H+,水解大于电离,所以溶液显碱性
20.O=C=O AgCl和AgI CH3MgI 2CH3MgI+2HC=2CH4↑+MgI2+MgCl2 2NH3+3CuON2+3H2O+Cu CDE
21.产生HBr 试管Ⅱ中出现分层,下层为无色油状液体 CH2=CH2或CH3CH2OCH2CH3 除去乙烯中的乙醇
22.应将浓硫酸缓慢的滴加到乙醇中,边加边搅拌 球形干燥管 原料利用率低(或容易发生副反应) +H2O +OH﹣ 挥发出的乙酸不能完全中和Na2CO3而使下层液体褪色 酚酞在乙酸乙酯中溶解度更大,乙酸乙酯萃取酚酞,使下层液体褪色
23.冷凝管 冷凝回流,增加反应物利用率 Br2 SO2、Br2、HBr CH3CH2Br+NaOHCH3CH2OH+NaBr 吸收乙醇 溴水(或溴的CCl4溶液)
一、单选题(共15题)
1.我们的生活和科技领域很多与化学密切相关。下列说法正确的是
A.煤的液化、气化主要是为了减少的排放
B.北斗三号全球卫星导航系统正式开通,其导航芯片的主要成分是二氧化硅
C.缺铁性贫血患者服用补铁剂时,与维生素同时服用效果更好
D.新冠病毒可用酒精或双氧水消毒,其消毒原理相同
2.化学反应经常伴随着颜色变化,下列有关反应显示的颜色正确的有
①蛋白质遇浓硝酸一黄色; ②淀粉溶液遇单质碘一蓝色;
③溴化银见光分解一银白色; ④热的氧化铜遇乙醇一绿色;
⑤新制氯水久置后一无色; ⑥苯酚在空气中氧化一粉红色。
A.2个 B.3个 C.4个 D.5个
3.下列说法不正确的是
A.糯米中的1mol淀粉能完全水解生成2mol葡萄糖
B.葡萄糖能发生银镜反应,说明其含有醛基,具有还原性
C.环式核糖与碱基、磷酸基团共同组成核糖核苷酸
D.蛋白质是含肽键的生物大分子
4.随着科学的发展,学科间的交叉和综合越来越多,学科之间的界限越来越不明显。下列研究或变化不属于化学研究范畴的是
A.MERS病毒疫苗的研制 B.近期出现雾霾的原因探究
C.朝鲜的原子弹爆炸实验 D.济南钢铁集团冶炼特种钢
5.可用于鉴别乙醇、乙醛、乙酸三种无色液体的一种试剂是
A.水 B.新制Cu(OH)2悬浊液
C.NaOH溶液 D.酚酞溶液
6.下列说法不正确的是
A.用稀盐酸清洗铜器表面
B.明矾可以对自来水消毒杀菌
C.KMnO4具有氧化性,其稀溶液可用于消毒
D.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
7.对以下古诗文中的现象,分析正确的是
A.“以硫黄、雄黄合硝石并蜜烧之,焰起烧手、面及屋舍”,指的是黑火药爆炸,其主要反应的方程式为:S+2KNO3+3C=K2S+N2↑+3CO2↑
B.“司南之杓(勺),投之于地,其杓指南”,司南中“杓”的主要成分为Fe2O3
C.“试玉要烧三日满,辨才须待七年期”,此文中“玉”的主要成分为硅酸盐,该诗句表明玉的硬度很大
D.“自古书契多编以竹简,其用缣帛者(丝织品)谓之为纸”,文中“纸”的主要成分是纤维素
8.乌洛托品( 分子式为 C6H12N4 )在医药、染料等工业中有广泛用途,是一种无色晶体,熔点263℃,高于此温度即升华或分解。下图是实验室用过量氨气与甲醛水溶液反应制乌洛托品的装置。下列说法正确的是
A.氨气与甲醛生成乌洛托品的反应属于加成反应
B.B装置内的长导管不能插入甲醛溶液中,是防倒吸
C.C装置中CaCl2的作用是防止空气中的水分进入合成装置中
D.反应一段时间后把B中的溶液转移到坩埚中蒸发结晶得到产品
9.某有机物分子结构如图,有关该有机物说法错误的是
A.分子式为C14H10O5
B.该有机物有3种含氧官能团
C.苯环上的一氯取代物有4种
D.1mol该有机物完全燃烧耗氧量大于等物质的量的C12H8完全燃烧的耗氧量
10.环丙叉环丙烷(b)由于其特殊的结构,一直受到结构和理论化学家的注意,根据其转化关系,下列说法正确的是
A.b的所有原子都在一个平面内
B.m的同分异构体中属于芳香族化合物的共有5种
C.p在氢氧化钠的乙醇溶液中加热生成烯烃
D.反应①是加成反应,反应②是消去反应
11.下列有关实验装置及用途叙述完全正确的是
A.a装置检验消去反应的产物丙烯 B.b装置检验酸性:盐酸>碳酸>硅酸
C.c装置用于实验室制取并收集乙烯 D.d装置用于实验室制硝基苯
12.下列说法不正确的是
A.固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,难溶于有机溶剂
B.盐析作用析出的蛋白质仍具有原来的活性,因此盐析可用于分离、提纯蛋白质
C.葵花籽油不能使酸性高锰酸钾溶液紫色褪去
D.石油减压分馏可得到重柴油、润滑油、石蜡等馏分,未被汽化的剩余物质是沥青
13.用括号中的试剂除去各组中的杂质,不正确的是
A.苯中的甲苯(溴水) B.乙醇中的水(新制CaO)
C.乙醛中的乙酸(NaOH) D.苯中的苯酚(NaOH)
14.足量的金属钠分别与甲醇、乙二醇、丙三醇反应,放出等体积的氢气,消耗这三种醇的物质的量之比是
A.6:3:2 B.2:3:6 C.3:2:1 D.1:2:3
15.下列实验能达到目的的是
A.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中含有乙烯
B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡
C.淀粉溶液和稀H2SO4混合加热,加入新制的Cu(OH)2悬浊液加热至沸腾,检验淀粉水解产物有还原性
D.利用图示装置并根据有关实验现象能推知酸性: CH3COOH> H2CO3>C6H5OH
二、填空题(共8题)
16.在① ② ③ ④ ⑤ (过氧乙酸),五种有机物中:
(1)能制成防疫口罩主要材料聚丙烯无纺布的是______(写名称,下同);能发生消法反应的是______;能发生银镜反应的是______;能与溶液显紫色的是______。
(2)可以由轻质油通过______(填“分馏”或“裂解”)制得。由在一定条件下合成聚丙烯的化学方程式是______。
(3)因具有强氧化性可作消毒剂的是______(填序号)。
17.(1)乙二酸、苯甲酸、硬脂酸、石炭酸都属于羧酸类有机物_____
(2)酯的官能团是酯基_____
(3)乙酸乙酯分子中含有甲基、乙基和酯基_____
(4)用CH3CH218OH与CH3COOH发生酯化反应,生成H218O_____
(5)用碳酸钠溶液可鉴别乙醇、乙酸和乙酸乙酯____
(6)在酸性条件下,的水解产物是CH3CO18OH和C2H5OH_____
(7)羧基和酯基中的均能与H2加成____
(8)C4H8O2同分异构体的类型有羧酸、酯、羟基醛等_____
18.已知下面两个反应,其中A为氯代烃,B为烯烃(其相对分子质量为42)。
反应①:
反应②:
请回答下列问题:
(1)化合物B的分子式为_____________.
(2)假设A分子中有两种等效氢且比例为6∶1,则反应①的化学方程式为_______;
(3)写出B在有机过氧化物()中与反应的化学方程式:_____;
(4)下列有关实验室检验A中是否有氯元素的方法或试剂正确的是______(填字母)。
a.燃烧法 b.溶液
c.溶液+稀硝酸溶液 d.醇溶液溶液
19.短周期元素A、B、C、D、E ,A为原子半径最小的元素,A、D同主族,D、E同周期,C、E同主族且E的原子序数为C的原子序数的2倍,B为组成物质种类最多的元素。
(1)E离子的原子结构示意图_______。
(2)分别由A、C、D、E四种元素组成的两种盐可相互反应得到气体,写出这个反应的离子方程式_______。
(3)由A、B、C三种元素组成的物质X,式量为46,在一定条件下与C、D两种元素的单质均可反应。写出X与C单质在红热的铜丝存在时反应的化学方程式_______。
(4)A、C、D三种元素组成的化合物Y中含有的化学键为_______,B的最高价氧化物与等物质的量的Y溶液反应后,溶液显_______(“酸”“碱”或“中”)性,原因是:_______。
20.I.X由四种常见元素组成的化合物,其中一种是氢元素,其摩尔质量小于200g·mol-1。某学习小组进行了如下实验:
已知:气体A在标况下的密度为0.714g·L-1,A完全燃烧的气体产物E能使澄清石灰水变浑浊,沉淀D是混合物。
请回答:
(1)气体E的结构式_______,沉淀D是______(写化学式),X的化学式______。
(2)写出化合物X与足量盐酸反应的化学方程式________。
II.纯净的氮化镁(Mg3N2)是淡黄色固体,热稳定性较好,遇水极易发生反应。某同学初步设计了如图实验装置制备氮化镁(夹持及加热仪器没有画出)。
已知:Mg+2NH3Mg(NH2)2+H2↑。
请回答:
(1)写出A中反应的化学方程式________。
(2)下列说法不正确的是________。
A.为了得到纯净的氮化镁,实验前需要排除装置中的空气
B.装置B起到了缓冲、安全的作用
C.装置C只吸收水,避免镁和水反应产生副产物
D.将装置B、C简化成装有碱石灰的U形管,也能达到实验目的
E.实验后,取D中固体加少量水,能生成使湿润的蓝色石蕊试纸变红的气体
21.下面的实验可以帮助我们认识乙醇与氢卤酸的反应,组装如图装置。在试管I中依次加入2mL蒸馏水,4mL浓硫酸,2mL 95%的乙醇和3g溴化钠粉末,在试管II中注入蒸馏水,烧杯中注入自来水。加热试管I至微沸状态数分钟,冷却。
(1)该反应中,加入蒸馏水,浓硫酸,溴化钠固体的目的是_______。
(2)判断有溴乙烷生成的现象是_______。
(3)试管I中反应除了生成溴乙烷,还可能生成的有机物有_______(任写一种结构简式)。
(4)为检验溴乙烷与NaOH乙醇溶液发生消去反应后生成的气体中是否含乙烯,设计出实验装置图(如图)。其中洗气瓶中水的作用是_______。
22.实验室制备乙酸乙酯的实验装置如图所示,回答下列问题:
(1)该实验中混合乙醇和浓硫酸的方法是_____。
(2)该装置与教材上的相比做了一些改进,其中仪器a的名称_____,改进后的装置仍然存在一定的不足,请指出其中的一点_____。
(3)试管②中溶液呈红色的原因是_____。(用离子方程式表示)。
(4)某实验小组在分离操作中,摇晃了试管②,发现上下两层溶液均变为无色,该小组对褪色原因进行探究。
Ⅰ.经过讨论猜想褪色原因是挥发的乙酸中和碳酸钠。
编号 操作 现象
实验1 用pH计测量饱和碳酸钠溶液pH pH=12.23
实验2 分离出试管②下层液体,用pH计测定pH pH=12.21
由实验1、2得出的结论是_____。
Ⅱ.查阅资料:酚酞是一种白色晶状粉末,不溶于水,1g酚酞可溶于13mL乙醇或70mL乙醚中。
编号 操作 现象
实验3 取5mL饱和碳酸钠溶液,滴入几滴酚酞溶液,再加入3mL纯净的乙酸乙酯,振荡 碳酸钠溶液先变红,加入乙酸乙酯振荡后褪色
实验4 分离出试管②上层液体,加入饱和碳酸钠溶液,振荡 溶液变成浅红色,静置分层后红色消失
由实验3、4得出的结论是_____。
23.某兴趣小组在实验室用乙醇、浓硫酸、溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。有关数据见下表:
乙醇 溴乙烷 液溴
相对分子质量 46 109 160
状态 无色液体 无色液体 深红色液体
密度/(g·cm-3) 0.79 1.44 3.1
沸点/℃ 78.5 38.4 59
I.溴乙烷的制备:
反应原理如下:
H2SO4+NaBrNaHSO4+HBr↑
CH3CH2OH+HBrCH3CH2Br+H2O
实验装置如图(加热装置夹持装置均省略):
(1)图甲中B仪器的名称_______,作用为_______。
(2)若图甲中A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应生成了_______;F连接导管通入稀NaOH溶液中,其目的主要是吸收_______等尾气防止污染空气。
II.溴乙烷性质的探究。用如图实验装置验证溴乙烷的性质:
(3)在乙中试管内加入10 mL 6 mol·L-1 NaOH溶液和2 mL溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______。
(4)若将乙中试管里的NaOH溶液换成NaOH乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a试管中的水的作用是_______;若无a试管,将生成的气体直接通入b试管中,则b中的试剂可以为_______。
参考答案
1.C 2.C 3.A 4.C 5.B 6.B 7.A 8.B 9.D 10.B 11.D 12.C 13.A 14.A 15.B
16.丙烯 溴乙烷 乙醛 苯酚 裂解 ⑤
17.错误 正确 正确 错误 正确 错误 错误 正确
18. c
19. H++HSO=H2O+SO2↑ 2C2H5OH+O22CH3CHO+2H2O 共价键和离子键 碱 反应后所得溶液为NaHCO3,HCO发生水解和电离:HCO+H2O H2CO3+OH- ,HCO CO+H+,水解大于电离,所以溶液显碱性
20.O=C=O AgCl和AgI CH3MgI 2CH3MgI+2HC=2CH4↑+MgI2+MgCl2 2NH3+3CuON2+3H2O+Cu CDE
21.产生HBr 试管Ⅱ中出现分层,下层为无色油状液体 CH2=CH2或CH3CH2OCH2CH3 除去乙烯中的乙醇
22.应将浓硫酸缓慢的滴加到乙醇中,边加边搅拌 球形干燥管 原料利用率低(或容易发生副反应) +H2O +OH﹣ 挥发出的乙酸不能完全中和Na2CO3而使下层液体褪色 酚酞在乙酸乙酯中溶解度更大,乙酸乙酯萃取酚酞,使下层液体褪色
23.冷凝管 冷凝回流,增加反应物利用率 Br2 SO2、Br2、HBr CH3CH2Br+NaOHCH3CH2OH+NaBr 吸收乙醇 溴水(或溴的CCl4溶液)
