5.1.1 质量守恒定律课后作业—2021-2022学年九年级化学人教版上册(word版 含答案)
文档属性
| 名称 | 5.1.1 质量守恒定律课后作业—2021-2022学年九年级化学人教版上册(word版 含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 169.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-08 22:06:14 | ||
图片预览

文档简介
5.1.1质量守恒定律课后作业
一、夯实基础
1.下列有关质量守恒 定律的认识,不正确的是( )
A.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关
B.通过化学变化,只能改变世界上物质的种类,不能改变物质的总质量
C.质量守恒定律为定量揭示化学变化的规律,提供了理论依据
D.随着科技的发展,精密仪器为我们定量研究化学变化创造了条件
2.根据质量守恒定律,电解NaCl的水溶液,不可能得到的生成物是( )
A.KNO3 B.C12 C.H2 D.NaOH
3.下列现象不能用质量守恒定律解释的是( )
A.将2g氢气在20g氧气中燃烧,生成18g水
B.将20mL酒精与20mL水混合,总体积小于40mL
C.将浓硫酸置于空气中一段时间,溶液质量增加
D.将二氧化碳的水溶液加热,溶液质量减轻
4.某有机物与氧气充分反应,产物只有二氧化碳和水,则该有机物一定含有的元素是( )
A.C、O B.H、O C.C、H D.C、H、O
5.(安顺)双氧水分解成水和氧气的反应前后,发生改变的是( )
A.元素种类 B.原子种类 C.分子种类 D.原子数量
6.图是某个化学反应的微观模拟图,下列关于该反应前,后的说法正确的是( )
A.均为混合物
B.质量减少
C.原子总数减少
D.分子总数不变
二、能力提升
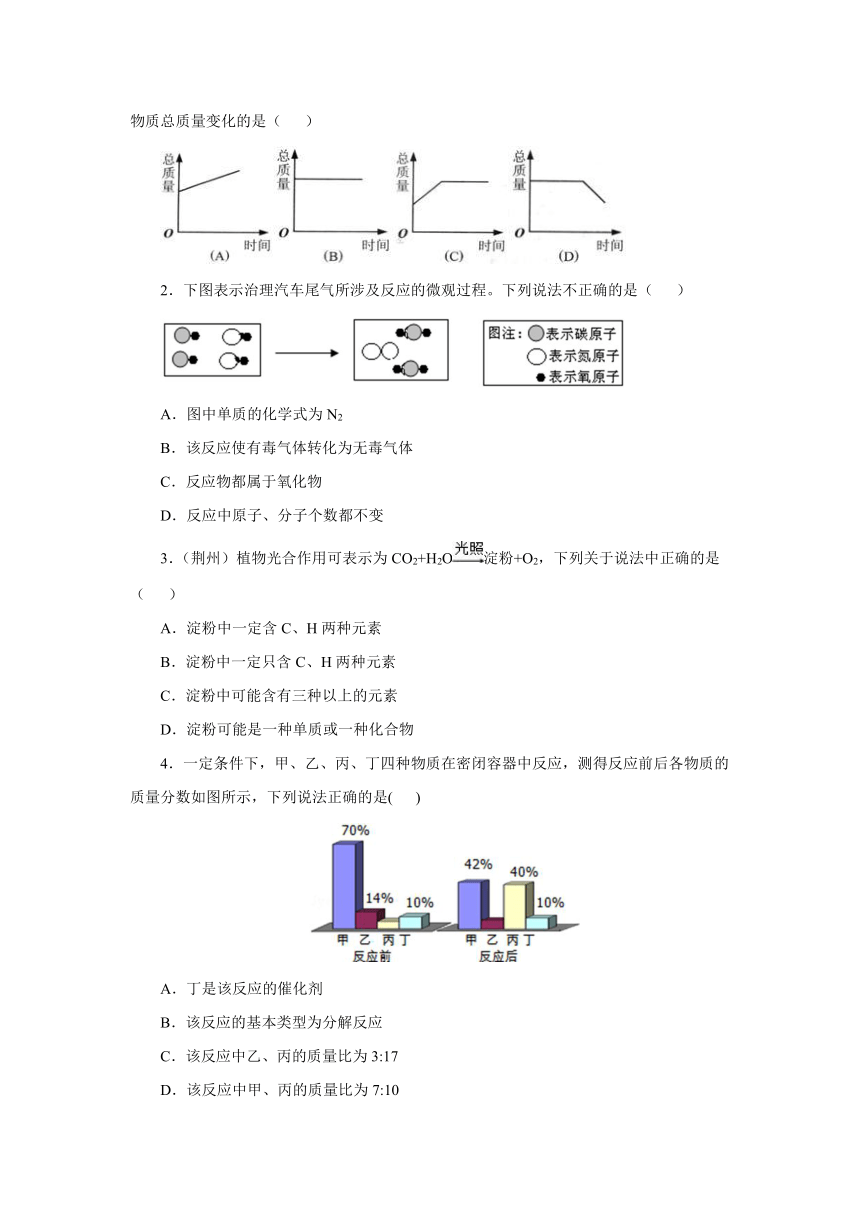
1.镁带在耐高温的容器中密封(内含空气)加热,在图中,能正确表示容器里所盛的物质总质量变化的是( )
2.下图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是( )
A.图中单质的化学式为N2
B.该反应使有毒气体转化为无毒气体
C.反应物都属于氧化物
D.反应中原子、分子个数都不变
3.(荆州)植物光合作用可表示为CO2+H2O淀粉+O2,下列关于说法中正确的是( )
A.淀粉中一定含C、H两种元素
B.淀粉中一定只含C、H两种元素
C.淀粉中可能含有三种以上的元素
D.淀粉可能是一种单质或一种化合物
4.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
A.丁是该反应的催化剂
B.该反应的基本类型为分解反应
C.该反应中乙、丙的质量比为3:17
D.该反应中甲、丙的质量比为7:10
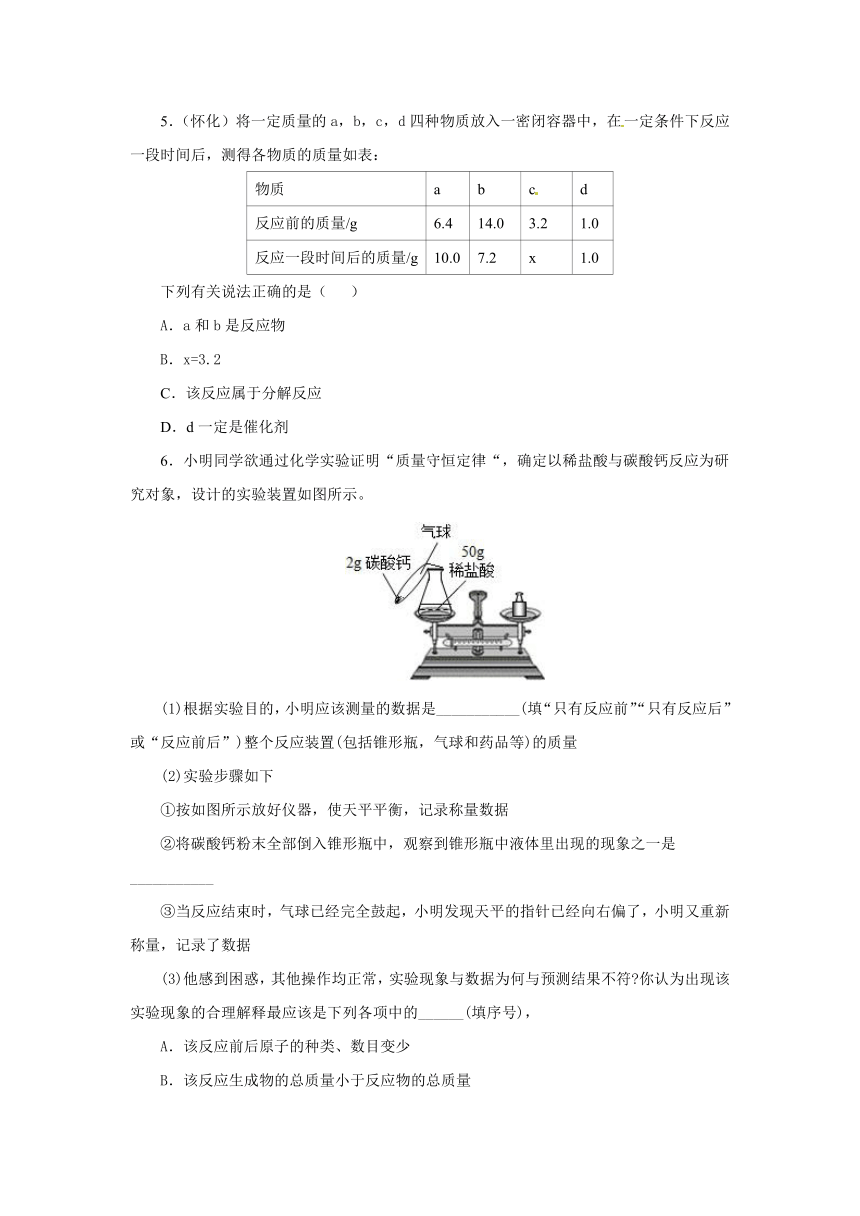
5.(怀化)将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:
物质 a b c d
反应前的质量/g 6.4 14.0 3.2 1.0
反应一段时间后的质量/g 10.0 7.2 x 1.0
下列有关说法正确的是( )
A.a和b是反应物
B.x=3.2
C.该反应属于分解反应
D.d一定是催化剂
6.小明同学欲通过化学实验证明“质量守恒定律“,确定以稀盐酸与碳酸钙反应为研究对象,设计的实验装置如图所示。
(1)根据实验目的,小明应该测量的数据是___________(填“只有反应前”“只有反应后”或“反应前后”)整个反应装置(包括锥形瓶,气球和药品等)的质量
(2)实验步骤如下
①按如图所示放好仪器,使天平平衡,记录称量数据
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象之一是___________
③当反应结束时,气球已经完全鼓起,小明发现天平的指针已经向右偏了,小明又重新称量,记录了数据
(3)他感到困惑,其他操作均正常,实验现象与数据为何与预测结果不符 你认为出现该实验现象的合理解释最应该是下列各项中的______(填序号),
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不理守质量守恒定律
三、课外拓展
1.在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示。请回答下列问题:
(1)实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是________________________________________;
(2)将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从具体的反应物和生成物分析天平平衡的原因是________________________________________。
2.化学中质量守恒定律是一个非常重要的定律
(1)某化学小组同学,用如图所示装置探究质量守恒定律分反应并冷却后,天平不能平衡的是________(填字母序号)
(2)在化学反应前后,一定不变的是________ (填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类
(3)请从微观角度解释质量守恒的原因________________________
(4)红热的铁能与水蒸气反应,放出气体X,同时生成固体Y。X气体靠近火焰点火时,能燃烧或发出爆鸣声,其反应的化学方程式为:3Fe+4H2O4X+Y。则X的化学式为________,Y的化学式为________。
四、中考真题链接
1.(四川达州)某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水,下列说法不正确的是( )
A.该纯净物中含有C、H元素,不含O元素
B.该反应中O和CO2的质量比为14:11
C.该反应中O2和H2O的分子数之比为7:6
D.该纯净物中C、H原子的个数比为1:4
2.(湘潭)在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量变化情况如图所示,下列说法错误的是( )
A.该物质为化合反应
B.丙可能是该反应的催化剂
C.该化学反应中甲、丁的质量变化之比为5:7
D.该化学反应中乙、丁的质量变化之比为1:4
参考答案
一、夯实基础
1.A
2.A
3.B
4.C
【解析】生成物二氧化碳、水中含有C,H,O元素,则反应物中也一定含有这三种元素 .物质在空气中燃烧是和空气中的氧气反应,氧气由O元素组成,则C,H一定是从某物质中来,而某物质中也可能含有O元素.故这种物质中一定含有含C和H,可能含O.
5.C
【解析】化学变化的实质是分子分成原子,原子再重新组合成新分子,在反应前后,原子的种类、数目、元素种类都不变,分子种类改变.
6.A
二、能力提升
1.B
【解析】反应前后密闭容器的质量不变
2.D
3.A
【解析】CO2和H2O两种物质中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,生成物氧气中只含有氧元素,则淀粉中一定含有碳、氢两种元素,可能含有氧元素.
A、淀粉中一定含C、H两种元素,故选项说法正确.
B、淀粉中一定含C、H两种元素,可能含有氧元素,故选项说法错误.
C、淀粉中一定含C、H两种元素,可能含有氧元素,最多含有三种元素,故选项说法错误.
D、淀粉中一定含C、H两种元素,不可能是单质,故选项说法错误.
4.C
【解析】根据质量守恒定律,化学反应前后物质的总质量不变。设物质总质量为100g,则反应前甲、乙,丙,丁的质量分别为70g,14g,6g、10g反应后分别为42g、8g、40g,10g;反应后质量增加的为生成物,质量减少的为反应物,质量不变的可能是催化剂,也可能是无关杂质,因此对比四种物质反应前后质量变化,甲减少了28g,乙减少了6g,丙增加了34g,丁质量不变丁可能是催化剂;该反应的文字表达式为甲+乙→丙,属于化合反应,反应中乙,丙的质量比为6g:34g=3:17,甲、丙的质量比为28g:34g=14:17.
5.C
【解析】由表格信息可知反应后a质量增加了10﹣6.4g=3.6克,是生成物;b质量减少了14g﹣7.2g=6.8克,是反应物;d质量不变,做催化剂或者是杂质.生成物还少3.2克,所以c是生成物,所以反应后物质c的质量为3.2g+3.2g=6.4g,反应物是b,生成物是a、c,反应符合“一变多”的特点,属于分解反应;
A、反应物是b,生成物是a、c,错误;
B、反应后物质c的质量为3.2g+3.2g=6.4g,x=6.4,错误;
C、该反应属于分解反应,正确;
D、d质量不变,做催化剂或者是杂质,错误.
6.(1)反应前后 (2)有气泡产生 (3)C
【解析】质量守恒定律是指化学反应前后物质的总质量不变,因此探究质量守恒定律应该称量反且前后物质的总盾量。碳酸钠与稀盐酸反应产生气泡,该实验在密闭容器中进行,天平不平衡的原因与气球的变化有关,反应过程中产生大量气体,气球胀大,所受的空气浮力增大,导致反应后天干不平衡
三、课外拓展
1.(1)白磷燃烧消耗氧气,生成固体五氧化二磷,使瓶中压强变小,小于外界大气压,在大气压的作用下,C中气球变小,A内压强等于外界大气压,所以A、C中气球大小不同
(2)参加化学变化(或消耗;或反应掉)的白磷的质量和氧气的质量总和等于生成的五氧化二磷的质量。
2.(1)B (2)①②⑤ (3)在化学反应前后,原子的种类没有改变、原子的数目没有增减、原子的质量没有变化 (4)H2 Fe3O4
四、中考链接
1.D
2.D
【解析】A、该反应是化合反应,正确;B、丙质量不变,可能做催化剂,正确;C、反应中甲、丁的质量比5g:7g=5:7,正确;D、乙、丁的质量变化之比为2:7,错误.故选D
一、夯实基础
1.下列有关质量守恒 定律的认识,不正确的是( )
A.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关
B.通过化学变化,只能改变世界上物质的种类,不能改变物质的总质量
C.质量守恒定律为定量揭示化学变化的规律,提供了理论依据
D.随着科技的发展,精密仪器为我们定量研究化学变化创造了条件
2.根据质量守恒定律,电解NaCl的水溶液,不可能得到的生成物是( )
A.KNO3 B.C12 C.H2 D.NaOH
3.下列现象不能用质量守恒定律解释的是( )
A.将2g氢气在20g氧气中燃烧,生成18g水
B.将20mL酒精与20mL水混合,总体积小于40mL
C.将浓硫酸置于空气中一段时间,溶液质量增加
D.将二氧化碳的水溶液加热,溶液质量减轻
4.某有机物与氧气充分反应,产物只有二氧化碳和水,则该有机物一定含有的元素是( )
A.C、O B.H、O C.C、H D.C、H、O
5.(安顺)双氧水分解成水和氧气的反应前后,发生改变的是( )
A.元素种类 B.原子种类 C.分子种类 D.原子数量
6.图是某个化学反应的微观模拟图,下列关于该反应前,后的说法正确的是( )
A.均为混合物
B.质量减少
C.原子总数减少
D.分子总数不变
二、能力提升
1.镁带在耐高温的容器中密封(内含空气)加热,在图中,能正确表示容器里所盛的物质总质量变化的是( )
2.下图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是( )
A.图中单质的化学式为N2
B.该反应使有毒气体转化为无毒气体
C.反应物都属于氧化物
D.反应中原子、分子个数都不变
3.(荆州)植物光合作用可表示为CO2+H2O淀粉+O2,下列关于说法中正确的是( )
A.淀粉中一定含C、H两种元素
B.淀粉中一定只含C、H两种元素
C.淀粉中可能含有三种以上的元素
D.淀粉可能是一种单质或一种化合物
4.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
A.丁是该反应的催化剂
B.该反应的基本类型为分解反应
C.该反应中乙、丙的质量比为3:17
D.该反应中甲、丙的质量比为7:10
5.(怀化)将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:
物质 a b c d
反应前的质量/g 6.4 14.0 3.2 1.0
反应一段时间后的质量/g 10.0 7.2 x 1.0
下列有关说法正确的是( )
A.a和b是反应物
B.x=3.2
C.该反应属于分解反应
D.d一定是催化剂
6.小明同学欲通过化学实验证明“质量守恒定律“,确定以稀盐酸与碳酸钙反应为研究对象,设计的实验装置如图所示。
(1)根据实验目的,小明应该测量的数据是___________(填“只有反应前”“只有反应后”或“反应前后”)整个反应装置(包括锥形瓶,气球和药品等)的质量
(2)实验步骤如下
①按如图所示放好仪器,使天平平衡,记录称量数据
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象之一是___________
③当反应结束时,气球已经完全鼓起,小明发现天平的指针已经向右偏了,小明又重新称量,记录了数据
(3)他感到困惑,其他操作均正常,实验现象与数据为何与预测结果不符 你认为出现该实验现象的合理解释最应该是下列各项中的______(填序号),
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不理守质量守恒定律
三、课外拓展
1.在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示。请回答下列问题:
(1)实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是________________________________________;
(2)将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从具体的反应物和生成物分析天平平衡的原因是________________________________________。
2.化学中质量守恒定律是一个非常重要的定律
(1)某化学小组同学,用如图所示装置探究质量守恒定律分反应并冷却后,天平不能平衡的是________(填字母序号)
(2)在化学反应前后,一定不变的是________ (填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类
(3)请从微观角度解释质量守恒的原因________________________
(4)红热的铁能与水蒸气反应,放出气体X,同时生成固体Y。X气体靠近火焰点火时,能燃烧或发出爆鸣声,其反应的化学方程式为:3Fe+4H2O4X+Y。则X的化学式为________,Y的化学式为________。
四、中考真题链接
1.(四川达州)某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水,下列说法不正确的是( )
A.该纯净物中含有C、H元素,不含O元素
B.该反应中O和CO2的质量比为14:11
C.该反应中O2和H2O的分子数之比为7:6
D.该纯净物中C、H原子的个数比为1:4
2.(湘潭)在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量变化情况如图所示,下列说法错误的是( )
A.该物质为化合反应
B.丙可能是该反应的催化剂
C.该化学反应中甲、丁的质量变化之比为5:7
D.该化学反应中乙、丁的质量变化之比为1:4
参考答案
一、夯实基础
1.A
2.A
3.B
4.C
【解析】生成物二氧化碳、水中含有C,H,O元素,则反应物中也一定含有这三种元素 .物质在空气中燃烧是和空气中的氧气反应,氧气由O元素组成,则C,H一定是从某物质中来,而某物质中也可能含有O元素.故这种物质中一定含有含C和H,可能含O.
5.C
【解析】化学变化的实质是分子分成原子,原子再重新组合成新分子,在反应前后,原子的种类、数目、元素种类都不变,分子种类改变.
6.A
二、能力提升
1.B
【解析】反应前后密闭容器的质量不变
2.D
3.A
【解析】CO2和H2O两种物质中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,生成物氧气中只含有氧元素,则淀粉中一定含有碳、氢两种元素,可能含有氧元素.
A、淀粉中一定含C、H两种元素,故选项说法正确.
B、淀粉中一定含C、H两种元素,可能含有氧元素,故选项说法错误.
C、淀粉中一定含C、H两种元素,可能含有氧元素,最多含有三种元素,故选项说法错误.
D、淀粉中一定含C、H两种元素,不可能是单质,故选项说法错误.
4.C
【解析】根据质量守恒定律,化学反应前后物质的总质量不变。设物质总质量为100g,则反应前甲、乙,丙,丁的质量分别为70g,14g,6g、10g反应后分别为42g、8g、40g,10g;反应后质量增加的为生成物,质量减少的为反应物,质量不变的可能是催化剂,也可能是无关杂质,因此对比四种物质反应前后质量变化,甲减少了28g,乙减少了6g,丙增加了34g,丁质量不变丁可能是催化剂;该反应的文字表达式为甲+乙→丙,属于化合反应,反应中乙,丙的质量比为6g:34g=3:17,甲、丙的质量比为28g:34g=14:17.
5.C
【解析】由表格信息可知反应后a质量增加了10﹣6.4g=3.6克,是生成物;b质量减少了14g﹣7.2g=6.8克,是反应物;d质量不变,做催化剂或者是杂质.生成物还少3.2克,所以c是生成物,所以反应后物质c的质量为3.2g+3.2g=6.4g,反应物是b,生成物是a、c,反应符合“一变多”的特点,属于分解反应;
A、反应物是b,生成物是a、c,错误;
B、反应后物质c的质量为3.2g+3.2g=6.4g,x=6.4,错误;
C、该反应属于分解反应,正确;
D、d质量不变,做催化剂或者是杂质,错误.
6.(1)反应前后 (2)有气泡产生 (3)C
【解析】质量守恒定律是指化学反应前后物质的总质量不变,因此探究质量守恒定律应该称量反且前后物质的总盾量。碳酸钠与稀盐酸反应产生气泡,该实验在密闭容器中进行,天平不平衡的原因与气球的变化有关,反应过程中产生大量气体,气球胀大,所受的空气浮力增大,导致反应后天干不平衡
三、课外拓展
1.(1)白磷燃烧消耗氧气,生成固体五氧化二磷,使瓶中压强变小,小于外界大气压,在大气压的作用下,C中气球变小,A内压强等于外界大气压,所以A、C中气球大小不同
(2)参加化学变化(或消耗;或反应掉)的白磷的质量和氧气的质量总和等于生成的五氧化二磷的质量。
2.(1)B (2)①②⑤ (3)在化学反应前后,原子的种类没有改变、原子的数目没有增减、原子的质量没有变化 (4)H2 Fe3O4
四、中考链接
1.D
2.D
【解析】A、该反应是化合反应,正确;B、丙质量不变,可能做催化剂,正确;C、反应中甲、丁的质量比5g:7g=5:7,正确;D、乙、丁的质量变化之比为2:7,错误.故选D
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
