3.4物质组成的表达式同步练习-2021-2022学年九年级化学科粤版(2012)上册(含解析)
文档属性
| 名称 | 3.4物质组成的表达式同步练习-2021-2022学年九年级化学科粤版(2012)上册(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 98.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-10 00:00:00 | ||
图片预览





文档简介
第3章维持生命之气---氧气3.4物质组成的表达式同步练习九年级化学上学期(科粤版2012)
练习
一、单选题,共12小题
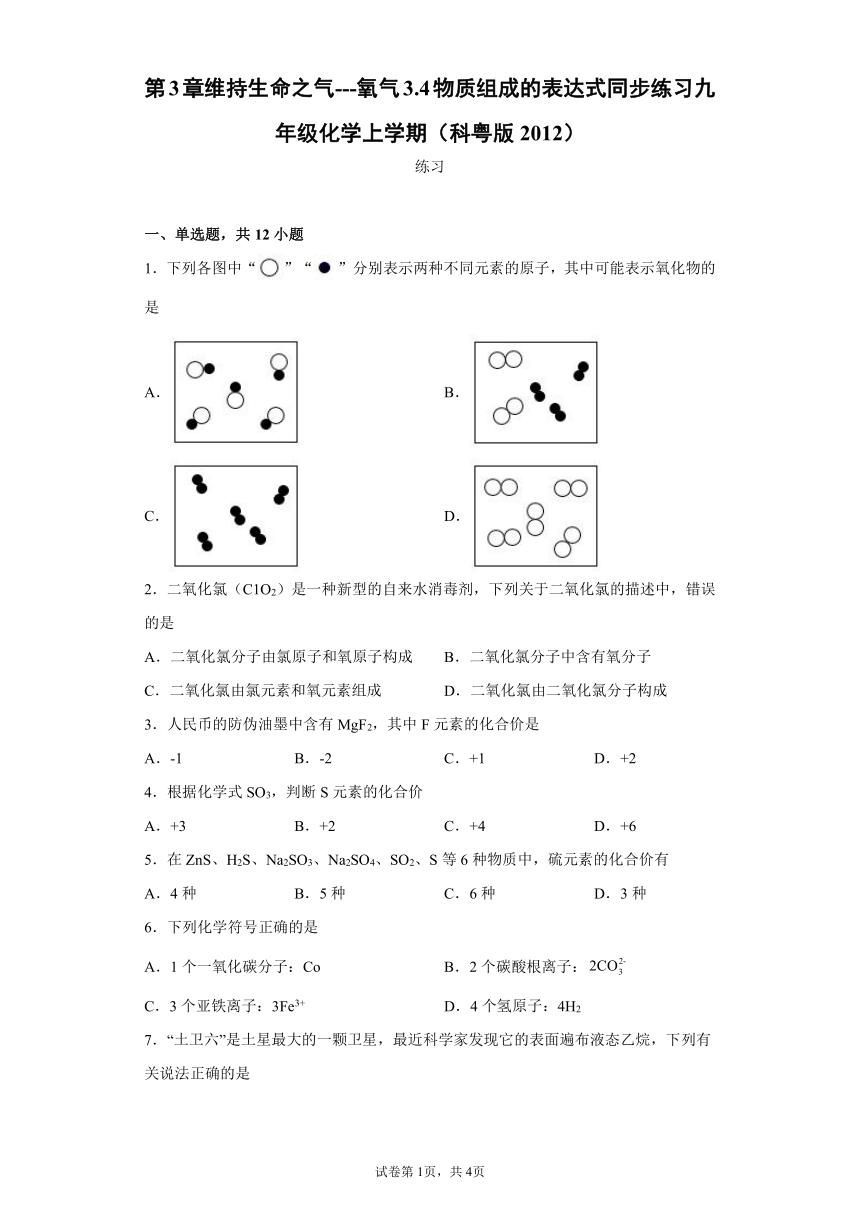
1.下列各图中“”“”分别表示两种不同元素的原子,其中可能表示氧化物的是
A. B.
C. D.
2.二氧化氯(C1O2)是一种新型的自来水消毒剂,下列关于二氧化氯的描述中,错误的是
A.二氧化氯分子由氯原子和氧原子构成 B.二氧化氯分子中含有氧分子
C.二氧化氯由氯元素和氧元素组成 D.二氧化氯由二氧化氯分子构成
3.人民币的防伪油墨中含有MgF2,其中F元素的化合价是
A.-1 B.-2 C.+1 D.+2
4.根据化学式SO3,判断S元素的化合价
A.+3 B.+2 C.+4 D.+6
5.在ZnS、H2S、Na2SO3、Na2SO4、SO2、S等6种物质中,硫元素的化合价有
A.4种 B.5种 C.6种 D.3种
6.下列化学符号正确的是
A.1个一氧化碳分子:Co B.2个碳酸根离子:
C.3个亚铁离子:3Fe3+ D.4个氢原子:4H2
7.“土卫六”是土星最大的一颗卫星,最近科学家发现它的表面遍布液态乙烷,下列有关说法正确的是
A.乙烷是由碳、氢原子直接构成的化合物
B.乙烷中氢元素的质量分数为80%
C.乙烷分子中碳、氢元素的质量比是1:3
D.每个乙烷分子中含有8个原子
8.某物质化学式为M2O3,其中M与O的质量比为9:8,O的相对原子质量为16,M的相对原子质量是
A.27 B.56 C.14 D.31
9.在“宏观一微观一符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是
A.图①是氖原子的结构示意图,氖气的化学式为Ne
B.图②④表示的元素是金属元素
C.图③对应的粒子符号为S2-
D.图⑤对应的原子,原子核中没有中子
10.下列有关微粒的说法错误的是
A.原子、分子、离子都是构成物质的微粒,构成物质的微粒都在不停的运动
B.钠原子失去一个电子形成钠离子,钠原子和钠离子的化学性质不同
C.过氧化氢是由氢原子和氧原子构成,它和水的组成元素相同,都是氧化物
D.原子中不一定含有中子,质子与中子的质量近似相等,电性不同,数目可能相同
11.在N2O5、NO2、N2O、X、NH3五种物质中,氮元素的化合价按一定顺序排列,则X是下列物质中的哪种物质
A.N2 B.NaNO3 C.NH4Cl D.NO
12.如下图是五种微粒的结构示意图,下列说法正确的是
A.①④属于金属元素 B.②的微粒符号是A13+
C.②③⑤属于阳离子 D.②和⑤所表示的粒子化学性质相似
二、非选择题,共5小题
13.碘酸钾(KIO3)中碘元素的化合价为______价.
14.化学用语是国际通用语言,是学习化学的重要工具。
(1)用化学用语填空
①2个氖气分子________;
②三个亚铁离子_______;
③4个硝酸根离子_______;
④地壳中含量第二的元素________;
⑤标出锰酸钾中锰元素的化合价_______。
(2)写出下列符号中数字“2”的含义
①SO2____________________;
②Ca2+________________;
③__________。
15.按要求写出相应的化学用语
(1)钠离子___________;
(2)4个氢氧根离子___________;
(3)2个氢原子___________;
(4)保持水化学性质的最小粒子___________;
(5)氩气___________。
16.观察下列原子结构示意图和元素周期表(部分),回答有关问题。
(1)图1中,具有相对稳定结构的原子是______(填元素符号)。
(2)图1中,属于金属元素的是______(填元素名称)。
(3)含有X元素的化合物常用作化肥,X元素的原子序数是______,相对原子质量为______。
(4)硅元素的氧化物是天然水晶的主要成分。在该氧化物中,硅元素的化合价为+4价,则其化学式为______。
17.化学符号是学习化学的工具,从现在起,我们就要开始与它密切接触,做到见到名称能立即写出符号,根据符号能准确地叫出名称。
(1)写出元素的符号或名称:
H_________,氧_________,C_________,铁_________,镁_________,铜_________,锰_________。
(2)写出下列物质的化学式:
水__________,二氧化碳__________,氧气__________,氨气__________,氮气__________。
(3)写出以下两个化学实验中观察到的主要现象和文字或符号表达式。
A碳酸氢铵受热分解现象:___________。
文字或符号表达式:___________。
B蜡烛在空气中燃烧现象:___________。
文字或符号表达式:___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
略
2.B
【详解】
A、二氧化氯分子由氯原子和氧原子构成,A正确。
B、二氧化氯分子中含有氧原子,不含氧分子,B错误。
C、由化学式可知,二氧化氯由氯元素和氧元素组成,C正确。
D、二氧化氯由二氧化氯分子构成,D正确。
故选:B。
3.A
【详解】
MgF2中镁元素化合价为+2价,设F元素的化合价为x,根据在化合物中正负化合价代数和为零,可得(+2)+2x=0,则x=-1;
故选A。
4.D
【详解】
SO3中氧元素的化合价为-2价,化合物中正负化合价代数和为零,则硫元素的化合价为+6。
故选:D。
5.A
【详解】
单质中元素的化合价为0。
化合物中各元素的化合价代数和为0。锌通常为+2价,氢通常为+1价,钠通常为+1价,氧通常为-2价。所以ZnS、H2S、Na2SO3、Na2SO4、SO2中硫元素的化合价分别为-2价,-2价,+4价,+6价,+4价。
硫元素的化合价有4种,故选A。
【点睛】
6.B
【详解】
A、1个一氧化碳分子是由1个碳原子和1个氧原子构成的,化学式为:CO,选项A不正确;
B、离子符号前的数字表示离子个数,2个碳酸根离子为:2,选项B正确;
C、1个亚铁离子带2个单位正电荷,符号为Fe2+,因此3个亚铁离子为:3Fe2+,选项C不正确;
D、元素符号表示这种元素的1个原子,因此4个氢原子为:4H,选项D不正确。
故选B。
7.D
【分析】
从示意图可知,乙烷的化学式为C2H6。
【详解】
A、乙烷是乙烷分子构成的,错误。
B、乙烷中氢元素的质量分数为,错误。
C、乙烷分子中碳、氢元素的质量比是24:6=4:1,错误。
D、每个乙烷分子中含有2个碳原子,6个氢原子,共8个原子。正确。
故选D。
【点睛】
8.A
【分析】
化合物中各元素质量比=各原子的相对原子质量与原子个数乘积之比
【详解】
设M的相对原子质量为x,由题意,M与O的质量比为9:8,O的相对原子质量为16,则(2×x):(16×3)=9:8,解得x=27。
故选:A。
9.B
【详解】
A、图①质子数=核外电子数=10,是氖原子的结构示意图。氖气是稀有气体由原子直接构成,化学式为Ne。正确。
B、图②④质子数分别为11和17,质子数=原子序数,分别为钠元素和氯元素,钠元素属于金属元素,氯元素属于非金属元素,错误。
C、图③质子数=16,电子数=18,是硫原子得到2个电子形成的硫离子,符号为S2-。正确。
D、图⑤对应的是氢元素的原子,氢原子原子核内没有中子,正确。
故选B。
10.C
【详解】
A、原子、分子、离子都是构成物质的微粒,构成物质的微粒都在不停的运动,说法正确,不符合题意;
B、钠原子失去一个电子形成钠离子,钠原子和钠离子的化学性质不同,因为它们的最外层电子数不同,说法正确,不符合题意;
C、过氧化氢是由氢原子和氧原子构成,说法错误,应该是过氧化氢由过氧化氢分子构成,故符合题意;
D、原子中不一定含有中子,质子与中子的质量近似相等,电性不同,数目可能相同,说法正确。不符合题意;
故选C。
11.A
【分析】
氧元素的化合价通常为-2,氢元素化合价通常为+1,根据化合物中各元素正负化合价代数和为0,N2O5、NO2、N2O、NH3中氮元素的化合价分别为+5,+4,+1,-3。所以X中氮元素的化合价为0或-1,或-2。
【详解】
A、N2中氮元素的化合价为0,符合分析要求。
B、NaNO3中氮元素的化合价为+5,不符合分析要求。
C、NH4Cl中氮元素的化合价为-3,不符合分析要求。
D、NO中氮元素的化合价为+2,不符合分析要求。
故选A。
【点睛】
12.B
【分析】
【详解】
A、①④的核内质子数分别是9、13,分别是氟元素和铝元素,分别属于非金属元素、金属元素,故选项说法错误。
B、②质子数=13,核外电子数=10,质子数>核外电子数,为带3个单位正电荷的铝离子,符号是Al3+,故选项说法正确。
C、②③,质子数>核外电子数,为阳离子;⑤质子数=核外电子数=10,为原子,故选项说法错误。
D、②是原子失去3个电子得到的,②和⑤所表示的粒子分别是铝离子和氖原子,它们的化学性质不相似,故选项说法错误。
故选B。
【点睛】
明确粒子中核内质子数和核外电子数之间的关系是正确解题的关键。
13.+5
【详解】
根据在化合物中正负化合价代数和为零,钾元素的化合价为+1价,氧元素的化合价为﹣2价,设碘酸钾(KIO3)中碘元素的化合价为x,则(+1)+x+(﹣2)×3=0,解得x=+5;
故答案为:+5.
14.
(1) 2Ne 3Fe2+ Si
(2) 一个二氧化硫分子中含有两个氧原子 一个钙离子带两个单位的正电荷 氧化汞中氧元素显-2价
【分析】
(1)
①分子的表示方法是正确书写物质的化学式,表示多个该分子,在其化学式前加上相应的数字。2个氖气分子表示为:2Ne;
②离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字。三个亚铁离子表示为:3Fe2+;
③离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字。4个硝酸根离子表示为:;
④地壳中含量第二的元素是硅元素,其元素符号表示为:Si;
⑤在锰酸钾中,钾元素显+1价,氧元素显-2价,根据化合物各元素的化合价为零,可知锰元素的化合价为+6价。元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后。锰酸钾中锰元素的化合价表示为:。
(2)
①化学式中元素符号右下角数字表示一个分子中含原子的数目。SO2中数字“2”表示为:一个二氧化硫分子中含有两个氧原子;
②离子符号右上角的数字表示该离子所带电荷的数目。Ca2+中数字“2”表示为:一个钙离子带两个单位的正电荷;
③化学式中元素符号正上方的数字表示元素的化合价。中数字“2”表示为:氧化汞中氧元素显-2价。
15.
(1)Na+
(2)4OH-
(3)2H
(4)H2O
(5)Ar
【分析】
(1)
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。钠离子表示为:Na+;
(2)
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字。4个氢氧根离子表示为:4OH-;
(3)
原子的表示方法是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应的数字。2个氢原子表示为:2H;
(4)
水是由水分子构成,保持水化学性质的最小粒子是水分子,表示为:H2O;
(5)
氩气是稀有气体,化学式直接用元素符号表示,表示为:Ar。
16.
(1)Ne
(2)钠,铝
(3) 15 30.97
(4)SiO2
【分析】
(1)
Ne的最外层电子数是8,是具有相对稳定结构的原子;
(2)
由原子结构示意图可知,图1中,属于金属元素的是钠、铝;
(3)
由元素周期比表中一个格的含义可知,含有X元素的化合物常用作化肥,X元素是磷元素,原子序数是15,相对原子质量为30.97。
(4)
硅元素的化合价为+4价,氧元素的化合价为-2价。根据化合物中各元素的化合价代数和为零,该氧化物的化学式为SiO2。
【点睛】
17.
(1) 氢 O 碳 Fe Mg Cu Mn
(2) H2O CO2 O2 NH3 N2
(3) 固体消失,有刺激性气味的气体产生(或试管管壁上有水珠出现) ( ) 产生黄色火焰,发光发热 蜡烛+氧气二氧化碳+水(或蜡烛+O2CO2+H2O)
【解析】
(1)
H是氢元素,氧符号是O,C是碳元素,铁符号是Fe,镁符号是Mg,铜符号是Cu,锰符号是Mn;
(2)
水的化学式是H2O,二氧化碳:CO2,氧气:O2,氨气:NH3,氮气:N2;
(3)
A碳酸氢铵受热时,固体逐渐消失,有刺激性气味气体产生,管口还有小水珠;文字表达式为:碳酸氢铵氨气+水+二氧化碳,符号表达式为:NH4HCO3NH3+CO2+H2O ;
B蜡烛在空气中燃烧,发出黄色火焰,并发光发热,文字表达式为:蜡烛+氧气 二氧化碳+水,符号表达式为:蜡烛+O2 CO2+H2O);答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共12小题
1.下列各图中“”“”分别表示两种不同元素的原子,其中可能表示氧化物的是
A. B.
C. D.
2.二氧化氯(C1O2)是一种新型的自来水消毒剂,下列关于二氧化氯的描述中,错误的是
A.二氧化氯分子由氯原子和氧原子构成 B.二氧化氯分子中含有氧分子
C.二氧化氯由氯元素和氧元素组成 D.二氧化氯由二氧化氯分子构成
3.人民币的防伪油墨中含有MgF2,其中F元素的化合价是
A.-1 B.-2 C.+1 D.+2
4.根据化学式SO3,判断S元素的化合价
A.+3 B.+2 C.+4 D.+6
5.在ZnS、H2S、Na2SO3、Na2SO4、SO2、S等6种物质中,硫元素的化合价有
A.4种 B.5种 C.6种 D.3种
6.下列化学符号正确的是
A.1个一氧化碳分子:Co B.2个碳酸根离子:
C.3个亚铁离子:3Fe3+ D.4个氢原子:4H2
7.“土卫六”是土星最大的一颗卫星,最近科学家发现它的表面遍布液态乙烷,下列有关说法正确的是
A.乙烷是由碳、氢原子直接构成的化合物
B.乙烷中氢元素的质量分数为80%
C.乙烷分子中碳、氢元素的质量比是1:3
D.每个乙烷分子中含有8个原子
8.某物质化学式为M2O3,其中M与O的质量比为9:8,O的相对原子质量为16,M的相对原子质量是
A.27 B.56 C.14 D.31
9.在“宏观一微观一符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是
A.图①是氖原子的结构示意图,氖气的化学式为Ne
B.图②④表示的元素是金属元素
C.图③对应的粒子符号为S2-
D.图⑤对应的原子,原子核中没有中子
10.下列有关微粒的说法错误的是
A.原子、分子、离子都是构成物质的微粒,构成物质的微粒都在不停的运动
B.钠原子失去一个电子形成钠离子,钠原子和钠离子的化学性质不同
C.过氧化氢是由氢原子和氧原子构成,它和水的组成元素相同,都是氧化物
D.原子中不一定含有中子,质子与中子的质量近似相等,电性不同,数目可能相同
11.在N2O5、NO2、N2O、X、NH3五种物质中,氮元素的化合价按一定顺序排列,则X是下列物质中的哪种物质
A.N2 B.NaNO3 C.NH4Cl D.NO
12.如下图是五种微粒的结构示意图,下列说法正确的是
A.①④属于金属元素 B.②的微粒符号是A13+
C.②③⑤属于阳离子 D.②和⑤所表示的粒子化学性质相似
二、非选择题,共5小题
13.碘酸钾(KIO3)中碘元素的化合价为______价.
14.化学用语是国际通用语言,是学习化学的重要工具。
(1)用化学用语填空
①2个氖气分子________;
②三个亚铁离子_______;
③4个硝酸根离子_______;
④地壳中含量第二的元素________;
⑤标出锰酸钾中锰元素的化合价_______。
(2)写出下列符号中数字“2”的含义
①SO2____________________;
②Ca2+________________;
③__________。
15.按要求写出相应的化学用语
(1)钠离子___________;
(2)4个氢氧根离子___________;
(3)2个氢原子___________;
(4)保持水化学性质的最小粒子___________;
(5)氩气___________。
16.观察下列原子结构示意图和元素周期表(部分),回答有关问题。
(1)图1中,具有相对稳定结构的原子是______(填元素符号)。
(2)图1中,属于金属元素的是______(填元素名称)。
(3)含有X元素的化合物常用作化肥,X元素的原子序数是______,相对原子质量为______。
(4)硅元素的氧化物是天然水晶的主要成分。在该氧化物中,硅元素的化合价为+4价,则其化学式为______。
17.化学符号是学习化学的工具,从现在起,我们就要开始与它密切接触,做到见到名称能立即写出符号,根据符号能准确地叫出名称。
(1)写出元素的符号或名称:
H_________,氧_________,C_________,铁_________,镁_________,铜_________,锰_________。
(2)写出下列物质的化学式:
水__________,二氧化碳__________,氧气__________,氨气__________,氮气__________。
(3)写出以下两个化学实验中观察到的主要现象和文字或符号表达式。
A碳酸氢铵受热分解现象:___________。
文字或符号表达式:___________。
B蜡烛在空气中燃烧现象:___________。
文字或符号表达式:___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
略
2.B
【详解】
A、二氧化氯分子由氯原子和氧原子构成,A正确。
B、二氧化氯分子中含有氧原子,不含氧分子,B错误。
C、由化学式可知,二氧化氯由氯元素和氧元素组成,C正确。
D、二氧化氯由二氧化氯分子构成,D正确。
故选:B。
3.A
【详解】
MgF2中镁元素化合价为+2价,设F元素的化合价为x,根据在化合物中正负化合价代数和为零,可得(+2)+2x=0,则x=-1;
故选A。
4.D
【详解】
SO3中氧元素的化合价为-2价,化合物中正负化合价代数和为零,则硫元素的化合价为+6。
故选:D。
5.A
【详解】
单质中元素的化合价为0。
化合物中各元素的化合价代数和为0。锌通常为+2价,氢通常为+1价,钠通常为+1价,氧通常为-2价。所以ZnS、H2S、Na2SO3、Na2SO4、SO2中硫元素的化合价分别为-2价,-2价,+4价,+6价,+4价。
硫元素的化合价有4种,故选A。
【点睛】
6.B
【详解】
A、1个一氧化碳分子是由1个碳原子和1个氧原子构成的,化学式为:CO,选项A不正确;
B、离子符号前的数字表示离子个数,2个碳酸根离子为:2,选项B正确;
C、1个亚铁离子带2个单位正电荷,符号为Fe2+,因此3个亚铁离子为:3Fe2+,选项C不正确;
D、元素符号表示这种元素的1个原子,因此4个氢原子为:4H,选项D不正确。
故选B。
7.D
【分析】
从示意图可知,乙烷的化学式为C2H6。
【详解】
A、乙烷是乙烷分子构成的,错误。
B、乙烷中氢元素的质量分数为,错误。
C、乙烷分子中碳、氢元素的质量比是24:6=4:1,错误。
D、每个乙烷分子中含有2个碳原子,6个氢原子,共8个原子。正确。
故选D。
【点睛】
8.A
【分析】
化合物中各元素质量比=各原子的相对原子质量与原子个数乘积之比
【详解】
设M的相对原子质量为x,由题意,M与O的质量比为9:8,O的相对原子质量为16,则(2×x):(16×3)=9:8,解得x=27。
故选:A。
9.B
【详解】
A、图①质子数=核外电子数=10,是氖原子的结构示意图。氖气是稀有气体由原子直接构成,化学式为Ne。正确。
B、图②④质子数分别为11和17,质子数=原子序数,分别为钠元素和氯元素,钠元素属于金属元素,氯元素属于非金属元素,错误。
C、图③质子数=16,电子数=18,是硫原子得到2个电子形成的硫离子,符号为S2-。正确。
D、图⑤对应的是氢元素的原子,氢原子原子核内没有中子,正确。
故选B。
10.C
【详解】
A、原子、分子、离子都是构成物质的微粒,构成物质的微粒都在不停的运动,说法正确,不符合题意;
B、钠原子失去一个电子形成钠离子,钠原子和钠离子的化学性质不同,因为它们的最外层电子数不同,说法正确,不符合题意;
C、过氧化氢是由氢原子和氧原子构成,说法错误,应该是过氧化氢由过氧化氢分子构成,故符合题意;
D、原子中不一定含有中子,质子与中子的质量近似相等,电性不同,数目可能相同,说法正确。不符合题意;
故选C。
11.A
【分析】
氧元素的化合价通常为-2,氢元素化合价通常为+1,根据化合物中各元素正负化合价代数和为0,N2O5、NO2、N2O、NH3中氮元素的化合价分别为+5,+4,+1,-3。所以X中氮元素的化合价为0或-1,或-2。
【详解】
A、N2中氮元素的化合价为0,符合分析要求。
B、NaNO3中氮元素的化合价为+5,不符合分析要求。
C、NH4Cl中氮元素的化合价为-3,不符合分析要求。
D、NO中氮元素的化合价为+2,不符合分析要求。
故选A。
【点睛】
12.B
【分析】
【详解】
A、①④的核内质子数分别是9、13,分别是氟元素和铝元素,分别属于非金属元素、金属元素,故选项说法错误。
B、②质子数=13,核外电子数=10,质子数>核外电子数,为带3个单位正电荷的铝离子,符号是Al3+,故选项说法正确。
C、②③,质子数>核外电子数,为阳离子;⑤质子数=核外电子数=10,为原子,故选项说法错误。
D、②是原子失去3个电子得到的,②和⑤所表示的粒子分别是铝离子和氖原子,它们的化学性质不相似,故选项说法错误。
故选B。
【点睛】
明确粒子中核内质子数和核外电子数之间的关系是正确解题的关键。
13.+5
【详解】
根据在化合物中正负化合价代数和为零,钾元素的化合价为+1价,氧元素的化合价为﹣2价,设碘酸钾(KIO3)中碘元素的化合价为x,则(+1)+x+(﹣2)×3=0,解得x=+5;
故答案为:+5.
14.
(1) 2Ne 3Fe2+ Si
(2) 一个二氧化硫分子中含有两个氧原子 一个钙离子带两个单位的正电荷 氧化汞中氧元素显-2价
【分析】
(1)
①分子的表示方法是正确书写物质的化学式,表示多个该分子,在其化学式前加上相应的数字。2个氖气分子表示为:2Ne;
②离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字。三个亚铁离子表示为:3Fe2+;
③离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字。4个硝酸根离子表示为:;
④地壳中含量第二的元素是硅元素,其元素符号表示为:Si;
⑤在锰酸钾中,钾元素显+1价,氧元素显-2价,根据化合物各元素的化合价为零,可知锰元素的化合价为+6价。元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后。锰酸钾中锰元素的化合价表示为:。
(2)
①化学式中元素符号右下角数字表示一个分子中含原子的数目。SO2中数字“2”表示为:一个二氧化硫分子中含有两个氧原子;
②离子符号右上角的数字表示该离子所带电荷的数目。Ca2+中数字“2”表示为:一个钙离子带两个单位的正电荷;
③化学式中元素符号正上方的数字表示元素的化合价。中数字“2”表示为:氧化汞中氧元素显-2价。
15.
(1)Na+
(2)4OH-
(3)2H
(4)H2O
(5)Ar
【分析】
(1)
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。钠离子表示为:Na+;
(2)
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字。4个氢氧根离子表示为:4OH-;
(3)
原子的表示方法是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应的数字。2个氢原子表示为:2H;
(4)
水是由水分子构成,保持水化学性质的最小粒子是水分子,表示为:H2O;
(5)
氩气是稀有气体,化学式直接用元素符号表示,表示为:Ar。
16.
(1)Ne
(2)钠,铝
(3) 15 30.97
(4)SiO2
【分析】
(1)
Ne的最外层电子数是8,是具有相对稳定结构的原子;
(2)
由原子结构示意图可知,图1中,属于金属元素的是钠、铝;
(3)
由元素周期比表中一个格的含义可知,含有X元素的化合物常用作化肥,X元素是磷元素,原子序数是15,相对原子质量为30.97。
(4)
硅元素的化合价为+4价,氧元素的化合价为-2价。根据化合物中各元素的化合价代数和为零,该氧化物的化学式为SiO2。
【点睛】
17.
(1) 氢 O 碳 Fe Mg Cu Mn
(2) H2O CO2 O2 NH3 N2
(3) 固体消失,有刺激性气味的气体产生(或试管管壁上有水珠出现) ( ) 产生黄色火焰,发光发热 蜡烛+氧气二氧化碳+水(或蜡烛+O2CO2+H2O)
【解析】
(1)
H是氢元素,氧符号是O,C是碳元素,铁符号是Fe,镁符号是Mg,铜符号是Cu,锰符号是Mn;
(2)
水的化学式是H2O,二氧化碳:CO2,氧气:O2,氨气:NH3,氮气:N2;
(3)
A碳酸氢铵受热时,固体逐渐消失,有刺激性气味气体产生,管口还有小水珠;文字表达式为:碳酸氢铵氨气+水+二氧化碳,符号表达式为:NH4HCO3NH3+CO2+H2O ;
B蜡烛在空气中燃烧,发出黄色火焰,并发光发热,文字表达式为:蜡烛+氧气 二氧化碳+水,符号表达式为:蜡烛+O2 CO2+H2O);答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
