第三单元物质构成的奥秘单元测试-2020-2021学年人教版化学九年级(含解析)
文档属性
| 名称 | 第三单元物质构成的奥秘单元测试-2020-2021学年人教版化学九年级(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 130.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-10 00:00:00 | ||
图片预览




文档简介
第三单元物质构成的奥秘22020-2021学年人教版化学九年级
姓名:___________班级:___________
一、单选题
1.用“分子的观点”解释下列现象,不正确的是
A.湿衣晾干——分子不停地运动
B.水结成冰——分子发生变化
C.干冰升华——分子间间隔变大
D.轮胎充气——分子间有间隔
2.若氧原子用表示,氢原子用表示,则下列可保持水的化学性质的微粒是
A. B. C.
D.
3.一定条件下,水在密闭容器里的冷却过程中,温度和时间的关系如图所示。①、②、③表示水在不同时刻的存在状态,下列有关判断正确的是
A.水分子间的间隔:③>②
B.水分子的运动速率:②>①
C.状态③的水分子静止不动
D.①→②发生了化学变化
4.如图是X、Y两种元素的原子结构示意图。据图分析,下列判断错误的是
A.X原子的核外电子数为12 B.Y元素的原子在化学反应中易得电子
C.X和Y形成化合物的1为XY2 D.X、Y两种元素的化学性质相似
5.下列物质中,由分子直接构成的是
A.氯化钠 B.金刚石 C.甲烷 D.硫酸铜
6.下列现象能说明分子间存在间隔的是
A.分离液态空气制氧气
B.桂花开放时满园飘香
C.25m3氧气压缩后可装入0.024m3的钢瓶中
D.品红在热水中扩散比冷水中要快
7.已知碳-12 原子的质量是 a kg,如果另一种原子的质量为 b kg,则该原子的相对原子质量为
A.ab/12 B.12a/b C.12b/a D.b/12a
8.如图是某些物质的微观示意图,其中能够表示纯净物的是
A. B. C. D.
9.近来有研究报告称,除去“普通水”里含有的氮气和氧气后,水的去污能力将大大增强。对此的下列理不解不正确的是
A.“普通水”含有氮分子 B.除去氧气后的水就是纯净物了
C.“普通水”含有氧分子 D.氮气和氧气在水中有一定的溶解性
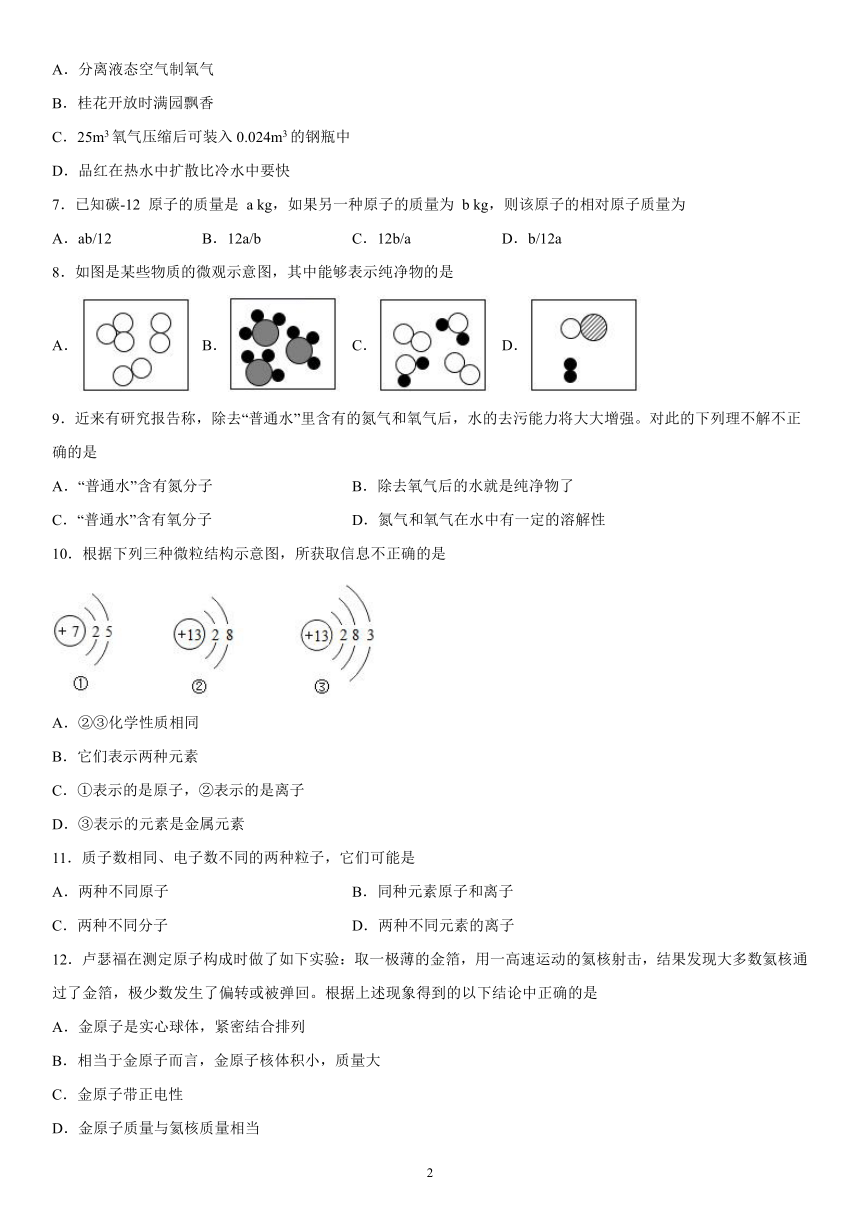
10.根据下列三种微粒结构示意图,所获取信息不正确的是
A.②③化学性质相同
B.它们表示两种元素
C.①表示的是原子,②表示的是离子
D.③表示的元素是金属元素
11.质子数相同、电子数不同的两种粒子,它们可能是
A.两种不同原子 B.同种元素原子和离子
C.两种不同分子 D.两种不同元素的离子
12.卢瑟福在测定原子构成时做了如下实验:取一极薄的金箔,用一高速运动的氦核射击,结果发现大多数氦核通过了金箔,极少数发生了偏转或被弹回。根据上述现象得到的以下结论中正确的是
A.金原子是实心球体,紧密结合排列
B.相当于金原子而言,金原子核体积小,质量大
C.金原子带正电性
D.金原子质量与氦核质量相当
13.用分子的观点解释下列现象,不合理的是
A.液化石油气加压后能贮存在钢瓶中,说明加压后分子变小了
B.湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关
C.氧气具有助燃性,而二氧化碳不可燃,不助燃。说明分子是保持物质化学性质的最小微粒
D.水通电分解后变成了氢气和氧气。说明在化学变化中分子可再分
14.日本福岛第一核电站发生严重的核泄漏,日本政府向福岛核电站附近居民发放碘片(I-127),以降低放射性碘对人体的伤害。已知核辐射中放射性碘(I-131)的核电荷数为53,则下列说法不正确的是
A.核裂变是一种化学变化 B.I-127原子和I-131原子的相对原子质量不相同
C.核能的利用证实原子的可分性 D.I-127原子与I-131原子属于同种元素
二、填空题
15.用化学用语填空:
(1)2个氢原子______;
(2)构成硫酸铜的阴离子______;
16.请用微观粒子的相关知识解释如下现象。
(1)走到天颐路正道小磨香油厂附近闻到油香___________。
(2)用水银温度计测量体温,发现水银柱升高___________。
17.元素锶形成的粒子结构示意图如图1所示,锶的元素符号为Sr。
(1)锶元素位于元素周期表中的第______周期。锶离子的化学符号是______。
(2)图2表示的微粒中,具有相对稳定结构的原子是______(填字母序号,下同),与锶元素化学性质相似的是______。
18.根据下面五种微粒的结构示意图,回答下列问题:
(1)图中微粒共能表示________种元素。
(2)表示原子结构示意图的有(填序号)____________。
(3)图中表示的阴离子是(用离子符号表示)___________。
19.某同学为了研究影响分子运动速率的因素,利用浓氨水挥发出来的氨气和浓盐酸挥发出来的氯化氢气体发生反应生成白色氯化固体的原理,设计了如图所示的实验。实验开始时,两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,一段时间后,先在A处产生大量白烟,然后白烟逐渐充满整个玻璃管。
回答下列问题:
(1)先在A处产生大量白烟的原因是______。
(2)此实验说明影响分子运动速率的因素是______。
三、简答题
20.核电荷数为1﹣18的原子结构示意图等信息如下,请回答下列问题:
第一周期 1H 2He
第二周期 3Li 4Be 5B 6C 7N 8O 9F 10Ne
第三周期 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar
(1)不同种元素最本质的区别是_____(选填序号)
A质子数不同 B最外层电子数不同 C中子数不同 D相对原子质量不同
(2)在第三周期中,各原子结构的共同之处是_____;该周期中,各原子核外电子排布的变化规律是_____.
(3)在第三周期中,元素类型的变化情况是:从左到右由_____元素过渡到_____元素,并以稀有气体元素结尾.
(4)写出核外电子排布与氖原子相同的阳离子和阴离子各一个:阳离子_____,阴离子_____.
21.用事实来证明分子的特性:例如1个水分子的质量约为3×10-26kg,一滴水中大约有1.67×1021个水分子,说明分子的质量和体积小。请再举二例说明分子的另外两个特性:
(1)分子是不停运动的:______;
(2)分子间有间隔:______。
22.50毫升的水与50毫升的酒精混合后为什么体积小于100毫升?
23.用微粒的观点解释下列事实.
(1)碘固体(I2)和碘蒸气都能使淀粉变蓝___________________.
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体___________________.
24.用微粒的观点解释下列实验事实。把充满氧气的集气瓶口的玻璃片错开,将盛有燃着的硫(由S分子构成)的燃烧匙伸入瓶内,硫燃烧发出蓝紫色火焰,瓶外很快闻到刺激性气味,待火焰熄灭后,取出燃烧匙,迅速用玻璃片将集气瓶口盖严。_____________
(
2
)
(
1
)
参考答案
1.B
【详解】
A、湿衣晾干证明水分子不停的运动,正确;
B、水结成冰,没有新物质生成只是物态发生变化,分子种类不变,错误;
C、干冰是固态二氧化碳,升华后由固态变为气态,分子间隔变大,正确;
D、轮胎充气是分子间距离发生变化而引起的现象,说明分子间有间隔,正确。
故选B。
2.B
【详解】
水是由水分子构成的,所以水的化学性质是由水分子保持的,每个水分子由两个氢原子和一个氧原子构成,对应的1图示为B,故选B。
3.A
【分析】
一切物质的分子都在不停地运动,且是无规则的运动。分子的热运动跟物体的温度有关,物体的温度越高,其分子的运动越快。
【详解】
A、由图可知,水在②处为液态水,水在③处为固态水即冰,水变成冰时,体积变大,分子间隔变大,则水分子间的间隔:③>②,正确;
B、水在①处的温度高于②处,物体的温度越高,其分子的运动越快,则水分子的运动速率:①>②,错误;
C、构成物质的分子在永不停息的做无规则运动,状态③的水分子在运动,错误;
D、①→②只是物质状态的变化,没有新物质生成,发生物理变化,错误。
故选A。
【点睛】
化学变化是物质在变化过程中有新物质生成。
4.D
【详解】
A、X原子的核外电子数为12,故选项说法正确。
B、Y的最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,故选项说法正确。
C、X和Y分别是镁元素和氯元素,镁原子的最外层电子数为2,镁原子在化学反应中易失去2个电子而形成带2个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+2价;氯原子的最外层电子数为7,在化学反应中易得到1个电子而形成1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为-1价;镁元素显+2价,氯元素显-1价,镁和氯组成化合物的1为,即X和Y形成化合物的1为XY2,故选项说法正确。
D、元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是最外层电子数,X、Y两种元素原子的最外层电子数不同,化学性质不相似,故选项说法错误。
故选:D。
5.C
【详解】
A、氯化钠由钠离子和氯离子构成。
B、金刚石由碳原子构成。
C、甲烷由甲烷分子构成。
D、硫酸铜由铜离子和硫酸根离子构成。
故选C。
6.C
【详解】
A、分离液态空气制氧气,是利用了液态氮和液态氧沸点的不同,不能说明分子间存在间隔,故不符合题意;
B、桂花开放时满园飘香,是因为桂花花香中含有的分子是在不断地运动的,向四周扩散,使人们闻到桂花花香,故不符合题意;
C、25m3氧气压缩后可装入0.024m3的钢瓶中,是因为分子间有间隔,气体受压后,分子间隔变小,故符合题意;
D、品红在热水中比在冷水中扩散得快,是因为热水中温度高,温度越高,分子运动越快,故不符合题意;
故选:C。
7.C
【详解】
由相对原子质量的计算公式可知,该原子的相对原子质量==,故选C。
8.B
【详解】
A、图A属于两种单质组成的混合物,故选项错误;
B、图B属于纯净物中的化合物,故选项正确;
C、图C属于一种单质和一种化合物组成的混合物,故选项错误;
D、图D属于一种单质和一种化合物组成的混合物,故选项错误。
故选:B。
9.B
【详解】
A、通过题干可知“普通水”中含有氮气,氮气由氮分子构成,所以“普通水”含有氮分子,正确。
B、除去氧气后的水还含有氮气、可溶性盐等多种物质,仍为混合物。错误。
C、通过题干可知“普通水”中含有氧气,氧气由氧分子构成,所以“普通水”含有氧分子,正确。
D、从题干可知“普通水”里含有的氮气和氧气,说明氮气和氧气在水中有一定的溶解性,能溶解在水中。正确。
故选B。
10.A
【详解】
A、微粒的最外层电子数相同,化学性质相似。②③最外层电子数不同,化学性质不同。错误。
B、元素是具有相同质子数的一类原子的总称。②③质子数相同是同种元素,图中一共表示两种元素。正确。
C、①质子数(7)=电子数(2+5)是原子,②质子数(13)>电子数(2+8)是阳离子,正确。
D、③有13个质子,是13号元素铝元素的微粒,铝元素是金属元素,正确。
故选A。
11.B
【分析】
元素是具有相同核电荷数(质子数)的一类原子的总称。
【详解】
A、质子数相同的原子属于同种原子,A错误;
B、同种元素的质子数肯定相同,又因一种是原子,一种是离子,电子数肯定不同,B正确;
C、质子数相同的两种分子,因没有得失电子,故电子数也应相同,C错误;
D、元素不同,则质子数不同,D错误;
故选B。
12.B
【详解】
A、大多数氦核通过了金箔,则不是实心球体,故A错误;
B、大多数氦核通过了金箔,极少数发生了偏转或被弹回,则相当于金原子而言,金原子核体积小,故B正确;
C、原子不带电,故C错误;
D、极少数发生了偏转或被弹回,则金原子质量比氦核质量大的多,故D错误;
故选B。
13.A
【详解】
A、液化石油气加压后能贮存在钢瓶中,说明加压后分子间隔变小了,A错误。
B、湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关,B正确。
C、氧气具有助燃性,而二氧化碳不可燃,不助燃,说明分子是保持物质化学性质的最小微粒,不同分子化学性质不同,C正确。
D、水通电分解后变成了氢气和氧气。说明在化学变化中分子可再分,D正确。
故选:A。
14.A
【详解】
A、核裂变是原子核发生裂变,原子发生了变化,属于核物理研究的范畴,而化学变化中原子核不发生变化,因此核裂变不是化学变化,符合题意;
B、因为“相对原子质量≈质子数+中子数”,虽然I-127原子和I-131原子质子数相同,但中子数不同,所以相对原子质量不相同,正确,不符合题意;
C、核能的利用证实了原子是可分的,正确,不符合题意;
D、I-127原子和I-131原子属于同种元素,因为它们是质子数相同的原子,所以属于同种元素,正确,不符合题意。
故选:A。
15.
(1)2H
(2)
【分析】
(1)
氢原子的化学符号为:H,两个氢原子即为:2H
(2)
硫酸铜中的阴离子为硫酸根离子,硫酸根离子的化学符号为
【点睛】
16.分子是不断运动的 温度升高,汞原子间隔变大
【详解】
(1)走到天颐路正道小磨香油厂附近闻到油香,是因为小磨香油中含有的分子是在不断运动的,向四周扩散,使人们闻到酒香,故填:分子是不断运动的。
(2)水银是金属汞的俗称,用水银温度计测量体温水银柱升高,是因为汞原子间的间隔随温度的升高而增大,故填:温度升高,汞原子间隔变大。
17.
(1) 五
(2) AC B
【分析】
(1)
锶元素的质子数是38可知,锶原子的核外有5个电子层,锶元素位于元素周期表中的第五周期;锶离子带两个单位的正电荷,化学符号是。
(2)
由粒子结构示意图可知,A的质子数等于电子数,最外层也是第一层,有2个电子,属于稳定结构的原子,在C中质子数等于电子数,最外层电子数是8,属于稳定结构的原子;由图1可知,锶原子最外层电子数为2,B的最外层电子数是2,与锶原子的最外层电子数相同,化学性质相似;A的最外层也是第一层,有2个电子,但其属于稳定结构,与锶原子的化学性质不相似。
18.
(1)3
(2)A、B、E
(3)O2-
【分析】
(1)
由五种微粒的结构示意图可知,微粒共由三种质子数,能表示3种元素,分别是氢、氧、钠三种元素,故填:3;
(2)
由五种微粒的结构示意图可知,在A、B、E微粒中,核内质子数=核外电子数,A、B、E表示原子结构示意图,故填:A、B、E;
(3)
当核内质子数小于核外电子数时,为阴离子,C微粒中,核内质子数为8,核外电子数为10,核内质子数<核外电子数,为带两个单位负电荷的氧离子,故填:O2-。
【点睛】
19.
(1)氨分子的运动速率比氯化氢分子快
(2)相对分子质量
【详解】
略
20.A 核外电子层数都是3 从左至右原子核外最外层电子数依次增加等 金属 非金属 Na+(或Mg2+或Al3+) O2﹣(或F﹣)
【详解】
(1)根据决定元素种类的是核内质子数,不同种元素最本质的区别是核内质子数不同;
(2)在第三周期中,各原子结构的共同之处是核外电子层数都是3;从左至右原子核外最外层电子数依次增加等;
(3)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结尾;
(4)氖原子核外有2个电子层,第一层上有2个电子,第二层上有8个电子,钠离子、镁离子、铝离子属于阳离子,氧离子、氟离子属于阴离子,核外电子排布均与氖原子相同;离子符号分别是Na+(或Mg2+或Al3+)、O2﹣(或F﹣)。
21.湿衣服能变干 50mL酒精与50mL水混合后,体积小100mL
【解析】
【详解】
(1)湿衣服上的水分子是在不断运动的,向四周扩散,所以湿衣服能变干,说明分子在不断运动;
(2)50mL酒精与50mL水混合后,体积小100mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔。
故答案为:(1)湿衣服能变干;(2)50mL酒精与50mL水混合后,体积小100m。
【点睛】
根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;结合事实进行分析判断即可。
22.分子之间有间隔
【详解】
分子之间有间隔,水分子和酒精分子,间隔大小不同,彼此进入对方间隙,混合后体积小于100毫升。
23.碘固体是由碘分子构成的,碘蒸气也是由碘分子构成的,同种物质的分子性质相同; 由于碘固体和碘蒸气的质量相等,说明二者含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体分子之间的间隔,所以碘蒸气的体积远大于碘固体。
【详解】
(1)分子是保持物质化学性质的最小粒子,保持碘的化学性质的最小粒子是碘分子.碘固体是由碘分子构成的,碘蒸气也是由碘分子构成的,同种物质的分子性质相同,所以碘固体(I2)和碘蒸气都能使淀粉变蓝。
(2)由于碘固体和碘蒸气的质量相等,说明二者含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体分子之间的间隔,所以碘蒸气的体积远大于碘固体。
24.分子在做无规则的运动,硫与氧气反应生成二氧化硫气体有刺激性气味,二氧化硫分子做无规则的运动,故可以闻到刺激性气味
【详解】
分子在做无规则的运动,硫与氧气反应生成二氧化硫气体有刺激性气味,二氧化硫分子做无规则的运动,故可以闻到刺激性气味。
(
2
)
(
1
)
姓名:___________班级:___________
一、单选题
1.用“分子的观点”解释下列现象,不正确的是
A.湿衣晾干——分子不停地运动
B.水结成冰——分子发生变化
C.干冰升华——分子间间隔变大
D.轮胎充气——分子间有间隔
2.若氧原子用表示,氢原子用表示,则下列可保持水的化学性质的微粒是
A. B. C.
D.
3.一定条件下,水在密闭容器里的冷却过程中,温度和时间的关系如图所示。①、②、③表示水在不同时刻的存在状态,下列有关判断正确的是
A.水分子间的间隔:③>②
B.水分子的运动速率:②>①
C.状态③的水分子静止不动
D.①→②发生了化学变化
4.如图是X、Y两种元素的原子结构示意图。据图分析,下列判断错误的是
A.X原子的核外电子数为12 B.Y元素的原子在化学反应中易得电子
C.X和Y形成化合物的1为XY2 D.X、Y两种元素的化学性质相似
5.下列物质中,由分子直接构成的是
A.氯化钠 B.金刚石 C.甲烷 D.硫酸铜
6.下列现象能说明分子间存在间隔的是
A.分离液态空气制氧气
B.桂花开放时满园飘香
C.25m3氧气压缩后可装入0.024m3的钢瓶中
D.品红在热水中扩散比冷水中要快
7.已知碳-12 原子的质量是 a kg,如果另一种原子的质量为 b kg,则该原子的相对原子质量为
A.ab/12 B.12a/b C.12b/a D.b/12a
8.如图是某些物质的微观示意图,其中能够表示纯净物的是
A. B. C. D.
9.近来有研究报告称,除去“普通水”里含有的氮气和氧气后,水的去污能力将大大增强。对此的下列理不解不正确的是
A.“普通水”含有氮分子 B.除去氧气后的水就是纯净物了
C.“普通水”含有氧分子 D.氮气和氧气在水中有一定的溶解性
10.根据下列三种微粒结构示意图,所获取信息不正确的是
A.②③化学性质相同
B.它们表示两种元素
C.①表示的是原子,②表示的是离子
D.③表示的元素是金属元素
11.质子数相同、电子数不同的两种粒子,它们可能是
A.两种不同原子 B.同种元素原子和离子
C.两种不同分子 D.两种不同元素的离子
12.卢瑟福在测定原子构成时做了如下实验:取一极薄的金箔,用一高速运动的氦核射击,结果发现大多数氦核通过了金箔,极少数发生了偏转或被弹回。根据上述现象得到的以下结论中正确的是
A.金原子是实心球体,紧密结合排列
B.相当于金原子而言,金原子核体积小,质量大
C.金原子带正电性
D.金原子质量与氦核质量相当
13.用分子的观点解释下列现象,不合理的是
A.液化石油气加压后能贮存在钢瓶中,说明加压后分子变小了
B.湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关
C.氧气具有助燃性,而二氧化碳不可燃,不助燃。说明分子是保持物质化学性质的最小微粒
D.水通电分解后变成了氢气和氧气。说明在化学变化中分子可再分
14.日本福岛第一核电站发生严重的核泄漏,日本政府向福岛核电站附近居民发放碘片(I-127),以降低放射性碘对人体的伤害。已知核辐射中放射性碘(I-131)的核电荷数为53,则下列说法不正确的是
A.核裂变是一种化学变化 B.I-127原子和I-131原子的相对原子质量不相同
C.核能的利用证实原子的可分性 D.I-127原子与I-131原子属于同种元素
二、填空题
15.用化学用语填空:
(1)2个氢原子______;
(2)构成硫酸铜的阴离子______;
16.请用微观粒子的相关知识解释如下现象。
(1)走到天颐路正道小磨香油厂附近闻到油香___________。
(2)用水银温度计测量体温,发现水银柱升高___________。
17.元素锶形成的粒子结构示意图如图1所示,锶的元素符号为Sr。
(1)锶元素位于元素周期表中的第______周期。锶离子的化学符号是______。
(2)图2表示的微粒中,具有相对稳定结构的原子是______(填字母序号,下同),与锶元素化学性质相似的是______。
18.根据下面五种微粒的结构示意图,回答下列问题:
(1)图中微粒共能表示________种元素。
(2)表示原子结构示意图的有(填序号)____________。
(3)图中表示的阴离子是(用离子符号表示)___________。
19.某同学为了研究影响分子运动速率的因素,利用浓氨水挥发出来的氨气和浓盐酸挥发出来的氯化氢气体发生反应生成白色氯化固体的原理,设计了如图所示的实验。实验开始时,两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,一段时间后,先在A处产生大量白烟,然后白烟逐渐充满整个玻璃管。
回答下列问题:
(1)先在A处产生大量白烟的原因是______。
(2)此实验说明影响分子运动速率的因素是______。
三、简答题
20.核电荷数为1﹣18的原子结构示意图等信息如下,请回答下列问题:
第一周期 1H 2He
第二周期 3Li 4Be 5B 6C 7N 8O 9F 10Ne
第三周期 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar
(1)不同种元素最本质的区别是_____(选填序号)
A质子数不同 B最外层电子数不同 C中子数不同 D相对原子质量不同
(2)在第三周期中,各原子结构的共同之处是_____;该周期中,各原子核外电子排布的变化规律是_____.
(3)在第三周期中,元素类型的变化情况是:从左到右由_____元素过渡到_____元素,并以稀有气体元素结尾.
(4)写出核外电子排布与氖原子相同的阳离子和阴离子各一个:阳离子_____,阴离子_____.
21.用事实来证明分子的特性:例如1个水分子的质量约为3×10-26kg,一滴水中大约有1.67×1021个水分子,说明分子的质量和体积小。请再举二例说明分子的另外两个特性:
(1)分子是不停运动的:______;
(2)分子间有间隔:______。
22.50毫升的水与50毫升的酒精混合后为什么体积小于100毫升?
23.用微粒的观点解释下列事实.
(1)碘固体(I2)和碘蒸气都能使淀粉变蓝___________________.
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体___________________.
24.用微粒的观点解释下列实验事实。把充满氧气的集气瓶口的玻璃片错开,将盛有燃着的硫(由S分子构成)的燃烧匙伸入瓶内,硫燃烧发出蓝紫色火焰,瓶外很快闻到刺激性气味,待火焰熄灭后,取出燃烧匙,迅速用玻璃片将集气瓶口盖严。_____________
(
2
)
(
1
)
参考答案
1.B
【详解】
A、湿衣晾干证明水分子不停的运动,正确;
B、水结成冰,没有新物质生成只是物态发生变化,分子种类不变,错误;
C、干冰是固态二氧化碳,升华后由固态变为气态,分子间隔变大,正确;
D、轮胎充气是分子间距离发生变化而引起的现象,说明分子间有间隔,正确。
故选B。
2.B
【详解】
水是由水分子构成的,所以水的化学性质是由水分子保持的,每个水分子由两个氢原子和一个氧原子构成,对应的1图示为B,故选B。
3.A
【分析】
一切物质的分子都在不停地运动,且是无规则的运动。分子的热运动跟物体的温度有关,物体的温度越高,其分子的运动越快。
【详解】
A、由图可知,水在②处为液态水,水在③处为固态水即冰,水变成冰时,体积变大,分子间隔变大,则水分子间的间隔:③>②,正确;
B、水在①处的温度高于②处,物体的温度越高,其分子的运动越快,则水分子的运动速率:①>②,错误;
C、构成物质的分子在永不停息的做无规则运动,状态③的水分子在运动,错误;
D、①→②只是物质状态的变化,没有新物质生成,发生物理变化,错误。
故选A。
【点睛】
化学变化是物质在变化过程中有新物质生成。
4.D
【详解】
A、X原子的核外电子数为12,故选项说法正确。
B、Y的最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,故选项说法正确。
C、X和Y分别是镁元素和氯元素,镁原子的最外层电子数为2,镁原子在化学反应中易失去2个电子而形成带2个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+2价;氯原子的最外层电子数为7,在化学反应中易得到1个电子而形成1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为-1价;镁元素显+2价,氯元素显-1价,镁和氯组成化合物的1为,即X和Y形成化合物的1为XY2,故选项说法正确。
D、元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是最外层电子数,X、Y两种元素原子的最外层电子数不同,化学性质不相似,故选项说法错误。
故选:D。
5.C
【详解】
A、氯化钠由钠离子和氯离子构成。
B、金刚石由碳原子构成。
C、甲烷由甲烷分子构成。
D、硫酸铜由铜离子和硫酸根离子构成。
故选C。
6.C
【详解】
A、分离液态空气制氧气,是利用了液态氮和液态氧沸点的不同,不能说明分子间存在间隔,故不符合题意;
B、桂花开放时满园飘香,是因为桂花花香中含有的分子是在不断地运动的,向四周扩散,使人们闻到桂花花香,故不符合题意;
C、25m3氧气压缩后可装入0.024m3的钢瓶中,是因为分子间有间隔,气体受压后,分子间隔变小,故符合题意;
D、品红在热水中比在冷水中扩散得快,是因为热水中温度高,温度越高,分子运动越快,故不符合题意;
故选:C。
7.C
【详解】
由相对原子质量的计算公式可知,该原子的相对原子质量==,故选C。
8.B
【详解】
A、图A属于两种单质组成的混合物,故选项错误;
B、图B属于纯净物中的化合物,故选项正确;
C、图C属于一种单质和一种化合物组成的混合物,故选项错误;
D、图D属于一种单质和一种化合物组成的混合物,故选项错误。
故选:B。
9.B
【详解】
A、通过题干可知“普通水”中含有氮气,氮气由氮分子构成,所以“普通水”含有氮分子,正确。
B、除去氧气后的水还含有氮气、可溶性盐等多种物质,仍为混合物。错误。
C、通过题干可知“普通水”中含有氧气,氧气由氧分子构成,所以“普通水”含有氧分子,正确。
D、从题干可知“普通水”里含有的氮气和氧气,说明氮气和氧气在水中有一定的溶解性,能溶解在水中。正确。
故选B。
10.A
【详解】
A、微粒的最外层电子数相同,化学性质相似。②③最外层电子数不同,化学性质不同。错误。
B、元素是具有相同质子数的一类原子的总称。②③质子数相同是同种元素,图中一共表示两种元素。正确。
C、①质子数(7)=电子数(2+5)是原子,②质子数(13)>电子数(2+8)是阳离子,正确。
D、③有13个质子,是13号元素铝元素的微粒,铝元素是金属元素,正确。
故选A。
11.B
【分析】
元素是具有相同核电荷数(质子数)的一类原子的总称。
【详解】
A、质子数相同的原子属于同种原子,A错误;
B、同种元素的质子数肯定相同,又因一种是原子,一种是离子,电子数肯定不同,B正确;
C、质子数相同的两种分子,因没有得失电子,故电子数也应相同,C错误;
D、元素不同,则质子数不同,D错误;
故选B。
12.B
【详解】
A、大多数氦核通过了金箔,则不是实心球体,故A错误;
B、大多数氦核通过了金箔,极少数发生了偏转或被弹回,则相当于金原子而言,金原子核体积小,故B正确;
C、原子不带电,故C错误;
D、极少数发生了偏转或被弹回,则金原子质量比氦核质量大的多,故D错误;
故选B。
13.A
【详解】
A、液化石油气加压后能贮存在钢瓶中,说明加压后分子间隔变小了,A错误。
B、湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关,B正确。
C、氧气具有助燃性,而二氧化碳不可燃,不助燃,说明分子是保持物质化学性质的最小微粒,不同分子化学性质不同,C正确。
D、水通电分解后变成了氢气和氧气。说明在化学变化中分子可再分,D正确。
故选:A。
14.A
【详解】
A、核裂变是原子核发生裂变,原子发生了变化,属于核物理研究的范畴,而化学变化中原子核不发生变化,因此核裂变不是化学变化,符合题意;
B、因为“相对原子质量≈质子数+中子数”,虽然I-127原子和I-131原子质子数相同,但中子数不同,所以相对原子质量不相同,正确,不符合题意;
C、核能的利用证实了原子是可分的,正确,不符合题意;
D、I-127原子和I-131原子属于同种元素,因为它们是质子数相同的原子,所以属于同种元素,正确,不符合题意。
故选:A。
15.
(1)2H
(2)
【分析】
(1)
氢原子的化学符号为:H,两个氢原子即为:2H
(2)
硫酸铜中的阴离子为硫酸根离子,硫酸根离子的化学符号为
【点睛】
16.分子是不断运动的 温度升高,汞原子间隔变大
【详解】
(1)走到天颐路正道小磨香油厂附近闻到油香,是因为小磨香油中含有的分子是在不断运动的,向四周扩散,使人们闻到酒香,故填:分子是不断运动的。
(2)水银是金属汞的俗称,用水银温度计测量体温水银柱升高,是因为汞原子间的间隔随温度的升高而增大,故填:温度升高,汞原子间隔变大。
17.
(1) 五
(2) AC B
【分析】
(1)
锶元素的质子数是38可知,锶原子的核外有5个电子层,锶元素位于元素周期表中的第五周期;锶离子带两个单位的正电荷,化学符号是。
(2)
由粒子结构示意图可知,A的质子数等于电子数,最外层也是第一层,有2个电子,属于稳定结构的原子,在C中质子数等于电子数,最外层电子数是8,属于稳定结构的原子;由图1可知,锶原子最外层电子数为2,B的最外层电子数是2,与锶原子的最外层电子数相同,化学性质相似;A的最外层也是第一层,有2个电子,但其属于稳定结构,与锶原子的化学性质不相似。
18.
(1)3
(2)A、B、E
(3)O2-
【分析】
(1)
由五种微粒的结构示意图可知,微粒共由三种质子数,能表示3种元素,分别是氢、氧、钠三种元素,故填:3;
(2)
由五种微粒的结构示意图可知,在A、B、E微粒中,核内质子数=核外电子数,A、B、E表示原子结构示意图,故填:A、B、E;
(3)
当核内质子数小于核外电子数时,为阴离子,C微粒中,核内质子数为8,核外电子数为10,核内质子数<核外电子数,为带两个单位负电荷的氧离子,故填:O2-。
【点睛】
19.
(1)氨分子的运动速率比氯化氢分子快
(2)相对分子质量
【详解】
略
20.A 核外电子层数都是3 从左至右原子核外最外层电子数依次增加等 金属 非金属 Na+(或Mg2+或Al3+) O2﹣(或F﹣)
【详解】
(1)根据决定元素种类的是核内质子数,不同种元素最本质的区别是核内质子数不同;
(2)在第三周期中,各原子结构的共同之处是核外电子层数都是3;从左至右原子核外最外层电子数依次增加等;
(3)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结尾;
(4)氖原子核外有2个电子层,第一层上有2个电子,第二层上有8个电子,钠离子、镁离子、铝离子属于阳离子,氧离子、氟离子属于阴离子,核外电子排布均与氖原子相同;离子符号分别是Na+(或Mg2+或Al3+)、O2﹣(或F﹣)。
21.湿衣服能变干 50mL酒精与50mL水混合后,体积小100mL
【解析】
【详解】
(1)湿衣服上的水分子是在不断运动的,向四周扩散,所以湿衣服能变干,说明分子在不断运动;
(2)50mL酒精与50mL水混合后,体积小100mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔。
故答案为:(1)湿衣服能变干;(2)50mL酒精与50mL水混合后,体积小100m。
【点睛】
根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;结合事实进行分析判断即可。
22.分子之间有间隔
【详解】
分子之间有间隔,水分子和酒精分子,间隔大小不同,彼此进入对方间隙,混合后体积小于100毫升。
23.碘固体是由碘分子构成的,碘蒸气也是由碘分子构成的,同种物质的分子性质相同; 由于碘固体和碘蒸气的质量相等,说明二者含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体分子之间的间隔,所以碘蒸气的体积远大于碘固体。
【详解】
(1)分子是保持物质化学性质的最小粒子,保持碘的化学性质的最小粒子是碘分子.碘固体是由碘分子构成的,碘蒸气也是由碘分子构成的,同种物质的分子性质相同,所以碘固体(I2)和碘蒸气都能使淀粉变蓝。
(2)由于碘固体和碘蒸气的质量相等,说明二者含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体分子之间的间隔,所以碘蒸气的体积远大于碘固体。
24.分子在做无规则的运动,硫与氧气反应生成二氧化硫气体有刺激性气味,二氧化硫分子做无规则的运动,故可以闻到刺激性气味
【详解】
分子在做无规则的运动,硫与氧气反应生成二氧化硫气体有刺激性气味,二氧化硫分子做无规则的运动,故可以闻到刺激性气味。
(
2
)
(
1
)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
