2021-2022学年鲁教版(五四制)八年级化学 第三单元 第二节 元素 同步练习(word版 含解析)
文档属性
| 名称 | 2021-2022学年鲁教版(五四制)八年级化学 第三单元 第二节 元素 同步练习(word版 含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 91.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-11 00:00:00 | ||
图片预览



文档简介
元素
一、单选题
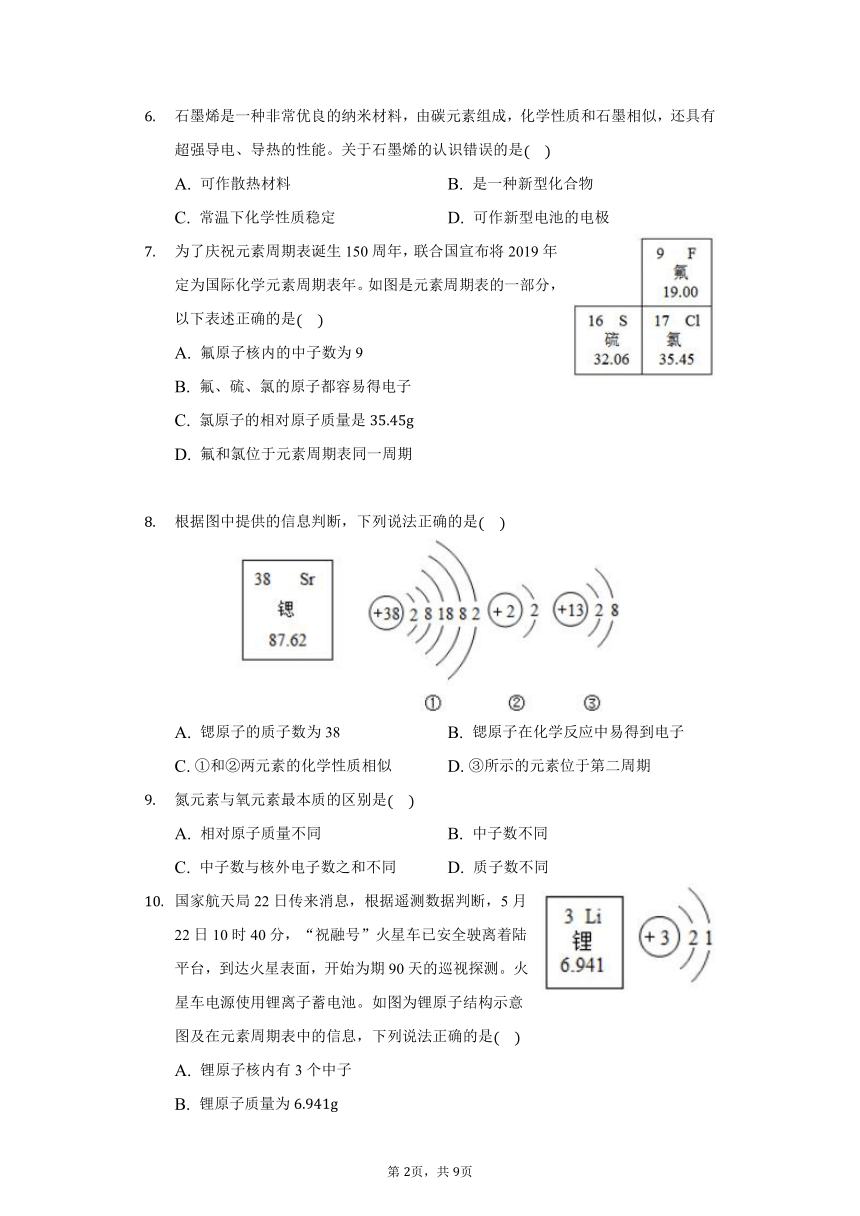
钽是一种坚硬蓝灰色的稀有过渡金属,抗腐蚀能力极强。关于该元素的说法不正确的是
A. 属于金属元素
B. 原子序数为73
C. 元素符号为Ta
D. 相对原子质量为
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品,这里的碘、铁、钙、硒、氟应理解为
A. 元素 B. 原子 C. 分子 D. 单质
“中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是
A. 属于金属元素 B. 元素符号为SI
C. 硅是地壳中含量最多的元素 D. 单质硅由原子构成
根据示意图提供的信息进行判断,下列说法中不正确的是
A. 表示阳离子
B. 易失去电子
C. 表示阴离子
D. 中氯原子的相对原子质量为
生产太阳能电池需要使用精制锗片。锗的化学性质与硅相似,如图是两者在元素周期表中的信息,下列说法正确的是
A. 锗属于非金属元素
B. 硅、锗原子的质子数相等
C. 锗原子最外层有4个电子
D. 锗的相对原子质量为
石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是
A. 可作散热材料 B. 是一种新型化合物
C. 常温下化学性质稳定 D. 可作新型电池的电极
为了庆祝元素周期表诞生150周年,联合国宣布将2019年定为国际化学元素周期表年。如图是元素周期表的一部分,以下表述正确的是
A. 氟原子核内的中子数为9
B. 氟、硫、氯的原子都容易得电子
C. 氯原子的相对原子质量是
D. 氟和氯位于元素周期表同一周期
根据图中提供的信息判断,下列说法正确的是
A. 锶原子的质子数为38 B. 锶原子在化学反应中易得到电子
C. 和两元素的化学性质相似 D. 所示的元素位于第二周期
氮元素与氧元素最本质的区别是
A. 相对原子质量不同 B. 中子数不同
C. 中子数与核外电子数之和不同 D. 质子数不同
国家航天局22日传来消息,根据遥测数据判断,5月22日10时40分,“祝融号”火星车已安全驶离着陆平台,到达火星表面,开始为期90天的巡视探测。火星车电源使用锂离子蓄电池。如图为锂原子结构示意图及在元素周期表中的信息,下列说法正确的是
A. 锂原子核内有3个中子
B. 锂原子质量为
C. 锂原子在化学反应中易失去电子
D. 蓄电池充电是把化学能转化为电能
二、填空题
元素周期表是学习化学的重要工具,下表为元素周期表中部分元素的相关信息,利用图示回答相关问题。
原子序数为14的元素符号为 ______,属于 ______填“金属”或“非金属”元素。
、N、O三种元素排在同一周期是因为 ______填“质子数”“电子层数”或“最外层电子数”相同。
和Mg的化学性质 ______填“相似”或“不相似”。
钠离子核外电子排布与 ______填元素符号原子核外电子排布相同。
一个磷原子含有 ______个质子,一个含有 ______个电子。
图中的和是氟元素和钙元素在元素周期表中的信息,A、B、C、D是4种粒子的结构示意图.请完成下列空白.
钙元素的相对原子质量为______,氟元素的原子序数为______;D中的x为______.
和是不同种元素,它们的最本质的区别是______不同.
、B、C、D结构示意图中,属于同种元素的粒子是______填字母.
粒子的化学性质与B、C、D中哪一种粒子的化学性质相似______填字母.
答案和解析
1.【答案】D
【解析】解:A、钽是“钅”旁,属于金属元素,故A正确不符合题意;
B、左上角是原子序数,钽的原子序数为73,故B正确不符合题意;
C、钽元素符号为Ta,故C正确不符合题意;
D、钽相对原子质量为,单位不是“g”,故D错误符合题意。
故选:D。
元素周期表中,每种元素占据的空格中,左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量。
本题难度不大,考查学生灵活运用元素周期表中元素的信息进行分析解题的能力。
2.【答案】A
【解析】解:物质是由元素组成的,故所有物质中含有的是元素,故选A
根据物质、元素、分子、原子、离子之间的关系进行解答:物质是由元素组成,由分子、原子、离子构成,
明确物质、元素、分子、原子、离子之间的关系是解答本类型关健.
3.【答案】D
【解析】解:A、硅是非金属元素;故说法错误;
B、硅元素符号为Si,故说法错误;
C、硅是地壳中含量排第二的元素,故说法错误;
D、单质硅是由硅原子构成的,故说法正确。
故选:D。
此题难度不大,掌握硅的有关知识即可顺利解答。
4.【答案】D
【解析】解:A、阳离子中:质子数核外电子数,中质子数为13,电子数为10,所以表示阳离子,正确;
B、一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,最外层电子数大于1,易失去电子,正确;
C、阴离子中:质子数核外电子数;质子数为17,电子数为18,表示阴离子,正确;
D、元素周期表中,每种元素占据的空格中,左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;中氯原子的相对原子质量为,单位不是”g“,错误。
故选:D。
根据结构示意图及元素周期表信息分析。
本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子中核内质子数和核外电子数之间的关系等进行分析解题的能力。
5.【答案】C
【解析】解:A、根据锗元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锗,带“钅”字旁,属于金属元素,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,硅、锗原子的原子序数分别为14、32;根据原子中原子序数核电荷数质子数核外电子数,则硅、锗原子的质子数不相等,故选项说法错误。
C、根据硅元素周期表中的一格可知,左上角的数字为14,表示原子序数为14;根据原子序数原子序数核电荷数质子数核外电子数,则该元素的原子核外电子数为14;核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有4个电子;硅、锗是同一族元素,它们的最外层电子数相同,则锗原子最外层有4个电子,故选项说法正确。
D、根据锗元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为,相对原子质量单位是“1”,不是“克”,故选项说法错误。
故选:C。
根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
本题难度不大,灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量是正确解答本题的关键。
6.【答案】B
【解析】解:石墨烯具有超强的导热性,所以可用来作散热材料,故正确;
B.石墨烯是一种由同种元素组成的纯净物,属于单质,故错误;
C.石墨烯是一种碳的单质,常温下化学性质稳定,故正确;
D.石墨烯具有超强的导电性,所以可作新型电池的电极,故正确。
故选:B。
A.根据石墨烯具有超强的导热性来分析;
B.根据物质的分类来分析;
C.根据物质的性质来分析;
D.根据物质的导电性来分析。
解答本题关键是要知道根据题干提供信息,去提取有用信息。
7.【答案】B
【解析】解:A、根据元素周期表中的一格可知,左上角的数字为9,表示原子序数为9;根据原子中原子序数核电荷数质子数核外电子数,则该元素的原子核内质子数与核外电子数为9而不是中子数为9,故选项说法错误。
B、氟、硫、氯的原子的原子最外层电子数均多于4,都容易得电子,故选项说法正确。
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,氯原子的相对原子质量是,相对原子质量单位是“1”,不是“克”,故选项说法错误。
D、同一横行叫一个周期,氟和氯不位于元素周期表同一周期,故选项说法错误。
故选:B。
根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
本题难度不大,考查学生灵活运用元素周期表中元素的信息、排列规律等进行分析解题的能力。
8.【答案】A
【解析】解:A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为38;根据原子中原子序数核电荷数质子数核外电子数,则锶原子的质子数为38,故选项说法正确。
B、锶原子的最外层电子数是2,在化学反应中易失去2个电子而形成阳离子,故选项说法错误。
C、中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;的最外层电子数为2,在化学反应中易失去2个电子而形成阳离子;尽管最外层电子数相同,但它们化学性质不相似,故选项说法错误。
D、是原子失去2个电子得到的,周期数原子核外电子层数,中元素的原子核外有3个电子层,则在元素周期表中,位于第三周期,故选项说法错误。
故选:A。
A、根据图中元素周期表可以获得的信息:左上角的数字表示原子序数,进行分析判断。
B、若最外层电子数,在化学反应中易得电子,若最外层电子数,在化学反应中易失去电子。
C、根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析判断。
D、根据周期数原子核外电子层数,进行分析判断。
本题难度不大,灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量、粒子结构示意图的含义是正确解答本题的关键。
9.【答案】D
【解析】解:元素是质子数即核电荷数相同的一类原子的总称,不同种元素最本质的区别是质子数即核电荷数不同,所以氧元素与氮元素的本质区别是质子数即核电荷数不同。
故选:D。
根据元素是质子数即核电荷数相同的一类原子的总称,决定元素种类的是质子数即核电荷数,据此进行分析解答。
本题难度不大,考查学生对元素的概念的理解和不同种元素之间的本质区别是质子数不同进行解题的能力。
10.【答案】C
【解析】解:A、锂原子核内中子数大约是个,故说法错误;
B、锂原子质量为,单位不是g,故说法错误;
C、锂原子的最外层电子数为1,在化学反应中易失去电子,故说法正确;
D、蓄电池充电是把电能转化为化学能,故说法错误;
故选:C。
根据元素表中一个单元格的意义进行分析解答即可。
加强对元素周期表中一个单元格的意义的掌握是正确解答本题的关键。
11.【答案】Si 非金属 电子层数 不相似 Ne 15 10
【解析】解:由元素周期表可知原子序数为14的元素符号为Si,硅属于非金属元素。
、N、O三种元素的原子电子层数相同,排在同一周期。
和Mg的最外层电子数相同,但是氦原子是稳定结构,镁原子最外层2个电子容易失去,不稳定,所以化学性质不相似。
钠原子失去最外层的1个电子形成钠离子,钠离子核外电子排布与氖原子核外电子排布相同。
原子中核电荷数核内质子数核外电子数,一个磷原子含有15个质子,一个含有的电子数为。
故答案为:
;非金属;
电子层数;
不相似;
;
;10。
根据元素周期表信息分析;
原子核外电子层数与周期数相同。
和Mg的最外层电子数相同,但是氦原子是稳定结构,镁原子最外层2个电子容易失去,不稳定。
钠原子失去最外层的1个电子形成钠离子,钠离子核外电子排布与氖原子核外电子排布相同。
根据原子中核电荷数核内质子数核外电子数分析。
本题难度不大,考查学生灵活运用元素周期表中元素的信息、了解粒子结构示意图的意义进行分析解题的能力。
12.【答案】 9 8
质子数
、C
【解析】
【分析】
本题难度不大,灵活运用元素周期表中元素的信息、明确粒子中核内质子数和核外电子数之间的关系、决定元素化学性质的因素等是正确解答本题的关键.
根据元素周期表的信息以及原子结构来分析;
根据元素的种类由质子数决定;
根据元素是具有相同核电荷数即核内质子数的一类原子的总称,决定元素种类的是核电荷数即核内质子数,据此进行分析解答;
根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,进行分析解答.
【解答】
根据氟元素、钙元素在元素周期表中的信息,可知钙元素的相对原子质量为,氟元素的原子序数为9;根据在原子中,原子序数质子数核电荷数核外电子数,可得,则;故填:;9;8;
元素的种类由质子数决定,故填:质子数;
根据元素的种类由质子数决定,因为B、C的质子数相同,所以B、C属于同种元素的粒子;故填:B、C;
根据元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似,A粒子的化学性质与B粒子化学性质相似.故填:B.
第2页,共2页
第1页,共1页
一、单选题
钽是一种坚硬蓝灰色的稀有过渡金属,抗腐蚀能力极强。关于该元素的说法不正确的是
A. 属于金属元素
B. 原子序数为73
C. 元素符号为Ta
D. 相对原子质量为
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品,这里的碘、铁、钙、硒、氟应理解为
A. 元素 B. 原子 C. 分子 D. 单质
“中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是
A. 属于金属元素 B. 元素符号为SI
C. 硅是地壳中含量最多的元素 D. 单质硅由原子构成
根据示意图提供的信息进行判断,下列说法中不正确的是
A. 表示阳离子
B. 易失去电子
C. 表示阴离子
D. 中氯原子的相对原子质量为
生产太阳能电池需要使用精制锗片。锗的化学性质与硅相似,如图是两者在元素周期表中的信息,下列说法正确的是
A. 锗属于非金属元素
B. 硅、锗原子的质子数相等
C. 锗原子最外层有4个电子
D. 锗的相对原子质量为
石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是
A. 可作散热材料 B. 是一种新型化合物
C. 常温下化学性质稳定 D. 可作新型电池的电极
为了庆祝元素周期表诞生150周年,联合国宣布将2019年定为国际化学元素周期表年。如图是元素周期表的一部分,以下表述正确的是
A. 氟原子核内的中子数为9
B. 氟、硫、氯的原子都容易得电子
C. 氯原子的相对原子质量是
D. 氟和氯位于元素周期表同一周期
根据图中提供的信息判断,下列说法正确的是
A. 锶原子的质子数为38 B. 锶原子在化学反应中易得到电子
C. 和两元素的化学性质相似 D. 所示的元素位于第二周期
氮元素与氧元素最本质的区别是
A. 相对原子质量不同 B. 中子数不同
C. 中子数与核外电子数之和不同 D. 质子数不同
国家航天局22日传来消息,根据遥测数据判断,5月22日10时40分,“祝融号”火星车已安全驶离着陆平台,到达火星表面,开始为期90天的巡视探测。火星车电源使用锂离子蓄电池。如图为锂原子结构示意图及在元素周期表中的信息,下列说法正确的是
A. 锂原子核内有3个中子
B. 锂原子质量为
C. 锂原子在化学反应中易失去电子
D. 蓄电池充电是把化学能转化为电能
二、填空题
元素周期表是学习化学的重要工具,下表为元素周期表中部分元素的相关信息,利用图示回答相关问题。
原子序数为14的元素符号为 ______,属于 ______填“金属”或“非金属”元素。
、N、O三种元素排在同一周期是因为 ______填“质子数”“电子层数”或“最外层电子数”相同。
和Mg的化学性质 ______填“相似”或“不相似”。
钠离子核外电子排布与 ______填元素符号原子核外电子排布相同。
一个磷原子含有 ______个质子,一个含有 ______个电子。
图中的和是氟元素和钙元素在元素周期表中的信息,A、B、C、D是4种粒子的结构示意图.请完成下列空白.
钙元素的相对原子质量为______,氟元素的原子序数为______;D中的x为______.
和是不同种元素,它们的最本质的区别是______不同.
、B、C、D结构示意图中,属于同种元素的粒子是______填字母.
粒子的化学性质与B、C、D中哪一种粒子的化学性质相似______填字母.
答案和解析
1.【答案】D
【解析】解:A、钽是“钅”旁,属于金属元素,故A正确不符合题意;
B、左上角是原子序数,钽的原子序数为73,故B正确不符合题意;
C、钽元素符号为Ta,故C正确不符合题意;
D、钽相对原子质量为,单位不是“g”,故D错误符合题意。
故选:D。
元素周期表中,每种元素占据的空格中,左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量。
本题难度不大,考查学生灵活运用元素周期表中元素的信息进行分析解题的能力。
2.【答案】A
【解析】解:物质是由元素组成的,故所有物质中含有的是元素,故选A
根据物质、元素、分子、原子、离子之间的关系进行解答:物质是由元素组成,由分子、原子、离子构成,
明确物质、元素、分子、原子、离子之间的关系是解答本类型关健.
3.【答案】D
【解析】解:A、硅是非金属元素;故说法错误;
B、硅元素符号为Si,故说法错误;
C、硅是地壳中含量排第二的元素,故说法错误;
D、单质硅是由硅原子构成的,故说法正确。
故选:D。
此题难度不大,掌握硅的有关知识即可顺利解答。
4.【答案】D
【解析】解:A、阳离子中:质子数核外电子数,中质子数为13,电子数为10,所以表示阳离子,正确;
B、一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,最外层电子数大于1,易失去电子,正确;
C、阴离子中:质子数核外电子数;质子数为17,电子数为18,表示阴离子,正确;
D、元素周期表中,每种元素占据的空格中,左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;中氯原子的相对原子质量为,单位不是”g“,错误。
故选:D。
根据结构示意图及元素周期表信息分析。
本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子中核内质子数和核外电子数之间的关系等进行分析解题的能力。
5.【答案】C
【解析】解:A、根据锗元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锗,带“钅”字旁,属于金属元素,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,硅、锗原子的原子序数分别为14、32;根据原子中原子序数核电荷数质子数核外电子数,则硅、锗原子的质子数不相等,故选项说法错误。
C、根据硅元素周期表中的一格可知,左上角的数字为14,表示原子序数为14;根据原子序数原子序数核电荷数质子数核外电子数,则该元素的原子核外电子数为14;核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有4个电子;硅、锗是同一族元素,它们的最外层电子数相同,则锗原子最外层有4个电子,故选项说法正确。
D、根据锗元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为,相对原子质量单位是“1”,不是“克”,故选项说法错误。
故选:C。
根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
本题难度不大,灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量是正确解答本题的关键。
6.【答案】B
【解析】解:石墨烯具有超强的导热性,所以可用来作散热材料,故正确;
B.石墨烯是一种由同种元素组成的纯净物,属于单质,故错误;
C.石墨烯是一种碳的单质,常温下化学性质稳定,故正确;
D.石墨烯具有超强的导电性,所以可作新型电池的电极,故正确。
故选:B。
A.根据石墨烯具有超强的导热性来分析;
B.根据物质的分类来分析;
C.根据物质的性质来分析;
D.根据物质的导电性来分析。
解答本题关键是要知道根据题干提供信息,去提取有用信息。
7.【答案】B
【解析】解:A、根据元素周期表中的一格可知,左上角的数字为9,表示原子序数为9;根据原子中原子序数核电荷数质子数核外电子数,则该元素的原子核内质子数与核外电子数为9而不是中子数为9,故选项说法错误。
B、氟、硫、氯的原子的原子最外层电子数均多于4,都容易得电子,故选项说法正确。
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,氯原子的相对原子质量是,相对原子质量单位是“1”,不是“克”,故选项说法错误。
D、同一横行叫一个周期,氟和氯不位于元素周期表同一周期,故选项说法错误。
故选:B。
根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
本题难度不大,考查学生灵活运用元素周期表中元素的信息、排列规律等进行分析解题的能力。
8.【答案】A
【解析】解:A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为38;根据原子中原子序数核电荷数质子数核外电子数,则锶原子的质子数为38,故选项说法正确。
B、锶原子的最外层电子数是2,在化学反应中易失去2个电子而形成阳离子,故选项说法错误。
C、中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;的最外层电子数为2,在化学反应中易失去2个电子而形成阳离子;尽管最外层电子数相同,但它们化学性质不相似,故选项说法错误。
D、是原子失去2个电子得到的,周期数原子核外电子层数,中元素的原子核外有3个电子层,则在元素周期表中,位于第三周期,故选项说法错误。
故选:A。
A、根据图中元素周期表可以获得的信息:左上角的数字表示原子序数,进行分析判断。
B、若最外层电子数,在化学反应中易得电子,若最外层电子数,在化学反应中易失去电子。
C、根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析判断。
D、根据周期数原子核外电子层数,进行分析判断。
本题难度不大,灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量、粒子结构示意图的含义是正确解答本题的关键。
9.【答案】D
【解析】解:元素是质子数即核电荷数相同的一类原子的总称,不同种元素最本质的区别是质子数即核电荷数不同,所以氧元素与氮元素的本质区别是质子数即核电荷数不同。
故选:D。
根据元素是质子数即核电荷数相同的一类原子的总称,决定元素种类的是质子数即核电荷数,据此进行分析解答。
本题难度不大,考查学生对元素的概念的理解和不同种元素之间的本质区别是质子数不同进行解题的能力。
10.【答案】C
【解析】解:A、锂原子核内中子数大约是个,故说法错误;
B、锂原子质量为,单位不是g,故说法错误;
C、锂原子的最外层电子数为1,在化学反应中易失去电子,故说法正确;
D、蓄电池充电是把电能转化为化学能,故说法错误;
故选:C。
根据元素表中一个单元格的意义进行分析解答即可。
加强对元素周期表中一个单元格的意义的掌握是正确解答本题的关键。
11.【答案】Si 非金属 电子层数 不相似 Ne 15 10
【解析】解:由元素周期表可知原子序数为14的元素符号为Si,硅属于非金属元素。
、N、O三种元素的原子电子层数相同,排在同一周期。
和Mg的最外层电子数相同,但是氦原子是稳定结构,镁原子最外层2个电子容易失去,不稳定,所以化学性质不相似。
钠原子失去最外层的1个电子形成钠离子,钠离子核外电子排布与氖原子核外电子排布相同。
原子中核电荷数核内质子数核外电子数,一个磷原子含有15个质子,一个含有的电子数为。
故答案为:
;非金属;
电子层数;
不相似;
;
;10。
根据元素周期表信息分析;
原子核外电子层数与周期数相同。
和Mg的最外层电子数相同,但是氦原子是稳定结构,镁原子最外层2个电子容易失去,不稳定。
钠原子失去最外层的1个电子形成钠离子,钠离子核外电子排布与氖原子核外电子排布相同。
根据原子中核电荷数核内质子数核外电子数分析。
本题难度不大,考查学生灵活运用元素周期表中元素的信息、了解粒子结构示意图的意义进行分析解题的能力。
12.【答案】 9 8
质子数
、C
【解析】
【分析】
本题难度不大,灵活运用元素周期表中元素的信息、明确粒子中核内质子数和核外电子数之间的关系、决定元素化学性质的因素等是正确解答本题的关键.
根据元素周期表的信息以及原子结构来分析;
根据元素的种类由质子数决定;
根据元素是具有相同核电荷数即核内质子数的一类原子的总称,决定元素种类的是核电荷数即核内质子数,据此进行分析解答;
根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,进行分析解答.
【解答】
根据氟元素、钙元素在元素周期表中的信息,可知钙元素的相对原子质量为,氟元素的原子序数为9;根据在原子中,原子序数质子数核电荷数核外电子数,可得,则;故填:;9;8;
元素的种类由质子数决定,故填:质子数;
根据元素的种类由质子数决定,因为B、C的质子数相同,所以B、C属于同种元素的粒子;故填:B、C;
根据元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似,A粒子的化学性质与B粒子化学性质相似.故填:B.
第2页,共2页
第1页,共1页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
