吉林省永吉县第四重点高中2021-2022学年高一9月月考化学试题(Word版含答案)
文档属性
| 名称 | 吉林省永吉县第四重点高中2021-2022学年高一9月月考化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 392.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-13 00:00:00 | ||
图片预览



文档简介
永吉县第四中学2021-2022学年高一9月月考
化学卷
一、单选题
1.下列属于纯净物的是
A.纯碱 B.石油 C.盐酸 D.空气
2.根据气象台报道,近年每到春季,沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列分散系中的
A.溶液 B.悬浊液 C.乳浊液 D.胶体
3.下列物质中均为化合物的一组是
A.金属钠、干冰、SO2 B.KCl、盐酸、NaOH
C.Na2CO3·10H2O、冰、AgCl D.液氧、CaCO3、石墨
4.若将工业用盐亚硝酸钠(NaNO2)误作食盐,会使人中毒死亡。亚硝酸钠中氮元素化合价是( )
A.+2 B.+3 C.+4 D.+5
5.《天工开物》是我国古代科技发展的智慧结晶,书中描述的下列制瓷工序涉及化学变化的是
图1 烧裂矿石 A.图2 粉碎矿石 C.图3淘洗矿粉 D.图4取泥制坯
6.金刚石硬度高、耐磨性好,可广泛用于切割、磨削、钻探等工业中。一种人造金刚石的生产方法为:4Na+CCl4C+4NaCl。该反应属于
A.非氧化还原反应 B.复分解反应 C.氧化还原反应 D.分解反应
7.合成新物质是研究化学的主要目的之一、意大利科学家合成了一种新型的氧分子O4,下列关于O4的说法中,正确的是
A.O4是一种新型的化合物 B.O4和O2互为同素异形体
C.1个O4分子由两个O2分子构成 D.O4和O2可通过物理变化实现转化
8.下列说法正确的是
A.氯化钠溶液在电流作用下电离成钠离子和氯离子
B.溶于水电离出H+的化合物都是酸
C.金属铜能导电,但它不是电解质,是非电解质
D.BaSO4难溶于水,但BaSO4属于电解质
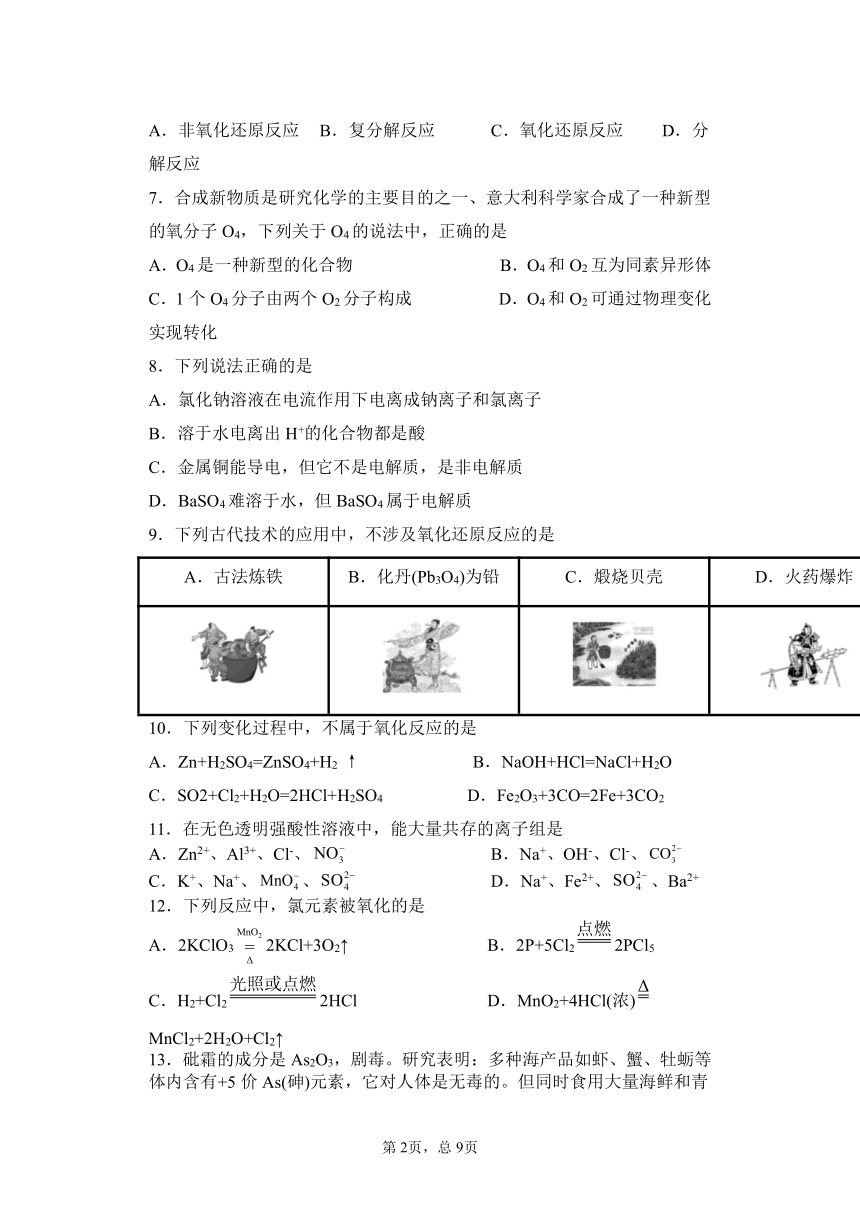
9.下列古代技术的应用中,不涉及氧化还原反应的是
A.古法炼铁 B.化丹(Pb3O4)为铅 C.煅烧贝壳 D.火药爆炸
10.下列变化过程中,不属于氧化反应的是
A.Zn+H2SO4=ZnSO4+H2 ↑ B.NaOH+HCl=NaCl+H2O
C.SO2+Cl2+H2O=2HCl+H2SO4 D.Fe2O3+3CO=2Fe+3CO2
11.在无色透明强酸性溶液中,能大量共存的离子组是
A.Zn2+、Al3+、Cl-、 B.Na+、OH-、Cl-、
C.K+、Na+、、 D.Na+、Fe2+、、Ba2+
12.下列反应中,氯元素被氧化的是
A.2KClO32KCl+3O2↑ B.2P+5Cl22PCl5
C.H2+Cl22HCl D.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
13.砒霜的成分是As2O3,剧毒。研究表明:多种海产品如虾、蟹、牡蛎等体内含有+5价As(砷)元素,它对人体是无毒的。但同时食用大量海鲜和青菜,易产生As2O3而中毒。专家给出的解释是:大量海鲜+大量维生素C=砒霜。下面有关解释不正确的是
A.青菜中含有维生素 B.维生素C能将+5价砷氧化成As2O3
C.维生素C具有还原性 D.致人中毒过程中+5价砷发生还原反应
14.反应SiO2+2CSi+2CO↑中,还原产物是A.SiO2 B.C C.Si D.CO
15.氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢气时的化学反应原理为:NaH+H2O=NaOH+H2↑。下列有关该反应的说法中,正确的是
A.该反应属于置换反应 B.该反应属于复分解反应
C.NaH是氧化剂 D.H2O中的氢元素被还原
16.过氧化氢(H2O2中氧元素为-1价)是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。在下列反应中只体现过氧化氢的还原性的反应是 ( )
A.5 H2O2+2KMnO4+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O B.H2O2+SO2=H2SO4
C.H2O2+HI=I2+2H2O D.2H2O2=2H2O+O2↑
17.用离子方程式H+ + OH-=H2O表示的是
A.3HCl + Fe(OH)3 = FeCl3 + 3H2O B.HNO3 + KOH = KNO3 + H2O
H2CO3 + 2NaOH = Na2CO3 + 2H2O D.2HCl + Cu(OH)2 = CuCl2 + 2H2O
18.实现下列物质之间的转化,需要加入还原剂才能实现的是
A.CuO→Cu B.SO3→H2SO4 C.Fe→Fe2+ D.CO→CO2
19.下列离子方程式书写正确的是
A.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑
B.碳酸钙与盐酸反应:CO+2H+=CO2↑+H2O
C.澄清石灰水中通入少量的二氧化碳:2OH-+CO2=CO+H2O
D.硫酸钠和氯化钡溶液反应:Ba2++SO=BaSO4↓
20.下列反应中,电子转移方向、数目和反应类型正确的是( )
A. B.
C. D.
二、填空题
21.阅读下列科普短文并填空。
燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,氢氧燃料电池在]
作时,从负极连续通入H2,从正极连续通入O2,二者在电池内部(含有H2SO4或KOH等物质的
① ② ③ ④
液)发生反应生成H2O,同时产生电能。除了H2,CH4、C2H5OH等也可以作为燃料电池的燃料。⑤ ⑥ ⑦
目前已研制成功Al-空气燃料电池,它可以代替汽油为汽车提供动力,也可以用作照明电源等。
⑧ ⑨ ⑩
(1)在上述短文标有序号的物质中,属于混合物的是 (填序号,下同);属于氧化物的是 ;属于酸的是 ;属于碱的是 ;属于有机物的是
(2)从物质的类别来看,H2、O2和A1都属于 单质; 请写出与O2互为同素异形体的物质的化学
式: 。
22.(1)汽车尾气(含CO、SO2、NO等)是城市空气的污染源之一,治理方法之一是在汽车的排气管上装一个“催化转化器”(用铂、钯合金作催化剂),它能使一氧化碳跟一氧化氮反应生成可参与大气循环的无毒气体。在汽车排气管上加装“催化转化器”,可使CO和NO反应产生可参与大气循环的无毒气体,请写出该反应的化学方程式: 。该反应的还原剂为:______氮元素的化合价_______(填“升高”或“降低”)。
(2)野外焊接铁轨常常采用铝热反应。
已知铝热反应的化学方程式为Fe2O3+2AlAl2O3+2Fe,该反应所属基本反应类型是________,在反应中铁元素的化合价________(填“升高”或“降低”),该元素的原子________(填“失去”或“得到”)电子。发生氧化反应的是________(填化学式,下同),发生还原反应的是________。
(3).用双线桥法标出电子转移的方向和数目
①Fe2O3+2AlAl2O3+2Fe ____________________
②Fe+2HCl=FeCl2+H2↑____________________
23.某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液,继续煮沸至液体呈透明的红褐色。FeCl3+3H2OFe(OH)3(胶体)+3HCl
(1)氢氧化铁胶体中粒子直径大小的范围是___________nm。
(2)你认为可以用什么方法判断胶体的制备是否成功?___________。
(3)净化氢氧化铁胶体的方法___________。
24.(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:___ __
常用澄清石灰水检验CO2气体的离子方程式是
(2)将表面附有铁锈(成分是Fe2O3)的铁钉放人稀硫酸中,开始反应的离子方程式是
反应片刻后,可观察到有气体产生,其离子方程式是
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
高一化学9月月考答题卡
班级 姓名 学号
一、单选题
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
答案 A D C B A C B D B A
二、填空题.(每空2分)
21.(1) (2)
22.(1)
(2)
(3)
23.(1) (2) (3)
(1)
(2)
(3)
第2页,总2页
第1页,总1页
化学卷
一、单选题
1.下列属于纯净物的是
A.纯碱 B.石油 C.盐酸 D.空气
2.根据气象台报道,近年每到春季,沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列分散系中的
A.溶液 B.悬浊液 C.乳浊液 D.胶体
3.下列物质中均为化合物的一组是
A.金属钠、干冰、SO2 B.KCl、盐酸、NaOH
C.Na2CO3·10H2O、冰、AgCl D.液氧、CaCO3、石墨
4.若将工业用盐亚硝酸钠(NaNO2)误作食盐,会使人中毒死亡。亚硝酸钠中氮元素化合价是( )
A.+2 B.+3 C.+4 D.+5
5.《天工开物》是我国古代科技发展的智慧结晶,书中描述的下列制瓷工序涉及化学变化的是
图1 烧裂矿石 A.图2 粉碎矿石 C.图3淘洗矿粉 D.图4取泥制坯
6.金刚石硬度高、耐磨性好,可广泛用于切割、磨削、钻探等工业中。一种人造金刚石的生产方法为:4Na+CCl4C+4NaCl。该反应属于
A.非氧化还原反应 B.复分解反应 C.氧化还原反应 D.分解反应
7.合成新物质是研究化学的主要目的之一、意大利科学家合成了一种新型的氧分子O4,下列关于O4的说法中,正确的是
A.O4是一种新型的化合物 B.O4和O2互为同素异形体
C.1个O4分子由两个O2分子构成 D.O4和O2可通过物理变化实现转化
8.下列说法正确的是
A.氯化钠溶液在电流作用下电离成钠离子和氯离子
B.溶于水电离出H+的化合物都是酸
C.金属铜能导电,但它不是电解质,是非电解质
D.BaSO4难溶于水,但BaSO4属于电解质
9.下列古代技术的应用中,不涉及氧化还原反应的是
A.古法炼铁 B.化丹(Pb3O4)为铅 C.煅烧贝壳 D.火药爆炸
10.下列变化过程中,不属于氧化反应的是
A.Zn+H2SO4=ZnSO4+H2 ↑ B.NaOH+HCl=NaCl+H2O
C.SO2+Cl2+H2O=2HCl+H2SO4 D.Fe2O3+3CO=2Fe+3CO2
11.在无色透明强酸性溶液中,能大量共存的离子组是
A.Zn2+、Al3+、Cl-、 B.Na+、OH-、Cl-、
C.K+、Na+、、 D.Na+、Fe2+、、Ba2+
12.下列反应中,氯元素被氧化的是
A.2KClO32KCl+3O2↑ B.2P+5Cl22PCl5
C.H2+Cl22HCl D.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
13.砒霜的成分是As2O3,剧毒。研究表明:多种海产品如虾、蟹、牡蛎等体内含有+5价As(砷)元素,它对人体是无毒的。但同时食用大量海鲜和青菜,易产生As2O3而中毒。专家给出的解释是:大量海鲜+大量维生素C=砒霜。下面有关解释不正确的是
A.青菜中含有维生素 B.维生素C能将+5价砷氧化成As2O3
C.维生素C具有还原性 D.致人中毒过程中+5价砷发生还原反应
14.反应SiO2+2CSi+2CO↑中,还原产物是A.SiO2 B.C C.Si D.CO
15.氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢气时的化学反应原理为:NaH+H2O=NaOH+H2↑。下列有关该反应的说法中,正确的是
A.该反应属于置换反应 B.该反应属于复分解反应
C.NaH是氧化剂 D.H2O中的氢元素被还原
16.过氧化氢(H2O2中氧元素为-1价)是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。在下列反应中只体现过氧化氢的还原性的反应是 ( )
A.5 H2O2+2KMnO4+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O B.H2O2+SO2=H2SO4
C.H2O2+HI=I2+2H2O D.2H2O2=2H2O+O2↑
17.用离子方程式H+ + OH-=H2O表示的是
A.3HCl + Fe(OH)3 = FeCl3 + 3H2O B.HNO3 + KOH = KNO3 + H2O
H2CO3 + 2NaOH = Na2CO3 + 2H2O D.2HCl + Cu(OH)2 = CuCl2 + 2H2O
18.实现下列物质之间的转化,需要加入还原剂才能实现的是
A.CuO→Cu B.SO3→H2SO4 C.Fe→Fe2+ D.CO→CO2
19.下列离子方程式书写正确的是
A.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑
B.碳酸钙与盐酸反应:CO+2H+=CO2↑+H2O
C.澄清石灰水中通入少量的二氧化碳:2OH-+CO2=CO+H2O
D.硫酸钠和氯化钡溶液反应:Ba2++SO=BaSO4↓
20.下列反应中,电子转移方向、数目和反应类型正确的是( )
A. B.
C. D.
二、填空题
21.阅读下列科普短文并填空。
燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,氢氧燃料电池在]
作时,从负极连续通入H2,从正极连续通入O2,二者在电池内部(含有H2SO4或KOH等物质的
① ② ③ ④
液)发生反应生成H2O,同时产生电能。除了H2,CH4、C2H5OH等也可以作为燃料电池的燃料。⑤ ⑥ ⑦
目前已研制成功Al-空气燃料电池,它可以代替汽油为汽车提供动力,也可以用作照明电源等。
⑧ ⑨ ⑩
(1)在上述短文标有序号的物质中,属于混合物的是 (填序号,下同);属于氧化物的是 ;属于酸的是 ;属于碱的是 ;属于有机物的是
(2)从物质的类别来看,H2、O2和A1都属于 单质; 请写出与O2互为同素异形体的物质的化学
式: 。
22.(1)汽车尾气(含CO、SO2、NO等)是城市空气的污染源之一,治理方法之一是在汽车的排气管上装一个“催化转化器”(用铂、钯合金作催化剂),它能使一氧化碳跟一氧化氮反应生成可参与大气循环的无毒气体。在汽车排气管上加装“催化转化器”,可使CO和NO反应产生可参与大气循环的无毒气体,请写出该反应的化学方程式: 。该反应的还原剂为:______氮元素的化合价_______(填“升高”或“降低”)。
(2)野外焊接铁轨常常采用铝热反应。
已知铝热反应的化学方程式为Fe2O3+2AlAl2O3+2Fe,该反应所属基本反应类型是________,在反应中铁元素的化合价________(填“升高”或“降低”),该元素的原子________(填“失去”或“得到”)电子。发生氧化反应的是________(填化学式,下同),发生还原反应的是________。
(3).用双线桥法标出电子转移的方向和数目
①Fe2O3+2AlAl2O3+2Fe ____________________
②Fe+2HCl=FeCl2+H2↑____________________
23.某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液,继续煮沸至液体呈透明的红褐色。FeCl3+3H2OFe(OH)3(胶体)+3HCl
(1)氢氧化铁胶体中粒子直径大小的范围是___________nm。
(2)你认为可以用什么方法判断胶体的制备是否成功?___________。
(3)净化氢氧化铁胶体的方法___________。
24.(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:___ __
常用澄清石灰水检验CO2气体的离子方程式是
(2)将表面附有铁锈(成分是Fe2O3)的铁钉放人稀硫酸中,开始反应的离子方程式是
反应片刻后,可观察到有气体产生,其离子方程式是
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
高一化学9月月考答题卡
班级 姓名 学号
一、单选题
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
答案 A D C B A C B D B A
二、填空题.(每空2分)
21.(1) (2)
22.(1)
(2)
(3)
23.(1) (2) (3)
(1)
(2)
(3)
第2页,总2页
第1页,总1页
同课章节目录
