化学高一人教版无机非金属材料的主角硅
文档属性
| 名称 | 化学高一人教版无机非金属材料的主角硅 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-08-12 00:00:00 | ||
图片预览










文档简介
(共36张PPT)
第四章 非金属及其化合物
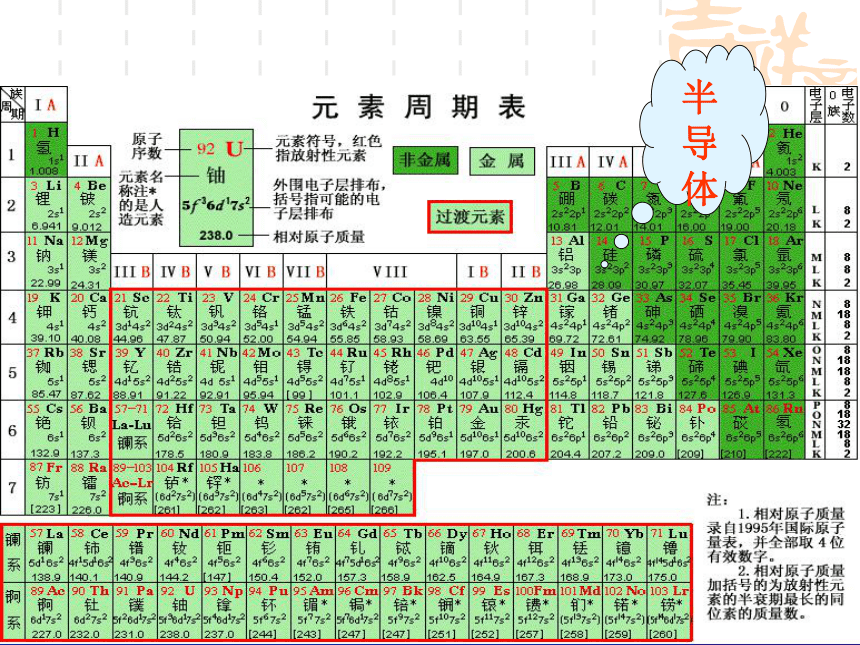
半导体
二氧化硅、硅酸盐
第一节 无机非金属材料的主角—硅
地壳中含量最多的前两种元素
是 和 ,它们构成了地壳的基本骨架。硅在地壳中的含量为 。硅的
及 构成了地壳中大部分的岩石、沙子和土壤,约占地壳质量的 以上。
Si
O
26.3%
氧化物
硅酸盐
90%
北京2008奥运会奖牌“金镶玉”
金玉良缘
中西合璧
中国玉文化
思考:
地球上的硅元素主要以什么形式存在?为什么?
硅是一种亲 元素,主要以熔点很高的 形式存在。而碳在地壳中主要形成 等矿物。
氧
氧化物、硅酸盐
石灰岩、碳酸盐
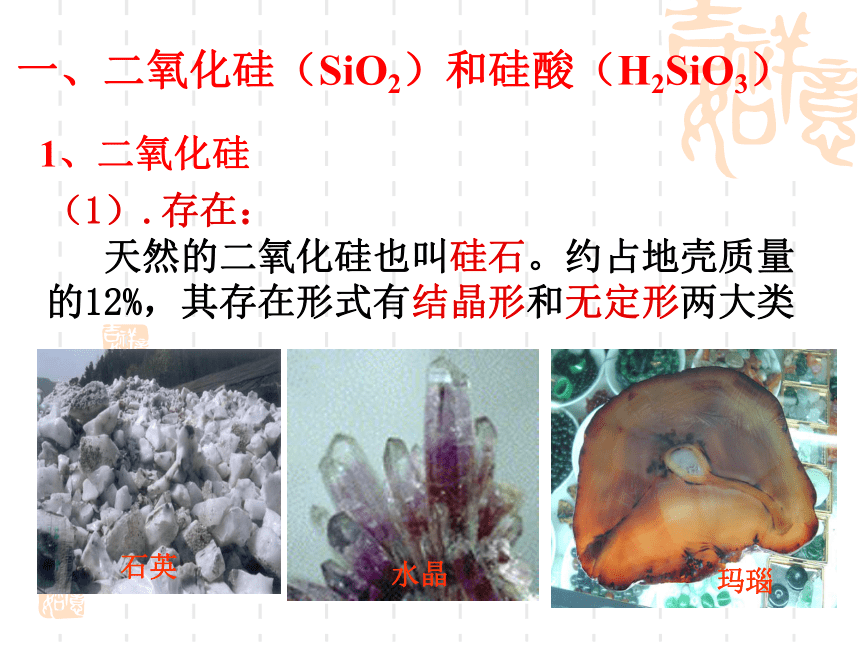
一、二氧化硅(SiO2)和硅酸(H2SiO3)
(1).存在:
天然的二氧化硅也叫硅石。约占地壳质量的12%,其存在形式有结晶形和无定形两大类
石英
水晶
玛瑙
1、二氧化硅
石英光导
纤维
石 英 制 品
水 晶 制 品
水
晶
制
品
玛 瑙
玛 瑙
(2) 、用途
①、制光导纤维
②、石英玻璃制化学仪器
③、石英表、石英钟
④、水晶制光学仪器和工艺品
⑤、玛瑙制精密轴承和装饰品
石英晶体是结晶的二氧化硅,石英中无色透明的晶体就是通常所说的水晶。
石英具有彩色环状或层状的称为玛瑙。
180
109 28
Si
o
(3)、网状结构决定了SiO2具有优良的性质
在基本结构单元中([SiO4]四面体)每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的四面体又通过顶角的O相连接,每个O为两个四面体共有,既每个O跟2个Si相结合。形成立体网状结构
物理性质
物质 SiO2 CO2
状态(常温) 气体
熔点 -56.6℃
沸点 -78.5℃
溶解性 1:1
硬度
固体
1610℃
2230℃
不溶
大
(4)性质
思考 1、实验室盛放NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞?
NaOH溶液能与玻璃中的SiO2反应生成Na2SiO3,使瓶塞部分粘结而无法打开。因此盛装NaOH溶液的试剂瓶不能用玻璃塞,用橡胶塞或塑料塞。
2、实验室如何贮存氢氟酸?
贮存在塑料瓶。
3、SiO2是什么类型的氧化物?
是酸性氧化物
1、化学性质很不活泼,氢氟酸( HF)是唯一可以与之反应的酸。
SiO2+4HF=SiF4 +2H2O
化学性质归纳:
2、酸性氧化物的通性:
SiO2+CaO===CaSiO3
SiO2+2NaOH==Na2SiO3+H2O
雕花玻璃
CO2 SiO2
物理性质
与水反应
与碱反应
与CaO反应
与氢氟酸反应
结论
CO2和SiO2的性质比较
无色无味气体,能溶于水,密度比空气大
固态、难溶于水、硬度大、熔点高
CO2+H2O=H2CO3
不反应
CO2+2NaOH=Na2CO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
CaO+CO2=CaCO3
CaO+SiO2 CaSiO3
高温
不反应
SiO2+4HF=SiF4+2H2O
CO2和SiO2都是酸性氧化物
二、硅酸
〖 探究·研讨 〗
(1)硅酸的酸酐为 ,因其不溶于水也不与水反应,所以一般不能直接用SiO2制备硅酸。
1.硅酸的制备
二氧化硅
(2)可通过 与 制得,所生成的H2SiO3易聚合形成 ;
可溶性硅酸盐
硅酸溶胶
其他酸
Na2SiO3溶液呈 性,硅酸盐与 反应可以制得硅酸。
滴加酚酞试液后溶液呈 色,滴加稀盐酸后溶液变为无色,有 生成。
结论
实验现象
实验操作
Na2SiO3溶液与盐酸和反应的化学方程式:
;
Na2SiO3溶液与CO2反应的化学方程式:
;
硅酸浓度较大时则形成 ;
硅酸凝胶干燥脱水——硅酸干凝胶,又称为 ,吸附水分能力强,常用作 ,也用作 的载体。
硅胶
硅酸凝胶
干燥剂
催化剂
2.硅酸的性质
(2)是一种很弱的酸,酸性:H2SiO3 (填“﹥”“﹤”)H2CO3。
(3)不稳定(比H2CO3稳定)受热易分解: 。
(1)硅酸在水中的溶解度 。
很小
﹤
物质 硅酸 碳酸
化学式
酸酐
制法
颜色与状态
水溶性
酸性比较
硅酸、碳酸的对比
H2SiO3
H2CO3
可溶性硅酸盐和强酸
碳酸盐和强酸
H2SiO3 ﹤ H2CO3
SiO2
CO2
白色,固体
无纯液态,只存在于水溶液中
难溶于水
只存在于水溶液中
〖 小结·比较 〗
3.下列物质中能与SiO2起化学反应的是( )
①浓H2SO4 ②H2O ③盐酸 ④HF ⑤ KOH溶液 ⑥氧化钙
A.①②⑥ B.②④ C.④⑤⑥ D.③④⑤⑥
2.下列溶液中,能用带磨口玻璃塞的试剂瓶盛放的是( )
A.浓H2SO4 B.水玻璃 C.氢氟酸 D.苛性钾溶液
4.要除去SiO2中混有的少量CaO杂质,最适宜的试剂是( )
A.纯碱溶液 B.盐酸 C.硫酸 D.苛性钠溶液
1.下列物质中,主要成分不是SiO2的是( )
A.金刚砂 B.玛瑙 C.水晶 D.石英
〖 测试·反馈 〗:
A
A
C
B.
6、CO2通入下列各溶液中,不会产生难溶物的是( )
A、水玻璃 B、石灰水
C、饱和Na2CO3 D、CaCl2
5.在无色的强酸性溶液中,能大量共存的是( )
A.Na+、Al3+、NO3-、Cl-
B.K+、Na+、Cl-、SiO32-
C.Fe2+、K+、SO42-、Cl-
D.Na+、HCO3-、K+、NO3-
A
D
A是一种天然透明晶体,B是一种常见的无色无味的气体,可使澄清石灰水变浑浊。A虽不能溶于强酸,但却能溶于氢氟酸,并生成气体C,A和烧碱溶液反应生成D的水溶液,
当气体B通入D的水溶液中,能生成白色胶状沉淀E,E加热后重新生成A。
(1)写出化学式
A 、B 、C 、D 、E 。
(2)写出有关反应的化学方程式。
第四章 非金属及其化合物
半导体
二氧化硅、硅酸盐
第一节 无机非金属材料的主角—硅
地壳中含量最多的前两种元素
是 和 ,它们构成了地壳的基本骨架。硅在地壳中的含量为 。硅的
及 构成了地壳中大部分的岩石、沙子和土壤,约占地壳质量的 以上。
Si
O
26.3%
氧化物
硅酸盐
90%
北京2008奥运会奖牌“金镶玉”
金玉良缘
中西合璧
中国玉文化
思考:
地球上的硅元素主要以什么形式存在?为什么?
硅是一种亲 元素,主要以熔点很高的 形式存在。而碳在地壳中主要形成 等矿物。
氧
氧化物、硅酸盐
石灰岩、碳酸盐
一、二氧化硅(SiO2)和硅酸(H2SiO3)
(1).存在:
天然的二氧化硅也叫硅石。约占地壳质量的12%,其存在形式有结晶形和无定形两大类
石英
水晶
玛瑙
1、二氧化硅
石英光导
纤维
石 英 制 品
水 晶 制 品
水
晶
制
品
玛 瑙
玛 瑙
(2) 、用途
①、制光导纤维
②、石英玻璃制化学仪器
③、石英表、石英钟
④、水晶制光学仪器和工艺品
⑤、玛瑙制精密轴承和装饰品
石英晶体是结晶的二氧化硅,石英中无色透明的晶体就是通常所说的水晶。
石英具有彩色环状或层状的称为玛瑙。
180
109 28
Si
o
(3)、网状结构决定了SiO2具有优良的性质
在基本结构单元中([SiO4]四面体)每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的四面体又通过顶角的O相连接,每个O为两个四面体共有,既每个O跟2个Si相结合。形成立体网状结构
物理性质
物质 SiO2 CO2
状态(常温) 气体
熔点 -56.6℃
沸点 -78.5℃
溶解性 1:1
硬度
固体
1610℃
2230℃
不溶
大
(4)性质
思考 1、实验室盛放NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞?
NaOH溶液能与玻璃中的SiO2反应生成Na2SiO3,使瓶塞部分粘结而无法打开。因此盛装NaOH溶液的试剂瓶不能用玻璃塞,用橡胶塞或塑料塞。
2、实验室如何贮存氢氟酸?
贮存在塑料瓶。
3、SiO2是什么类型的氧化物?
是酸性氧化物
1、化学性质很不活泼,氢氟酸( HF)是唯一可以与之反应的酸。
SiO2+4HF=SiF4 +2H2O
化学性质归纳:
2、酸性氧化物的通性:
SiO2+CaO===CaSiO3
SiO2+2NaOH==Na2SiO3+H2O
雕花玻璃
CO2 SiO2
物理性质
与水反应
与碱反应
与CaO反应
与氢氟酸反应
结论
CO2和SiO2的性质比较
无色无味气体,能溶于水,密度比空气大
固态、难溶于水、硬度大、熔点高
CO2+H2O=H2CO3
不反应
CO2+2NaOH=Na2CO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
CaO+CO2=CaCO3
CaO+SiO2 CaSiO3
高温
不反应
SiO2+4HF=SiF4+2H2O
CO2和SiO2都是酸性氧化物
二、硅酸
〖 探究·研讨 〗
(1)硅酸的酸酐为 ,因其不溶于水也不与水反应,所以一般不能直接用SiO2制备硅酸。
1.硅酸的制备
二氧化硅
(2)可通过 与 制得,所生成的H2SiO3易聚合形成 ;
可溶性硅酸盐
硅酸溶胶
其他酸
Na2SiO3溶液呈 性,硅酸盐与 反应可以制得硅酸。
滴加酚酞试液后溶液呈 色,滴加稀盐酸后溶液变为无色,有 生成。
结论
实验现象
实验操作
Na2SiO3溶液与盐酸和反应的化学方程式:
;
Na2SiO3溶液与CO2反应的化学方程式:
;
硅酸浓度较大时则形成 ;
硅酸凝胶干燥脱水——硅酸干凝胶,又称为 ,吸附水分能力强,常用作 ,也用作 的载体。
硅胶
硅酸凝胶
干燥剂
催化剂
2.硅酸的性质
(2)是一种很弱的酸,酸性:H2SiO3 (填“﹥”“﹤”)H2CO3。
(3)不稳定(比H2CO3稳定)受热易分解: 。
(1)硅酸在水中的溶解度 。
很小
﹤
物质 硅酸 碳酸
化学式
酸酐
制法
颜色与状态
水溶性
酸性比较
硅酸、碳酸的对比
H2SiO3
H2CO3
可溶性硅酸盐和强酸
碳酸盐和强酸
H2SiO3 ﹤ H2CO3
SiO2
CO2
白色,固体
无纯液态,只存在于水溶液中
难溶于水
只存在于水溶液中
〖 小结·比较 〗
3.下列物质中能与SiO2起化学反应的是( )
①浓H2SO4 ②H2O ③盐酸 ④HF ⑤ KOH溶液 ⑥氧化钙
A.①②⑥ B.②④ C.④⑤⑥ D.③④⑤⑥
2.下列溶液中,能用带磨口玻璃塞的试剂瓶盛放的是( )
A.浓H2SO4 B.水玻璃 C.氢氟酸 D.苛性钾溶液
4.要除去SiO2中混有的少量CaO杂质,最适宜的试剂是( )
A.纯碱溶液 B.盐酸 C.硫酸 D.苛性钠溶液
1.下列物质中,主要成分不是SiO2的是( )
A.金刚砂 B.玛瑙 C.水晶 D.石英
〖 测试·反馈 〗:
A
A
C
B.
6、CO2通入下列各溶液中,不会产生难溶物的是( )
A、水玻璃 B、石灰水
C、饱和Na2CO3 D、CaCl2
5.在无色的强酸性溶液中,能大量共存的是( )
A.Na+、Al3+、NO3-、Cl-
B.K+、Na+、Cl-、SiO32-
C.Fe2+、K+、SO42-、Cl-
D.Na+、HCO3-、K+、NO3-
A
D
A是一种天然透明晶体,B是一种常见的无色无味的气体,可使澄清石灰水变浑浊。A虽不能溶于强酸,但却能溶于氢氟酸,并生成气体C,A和烧碱溶液反应生成D的水溶液,
当气体B通入D的水溶液中,能生成白色胶状沉淀E,E加热后重新生成A。
(1)写出化学式
A 、B 、C 、D 、E 。
(2)写出有关反应的化学方程式。
