课时训练20燃料电池
图片预览

文档简介
课时训练20 燃料电池
1.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,已用于宇宙飞船及潜艇中,其电极反应式为:
负极:2H2+4OH--4e-4H2O
正极:O2+2H2O+4e-4OH-
所产生的水还可作为饮用水,今欲得常温下1 L水,则电池内电子转移的物质的量约为( )。
A.8.9×10-3 mol B.4.5×10-2 mol
C.1.1×102 mol D.5.6×10 mol
解析:正负极反应合并得:2H2+O22H2O,若转移4 mol电子,则生成2 mol H2O,欲生成1 L水即 mol,转移电子为×2 mol=1.1×102 mol。
答案:C
2.质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )。
①正极反应为:O2+4H++4e-2H2O
②负极反应为:2H2-4e-4H+
③总的化学反应为:2H2+O22H2O
④氢离子通过电解质向正极移动
A.①②③ B.②③④
C.①②④ D.①②③④
解析:燃料电池中的反应不是在点燃的条件下进行的,故③错。因为导电离子是H+,且向正极移动,所以正极反应为O2+4H++4e-2H2O,电子由负极通过外电路流向正极。
答案:C
3.美国加州Miramar海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。该电池的总反应为:2H2+O22H2O,负极反应为:H2+C-2e-H2O+CO2。则下列推断中正确的是( )。
A.正极反应:4OH--4e-2H2O+O2↑
B.当电池生成1 mol H2O时,转移4 mol电子
C.放电时C向负极移动
D.放电时C向正极移动
解析:总反应式减去负极反应式求得正极反应式为:O2+4e-+2CO22C,故A项错误;由总反应知每生成1 mol水,转移2 mol电子,故B项错误;放电时,C向负极移动,C项正确;D项错误。
答案:C
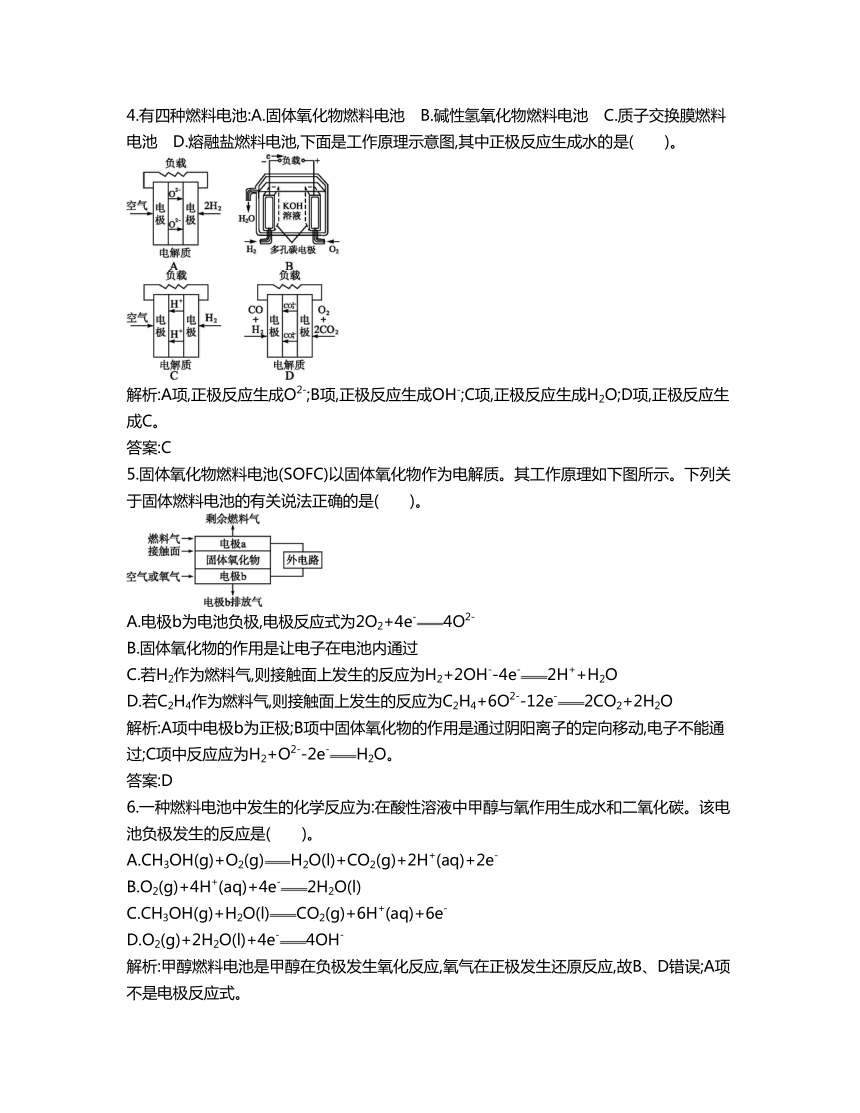
4.有四种燃料电池:A.固体氧化物燃料电池 B.碱性氢氧化物燃料电池 C.质子交换膜燃料电池 D.熔融盐燃料电池,下面是工作原理示意图,其中正极反应生成水的是( )。
解析:A项,正极反应生成O2-;B项,正极反应生成OH-;C项,正极反应生成H2O;D项,正极反应生成C。
答案:C
5.固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如下图所示。下列关于固体燃料电池的有关说法正确的是( )。
A.电极b为电池负极,电极反应式为2O2+4e-4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-2CO2+2H2O
解析:A项中电极b为正极;B项中固体氧化物的作用是通过阴阳离子的定向移动,电子不能通过;C项中反应应为H2+O2--2e-H2O。
答案:D
6.一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是( )。
A.CH3OH(g)+O2(g)H2O(l)+CO2(g)+2H+(aq)+2e-
B.O2(g)+4H+(aq)+4e-2H2O(l)
C.CH3OH(g)+H2O(l)CO2(g)+6H+(aq)+6e-
D.O2(g)+2H2O(l)+4e-4OH-
解析:甲醇燃料电池是甲醇在负极发生氧化反应,氧气在正极发生还原反应,故B、D错误;A项不是电极反应式。
答案:C
7.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )。
A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e-6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体L
解析:微生物主要成分是蛋白质,高温条件下蛋白质失去活性,A不正确。通入燃料C6H12O6的极为负极,负极反应为:C6H12O6+6H2O-24e-6CO2↑+24H+(能放出CO2应该是酸性,所以右边写H+。不能在左边加OH-、右边写H2O),B项正确。正极反应为:6O2+24H++24e-12H2O,从两极反应可知:负极生成H+,正极消耗H+,即通过质子交换膜从负极到正极传导H+,选项C不正确。从总反应C6H12O6+6O26CO2+6H2O可知,每消耗1 mol氧气,理论上能生成标准状况下CO2气体22.4 L,D项错。
答案:B
8.据报道,摩托罗拉公司研制了一种有甲醇和氧气,以及强碱作电解质的手机电池,电量可达到镍氢电池的10倍,有关此电池的叙述错误的是( )。
A.溶液中的阳离子移向正极
B.负极反应式:CH3OH+8OH--6e-C+6H2O
C.电池在使用过程中,电解质溶液的c(OH-)不变
D.当外电路通过6 mol电子时,理论上消耗1.5 mol O2
解析:A项,溶液中的阳离子移向发生还原反应的一极即正极;B项,负极CH3OH发生氧化反应;C项,电池在使用过程中,电解质溶液的c(OH-)减少;D项,1 mol O2消耗可转移4 mol电子,外电路通过6 mol e-时,消耗1.5 mol O2。
答案:C
9.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池的说法中正确的是( )。
A.在熔融电解质中O2-由负极移向正极
B.电池的总反应是2C4H10+13O28CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+4e-+2H2O4OH-
D.通入丁烷的一极是正极,电极反应为:C4H10-26e-+13O2-4CO2+5H2O
解析:本题以丁烷燃料电池为载体,综合考查了原电池原理涉及的有关“电子流向、电极反应式、总反应式”等内容,因正极上富集电子,根据电性关系,O2-不可能移向正极,A错。由丁烷的燃烧反应及电解质的特性知该电池的总反应式为2C4H10+13O28CO2+10H2O,B正确。在熔融状态下允许O2-在其间通过,故其正极反应式为O2+4e-2O2-,C不正确。通入丁烷的一极应为负极,D错。
答案:B
10.目前,汽车尾气对环境的污染越来越严重。为解决这一问题,大型汽车公司均在投巨资发展电动力汽车。燃料电池电动车实验证明,其性能可与内燃机汽车媲美。尤其当以纯氢为燃料时,它能达到真正的“零”排放。
(1)汽车尾气所产生的大气污染物主要是 、 (填两种)。
(2)氢氧燃料电池实现“零”排放的原因是 。
(3)氢氧燃料电池普及可能遇到的技术问题是 (答一种即可)。
答案:(1)CO NOx (2)产物只有水,无污染 (3)氢气的制取和储存
11.(1)据报道,科研人员新近开发出一种由甲醇和氧气以及强碱作电解质溶液的新型电池,可供手机连续使用一个月。据此请回答以下问题:
①甲醇是 极,电极反应是 。
②电池反应的离子方程式是 。
(2)一般说来,根据一个氧化还原反应便可设计一个原电池。例如,某种燃料电池的总反应是CH4+2O2+2OH-C+3H2O。在此燃料电池中,通CH4极是 极,通O2极是 极,每消耗1 mol CH4,转移电子 mol,此电池的电解质溶液为 ,负极发生的电极反应是 ,正极发生的电极反应是 。
答案:(1)①负 CH3OH-6e-+8OH-C+6H2O
②2CH3OH+3O2+4OH-2C+6H2O
(2)负 正 8 碱性介质如KOH溶液 负极:CH4-8e-+10OH-C+7H2O 正极:2O2+4H2O+8e-8OH-
12.可以将氧化还原反应2H2+O22H2O设计成原电池。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,则负极通的气体应是 ,正极通的气体就是 ,电极反应式为:正极 ,负极 。
(2)如果把KOH改为稀硫酸作电解质,则电极反应式为:正极: ,负极: 。
(3)(1)和(2)的电解质溶液不同,反应进行后,其溶液的pH各有何变化 。
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应式为:正极: ,负极: 。
解析:(1)根据电池反应式可知在反应中H2被氧化,O2被还原。H2应该在负极上反应,O2应该在正极上反应,又因为是碱性溶液不可能有H+参加或生成,故负极的电极反应为2H2+4OH--4e-4H2O,正极的电极反应为O2+2H2O+4e-4OH-。
(2)若将电解质溶液换为酸性溶液,此时应考虑不可能有OH-参加或生成,故负极的电极反应为2H2-4e-4H+,正极的电极反应为O2+4H++4e-2H2O。
(3)由于前者在碱性条件下反应,KOH的量不变,但工作时H2O增多,故溶液变稀,pH将变小;而后者为酸溶液,H2SO4的量不变,H2O增多,故溶液变稀,pH将变大。
(4)如把H2改为甲烷,KOH溶液作电解质,则正极反应为2O2+4H2O+8e-8OH-;负极反应为CH4+10OH--8e-C+7H2O,此时不会有CO2放出。
答案:(1)H2 O2 O2+2H2O+4e-4OH- H2+2OH--2e-2H2O
(2)O2+4H++4e-2H2O 2H2-4e-4H+
(3)前者变小,后者变大
(4)2O2+4H2O+8e-8OH- CH4+10OH--8e-C+7H2O
1.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,已用于宇宙飞船及潜艇中,其电极反应式为:
负极:2H2+4OH--4e-4H2O
正极:O2+2H2O+4e-4OH-
所产生的水还可作为饮用水,今欲得常温下1 L水,则电池内电子转移的物质的量约为( )。
A.8.9×10-3 mol B.4.5×10-2 mol
C.1.1×102 mol D.5.6×10 mol
解析:正负极反应合并得:2H2+O22H2O,若转移4 mol电子,则生成2 mol H2O,欲生成1 L水即 mol,转移电子为×2 mol=1.1×102 mol。
答案:C
2.质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )。
①正极反应为:O2+4H++4e-2H2O
②负极反应为:2H2-4e-4H+
③总的化学反应为:2H2+O22H2O
④氢离子通过电解质向正极移动
A.①②③ B.②③④
C.①②④ D.①②③④
解析:燃料电池中的反应不是在点燃的条件下进行的,故③错。因为导电离子是H+,且向正极移动,所以正极反应为O2+4H++4e-2H2O,电子由负极通过外电路流向正极。
答案:C
3.美国加州Miramar海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。该电池的总反应为:2H2+O22H2O,负极反应为:H2+C-2e-H2O+CO2。则下列推断中正确的是( )。
A.正极反应:4OH--4e-2H2O+O2↑
B.当电池生成1 mol H2O时,转移4 mol电子
C.放电时C向负极移动
D.放电时C向正极移动
解析:总反应式减去负极反应式求得正极反应式为:O2+4e-+2CO22C,故A项错误;由总反应知每生成1 mol水,转移2 mol电子,故B项错误;放电时,C向负极移动,C项正确;D项错误。
答案:C
4.有四种燃料电池:A.固体氧化物燃料电池 B.碱性氢氧化物燃料电池 C.质子交换膜燃料电池 D.熔融盐燃料电池,下面是工作原理示意图,其中正极反应生成水的是( )。
解析:A项,正极反应生成O2-;B项,正极反应生成OH-;C项,正极反应生成H2O;D项,正极反应生成C。
答案:C
5.固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如下图所示。下列关于固体燃料电池的有关说法正确的是( )。
A.电极b为电池负极,电极反应式为2O2+4e-4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-2CO2+2H2O
解析:A项中电极b为正极;B项中固体氧化物的作用是通过阴阳离子的定向移动,电子不能通过;C项中反应应为H2+O2--2e-H2O。
答案:D
6.一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是( )。
A.CH3OH(g)+O2(g)H2O(l)+CO2(g)+2H+(aq)+2e-
B.O2(g)+4H+(aq)+4e-2H2O(l)
C.CH3OH(g)+H2O(l)CO2(g)+6H+(aq)+6e-
D.O2(g)+2H2O(l)+4e-4OH-
解析:甲醇燃料电池是甲醇在负极发生氧化反应,氧气在正极发生还原反应,故B、D错误;A项不是电极反应式。
答案:C
7.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )。
A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e-6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体L
解析:微生物主要成分是蛋白质,高温条件下蛋白质失去活性,A不正确。通入燃料C6H12O6的极为负极,负极反应为:C6H12O6+6H2O-24e-6CO2↑+24H+(能放出CO2应该是酸性,所以右边写H+。不能在左边加OH-、右边写H2O),B项正确。正极反应为:6O2+24H++24e-12H2O,从两极反应可知:负极生成H+,正极消耗H+,即通过质子交换膜从负极到正极传导H+,选项C不正确。从总反应C6H12O6+6O26CO2+6H2O可知,每消耗1 mol氧气,理论上能生成标准状况下CO2气体22.4 L,D项错。
答案:B
8.据报道,摩托罗拉公司研制了一种有甲醇和氧气,以及强碱作电解质的手机电池,电量可达到镍氢电池的10倍,有关此电池的叙述错误的是( )。
A.溶液中的阳离子移向正极
B.负极反应式:CH3OH+8OH--6e-C+6H2O
C.电池在使用过程中,电解质溶液的c(OH-)不变
D.当外电路通过6 mol电子时,理论上消耗1.5 mol O2
解析:A项,溶液中的阳离子移向发生还原反应的一极即正极;B项,负极CH3OH发生氧化反应;C项,电池在使用过程中,电解质溶液的c(OH-)减少;D项,1 mol O2消耗可转移4 mol电子,外电路通过6 mol e-时,消耗1.5 mol O2。
答案:C
9.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池的说法中正确的是( )。
A.在熔融电解质中O2-由负极移向正极
B.电池的总反应是2C4H10+13O28CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+4e-+2H2O4OH-
D.通入丁烷的一极是正极,电极反应为:C4H10-26e-+13O2-4CO2+5H2O
解析:本题以丁烷燃料电池为载体,综合考查了原电池原理涉及的有关“电子流向、电极反应式、总反应式”等内容,因正极上富集电子,根据电性关系,O2-不可能移向正极,A错。由丁烷的燃烧反应及电解质的特性知该电池的总反应式为2C4H10+13O28CO2+10H2O,B正确。在熔融状态下允许O2-在其间通过,故其正极反应式为O2+4e-2O2-,C不正确。通入丁烷的一极应为负极,D错。
答案:B
10.目前,汽车尾气对环境的污染越来越严重。为解决这一问题,大型汽车公司均在投巨资发展电动力汽车。燃料电池电动车实验证明,其性能可与内燃机汽车媲美。尤其当以纯氢为燃料时,它能达到真正的“零”排放。
(1)汽车尾气所产生的大气污染物主要是 、 (填两种)。
(2)氢氧燃料电池实现“零”排放的原因是 。
(3)氢氧燃料电池普及可能遇到的技术问题是 (答一种即可)。
答案:(1)CO NOx (2)产物只有水,无污染 (3)氢气的制取和储存
11.(1)据报道,科研人员新近开发出一种由甲醇和氧气以及强碱作电解质溶液的新型电池,可供手机连续使用一个月。据此请回答以下问题:
①甲醇是 极,电极反应是 。
②电池反应的离子方程式是 。
(2)一般说来,根据一个氧化还原反应便可设计一个原电池。例如,某种燃料电池的总反应是CH4+2O2+2OH-C+3H2O。在此燃料电池中,通CH4极是 极,通O2极是 极,每消耗1 mol CH4,转移电子 mol,此电池的电解质溶液为 ,负极发生的电极反应是 ,正极发生的电极反应是 。
答案:(1)①负 CH3OH-6e-+8OH-C+6H2O
②2CH3OH+3O2+4OH-2C+6H2O
(2)负 正 8 碱性介质如KOH溶液 负极:CH4-8e-+10OH-C+7H2O 正极:2O2+4H2O+8e-8OH-
12.可以将氧化还原反应2H2+O22H2O设计成原电池。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,则负极通的气体应是 ,正极通的气体就是 ,电极反应式为:正极 ,负极 。
(2)如果把KOH改为稀硫酸作电解质,则电极反应式为:正极: ,负极: 。
(3)(1)和(2)的电解质溶液不同,反应进行后,其溶液的pH各有何变化 。
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应式为:正极: ,负极: 。
解析:(1)根据电池反应式可知在反应中H2被氧化,O2被还原。H2应该在负极上反应,O2应该在正极上反应,又因为是碱性溶液不可能有H+参加或生成,故负极的电极反应为2H2+4OH--4e-4H2O,正极的电极反应为O2+2H2O+4e-4OH-。
(2)若将电解质溶液换为酸性溶液,此时应考虑不可能有OH-参加或生成,故负极的电极反应为2H2-4e-4H+,正极的电极反应为O2+4H++4e-2H2O。
(3)由于前者在碱性条件下反应,KOH的量不变,但工作时H2O增多,故溶液变稀,pH将变小;而后者为酸溶液,H2SO4的量不变,H2O增多,故溶液变稀,pH将变大。
(4)如把H2改为甲烷,KOH溶液作电解质,则正极反应为2O2+4H2O+8e-8OH-;负极反应为CH4+10OH--8e-C+7H2O,此时不会有CO2放出。
答案:(1)H2 O2 O2+2H2O+4e-4OH- H2+2OH--2e-2H2O
(2)O2+4H++4e-2H2O 2H2-4e-4H+
(3)前者变小,后者变大
(4)2O2+4H2O+8e-8OH- CH4+10OH--8e-C+7H2O
