2.4辨别物质的元素组成课后练习基础过关-2021-2022学年九年级化学科粤版上册(含解析)
文档属性
| 名称 | 2.4辨别物质的元素组成课后练习基础过关-2021-2022学年九年级化学科粤版上册(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 98.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-14 00:00:00 | ||
图片预览




文档简介
第二章空气、物质的构成2.4辨别物质的元素组成课后练习基础过关九年级化学上学期(科粤版2012)
练习
一、单选题,共12小题
1.每100mL牛奶中含钙86mg,这的“钙”应理解为
A.元素 B.原子 C.离子 D.分子
2.下图是氩元素在元素周期表中的有关信息,下列说法错误的是
A.属于金属元素
B.氩的原子序数是18
C.氩原子具有稳定结构
D.相对原子质量是39.95
3.2020年6月23日,我国“北斗三号”全国卫星导航系统星座部署完美收官。该导航系统应用了星载氢原子钟和铷原子钟。如图所示,下列有关铷的说法错误的是
A.属于金属元素 B.元素符号是Rb
C.相对原子质量为85.47 D.Rb+核外电子数为37
4.黄金搭档能补充钙、铁、锌、硒、维生素,其中的钙、铁、锌、硒是指
A.单质 B.分子 C.原子 D.元素
5.下列是几种粒子的结构示意图,有关说法不正确的是
A.②和③属于同种元素 B.①属于稀有气体元素
C.①和③的化学性质相似 D.④属于非金属元素
6.近日,我国科学家利用铜、锌同位素揭示月球中月核形成过程。铜、锌元素的相关信息如图,有关说法正确的是
A.锌的相对原子质量为65.38g
B.铜的原子序数是29
C.锌的核外电子数为35
D.铜在常温下都能和氧气反应
7.如图为元素周期表第三周期的一部分。下列说法中正确的是
A.硅元素的核电荷数为14
B.Al的相对原子质量是26.98g
C.它们都属于金属元素
D.镁的元素符号为mg
8.下列是四种微观粒子的结构示意图,下列有关各粒子的说法中不正确的是
A.②③属于同种元素 B.③是一种阳离子
C.只有④形成稳定结构 D.②容易失去电子
9.下列各组元素中,元素符号的第一个字母不相同的一组是
A.锰、镁 B.氖、钠 C.氯、钙 D.银、汞
10.居里夫人发现了放射性元素镭,荣获诺贝尔物理奖和化学奖。如图是镭元素在元素周期表中的信息,下列有关该元素说法正确的是
A.镭元素属于非金属元素 B.镭的元素符号为Ra
C.镭的相对原子质量为226g D.镭原子的中子数为88
11.钛有“太空金属”的美誉。在元素周期表中,钛元素的信息如图所示,对图中信息解释不正确的是
A.原子序数为22 B.核外电子数为47
C.元素符号为Ti D.相对原子质量为47.87
12.如图为某元素的粒子结构示意图,下列说法错误的是
A.该元素属于金属元素 B.该粒子为Na+
C.该粒子核外电子数是10 D.该元素位于元素周期表第二周期
二、非选择题,共5小题
13.写出前20号元素的元素符号:
①______;②______;③______;④______;⑤______;⑥______;⑦______;⑧______;⑨______;⑩______; ______; ______; ______; ______; ______; ______; ______; ______; ______; ______。
14.如图摘自元素周期表,请写出除汉字“氧”以外其它数字及字母的意义________。
15.在“宏观一微观一符号”之间建立联系,是学习化学的一种重要思维方式。如图是几种常见粒子的结构示意图和元素周期表的部分内容。回答下列问题。
(1)如图A、B、C、D中,共包含__________种元素。
(2)B、C、D三种粒子中与A粒子化学性质相似的是__________(填字母序号)。
(3)E为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是________(填序号)。
①原子序数X>Z ②Y和Z位于同一周期 ③Z原子核外电子具有相对稳定结构
16.元素周期表是学习和研究化学的重要工具(下图是元素周期表中1~18号元素的原子结构示意图)。请回答下列问题:
(1)11号元素和17号元素组成的合物的化学式为______,该物质由______和______构成(填粒子符号)。
(2)C、N、O三种元素处于同一周期的依据是______。
(3)请写出与氖原子核外电子排布相同的阳离子的离子符号______。(任写一种)
(4)碘元素元素符号为I,其原子结构示意图如图二所示,它与第三周期中______(填名称)元素的化学性质相似,原因是______。
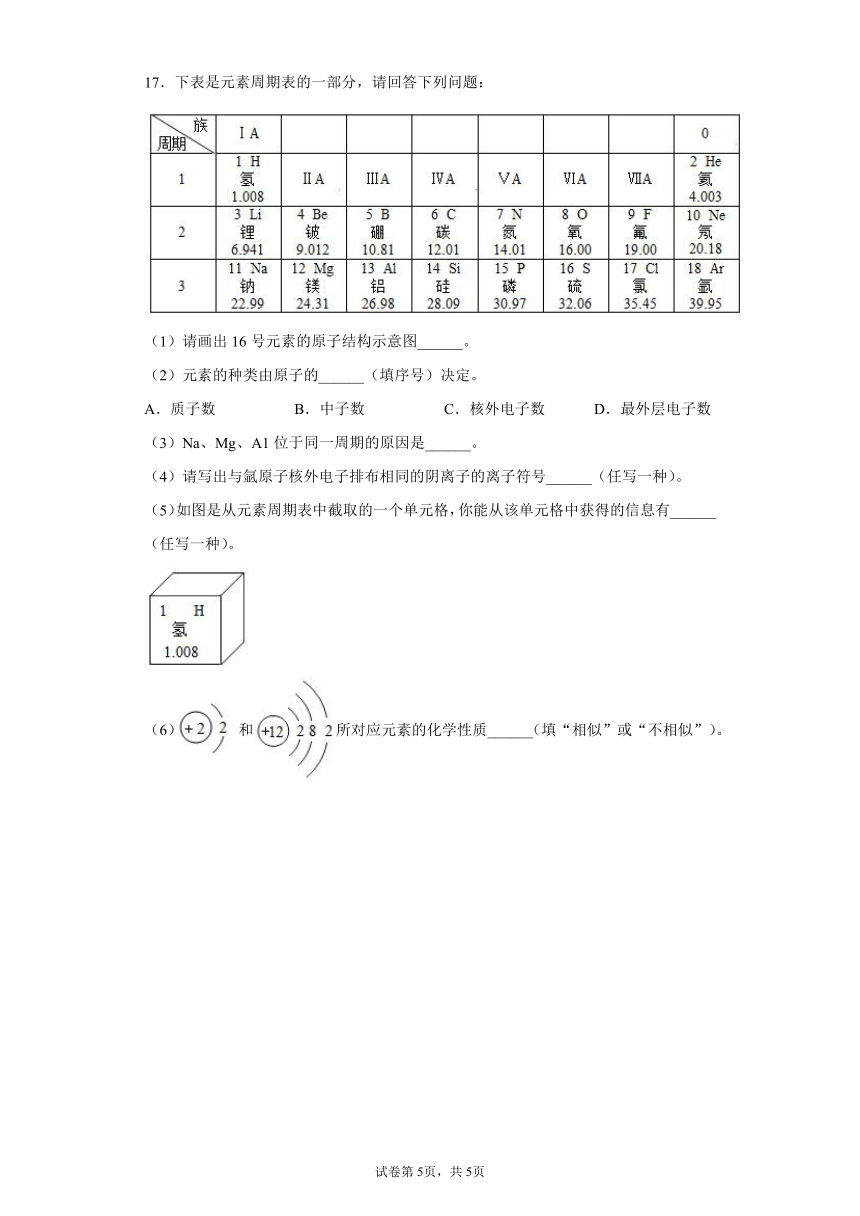
17.下表是元素周期表的一部分,请回答下列问题:
(1)请画出16号元素的原子结构示意图______。
(2)元素的种类由原子的______(填序号)决定。
A.质子数 B.中子数 C.核外电子数 D.最外层电子数
(3)Na、Mg、A1位于同一周期的原因是______。
(4)请写出与氩原子核外电子排布相同的阴离子的离子符号______(任写一种)。
(5)如图是从元素周期表中截取的一个单元格,你能从该单元格中获得的信息有______(任写一种)。
(6)和所对应元素的化学性质______(填“相似”或“不相似”)。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
物质中的营养元素都是以化合物(即化合态)的形式存在,所以食品中的钙、铁、锌等都是指食品中含有的相应元素,故选A。
2.A
【详解】
A、由汉字结构可知,氩属于非金属元素,错误;
B、氩的原子序数是18,正确;
C、氩原子最外层有8个电子,具有稳定结构,正确;
D、相对原子质量是39.95,正确。
故选A。
【点睛】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
3.D
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、由汉字结构可知,铷属于金属元素,此选项正确;
B、铷元素符号是Rb,此选项正确;
C、相对原子质量为85.47,此选项正确;
D、Rb原子序数为37,原子序数在数值上等于原子内的质子数,质子数=核外电子数,故核外电子数为37;Rb失去一个电子形成Rb+离子,则Rb+核外电子数为37-1=36,此选项错误。
故选D。
4.D
【详解】
其中的钙、铁、锌、硒不是以分子、原子、单质的形式存在,而是强调存在的元素,与具体形态无关。
故选D。
5.C
【详解】
A、不同种元素之间的本质区别是质子数不同,根据②③粒子结构示意图,质子数相同,属同种元素,说法正确;
B、稀有气体最外层均为8个电子(氦为2个),①是氦元素,属于稀有气体元素,说法正确;
C、①③最外层虽然都是稳定结构,①是氦原子,化学性质稳定,③是镁离子可得电子变成镁原子;说法错误;
D、在原子中质子数等于电子数,一般,金属元素最外层电子数小于4个,非金属元素最外层电子数大于或等于4个,稀有气体最外层电子数为8个(氦为2个),④是氯离子,得1个电子变成8 个电子稳定结构,因此原子的最外层电子数是7,大于4 个,属非金属元素;说法正确;
故选:C。
6.B
【详解】
A、锌的相对原子质量为65.38,单位不是“g”,故错误;
B、左上角的数字表示原子序数,由图示可知,铜的原子序数是29,故正确;
C、锌的质子数是30,则核外电子数也为30,故错误;
D、铜在常温下不能和氧气反应,故错误;
故选B。
7.A
【详解】
A、元素信息图中左上方的数字是原子序数,等于原子的核电荷数,由图可知,硅元素的原子序数为14,则硅元素的核电荷数为14,选项正确;
B、元素信息图中,正下方的数字就是元素原子的相对原子质量,由图可知,铝的相对原子质量为26.98,选项错误;
C、几种元素中,硅元素的名称带有石字旁,属于非金属元素,选项错误;
D、书写元素符号时,第一个字母大写,第二个字母小写,则镁的元素符号写为Mg,选项错误,故选A。
8.C
【详解】
A、②③的核电荷数都是11,核电荷数等于原子序数,11位元素是钠元素,不符合题意;
B、③的核电荷数是11,核外电子数是10,故其+1价阳离子,不符合题意;
C、①③④的最外层电子数都是8,电子完全充满最外层电子层,其都属于稳定结构,符合题意;
D、②的最外层电子数是1<4,易失去一个电子形成+1价阳离子,不符合题意。
故选C。
9.D
【详解】
A、锰的元素符号为Mn,镁的元素符号为Mg,元素符号的第一个字母相同,不符合题意;
B、氖的元素符号为Ne,钠的元素符号为Na,元素符号的第一个字母相同,不符合题意;
C、氯的元素符号为Cl,钙的元素符号为Ca,元素符号的第一个字母相同,不符合题意;
D、银的元素符号为Ag,汞的元素符号为Hg,元素符号的第一个字母不相同,符合题意。
故选D。
10.B
【详解】
A、由“钅”字旁可知,镭元素属于金属元素,不符合题意;
B、在元素周期表中,元素名称右上角的符号表示元素符号,故镭的元素符号为Ra,符合题意;
C、在元素周期表中,元素名称下方的数字表示相对原子质量,相对原子质量是一个比值,单位为“1”,常省略不写,故镭的相对原子质量为226,不符合题意;
D、在元素周期表中,元素名称左上角的数字表示原子序数,在原子中,原子序数=质子数=88,中子数=相对原子质量-质子数=226-88=138,不符合题意。
故选B。
11.B
【详解】
A. 根据元素周期表中的一格可知,左上角的数字为22,表示原子序数为22,故选项说法正确;
B. 根据元素周期表中的一格可知,左上角的数字为22,表示原子序数为22,根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为22,故选项说法错误;
C. 根据元素周期表中的一格可知,字母表示该元素的元素符号,元素符号为Ti,故选项说法正确;
D. 根据元素周期表中的一个小格所提供的信息可知,钛的相对原子质量是47. 87,故选项说法正确。
故选:B。
12.D
【详解】
A、质子数=原子序数,11号元素是钠元素,由“金”字旁可知,钠元素属于金属元素,不符合题意;
B、质子数大于核外电子数,表示阳离子,该粒子是钠原子失去最外层1个电子后形成的,表示为Na+,不符合题意;
C、由图可知,该粒子的核外电子数是2+8=10,不符合题意;
D、该粒子是钠原子失去最外层1个电子后形成的,该粒子的原子核外有三个电子层,位于第三周期,符合题意。
故选D。
13.H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
【分析】
元素符号的书写要注意:一个字母表示的要大写;二个字母表示的第一个字母大写,第二个字母小写。
【详解】
前二十号元素的名称和符号分别为
氢-H、氦-He、锂-Li、铍-Be、硼-B;
碳-C、氮-N、氧-O、氟-F、氖-Ne;
钠-Na、镁-Mg、铝-Al、硅-Si、磷-P;
硫-S、氯-Cl、氩-Ar、钾-K、钙-Ca。
【点睛】
元素符号是化学用语的基础,必须记熟。
14.8-核电荷数(或原子序数、质子数);O-元素符号;16.00-相对原子质量
【详解】
元素名称左上角的数字表示氧元素的质子数、核电荷数、原子序数是8;元素名称右上角的字母表示氧元素的元素符号是O;元素名称正下方的数字表示氧原子的性对原子质量是16.00。
15.3 C ②③
【详解】
(1)如图A、B、C、D中,共有9、13、17三种质子数,包含3种元素。
(2)B、C、D三种粒子中与A粒子化学性质相似的是C,因为AC最外层电子数相同,均为7。
(3) ①原子序数X小于Z,该选项说法不正确;
②Y和Z位于同一周期,该选项说法正确;
③Z与氦元素同族,其原子核外电子具有相对稳定结构,是因为最外层电子数是8,该选项说法正确。
故填:②③。
16.NaCl Na+ Cl- 电子层数相同,均为两层 (或) 氯 最外层电子数相同,均为7
【详解】
(1)11号元素为钠元素,17号元素为氯元素,组成的合物为氯化钠,其中钠元素为+1价,氯元素为-1价,氯化钠的化学式为NaCl,该物质由Na+和Cl-构成(填粒子符号)。
(2)C、N、O三种元素处于同一周期的依据是电子层数相同,均为两层。
(3)氖原子核外有2个电子层,从内到外电子数分别为2、8,与氖原子核外电子排布相同的阳离子的离子符号(或)。
(4)碘元素元素符号为I,其原子结构示意图如图二所示,原子中质子数=核外电子数,则X=53-2-8-18-18=7,它与第三周期中氯元素的化学性质相似,原因是最外层电子数相同,均为7。
17.
(1)
(2)A
(3)电子层数相同
(4)Cl-、S2-
(5)相对原子质量1.008
(6)不相似
【分析】
(1)
16号元素是硫元素,硫原子的原子结构示意图是;故填:。
(2)
元素的种类由原子的质子数决定,故填:A。
(3)
Na、Mg、Al位于同一周期的原因是它们原子的核外电子层数相同;故填:电子层数相同。
(4)
与氩原子核外电子排布相同的阴离子有氯离子、硫离子等,氯离子、硫离子的符号可以表示为Cl-、S2-;故填:Cl-、S2-。
(5)
如图是从元素周期表中截取的一个单元格,从该单元格中获取的信息有氢元素的原子序数、核电荷数、核内质子数都是1,相对原子质量为1.008,故填:相对原子质量1.008。
(6)
一个电子层,该层两个电子属于稳定结构,多个电子层最外层8个电子,属于稳定结构,故一个属于稳定结构,一个不稳定,故填:不相似。答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共12小题
1.每100mL牛奶中含钙86mg,这的“钙”应理解为
A.元素 B.原子 C.离子 D.分子
2.下图是氩元素在元素周期表中的有关信息,下列说法错误的是
A.属于金属元素
B.氩的原子序数是18
C.氩原子具有稳定结构
D.相对原子质量是39.95
3.2020年6月23日,我国“北斗三号”全国卫星导航系统星座部署完美收官。该导航系统应用了星载氢原子钟和铷原子钟。如图所示,下列有关铷的说法错误的是
A.属于金属元素 B.元素符号是Rb
C.相对原子质量为85.47 D.Rb+核外电子数为37
4.黄金搭档能补充钙、铁、锌、硒、维生素,其中的钙、铁、锌、硒是指
A.单质 B.分子 C.原子 D.元素
5.下列是几种粒子的结构示意图,有关说法不正确的是
A.②和③属于同种元素 B.①属于稀有气体元素
C.①和③的化学性质相似 D.④属于非金属元素
6.近日,我国科学家利用铜、锌同位素揭示月球中月核形成过程。铜、锌元素的相关信息如图,有关说法正确的是
A.锌的相对原子质量为65.38g
B.铜的原子序数是29
C.锌的核外电子数为35
D.铜在常温下都能和氧气反应
7.如图为元素周期表第三周期的一部分。下列说法中正确的是
A.硅元素的核电荷数为14
B.Al的相对原子质量是26.98g
C.它们都属于金属元素
D.镁的元素符号为mg
8.下列是四种微观粒子的结构示意图,下列有关各粒子的说法中不正确的是
A.②③属于同种元素 B.③是一种阳离子
C.只有④形成稳定结构 D.②容易失去电子
9.下列各组元素中,元素符号的第一个字母不相同的一组是
A.锰、镁 B.氖、钠 C.氯、钙 D.银、汞
10.居里夫人发现了放射性元素镭,荣获诺贝尔物理奖和化学奖。如图是镭元素在元素周期表中的信息,下列有关该元素说法正确的是
A.镭元素属于非金属元素 B.镭的元素符号为Ra
C.镭的相对原子质量为226g D.镭原子的中子数为88
11.钛有“太空金属”的美誉。在元素周期表中,钛元素的信息如图所示,对图中信息解释不正确的是
A.原子序数为22 B.核外电子数为47
C.元素符号为Ti D.相对原子质量为47.87
12.如图为某元素的粒子结构示意图,下列说法错误的是
A.该元素属于金属元素 B.该粒子为Na+
C.该粒子核外电子数是10 D.该元素位于元素周期表第二周期
二、非选择题,共5小题
13.写出前20号元素的元素符号:
①______;②______;③______;④______;⑤______;⑥______;⑦______;⑧______;⑨______;⑩______; ______; ______; ______; ______; ______; ______; ______; ______; ______; ______。
14.如图摘自元素周期表,请写出除汉字“氧”以外其它数字及字母的意义________。
15.在“宏观一微观一符号”之间建立联系,是学习化学的一种重要思维方式。如图是几种常见粒子的结构示意图和元素周期表的部分内容。回答下列问题。
(1)如图A、B、C、D中,共包含__________种元素。
(2)B、C、D三种粒子中与A粒子化学性质相似的是__________(填字母序号)。
(3)E为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是________(填序号)。
①原子序数X>Z ②Y和Z位于同一周期 ③Z原子核外电子具有相对稳定结构
16.元素周期表是学习和研究化学的重要工具(下图是元素周期表中1~18号元素的原子结构示意图)。请回答下列问题:
(1)11号元素和17号元素组成的合物的化学式为______,该物质由______和______构成(填粒子符号)。
(2)C、N、O三种元素处于同一周期的依据是______。
(3)请写出与氖原子核外电子排布相同的阳离子的离子符号______。(任写一种)
(4)碘元素元素符号为I,其原子结构示意图如图二所示,它与第三周期中______(填名称)元素的化学性质相似,原因是______。
17.下表是元素周期表的一部分,请回答下列问题:
(1)请画出16号元素的原子结构示意图______。
(2)元素的种类由原子的______(填序号)决定。
A.质子数 B.中子数 C.核外电子数 D.最外层电子数
(3)Na、Mg、A1位于同一周期的原因是______。
(4)请写出与氩原子核外电子排布相同的阴离子的离子符号______(任写一种)。
(5)如图是从元素周期表中截取的一个单元格,你能从该单元格中获得的信息有______(任写一种)。
(6)和所对应元素的化学性质______(填“相似”或“不相似”)。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
物质中的营养元素都是以化合物(即化合态)的形式存在,所以食品中的钙、铁、锌等都是指食品中含有的相应元素,故选A。
2.A
【详解】
A、由汉字结构可知,氩属于非金属元素,错误;
B、氩的原子序数是18,正确;
C、氩原子最外层有8个电子,具有稳定结构,正确;
D、相对原子质量是39.95,正确。
故选A。
【点睛】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
3.D
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、由汉字结构可知,铷属于金属元素,此选项正确;
B、铷元素符号是Rb,此选项正确;
C、相对原子质量为85.47,此选项正确;
D、Rb原子序数为37,原子序数在数值上等于原子内的质子数,质子数=核外电子数,故核外电子数为37;Rb失去一个电子形成Rb+离子,则Rb+核外电子数为37-1=36,此选项错误。
故选D。
4.D
【详解】
其中的钙、铁、锌、硒不是以分子、原子、单质的形式存在,而是强调存在的元素,与具体形态无关。
故选D。
5.C
【详解】
A、不同种元素之间的本质区别是质子数不同,根据②③粒子结构示意图,质子数相同,属同种元素,说法正确;
B、稀有气体最外层均为8个电子(氦为2个),①是氦元素,属于稀有气体元素,说法正确;
C、①③最外层虽然都是稳定结构,①是氦原子,化学性质稳定,③是镁离子可得电子变成镁原子;说法错误;
D、在原子中质子数等于电子数,一般,金属元素最外层电子数小于4个,非金属元素最外层电子数大于或等于4个,稀有气体最外层电子数为8个(氦为2个),④是氯离子,得1个电子变成8 个电子稳定结构,因此原子的最外层电子数是7,大于4 个,属非金属元素;说法正确;
故选:C。
6.B
【详解】
A、锌的相对原子质量为65.38,单位不是“g”,故错误;
B、左上角的数字表示原子序数,由图示可知,铜的原子序数是29,故正确;
C、锌的质子数是30,则核外电子数也为30,故错误;
D、铜在常温下不能和氧气反应,故错误;
故选B。
7.A
【详解】
A、元素信息图中左上方的数字是原子序数,等于原子的核电荷数,由图可知,硅元素的原子序数为14,则硅元素的核电荷数为14,选项正确;
B、元素信息图中,正下方的数字就是元素原子的相对原子质量,由图可知,铝的相对原子质量为26.98,选项错误;
C、几种元素中,硅元素的名称带有石字旁,属于非金属元素,选项错误;
D、书写元素符号时,第一个字母大写,第二个字母小写,则镁的元素符号写为Mg,选项错误,故选A。
8.C
【详解】
A、②③的核电荷数都是11,核电荷数等于原子序数,11位元素是钠元素,不符合题意;
B、③的核电荷数是11,核外电子数是10,故其+1价阳离子,不符合题意;
C、①③④的最外层电子数都是8,电子完全充满最外层电子层,其都属于稳定结构,符合题意;
D、②的最外层电子数是1<4,易失去一个电子形成+1价阳离子,不符合题意。
故选C。
9.D
【详解】
A、锰的元素符号为Mn,镁的元素符号为Mg,元素符号的第一个字母相同,不符合题意;
B、氖的元素符号为Ne,钠的元素符号为Na,元素符号的第一个字母相同,不符合题意;
C、氯的元素符号为Cl,钙的元素符号为Ca,元素符号的第一个字母相同,不符合题意;
D、银的元素符号为Ag,汞的元素符号为Hg,元素符号的第一个字母不相同,符合题意。
故选D。
10.B
【详解】
A、由“钅”字旁可知,镭元素属于金属元素,不符合题意;
B、在元素周期表中,元素名称右上角的符号表示元素符号,故镭的元素符号为Ra,符合题意;
C、在元素周期表中,元素名称下方的数字表示相对原子质量,相对原子质量是一个比值,单位为“1”,常省略不写,故镭的相对原子质量为226,不符合题意;
D、在元素周期表中,元素名称左上角的数字表示原子序数,在原子中,原子序数=质子数=88,中子数=相对原子质量-质子数=226-88=138,不符合题意。
故选B。
11.B
【详解】
A. 根据元素周期表中的一格可知,左上角的数字为22,表示原子序数为22,故选项说法正确;
B. 根据元素周期表中的一格可知,左上角的数字为22,表示原子序数为22,根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为22,故选项说法错误;
C. 根据元素周期表中的一格可知,字母表示该元素的元素符号,元素符号为Ti,故选项说法正确;
D. 根据元素周期表中的一个小格所提供的信息可知,钛的相对原子质量是47. 87,故选项说法正确。
故选:B。
12.D
【详解】
A、质子数=原子序数,11号元素是钠元素,由“金”字旁可知,钠元素属于金属元素,不符合题意;
B、质子数大于核外电子数,表示阳离子,该粒子是钠原子失去最外层1个电子后形成的,表示为Na+,不符合题意;
C、由图可知,该粒子的核外电子数是2+8=10,不符合题意;
D、该粒子是钠原子失去最外层1个电子后形成的,该粒子的原子核外有三个电子层,位于第三周期,符合题意。
故选D。
13.H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
【分析】
元素符号的书写要注意:一个字母表示的要大写;二个字母表示的第一个字母大写,第二个字母小写。
【详解】
前二十号元素的名称和符号分别为
氢-H、氦-He、锂-Li、铍-Be、硼-B;
碳-C、氮-N、氧-O、氟-F、氖-Ne;
钠-Na、镁-Mg、铝-Al、硅-Si、磷-P;
硫-S、氯-Cl、氩-Ar、钾-K、钙-Ca。
【点睛】
元素符号是化学用语的基础,必须记熟。
14.8-核电荷数(或原子序数、质子数);O-元素符号;16.00-相对原子质量
【详解】
元素名称左上角的数字表示氧元素的质子数、核电荷数、原子序数是8;元素名称右上角的字母表示氧元素的元素符号是O;元素名称正下方的数字表示氧原子的性对原子质量是16.00。
15.3 C ②③
【详解】
(1)如图A、B、C、D中,共有9、13、17三种质子数,包含3种元素。
(2)B、C、D三种粒子中与A粒子化学性质相似的是C,因为AC最外层电子数相同,均为7。
(3) ①原子序数X小于Z,该选项说法不正确;
②Y和Z位于同一周期,该选项说法正确;
③Z与氦元素同族,其原子核外电子具有相对稳定结构,是因为最外层电子数是8,该选项说法正确。
故填:②③。
16.NaCl Na+ Cl- 电子层数相同,均为两层 (或) 氯 最外层电子数相同,均为7
【详解】
(1)11号元素为钠元素,17号元素为氯元素,组成的合物为氯化钠,其中钠元素为+1价,氯元素为-1价,氯化钠的化学式为NaCl,该物质由Na+和Cl-构成(填粒子符号)。
(2)C、N、O三种元素处于同一周期的依据是电子层数相同,均为两层。
(3)氖原子核外有2个电子层,从内到外电子数分别为2、8,与氖原子核外电子排布相同的阳离子的离子符号(或)。
(4)碘元素元素符号为I,其原子结构示意图如图二所示,原子中质子数=核外电子数,则X=53-2-8-18-18=7,它与第三周期中氯元素的化学性质相似,原因是最外层电子数相同,均为7。
17.
(1)
(2)A
(3)电子层数相同
(4)Cl-、S2-
(5)相对原子质量1.008
(6)不相似
【分析】
(1)
16号元素是硫元素,硫原子的原子结构示意图是;故填:。
(2)
元素的种类由原子的质子数决定,故填:A。
(3)
Na、Mg、Al位于同一周期的原因是它们原子的核外电子层数相同;故填:电子层数相同。
(4)
与氩原子核外电子排布相同的阴离子有氯离子、硫离子等,氯离子、硫离子的符号可以表示为Cl-、S2-;故填:Cl-、S2-。
(5)
如图是从元素周期表中截取的一个单元格,从该单元格中获取的信息有氢元素的原子序数、核电荷数、核内质子数都是1,相对原子质量为1.008,故填:相对原子质量1.008。
(6)
一个电子层,该层两个电子属于稳定结构,多个电子层最外层8个电子,属于稳定结构,故一个属于稳定结构,一个不稳定,故填:不相似。答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
