2.2重要的酸 精选练习(含答案)
文档属性
| 名称 | 2.2重要的酸 精选练习(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 282.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-10-18 00:00:00 | ||
图片预览

文档简介
2021-2022学年华师大版九年级重要的酸的精选练习
一.选择题(共9小题)
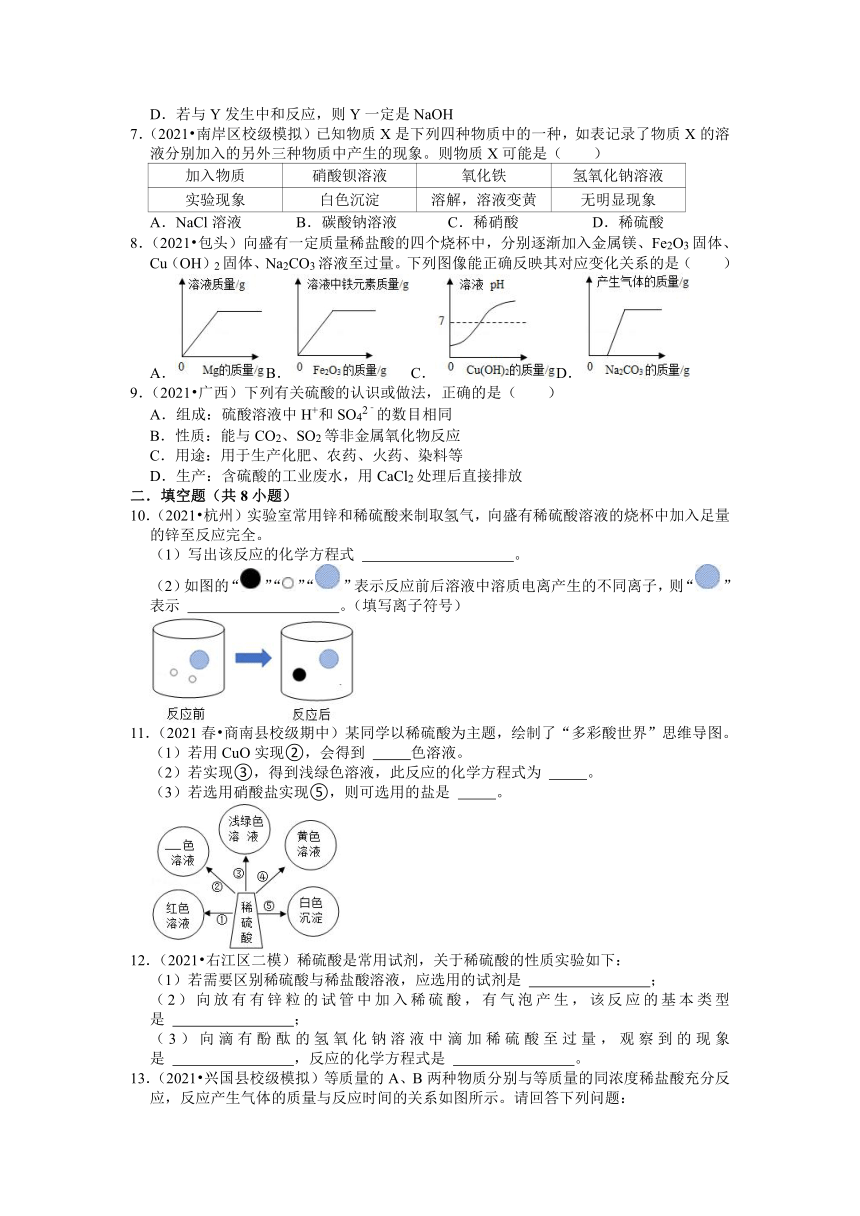
1.(2021 福建)甲、乙、丙三种物质有如下转化关系:甲乙丙。在不断搅拌下,往装有甲溶液的容器中逐滴加入稀盐酸依次发生了①②反应,同时测定容器中液体的透光度强度(液体越浑浊,透光强度越小),结果如图。下列分析错误的是( )
A.乙难溶于水
B.甲可能是NaOH
C.QM段对应的反应是②
D.E、F对应的液体组成不同
2.(2021 台州)盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )
A.B.C.D.
3.(2021 邵阳)推理是学习化学的一种常用方法,下列推理正确的是( )
A.阴离子带负电荷,则带负电荷的粒子一定是阴离子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素
D.碳酸盐与盐酸反应都有气体生成,则与盐酸反应有气体生成的物质一定是碳酸盐
4.(2021 黄石)思维导图是知识整理的重要工具,如图是某思维导图的一部分,可以填入括号中的是( )
A.能与活泼非金属反应 B.能与某些酸反应
C.能与非金属氧化物反应 D.能与某些盐反应
5.(2021 青海)下列物质不能与稀盐酸反应的是( )
A.铜 B.氧化铜 C.氢氧化钙 D.碳酸氢钠
6.(2021 深圳)小明在探究稀硫酸性质时,下列说法正确的是( )
A.稀H2SO4与紫色石蕊试液反应后,溶液变蓝
B.若能与X反应制取H2,则X是Cu
C.和金属氧化物反应,有盐和水生成
D.若与Y发生中和反应,则Y一定是NaOH
7.(2021 南岸区校级模拟)已知物质X是下列四种物质中的一种,如表记录了物质X的溶液分别加入的另外三种物质中产生的现象。则物质X可能是( )
加入物质 硝酸钡溶液 氧化铁 氢氧化钠溶液
实验现象 白色沉淀 溶解,溶液变黄 无明显现象
A.NaCl溶液 B.碳酸钠溶液 C.稀硝酸 D.稀硫酸
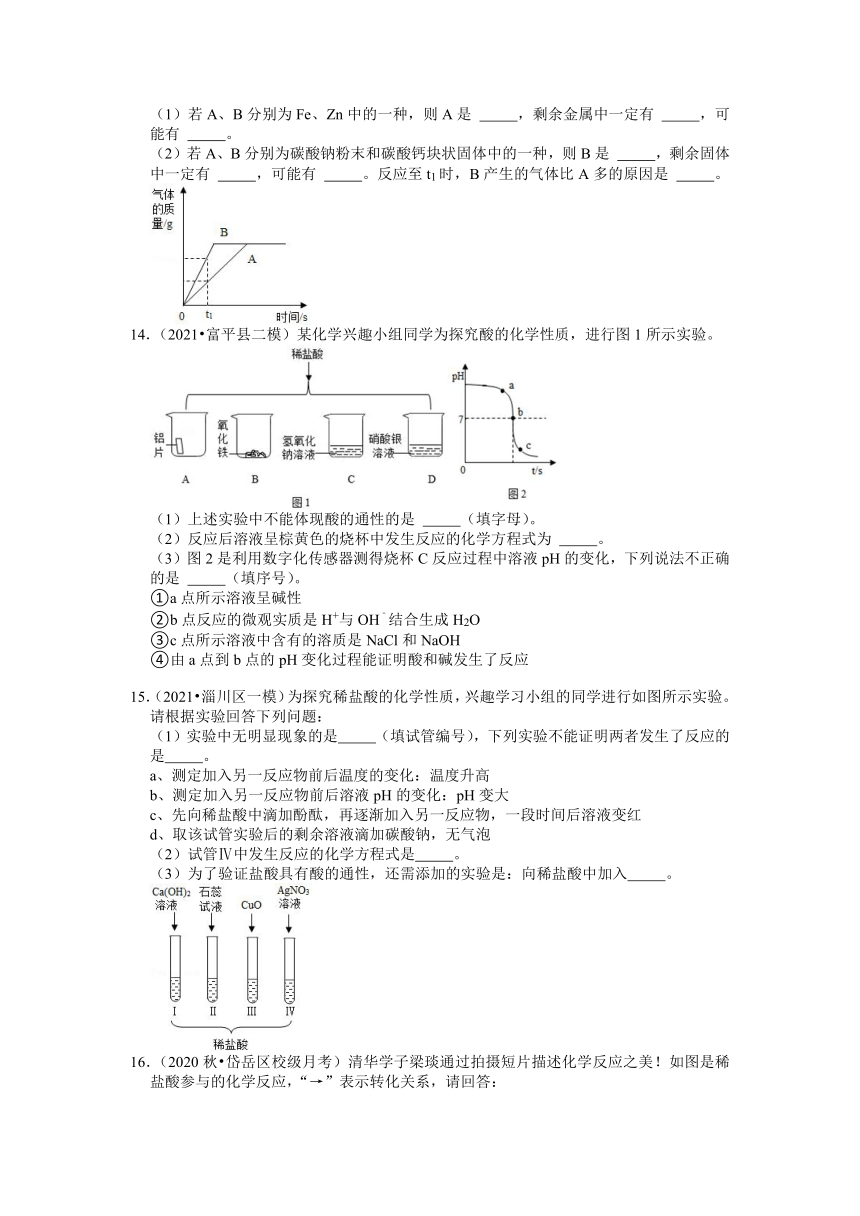
8.(2021 包头)向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe2O3固体、Cu(OH)2固体、Na2CO3溶液至过量。下列图像能正确反映其对应变化关系的是( )
A.B.C.D.
9.(2021 广西)下列有关硫酸的认识或做法,正确的是( )
A.组成:硫酸溶液中H+和SO42﹣的数目相同
B.性质:能与CO2、SO2等非金属氧化物反应
C.用途:用于生产化肥、农药、火药、染料等
D.生产:含硫酸的工业废水,用CaCl2处理后直接排放
二.填空题(共8小题)
10.(2021 杭州)实验室常用锌和稀硫酸来制取氢气,向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式 。
(2)如图的“”“”“”表示反应前后溶液中溶质电离产生的不同离子,则“”表示 。(填写离子符号)
11.(2021春 商南县校级期中)某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若用CuO实现②,会得到 色溶液。
(2)若实现③,得到浅绿色溶液,此反应的化学方程式为 。
(3)若选用硝酸盐实现⑤,则可选用的盐是 。
12.(2021 右江区二模)稀硫酸是常用试剂,关于稀硫酸的性质实验如下:
(1)若需要区别稀硫酸与稀盐酸溶液,应选用的试剂是 ;
(2)向放有有锌粒的试管中加入稀硫酸,有气泡产生,该反应的基本类型是 ;
(3)向滴有酚酞的氢氧化钠溶液中滴加稀硫酸至过量,观察到的现象是 ,反应的化学方程式是 。
13.(2021 兴国县校级模拟)等质量的A、B两种物质分别与等质量的同浓度稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图所示。请回答下列问题:
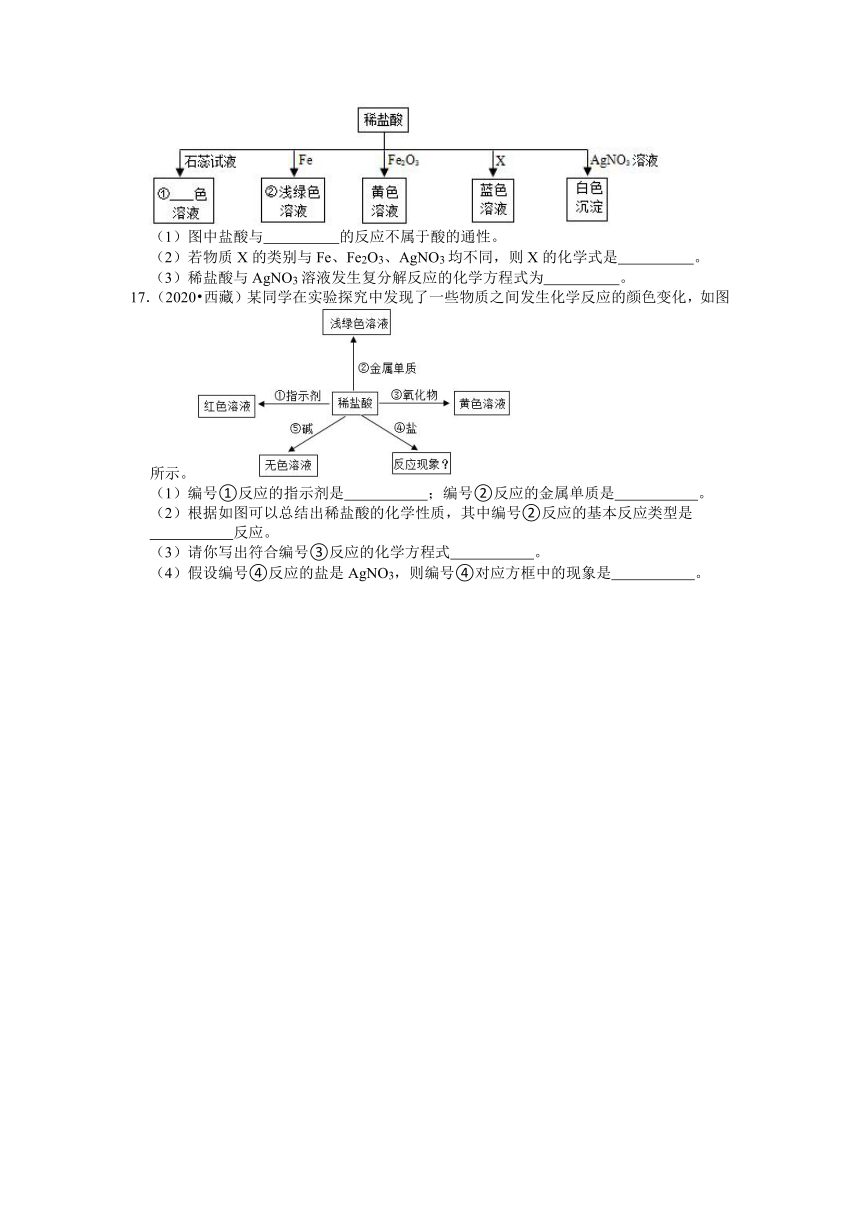
(1)若A、B分别为Fe、Zn中的一种,则A是 ,剩余金属中一定有 ,可能有 。
(2)若A、B分别为碳酸钠粉末和碳酸钙块状固体中的一种,则B是 ,剩余固体中一定有 ,可能有 。反应至t1时,B产生的气体比A多的原因是 。
14.(2021 富平县二模)某化学兴趣小组同学为探究酸的化学性质,进行图1所示实验。
(1)上述实验中不能体现酸的通性的是 (填字母)。
(2)反应后溶液呈棕黄色的烧杯中发生反应的化学方程式为 。
(3)图2是利用数字化传感器测得烧杯C反应过程中溶液pH的变化,下列说法不正确的是 (填序号)。
①a点所示溶液呈碱性
②b点反应的微观实质是H+与OH﹣结合生成H2O
③c点所示溶液中含有的溶质是NaCl和NaOH
④由a点到b点的pH变化过程能证明酸和碱发生了反应
15.(2021 淄川区一模)为探究稀盐酸的化学性质,兴趣学习小组的同学进行如图所示实验。请根据实验回答下列问题:
(1)实验中无明显现象的是 (填试管编号),下列实验不能证明两者发生了反应的是 。
a、测定加入另一反应物前后温度的变化:温度升高
b、测定加入另一反应物前后溶液pH的变化:pH变大
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(2)试管Ⅳ中发生反应的化学方程式是 。
(3)为了验证盐酸具有酸的通性,还需添加的实验是:向稀盐酸中加入 。
16.(2020秋 岱岳区校级月考)清华学子梁琰通过拍摄短片描述化学反应之美!如图是稀盐酸参与的化学反应,“→”表示转化关系,请回答:
(1)图中盐酸与 的反应不属于酸的通性。
(2)若物质X的类别与Fe、Fe2O3、AgNO3均不同,则X的化学式是 。
(3)稀盐酸与AgNO3溶液发生复分解反应的化学方程式为 。
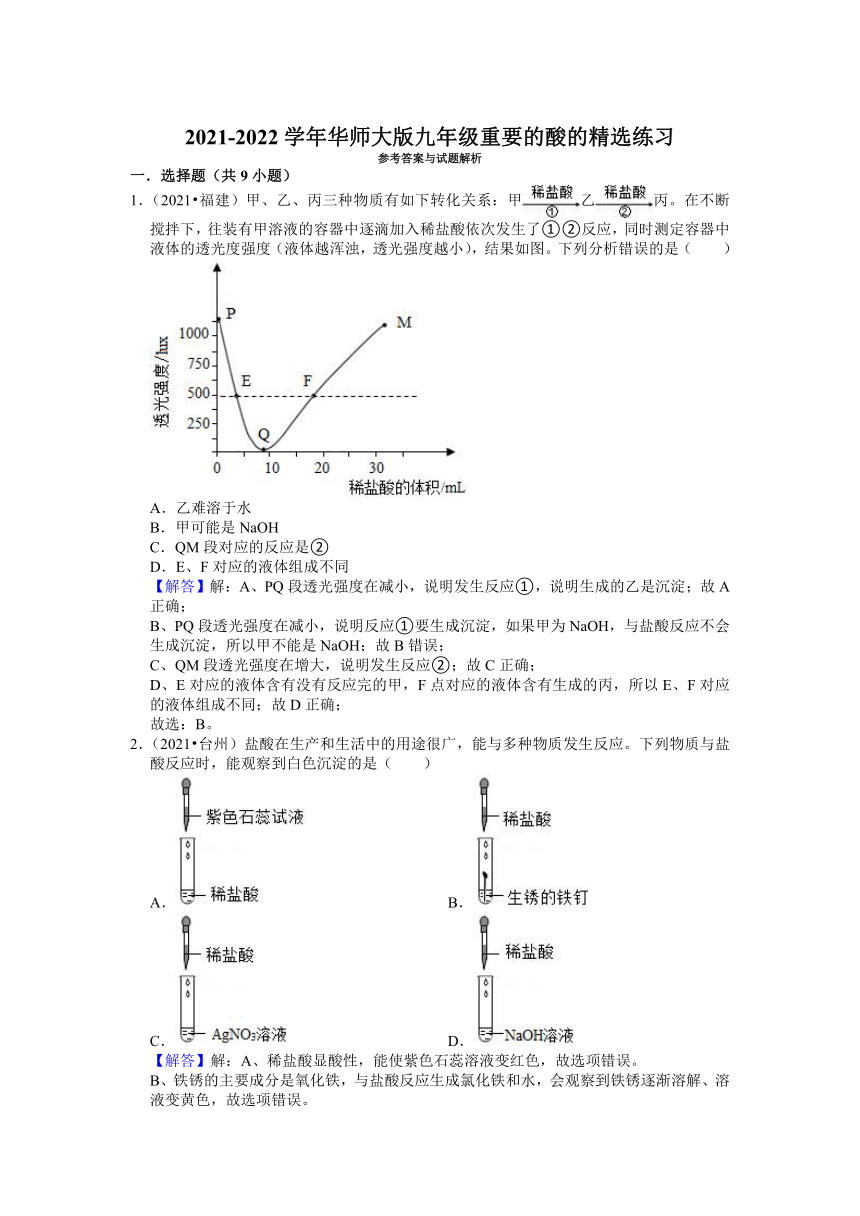
17.(2020 西藏)某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是 ;编号②反应的金属单质是 。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是
反应。
(3)请你写出符合编号③反应的化学方程式 。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是 。
2021-2022学年华师大版九年级重要的酸的精选练习
参考答案与试题解析
一.选择题(共9小题)
1.(2021 福建)甲、乙、丙三种物质有如下转化关系:甲乙丙。在不断搅拌下,往装有甲溶液的容器中逐滴加入稀盐酸依次发生了①②反应,同时测定容器中液体的透光度强度(液体越浑浊,透光强度越小),结果如图。下列分析错误的是( )
A.乙难溶于水
B.甲可能是NaOH
C.QM段对应的反应是②
D.E、F对应的液体组成不同
【解答】解:A、PQ段透光强度在减小,说明发生反应①,说明生成的乙是沉淀;故A正确;
B、PQ段透光强度在减小,说明反应①要生成沉淀,如果甲为NaOH,与盐酸反应不会生成沉淀,所以甲不能是NaOH;故B错误;
C、QM段透光强度在增大,说明发生反应②;故C正确;
D、E对应的液体含有没有反应完的甲,F点对应的液体含有生成的丙,所以E、F对应的液体组成不同;故D正确;
故选:B。
2.(2021 台州)盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )
A. B.
C. D.
【解答】解:A、稀盐酸显酸性,能使紫色石蕊溶液变红色,故选项错误。
B、铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,会观察到铁锈逐渐溶解、溶液变黄色,故选项错误。
C、稀盐酸能与硝酸银溶液反应生成氯化银沉淀和硝酸,能观察到白色沉淀,故选项正确。
D、稀盐酸与氢氧化钠反应生成氯化钠和水,但无明显现象,故选项错误。
故选:C。
3.(2021 邵阳)推理是学习化学的一种常用方法,下列推理正确的是( )
A.阴离子带负电荷,则带负电荷的粒子一定是阴离子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素
D.碳酸盐与盐酸反应都有气体生成,则与盐酸反应有气体生成的物质一定是碳酸盐
【解答】解:A、阴离子带负电荷,但带负电荷的粒子不一定是阴离子,也可能是电子等,故选项推理错误。
B、单质只含一种元素,但只含一种元素的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,故选项推理错误。
C、元素是质子数(即核电荷数)相同的一类原子的总称,元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素,故选项推理正确。
D、碳酸盐与盐酸反应都有气体生成,但与盐酸反应有气体生成的物质不一定是碳酸盐,也可能是活泼金属等,故选项推理错误。
故选:C。
4.(2021 黄石)思维导图是知识整理的重要工具,如图是某思维导图的一部分,可以填入括号中的是( )
A.能与活泼非金属反应 B.能与某些酸反应
C.能与非金属氧化物反应 D.能与某些盐反应
【解答】解:酸能与酸碱指示剂作用,能与活泼金属反应生成盐和氢气,能与金属氧化物反应生成盐和水,能与碱反应生成盐和水,能与某些盐反应反应新酸和新盐,可以填入括号中的是能与某些盐反应。
故选:D。
5.(2021 青海)下列物质不能与稀盐酸反应的是( )
A.铜 B.氧化铜 C.氢氧化钙 D.碳酸氢钠
【解答】解:A、在金属活动性顺序中,铜的位置排在氢的后面,不能与稀盐酸反应,故选项正确。
B、氧化铜能与稀盐酸反应生成氯化铜和水,故选项错误。
C、氢氧化钙能与稀盐酸反应生成氯化钙和水,故选项错误。
D、碳酸氢钠能与稀盐酸反应生成氯化钠、水和二氧化碳,故选项错误。
故选:A。
6.(2021 深圳)小明在探究稀硫酸性质时,下列说法正确的是( )
A.稀H2SO4与紫色石蕊试液反应后,溶液变蓝
B.若能与X反应制取H2,则X是Cu
C.和金属氧化物反应,有盐和水生成
D.若与Y发生中和反应,则Y一定是NaOH
【解答】解:A、稀H2SO4与紫色石蕊试液反应后,溶液变红色,故选项说法错误。
B、若能与X反应制取H2,则X不可能是Cu,在金属活动性顺序中,铜的位置排在氢的后面,不与稀硫酸反应,故选项说法错误。
C、稀硫酸和金属氧化物反应,有盐和水生成,故选项说法正确。
D、若与Y发生中和反应,但Y不一定是NaOH,也可能是氢氧化钙等碱,故选项说法错误。
故选:C。
7.(2021 南岸区校级模拟)已知物质X是下列四种物质中的一种,如表记录了物质X的溶液分别加入的另外三种物质中产生的现象。则物质X可能是( )
加入物质 硝酸钡溶液 氧化铁 氢氧化钠溶液
实验现象 白色沉淀 溶解,溶液变黄 无明显现象
A.NaCl溶液 B.碳酸钠溶液 C.稀硝酸 D.稀硫酸
【解答】解:A、NaCl溶液与硝酸钡溶液结合成分没有沉淀或气体或水生成,不能发生复分解反应,故选项错误。
B、碳酸钠溶液与硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠,与氧化铁不反应,故选项错误。
C、稀硝酸与硝酸钡溶液不反应,故选项错误。
D、稀硫酸能与硝酸钡溶液反应生成硫酸钡沉淀和硝酸;与氧化铁反应生成硫酸铁和水,氧化铁溶解,溶液变黄;与氢氧化钠溶液反应生成硫酸钠和水,无明显现象;故选项正确。
故选:D。
8.(2021 包头)向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe2O3固体、Cu(OH)2固体、Na2CO3溶液至过量。下列图像能正确反映其对应变化关系的是( )
A. B.
C. D.
【解答】解:A、镁和盐酸反应生成氯化镁和氢气,反应前的溶液是稀盐酸,所以溶液增加的起点不能从零开始,故A错误;
B、氧化铁和盐酸反应生成氯化铁和水,反应前的溶液中不含铁元素,随着反应的进行,溶液中铁元素的质量逐渐增加,盐酸完全反应后,铁元素质量不变,故B正确;
C、氢氧化铜和盐酸反应生成氯化铜和水,氢氧化铜难溶于水,盐酸消耗完后,溶液的pH值不会大于7,故C错误;
D、碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,二氧化碳气体的质量应该从零开始,故D错误。
故选:B。
9.(2021 广西)下列有关硫酸的认识或做法,正确的是( )
A.组成:硫酸溶液中H+和SO42﹣的数目相同
B.性质:能与CO2、SO2等非金属氧化物反应
C.用途:用于生产化肥、农药、火药、染料等
D.生产:含硫酸的工业废水,用CaCl2处理后直接排放
【解答】解:A、硫酸溶液中的正负电荷代数和为零,所以H+和SO42﹣的数目之比是2:1,故A错误;
B、酸会与金属氧化物反应,不会与非金属氧化物反应,故B错误;
C、硫酸用于生产化肥、农药、火药、染料等,故C正确;
D、硫酸不会与氯化钙反应,含硫酸的工业废水,用氢氧化钙处理后直接排放,故D错误。
故选:C。
二.填空题(共8小题)
10.(2021 杭州)实验室常用锌和稀硫酸来制取氢气,向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式 Zn+H2SO4=ZnSO4+H2↑ 。
(2)如图的“”“”“”表示反应前后溶液中溶质电离产生的不同离子,则“”表示 SO42﹣ 。(填写离子符号)
【解答】解:(1)锌和稀硫酸反应生成硫酸锌和氢气,方程式为:Zn+H2SO4=ZnSO4+H2↑,故填:Zn+H2SO4=ZnSO4+H2↑;
(2)反应前溶液是稀硫酸,其中溶质电离产生的离子为氢离子和硫酸根离子,反应完全后溶液是硫酸锌溶液,其中电离产生的离子是锌离子和硫酸根离子,反应前后不变的离子是硫酸根离子,故“”表示硫酸根离子,故填:SO42﹣。
11.(2021春 商南县校级期中)某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若用CuO实现②,会得到 蓝 色溶液。
(2)若实现③,得到浅绿色溶液,此反应的化学方程式为 Fe+H2SO4═FeSO4+H2↑ 。
(3)若选用硝酸盐实现⑤,则可选用的盐是 Ba(NO3)2 。
【解答】解:(1)若用CuO实现②,稀硫酸和氧化铜反应生成硫酸铜和水,会得到蓝色溶液。
故填:蓝。
(2)若实现③,得到浅绿色溶液,则稀硫酸和铁反应生成硫酸亚铁和氢气,此反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑。
故填:Fe+H2SO4═FeSO4+H2↑。
(3)若选用硝酸盐实现⑤,则可选用的盐是硝酸钡,是因为硝酸钡能和稀硫酸反应生成硫酸钡沉淀和硝酸。
故填:Ba(NO3)2。
12.(2021 右江区二模)稀硫酸是常用试剂,关于稀硫酸的性质实验如下:
(1)若需要区别稀硫酸与稀盐酸溶液,应选用的试剂是 氯化钡溶液(合理即可) ;
(2)向放有有锌粒的试管中加入稀硫酸,有气泡产生,该反应的基本类型是 置换反应 ;
(3)向滴有酚酞的氢氧化钠溶液中滴加稀硫酸至过量,观察到的现象是 溶液由红色变为无色 ,反应的化学方程式是 2NaOH+H2SO4═Na2SO4+2H2O 。
【解答】解:(1)若需要区别稀硫酸与稀盐酸溶液,应选用的试剂是氯化钡溶液,稀硫酸能与氯化钡溶液反应生成硫酸钡白色沉淀,稀盐酸不能与氯化钡溶液反应,能出现两种明显不同的现象,可以鉴别。
(2)向放有有锌粒的试管中加入稀硫酸,有气泡产生,是因为锌与硫酸反应生成硫酸锌和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
(3)滴有酚酞溶液的氢氧化钠溶液显红色,无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,逐滴滴入稀硫酸,至恰好完全反应,溶液显中性,溶液由红色变为无色,继续滴加稀硫酸,溶液显酸性,溶液颜色为无色。
稀硫酸与氢氧化钠溶液反应生成硫酸钠和水,反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O。
故答案为:
(1)氯化钡溶液(合理即可);
(2)置换反应;
(3)溶液由红色变为无色;2NaOH+H2SO4═Na2SO4+2H2O。
13.(2021 兴国县校级模拟)等质量的A、B两种物质分别与等质量的同浓度稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图所示。请回答下列问题:
(1)若A、B分别为Fe、Zn中的一种,则A是 铁 ,剩余金属中一定有 铁 ,可能有 锌 。
(2)若A、B分别为碳酸钠粉末和碳酸钙块状固体中的一种,则B是 碳酸钠粉末。 ,剩余固体中一定有 碳酸钙 ,可能有 碳酸钠 。反应至t1时,B产生的气体比A多的原因是 碳酸钠粉末与稀盐酸的接触面积大,反应速率快 。
【解答】解:(1)若A、B分别为Fe、Zn中的一种,锌的活动性比铁强,反应速率快,反应时间短;等质量的 A、B 两种金属分别与足量的同浓度的稀盐酸充分反应,铁生成氢气的质量比锌多,则A是铁;利用方程式,根据反应的质量比可知生成等质量的氢气,铁与氢气的质量比为56:2,锌与氢气的质量比为65:2,故反应后剩余金属中一定有铁,可能有锌;故答案为:铁;铁;锌;
(2)反物的接触面积越大,反应越剧烈,若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,则B是碳酸钠粉末;利用方程式,根据反应的质量比可知生成等质量的二氧化碳,碳酸钠与二氧化碳的质量比为106:44,碳酸钙与二氧化碳的质量比为100:44,故反应后剩余固体中一定有碳酸钙,可能有碳酸钠;反应至t1时,B 产生的气体比A多,是因为碳酸钠粉末与稀盐酸的接触面积大,反应速率快。故答案为:碳酸钠粉末;碳酸钙;碳酸钠;碳酸钠粉末与稀盐酸的接触面积大,反应速率快。
14.(2021 富平县二模)某化学兴趣小组同学为探究酸的化学性质,进行图1所示实验。
(1)上述实验中不能体现酸的通性的是 D (填字母)。
(2)反应后溶液呈棕黄色的烧杯中发生反应的化学方程式为 Fe2O3+6HCl═2FeCl3+3H2O 。
(3)图2是利用数字化传感器测得烧杯C反应过程中溶液pH的变化,下列说法不正确的是 ③ (填序号)。
①a点所示溶液呈碱性
②b点反应的微观实质是H+与OH﹣结合生成H2O
③c点所示溶液中含有的溶质是NaCl和NaOH
④由a点到b点的pH变化过程能证明酸和碱发生了反应
【解答】解:(1)上述实验中不能体现酸的通性的是D,是因为盐也能和硝酸银反应,例如氯化钠和硝酸银反应生成白色沉淀氯化银和硝酸钠。
故填:D。
(2)反应后溶液呈棕黄色的烧杯中,氧化铁和稀盐酸反应生成氯化铁和水,发生反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O。
故填:Fe2O3+6HCl═2FeCl3+3H2O。
(3)①a点所示溶液pH大于7,呈碱性,该选项说法正确;
②b点反应的微观实质是H+与OH﹣结合生成H2O,该选项说法正确;
③c点所示溶液中含有的溶质是NaCl和氯化氢,该选项说法不正确;
④由a点到b点的pH变化过程能证明酸和碱发生了反应,是因为碱消失,该选项说法正确。
故填:③。
15.(2021 淄川区一模)为探究稀盐酸的化学性质,兴趣学习小组的同学进行如图所示实验。请根据实验回答下列问题:
(1)实验中无明显现象的是 Ⅰ (填试管编号),下列实验不能证明两者发生了反应的是 。
a、测定加入另一反应物前后温度的变化:温度升高
b、测定加入另一反应物前后溶液pH的变化:pH变大
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(2)试管Ⅳ中发生反应的化学方程式是 AgNO3+HCl=AgCl↓+HNO3 。
(3)为了验证盐酸具有酸的通性,还需添加的实验是:向稀盐酸中加入 金属锌 。
【解答】解:(1)氢氧化钙和盐酸反应生成氯化钙和水,实验中无明显现象;
a、测定加入另一反应物前后温度的变化:温度升高,说明二者混合放热,能证明发生反应;
b、测定加入另一反应物前后溶液pH的变化:pH变大,氢氧化钙溶液中含有水,盐酸中加入水,酸性减弱,pH增大,不能证明发生反应;
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红,说明开始氢氧化钙的碱性没有体现出来,是盐酸和氢氧化钙反应,能证明发生反应;
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡,说明盐酸已经没有了,能证明发生反应;
故填:Ⅰ;b;
(2)试管Ⅳ中盐酸和硝酸银反应生成氯化银沉淀和硝酸,发生反应的化学方程式是AgNO3+HCl=AgCl↓+HNO3,故填:AgNO3+HCl=AgCl↓+HNO3;
(3)为了验证盐酸具有酸的通性,还需添加盐酸与金属的反应,故可以向稀盐酸中加入金属锌,故填:金属锌。
16.(2020秋 岱岳区校级月考)清华学子梁琰通过拍摄短片描述化学反应之美!如图是稀盐酸参与的化学反应,“→”表示转化关系,请回答:
(1)图中盐酸与 硝酸银溶液 的反应不属于酸的通性。
(2)若物质X的类别与Fe、Fe2O3、AgNO3均不同,则X的化学式是 Cu(OH)2 。
(3)稀盐酸与AgNO3溶液发生复分解反应的化学方程式为 HCl+AgNO3═HNO3+AgCl↓ 。
【解答】解:(1)图中盐酸与硝酸银溶液的反应不属于酸的通性,如硝酸不能与硝酸银溶液反应。
(2)若物质X的类别与Fe、Fe2O3、AgNO3均不同,由酸的化学性质,X应为碱,生成蓝色溶液,说明生成了铜盐的水溶液,则X为氢氧化铜,其化学式为Cu(OH)2。
(3)稀盐酸与AgNO3溶液反应生成氯化银沉淀和硝酸,反应的化学方程式为HCl+AgNO3═HNO3+AgCl↓。
故答案为:
(1)硝酸银溶液;
(2)Cu(OH)2;
(3)HCl+AgNO3═HNO3+AgCl↓。
17.(2020 西藏)某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是 紫色石蕊溶液 ;编号②反应的金属单质是 铁 。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是 置换 反应。
(3)请你写出符合编号③反应的化学方程式 Fe2O3+6HCl═2FeCl3+3H2O 。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是 产生白色沉淀 。
【解答】解:(1)紫色石蕊溶液遇酸性溶液变红,无色酚酞溶液遇酸性溶液不变色,编号①反应的指示剂是紫色石蕊溶液。
编号②反应的金属单质是铁,铁能与稀盐酸反应生成氯化亚铁溶液和氢气,氯化亚铁溶液显浅绿色。
(2)编号②的反应是金属和酸反应生成盐和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
(3)编号③,可以是稀盐酸与氧化铁反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O。
(4)编号④反应的盐是AgNO3,稀盐酸与硝酸银溶液反应生成氯化银沉淀和硝酸,对应方框中的现象是产生白色沉淀。
故答案为:
(1)紫色石蕊溶液;铁;
(2)置换;
(3)Fe2O3+6HCl═2FeCl3+3H2O;
(4)产生白色沉淀。
一.选择题(共9小题)
1.(2021 福建)甲、乙、丙三种物质有如下转化关系:甲乙丙。在不断搅拌下,往装有甲溶液的容器中逐滴加入稀盐酸依次发生了①②反应,同时测定容器中液体的透光度强度(液体越浑浊,透光强度越小),结果如图。下列分析错误的是( )
A.乙难溶于水
B.甲可能是NaOH
C.QM段对应的反应是②
D.E、F对应的液体组成不同
2.(2021 台州)盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )
A.B.C.D.
3.(2021 邵阳)推理是学习化学的一种常用方法,下列推理正确的是( )
A.阴离子带负电荷,则带负电荷的粒子一定是阴离子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素
D.碳酸盐与盐酸反应都有气体生成,则与盐酸反应有气体生成的物质一定是碳酸盐
4.(2021 黄石)思维导图是知识整理的重要工具,如图是某思维导图的一部分,可以填入括号中的是( )
A.能与活泼非金属反应 B.能与某些酸反应
C.能与非金属氧化物反应 D.能与某些盐反应
5.(2021 青海)下列物质不能与稀盐酸反应的是( )
A.铜 B.氧化铜 C.氢氧化钙 D.碳酸氢钠
6.(2021 深圳)小明在探究稀硫酸性质时,下列说法正确的是( )
A.稀H2SO4与紫色石蕊试液反应后,溶液变蓝
B.若能与X反应制取H2,则X是Cu
C.和金属氧化物反应,有盐和水生成
D.若与Y发生中和反应,则Y一定是NaOH
7.(2021 南岸区校级模拟)已知物质X是下列四种物质中的一种,如表记录了物质X的溶液分别加入的另外三种物质中产生的现象。则物质X可能是( )
加入物质 硝酸钡溶液 氧化铁 氢氧化钠溶液
实验现象 白色沉淀 溶解,溶液变黄 无明显现象
A.NaCl溶液 B.碳酸钠溶液 C.稀硝酸 D.稀硫酸
8.(2021 包头)向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe2O3固体、Cu(OH)2固体、Na2CO3溶液至过量。下列图像能正确反映其对应变化关系的是( )
A.B.C.D.
9.(2021 广西)下列有关硫酸的认识或做法,正确的是( )
A.组成:硫酸溶液中H+和SO42﹣的数目相同
B.性质:能与CO2、SO2等非金属氧化物反应
C.用途:用于生产化肥、农药、火药、染料等
D.生产:含硫酸的工业废水,用CaCl2处理后直接排放
二.填空题(共8小题)
10.(2021 杭州)实验室常用锌和稀硫酸来制取氢气,向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式 。
(2)如图的“”“”“”表示反应前后溶液中溶质电离产生的不同离子,则“”表示 。(填写离子符号)
11.(2021春 商南县校级期中)某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若用CuO实现②,会得到 色溶液。
(2)若实现③,得到浅绿色溶液,此反应的化学方程式为 。
(3)若选用硝酸盐实现⑤,则可选用的盐是 。
12.(2021 右江区二模)稀硫酸是常用试剂,关于稀硫酸的性质实验如下:
(1)若需要区别稀硫酸与稀盐酸溶液,应选用的试剂是 ;
(2)向放有有锌粒的试管中加入稀硫酸,有气泡产生,该反应的基本类型是 ;
(3)向滴有酚酞的氢氧化钠溶液中滴加稀硫酸至过量,观察到的现象是 ,反应的化学方程式是 。
13.(2021 兴国县校级模拟)等质量的A、B两种物质分别与等质量的同浓度稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图所示。请回答下列问题:
(1)若A、B分别为Fe、Zn中的一种,则A是 ,剩余金属中一定有 ,可能有 。
(2)若A、B分别为碳酸钠粉末和碳酸钙块状固体中的一种,则B是 ,剩余固体中一定有 ,可能有 。反应至t1时,B产生的气体比A多的原因是 。
14.(2021 富平县二模)某化学兴趣小组同学为探究酸的化学性质,进行图1所示实验。
(1)上述实验中不能体现酸的通性的是 (填字母)。
(2)反应后溶液呈棕黄色的烧杯中发生反应的化学方程式为 。
(3)图2是利用数字化传感器测得烧杯C反应过程中溶液pH的变化,下列说法不正确的是 (填序号)。
①a点所示溶液呈碱性
②b点反应的微观实质是H+与OH﹣结合生成H2O
③c点所示溶液中含有的溶质是NaCl和NaOH
④由a点到b点的pH变化过程能证明酸和碱发生了反应
15.(2021 淄川区一模)为探究稀盐酸的化学性质,兴趣学习小组的同学进行如图所示实验。请根据实验回答下列问题:
(1)实验中无明显现象的是 (填试管编号),下列实验不能证明两者发生了反应的是 。
a、测定加入另一反应物前后温度的变化:温度升高
b、测定加入另一反应物前后溶液pH的变化:pH变大
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(2)试管Ⅳ中发生反应的化学方程式是 。
(3)为了验证盐酸具有酸的通性,还需添加的实验是:向稀盐酸中加入 。
16.(2020秋 岱岳区校级月考)清华学子梁琰通过拍摄短片描述化学反应之美!如图是稀盐酸参与的化学反应,“→”表示转化关系,请回答:
(1)图中盐酸与 的反应不属于酸的通性。
(2)若物质X的类别与Fe、Fe2O3、AgNO3均不同,则X的化学式是 。
(3)稀盐酸与AgNO3溶液发生复分解反应的化学方程式为 。
17.(2020 西藏)某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是 ;编号②反应的金属单质是 。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是
反应。
(3)请你写出符合编号③反应的化学方程式 。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是 。
2021-2022学年华师大版九年级重要的酸的精选练习
参考答案与试题解析
一.选择题(共9小题)
1.(2021 福建)甲、乙、丙三种物质有如下转化关系:甲乙丙。在不断搅拌下,往装有甲溶液的容器中逐滴加入稀盐酸依次发生了①②反应,同时测定容器中液体的透光度强度(液体越浑浊,透光强度越小),结果如图。下列分析错误的是( )
A.乙难溶于水
B.甲可能是NaOH
C.QM段对应的反应是②
D.E、F对应的液体组成不同
【解答】解:A、PQ段透光强度在减小,说明发生反应①,说明生成的乙是沉淀;故A正确;
B、PQ段透光强度在减小,说明反应①要生成沉淀,如果甲为NaOH,与盐酸反应不会生成沉淀,所以甲不能是NaOH;故B错误;
C、QM段透光强度在增大,说明发生反应②;故C正确;
D、E对应的液体含有没有反应完的甲,F点对应的液体含有生成的丙,所以E、F对应的液体组成不同;故D正确;
故选:B。
2.(2021 台州)盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )
A. B.
C. D.
【解答】解:A、稀盐酸显酸性,能使紫色石蕊溶液变红色,故选项错误。
B、铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,会观察到铁锈逐渐溶解、溶液变黄色,故选项错误。
C、稀盐酸能与硝酸银溶液反应生成氯化银沉淀和硝酸,能观察到白色沉淀,故选项正确。
D、稀盐酸与氢氧化钠反应生成氯化钠和水,但无明显现象,故选项错误。
故选:C。
3.(2021 邵阳)推理是学习化学的一种常用方法,下列推理正确的是( )
A.阴离子带负电荷,则带负电荷的粒子一定是阴离子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素
D.碳酸盐与盐酸反应都有气体生成,则与盐酸反应有气体生成的物质一定是碳酸盐
【解答】解:A、阴离子带负电荷,但带负电荷的粒子不一定是阴离子,也可能是电子等,故选项推理错误。
B、单质只含一种元素,但只含一种元素的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,故选项推理错误。
C、元素是质子数(即核电荷数)相同的一类原子的总称,元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素,故选项推理正确。
D、碳酸盐与盐酸反应都有气体生成,但与盐酸反应有气体生成的物质不一定是碳酸盐,也可能是活泼金属等,故选项推理错误。
故选:C。
4.(2021 黄石)思维导图是知识整理的重要工具,如图是某思维导图的一部分,可以填入括号中的是( )
A.能与活泼非金属反应 B.能与某些酸反应
C.能与非金属氧化物反应 D.能与某些盐反应
【解答】解:酸能与酸碱指示剂作用,能与活泼金属反应生成盐和氢气,能与金属氧化物反应生成盐和水,能与碱反应生成盐和水,能与某些盐反应反应新酸和新盐,可以填入括号中的是能与某些盐反应。
故选:D。
5.(2021 青海)下列物质不能与稀盐酸反应的是( )
A.铜 B.氧化铜 C.氢氧化钙 D.碳酸氢钠
【解答】解:A、在金属活动性顺序中,铜的位置排在氢的后面,不能与稀盐酸反应,故选项正确。
B、氧化铜能与稀盐酸反应生成氯化铜和水,故选项错误。
C、氢氧化钙能与稀盐酸反应生成氯化钙和水,故选项错误。
D、碳酸氢钠能与稀盐酸反应生成氯化钠、水和二氧化碳,故选项错误。
故选:A。
6.(2021 深圳)小明在探究稀硫酸性质时,下列说法正确的是( )
A.稀H2SO4与紫色石蕊试液反应后,溶液变蓝
B.若能与X反应制取H2,则X是Cu
C.和金属氧化物反应,有盐和水生成
D.若与Y发生中和反应,则Y一定是NaOH
【解答】解:A、稀H2SO4与紫色石蕊试液反应后,溶液变红色,故选项说法错误。
B、若能与X反应制取H2,则X不可能是Cu,在金属活动性顺序中,铜的位置排在氢的后面,不与稀硫酸反应,故选项说法错误。
C、稀硫酸和金属氧化物反应,有盐和水生成,故选项说法正确。
D、若与Y发生中和反应,但Y不一定是NaOH,也可能是氢氧化钙等碱,故选项说法错误。
故选:C。
7.(2021 南岸区校级模拟)已知物质X是下列四种物质中的一种,如表记录了物质X的溶液分别加入的另外三种物质中产生的现象。则物质X可能是( )
加入物质 硝酸钡溶液 氧化铁 氢氧化钠溶液
实验现象 白色沉淀 溶解,溶液变黄 无明显现象
A.NaCl溶液 B.碳酸钠溶液 C.稀硝酸 D.稀硫酸
【解答】解:A、NaCl溶液与硝酸钡溶液结合成分没有沉淀或气体或水生成,不能发生复分解反应,故选项错误。
B、碳酸钠溶液与硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠,与氧化铁不反应,故选项错误。
C、稀硝酸与硝酸钡溶液不反应,故选项错误。
D、稀硫酸能与硝酸钡溶液反应生成硫酸钡沉淀和硝酸;与氧化铁反应生成硫酸铁和水,氧化铁溶解,溶液变黄;与氢氧化钠溶液反应生成硫酸钠和水,无明显现象;故选项正确。
故选:D。
8.(2021 包头)向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe2O3固体、Cu(OH)2固体、Na2CO3溶液至过量。下列图像能正确反映其对应变化关系的是( )
A. B.
C. D.
【解答】解:A、镁和盐酸反应生成氯化镁和氢气,反应前的溶液是稀盐酸,所以溶液增加的起点不能从零开始,故A错误;
B、氧化铁和盐酸反应生成氯化铁和水,反应前的溶液中不含铁元素,随着反应的进行,溶液中铁元素的质量逐渐增加,盐酸完全反应后,铁元素质量不变,故B正确;
C、氢氧化铜和盐酸反应生成氯化铜和水,氢氧化铜难溶于水,盐酸消耗完后,溶液的pH值不会大于7,故C错误;
D、碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,二氧化碳气体的质量应该从零开始,故D错误。
故选:B。
9.(2021 广西)下列有关硫酸的认识或做法,正确的是( )
A.组成:硫酸溶液中H+和SO42﹣的数目相同
B.性质:能与CO2、SO2等非金属氧化物反应
C.用途:用于生产化肥、农药、火药、染料等
D.生产:含硫酸的工业废水,用CaCl2处理后直接排放
【解答】解:A、硫酸溶液中的正负电荷代数和为零,所以H+和SO42﹣的数目之比是2:1,故A错误;
B、酸会与金属氧化物反应,不会与非金属氧化物反应,故B错误;
C、硫酸用于生产化肥、农药、火药、染料等,故C正确;
D、硫酸不会与氯化钙反应,含硫酸的工业废水,用氢氧化钙处理后直接排放,故D错误。
故选:C。
二.填空题(共8小题)
10.(2021 杭州)实验室常用锌和稀硫酸来制取氢气,向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式 Zn+H2SO4=ZnSO4+H2↑ 。
(2)如图的“”“”“”表示反应前后溶液中溶质电离产生的不同离子,则“”表示 SO42﹣ 。(填写离子符号)
【解答】解:(1)锌和稀硫酸反应生成硫酸锌和氢气,方程式为:Zn+H2SO4=ZnSO4+H2↑,故填:Zn+H2SO4=ZnSO4+H2↑;
(2)反应前溶液是稀硫酸,其中溶质电离产生的离子为氢离子和硫酸根离子,反应完全后溶液是硫酸锌溶液,其中电离产生的离子是锌离子和硫酸根离子,反应前后不变的离子是硫酸根离子,故“”表示硫酸根离子,故填:SO42﹣。
11.(2021春 商南县校级期中)某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若用CuO实现②,会得到 蓝 色溶液。
(2)若实现③,得到浅绿色溶液,此反应的化学方程式为 Fe+H2SO4═FeSO4+H2↑ 。
(3)若选用硝酸盐实现⑤,则可选用的盐是 Ba(NO3)2 。
【解答】解:(1)若用CuO实现②,稀硫酸和氧化铜反应生成硫酸铜和水,会得到蓝色溶液。
故填:蓝。
(2)若实现③,得到浅绿色溶液,则稀硫酸和铁反应生成硫酸亚铁和氢气,此反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑。
故填:Fe+H2SO4═FeSO4+H2↑。
(3)若选用硝酸盐实现⑤,则可选用的盐是硝酸钡,是因为硝酸钡能和稀硫酸反应生成硫酸钡沉淀和硝酸。
故填:Ba(NO3)2。
12.(2021 右江区二模)稀硫酸是常用试剂,关于稀硫酸的性质实验如下:
(1)若需要区别稀硫酸与稀盐酸溶液,应选用的试剂是 氯化钡溶液(合理即可) ;
(2)向放有有锌粒的试管中加入稀硫酸,有气泡产生,该反应的基本类型是 置换反应 ;
(3)向滴有酚酞的氢氧化钠溶液中滴加稀硫酸至过量,观察到的现象是 溶液由红色变为无色 ,反应的化学方程式是 2NaOH+H2SO4═Na2SO4+2H2O 。
【解答】解:(1)若需要区别稀硫酸与稀盐酸溶液,应选用的试剂是氯化钡溶液,稀硫酸能与氯化钡溶液反应生成硫酸钡白色沉淀,稀盐酸不能与氯化钡溶液反应,能出现两种明显不同的现象,可以鉴别。
(2)向放有有锌粒的试管中加入稀硫酸,有气泡产生,是因为锌与硫酸反应生成硫酸锌和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
(3)滴有酚酞溶液的氢氧化钠溶液显红色,无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,逐滴滴入稀硫酸,至恰好完全反应,溶液显中性,溶液由红色变为无色,继续滴加稀硫酸,溶液显酸性,溶液颜色为无色。
稀硫酸与氢氧化钠溶液反应生成硫酸钠和水,反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O。
故答案为:
(1)氯化钡溶液(合理即可);
(2)置换反应;
(3)溶液由红色变为无色;2NaOH+H2SO4═Na2SO4+2H2O。
13.(2021 兴国县校级模拟)等质量的A、B两种物质分别与等质量的同浓度稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图所示。请回答下列问题:
(1)若A、B分别为Fe、Zn中的一种,则A是 铁 ,剩余金属中一定有 铁 ,可能有 锌 。
(2)若A、B分别为碳酸钠粉末和碳酸钙块状固体中的一种,则B是 碳酸钠粉末。 ,剩余固体中一定有 碳酸钙 ,可能有 碳酸钠 。反应至t1时,B产生的气体比A多的原因是 碳酸钠粉末与稀盐酸的接触面积大,反应速率快 。
【解答】解:(1)若A、B分别为Fe、Zn中的一种,锌的活动性比铁强,反应速率快,反应时间短;等质量的 A、B 两种金属分别与足量的同浓度的稀盐酸充分反应,铁生成氢气的质量比锌多,则A是铁;利用方程式,根据反应的质量比可知生成等质量的氢气,铁与氢气的质量比为56:2,锌与氢气的质量比为65:2,故反应后剩余金属中一定有铁,可能有锌;故答案为:铁;铁;锌;
(2)反物的接触面积越大,反应越剧烈,若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,则B是碳酸钠粉末;利用方程式,根据反应的质量比可知生成等质量的二氧化碳,碳酸钠与二氧化碳的质量比为106:44,碳酸钙与二氧化碳的质量比为100:44,故反应后剩余固体中一定有碳酸钙,可能有碳酸钠;反应至t1时,B 产生的气体比A多,是因为碳酸钠粉末与稀盐酸的接触面积大,反应速率快。故答案为:碳酸钠粉末;碳酸钙;碳酸钠;碳酸钠粉末与稀盐酸的接触面积大,反应速率快。
14.(2021 富平县二模)某化学兴趣小组同学为探究酸的化学性质,进行图1所示实验。
(1)上述实验中不能体现酸的通性的是 D (填字母)。
(2)反应后溶液呈棕黄色的烧杯中发生反应的化学方程式为 Fe2O3+6HCl═2FeCl3+3H2O 。
(3)图2是利用数字化传感器测得烧杯C反应过程中溶液pH的变化,下列说法不正确的是 ③ (填序号)。
①a点所示溶液呈碱性
②b点反应的微观实质是H+与OH﹣结合生成H2O
③c点所示溶液中含有的溶质是NaCl和NaOH
④由a点到b点的pH变化过程能证明酸和碱发生了反应
【解答】解:(1)上述实验中不能体现酸的通性的是D,是因为盐也能和硝酸银反应,例如氯化钠和硝酸银反应生成白色沉淀氯化银和硝酸钠。
故填:D。
(2)反应后溶液呈棕黄色的烧杯中,氧化铁和稀盐酸反应生成氯化铁和水,发生反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O。
故填:Fe2O3+6HCl═2FeCl3+3H2O。
(3)①a点所示溶液pH大于7,呈碱性,该选项说法正确;
②b点反应的微观实质是H+与OH﹣结合生成H2O,该选项说法正确;
③c点所示溶液中含有的溶质是NaCl和氯化氢,该选项说法不正确;
④由a点到b点的pH变化过程能证明酸和碱发生了反应,是因为碱消失,该选项说法正确。
故填:③。
15.(2021 淄川区一模)为探究稀盐酸的化学性质,兴趣学习小组的同学进行如图所示实验。请根据实验回答下列问题:
(1)实验中无明显现象的是 Ⅰ (填试管编号),下列实验不能证明两者发生了反应的是 。
a、测定加入另一反应物前后温度的变化:温度升高
b、测定加入另一反应物前后溶液pH的变化:pH变大
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(2)试管Ⅳ中发生反应的化学方程式是 AgNO3+HCl=AgCl↓+HNO3 。
(3)为了验证盐酸具有酸的通性,还需添加的实验是:向稀盐酸中加入 金属锌 。
【解答】解:(1)氢氧化钙和盐酸反应生成氯化钙和水,实验中无明显现象;
a、测定加入另一反应物前后温度的变化:温度升高,说明二者混合放热,能证明发生反应;
b、测定加入另一反应物前后溶液pH的变化:pH变大,氢氧化钙溶液中含有水,盐酸中加入水,酸性减弱,pH增大,不能证明发生反应;
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红,说明开始氢氧化钙的碱性没有体现出来,是盐酸和氢氧化钙反应,能证明发生反应;
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡,说明盐酸已经没有了,能证明发生反应;
故填:Ⅰ;b;
(2)试管Ⅳ中盐酸和硝酸银反应生成氯化银沉淀和硝酸,发生反应的化学方程式是AgNO3+HCl=AgCl↓+HNO3,故填:AgNO3+HCl=AgCl↓+HNO3;
(3)为了验证盐酸具有酸的通性,还需添加盐酸与金属的反应,故可以向稀盐酸中加入金属锌,故填:金属锌。
16.(2020秋 岱岳区校级月考)清华学子梁琰通过拍摄短片描述化学反应之美!如图是稀盐酸参与的化学反应,“→”表示转化关系,请回答:
(1)图中盐酸与 硝酸银溶液 的反应不属于酸的通性。
(2)若物质X的类别与Fe、Fe2O3、AgNO3均不同,则X的化学式是 Cu(OH)2 。
(3)稀盐酸与AgNO3溶液发生复分解反应的化学方程式为 HCl+AgNO3═HNO3+AgCl↓ 。
【解答】解:(1)图中盐酸与硝酸银溶液的反应不属于酸的通性,如硝酸不能与硝酸银溶液反应。
(2)若物质X的类别与Fe、Fe2O3、AgNO3均不同,由酸的化学性质,X应为碱,生成蓝色溶液,说明生成了铜盐的水溶液,则X为氢氧化铜,其化学式为Cu(OH)2。
(3)稀盐酸与AgNO3溶液反应生成氯化银沉淀和硝酸,反应的化学方程式为HCl+AgNO3═HNO3+AgCl↓。
故答案为:
(1)硝酸银溶液;
(2)Cu(OH)2;
(3)HCl+AgNO3═HNO3+AgCl↓。
17.(2020 西藏)某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是 紫色石蕊溶液 ;编号②反应的金属单质是 铁 。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是 置换 反应。
(3)请你写出符合编号③反应的化学方程式 Fe2O3+6HCl═2FeCl3+3H2O 。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是 产生白色沉淀 。
【解答】解:(1)紫色石蕊溶液遇酸性溶液变红,无色酚酞溶液遇酸性溶液不变色,编号①反应的指示剂是紫色石蕊溶液。
编号②反应的金属单质是铁,铁能与稀盐酸反应生成氯化亚铁溶液和氢气,氯化亚铁溶液显浅绿色。
(2)编号②的反应是金属和酸反应生成盐和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
(3)编号③,可以是稀盐酸与氧化铁反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O。
(4)编号④反应的盐是AgNO3,稀盐酸与硝酸银溶液反应生成氯化银沉淀和硝酸,对应方框中的现象是产生白色沉淀。
故答案为:
(1)紫色石蕊溶液;铁;
(2)置换;
(3)Fe2O3+6HCl═2FeCl3+3H2O;
(4)产生白色沉淀。
