2021-2022学年九年级化学人教版上册 5.1 质量守恒定律(38张PPT)
文档属性
| 名称 | 2021-2022学年九年级化学人教版上册 5.1 质量守恒定律(38张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-19 00:00:00 | ||
图片预览









文档简介
(共38张PPT)
“水加入一种催化剂可变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?
廣而告之
课题1 质量守恒定律
第五单元 化学方程式
1.掌握质量守恒定律,能说明常见化学反应中的质量关系
2.能运用质量守恒定律解决一些相关问题
3.了解化学方程式的含义
学习目标
认知与了解
导入新课
第一课时
铁丝燃烧后,质量会
变大,所以化学反应
后质量是变大的.
木材燃烧完后,只剩下灰,所以化学反应后质量是变小的.
小强
小刚
这是真的吗?
PK
总质量是否相等?
化学反应前后物质
活动探究一
化学反应前后物质的总质量是否相等?
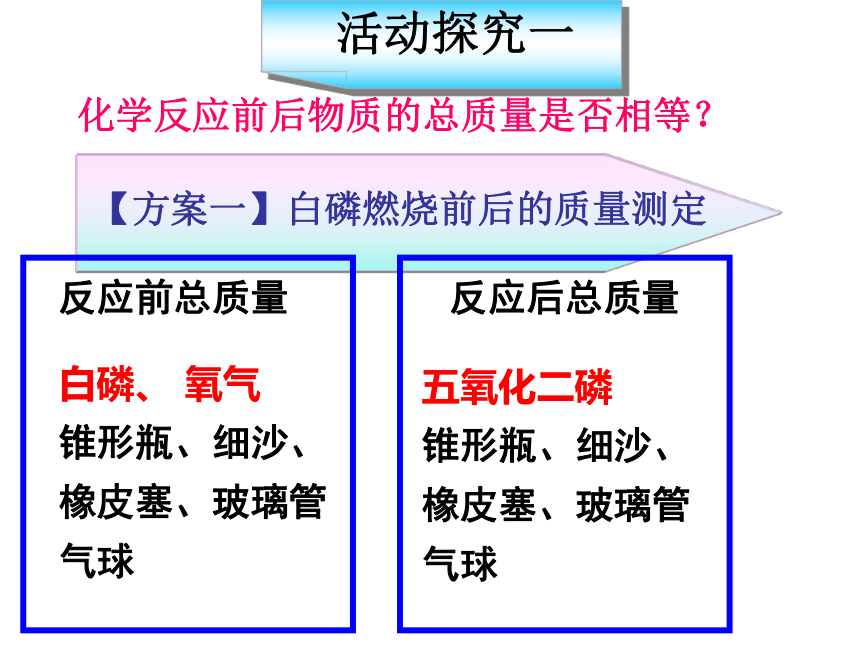
【方案一】白磷燃烧前后的质量测定
反应前总质量
反应后总质量
白磷、 氧气
锥形瓶、细沙、
橡皮塞、玻璃管
气球
五氧化二磷
锥形瓶、细沙、
橡皮塞、玻璃管
气球
反应原理:
磷+氧气
点燃
五氧化二磷
结论:反应物质量总和 生成物质量总和
实验现象:白磷燃烧产生大量白烟,气球先胀大
后变瘪
天平仍保持平衡。
m(P)+ m(O2)= m(P2O5)
=
实验前
实验中
实验后
白磷燃烧前后质量总和的测定
平衡气压,防止胶塞被冲开
注意:(1)气球的作用:
(2)细沙的作用:
防止锥形瓶底受热不均匀而炸裂
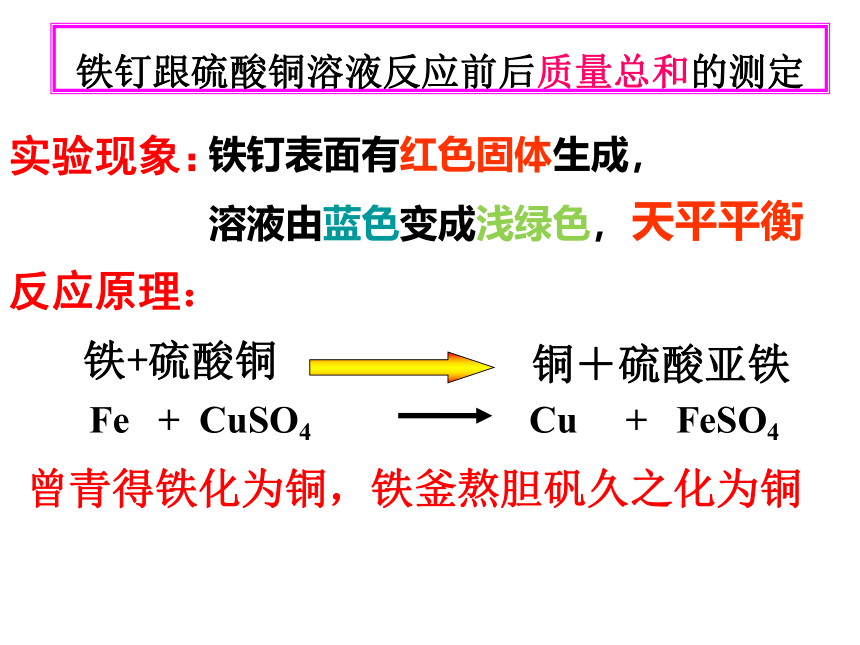
铁钉跟硫酸铜溶液反应前
后质量总和的测定
活动探究一
化学反应前后物质的总质量是否相等?
方案 2
实验现象:
反应原理:
铁+硫酸铜
铜+硫酸亚铁
铁钉表面有红色固体生成,
溶液由蓝色变成浅绿色,
Fe + CuSO4 Cu + FeSO4
天平平衡
铁钉跟硫酸铜溶液反应前后质量总和的测定
曾青得铁化为铜,铁釜熬胆矾久之化为铜
锥形瓶、橡皮塞
反应前总质量
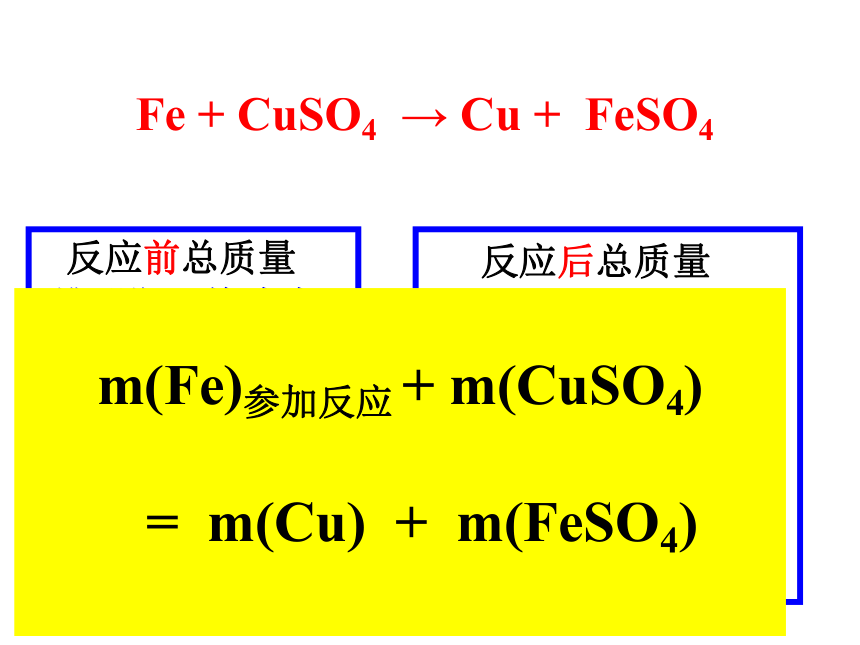
Fe + CuSO4 → Cu + FeSO4
锥形瓶、橡皮塞
铁钉
硫酸铜溶液
硫酸铜
水
反应后总质量
铜
硫酸亚铁溶液
硫酸亚铁
水
未反应的铁
已反应的铁
未反应的铁
m(Fe)参加反应 + m(CuSO4)
= m(Cu) + m(FeSO4)
实验结论
参加化学反应的各物质的质量总和
反应后生成的各物质的质量总和
=
质量守恒定律
再想想
是不是所有的化学反应都有这种规律呢?有没有特殊的情况?
活动探究二
【实验5—1】碳酸钠与盐酸的反应前后
的质量测定
【实验5—2】镁条在空气中燃烧前后质量
的测定。
质量守恒定律是否对任何化学反应都适用
实验现象:
固体粉末溶解,有大量的气泡产生;
碳酸钠 + 氯化氢 氯化钠 + 二氧化碳 + 水
Na2CO3 + HCl NaCl + CO2↑ + H2O
反应原理:
天平指针右偏(变轻)
天平平衡情况:
碳酸钠与盐酸的反应前后的质量测定
在敞口容器中:
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 > M2
探究实验5—1
讨论:稀盐酸和碳酸钠反应前
后为什么天平不平衡呢?
如何证明稀盐酸和碳酸钠反应
前后物质的总质量相等呢?
想一想:
1
3
2
讨论和评价
碳酸钠粉末
稀盐酸
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 = M2
在密闭容器中
探究实验3
讨论与交流
镁+氧气
氧化镁
点燃
Mg + O2 ——
MgO
点燃
思考:1、该实验的现象是什么?
发出耀眼的白光、放热,生成白色固体,还有白烟产生
思考:2、该反应的原理是什么?
天平?
思考3:如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么结果?
实验5—2
若用有气体参加或生成的反应
验证质量守恒定律,
装置必须密闭。
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
质量总和
化学反应
2、理解时注意:
参加:没有参加反应的物质其质量不计算在反应物内。
化学反应:只能解释化学变化。不能说某个
物理变化遵守质量守恒定律
质量:守恒的是质量,不是体积或分子个数。
总和:各状态的反应物、生成物,特别是气体
要考虑到。
第二课时
想一想
想一想
为什么化学反应前后的各物质的质量总和相等呢?
水分解示意图
H2O分子
H2分子
O2分子
H2分子
3、质量守恒的原因
在化学变化前后,原子的种类、数目、质量没有改变。
化学变化的实质是:
分子
原子
分解为
新分子
重组
你发现了吗?
O
H
H
O
O
O
H
H
H
H
H
H
H
H
H
O
O
原子种类变了吗?
原子数目变了吗?
原子质量呢?
化学反应前后
元素种类呢?
各元素质量
呢?
不变
不变
都不变
动动脑
物质的总质量呢?
分子数目变了吗?
化学反应前后
物质种类变了吗?
分子种类呢?
动动脑
改变
可能改变
元素化合价变了吗?
小结:4、化学反应前后
1、一定不变的:
宏观:元素的种类、质量,物质的总质量;
微观:原子的种类、个数、质量
2、一定改变的:物质的种类(宏观)、
分子的种类(微观)
3、可能改变的:元素的化合价(宏观)、
分子的总数目(微观)
1、现有31g红磷与40g氧气恰好完全反应,则生成五氧化二磷的质量____g。
2、6g的碳在充足的氧气中燃烧,生成二氧化碳22 g ,则有____g 氧气参加反应。
71
16
比一比,看谁快
学以致用
学以致用
3、对质量守恒定律的解释正确的是[ ]
A、化学反应前后原子种类不变,原子数目改变
B、化学反应前后原子种类改变,原子数目不变
C、在一切化学反应前后原子种类和原子数目都不变
D、在化学反应中反应物的分子数等于生成物的分子数
C
“水(由氢、氧元素组成)加入一种催化剂可变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,通过学习你还会加盟吗?
眼明心慧
2.某大师说他能发功使铝发生化学变化变成黄金。他的说法是否有科学道理?
1.铜粉在空气中加热后,生成物的质量比原来铜粉的质量增大,为什么?
铜粉在空气中加热,是Cu和氧气发生了化学反应。根据质量守恒定律,反应生成氧化铜的质量,一定等于参加反应的铜粉和氧气的质量总和,所以CuO的质量比原来Cu的质量大
没有。化学反应前后,原子和元素种类不变。
活学活用
碳+ 氧气 二氧化碳
点燃
将文字换成化学式,并使其反应前后的原子总数相等。
C + O2 CO2
点燃
请写出碳在氧气中燃烧的文字表达式,这种式子能体现质量守恒定律吗?
如何表示才能体现质量守恒定律?
点燃
4 P+5 O2 2 P2O5
点燃
2Mg+ O2 2MgO
1、定义:用化学式表示化学反应的式子
化学方程式
二、化学方程式
由下列化学方程式你能得到哪些信息?
意义
C + O2 CO2
点燃
反应物: C 和O2
生成物: CO2
条件:点燃
(1)宏观:表示反应物、生成物及反应条件
C + O2 CO2
点燃
12 : 16×2 : 12+16×2
12 : 32 : 44
(2)质量:表示各物质的质量比
物质的质量==
相对分子质量×化学计量数。
C + O2 CO2
点燃
1 : 1 : 1
(3)微观:表示各物质的粒子个数比
即各物质前面的化学计量数之比
2、意义
如何读下列化学方程式呢?
读法
C + O2 CO2
点燃
反应物: C 和O2
生成物: CO2
条件:点燃
(1)宏观:碳和氧气在点燃条件下生成二氧化碳。
C + O2 CO2
点燃
12 : 16×2 : 12+16×2
12 : 32 : 44
(2)质量:每12份质量的碳和32份质量的氧气在点燃条件下生成44份质量的二氧化碳。
C + O2 CO2
点燃
1 : 1 : 1
(3)微观:每1个碳原子和1个氧分子在点燃条件下生成1个二氧化碳分子。
3、读法
2、硫在氧气中燃烧的化学方程式是:S+O2 点燃 SO2。这个式子不仅表明了反应物是 ,生成物是 ,反应条件是 ,还表示了参与反应的各物质之间的质量关系,即在点燃条件下,每 份质量的硫与 份质量的氧气恰好完全反应生成 份质量的二氧化硫。
1、根据化学方程式不能获得的信息是( )
A.该反应中的反应物和生成物
B. 各反应物和生成物的质量比
C.反应发生所需要的条件
D.化学反应的快慢
D
硫和氧气
二氧化硫
点燃
32
32
64
本课题你有哪些收获?
质量守恒定律
内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
原因:反应前后原子的种类、数目、质量都没有改变
感受成功
化学方程式
定义:用化学式表示化学反应的式子
意义:宏观:表示反应物、生成物及反应条件;质量;表示各反应物、生成物的质量比;微观:表示各反应物、生成物的微粒个数比
读法:3个方面
“水加入一种催化剂可变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?
廣而告之
课题1 质量守恒定律
第五单元 化学方程式
1.掌握质量守恒定律,能说明常见化学反应中的质量关系
2.能运用质量守恒定律解决一些相关问题
3.了解化学方程式的含义
学习目标
认知与了解
导入新课
第一课时
铁丝燃烧后,质量会
变大,所以化学反应
后质量是变大的.
木材燃烧完后,只剩下灰,所以化学反应后质量是变小的.
小强
小刚
这是真的吗?
PK
总质量是否相等?
化学反应前后物质
活动探究一
化学反应前后物质的总质量是否相等?
【方案一】白磷燃烧前后的质量测定
反应前总质量
反应后总质量
白磷、 氧气
锥形瓶、细沙、
橡皮塞、玻璃管
气球
五氧化二磷
锥形瓶、细沙、
橡皮塞、玻璃管
气球
反应原理:
磷+氧气
点燃
五氧化二磷
结论:反应物质量总和 生成物质量总和
实验现象:白磷燃烧产生大量白烟,气球先胀大
后变瘪
天平仍保持平衡。
m(P)+ m(O2)= m(P2O5)
=
实验前
实验中
实验后
白磷燃烧前后质量总和的测定
平衡气压,防止胶塞被冲开
注意:(1)气球的作用:
(2)细沙的作用:
防止锥形瓶底受热不均匀而炸裂
铁钉跟硫酸铜溶液反应前
后质量总和的测定
活动探究一
化学反应前后物质的总质量是否相等?
方案 2
实验现象:
反应原理:
铁+硫酸铜
铜+硫酸亚铁
铁钉表面有红色固体生成,
溶液由蓝色变成浅绿色,
Fe + CuSO4 Cu + FeSO4
天平平衡
铁钉跟硫酸铜溶液反应前后质量总和的测定
曾青得铁化为铜,铁釜熬胆矾久之化为铜
锥形瓶、橡皮塞
反应前总质量
Fe + CuSO4 → Cu + FeSO4
锥形瓶、橡皮塞
铁钉
硫酸铜溶液
硫酸铜
水
反应后总质量
铜
硫酸亚铁溶液
硫酸亚铁
水
未反应的铁
已反应的铁
未反应的铁
m(Fe)参加反应 + m(CuSO4)
= m(Cu) + m(FeSO4)
实验结论
参加化学反应的各物质的质量总和
反应后生成的各物质的质量总和
=
质量守恒定律
再想想
是不是所有的化学反应都有这种规律呢?有没有特殊的情况?
活动探究二
【实验5—1】碳酸钠与盐酸的反应前后
的质量测定
【实验5—2】镁条在空气中燃烧前后质量
的测定。
质量守恒定律是否对任何化学反应都适用
实验现象:
固体粉末溶解,有大量的气泡产生;
碳酸钠 + 氯化氢 氯化钠 + 二氧化碳 + 水
Na2CO3 + HCl NaCl + CO2↑ + H2O
反应原理:
天平指针右偏(变轻)
天平平衡情况:
碳酸钠与盐酸的反应前后的质量测定
在敞口容器中:
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 > M2
探究实验5—1
讨论:稀盐酸和碳酸钠反应前
后为什么天平不平衡呢?
如何证明稀盐酸和碳酸钠反应
前后物质的总质量相等呢?
想一想:
1
3
2
讨论和评价
碳酸钠粉末
稀盐酸
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 = M2
在密闭容器中
探究实验3
讨论与交流
镁+氧气
氧化镁
点燃
Mg + O2 ——
MgO
点燃
思考:1、该实验的现象是什么?
发出耀眼的白光、放热,生成白色固体,还有白烟产生
思考:2、该反应的原理是什么?
天平?
思考3:如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么结果?
实验5—2
若用有气体参加或生成的反应
验证质量守恒定律,
装置必须密闭。
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
质量总和
化学反应
2、理解时注意:
参加:没有参加反应的物质其质量不计算在反应物内。
化学反应:只能解释化学变化。不能说某个
物理变化遵守质量守恒定律
质量:守恒的是质量,不是体积或分子个数。
总和:各状态的反应物、生成物,特别是气体
要考虑到。
第二课时
想一想
想一想
为什么化学反应前后的各物质的质量总和相等呢?
水分解示意图
H2O分子
H2分子
O2分子
H2分子
3、质量守恒的原因
在化学变化前后,原子的种类、数目、质量没有改变。
化学变化的实质是:
分子
原子
分解为
新分子
重组
你发现了吗?
O
H
H
O
O
O
H
H
H
H
H
H
H
H
H
O
O
原子种类变了吗?
原子数目变了吗?
原子质量呢?
化学反应前后
元素种类呢?
各元素质量
呢?
不变
不变
都不变
动动脑
物质的总质量呢?
分子数目变了吗?
化学反应前后
物质种类变了吗?
分子种类呢?
动动脑
改变
可能改变
元素化合价变了吗?
小结:4、化学反应前后
1、一定不变的:
宏观:元素的种类、质量,物质的总质量;
微观:原子的种类、个数、质量
2、一定改变的:物质的种类(宏观)、
分子的种类(微观)
3、可能改变的:元素的化合价(宏观)、
分子的总数目(微观)
1、现有31g红磷与40g氧气恰好完全反应,则生成五氧化二磷的质量____g。
2、6g的碳在充足的氧气中燃烧,生成二氧化碳22 g ,则有____g 氧气参加反应。
71
16
比一比,看谁快
学以致用
学以致用
3、对质量守恒定律的解释正确的是[ ]
A、化学反应前后原子种类不变,原子数目改变
B、化学反应前后原子种类改变,原子数目不变
C、在一切化学反应前后原子种类和原子数目都不变
D、在化学反应中反应物的分子数等于生成物的分子数
C
“水(由氢、氧元素组成)加入一种催化剂可变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,通过学习你还会加盟吗?
眼明心慧
2.某大师说他能发功使铝发生化学变化变成黄金。他的说法是否有科学道理?
1.铜粉在空气中加热后,生成物的质量比原来铜粉的质量增大,为什么?
铜粉在空气中加热,是Cu和氧气发生了化学反应。根据质量守恒定律,反应生成氧化铜的质量,一定等于参加反应的铜粉和氧气的质量总和,所以CuO的质量比原来Cu的质量大
没有。化学反应前后,原子和元素种类不变。
活学活用
碳+ 氧气 二氧化碳
点燃
将文字换成化学式,并使其反应前后的原子总数相等。
C + O2 CO2
点燃
请写出碳在氧气中燃烧的文字表达式,这种式子能体现质量守恒定律吗?
如何表示才能体现质量守恒定律?
点燃
4 P+5 O2 2 P2O5
点燃
2Mg+ O2 2MgO
1、定义:用化学式表示化学反应的式子
化学方程式
二、化学方程式
由下列化学方程式你能得到哪些信息?
意义
C + O2 CO2
点燃
反应物: C 和O2
生成物: CO2
条件:点燃
(1)宏观:表示反应物、生成物及反应条件
C + O2 CO2
点燃
12 : 16×2 : 12+16×2
12 : 32 : 44
(2)质量:表示各物质的质量比
物质的质量==
相对分子质量×化学计量数。
C + O2 CO2
点燃
1 : 1 : 1
(3)微观:表示各物质的粒子个数比
即各物质前面的化学计量数之比
2、意义
如何读下列化学方程式呢?
读法
C + O2 CO2
点燃
反应物: C 和O2
生成物: CO2
条件:点燃
(1)宏观:碳和氧气在点燃条件下生成二氧化碳。
C + O2 CO2
点燃
12 : 16×2 : 12+16×2
12 : 32 : 44
(2)质量:每12份质量的碳和32份质量的氧气在点燃条件下生成44份质量的二氧化碳。
C + O2 CO2
点燃
1 : 1 : 1
(3)微观:每1个碳原子和1个氧分子在点燃条件下生成1个二氧化碳分子。
3、读法
2、硫在氧气中燃烧的化学方程式是:S+O2 点燃 SO2。这个式子不仅表明了反应物是 ,生成物是 ,反应条件是 ,还表示了参与反应的各物质之间的质量关系,即在点燃条件下,每 份质量的硫与 份质量的氧气恰好完全反应生成 份质量的二氧化硫。
1、根据化学方程式不能获得的信息是( )
A.该反应中的反应物和生成物
B. 各反应物和生成物的质量比
C.反应发生所需要的条件
D.化学反应的快慢
D
硫和氧气
二氧化硫
点燃
32
32
64
本课题你有哪些收获?
质量守恒定律
内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
原因:反应前后原子的种类、数目、质量都没有改变
感受成功
化学方程式
定义:用化学式表示化学反应的式子
意义:宏观:表示反应物、生成物及反应条件;质量;表示各反应物、生成物的质量比;微观:表示各反应物、生成物的微粒个数比
读法:3个方面
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
