鲁教版九年级化学上册 3.2 溶液组成的定量表示 第二课时溶液的配制 课件(共22张PPT)
文档属性
| 名称 | 鲁教版九年级化学上册 3.2 溶液组成的定量表示 第二课时溶液的配制 课件(共22张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 8.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-19 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
溶液组成的定量表示(第二课时)
溶液的配制
鲁教版九年级化学上册
学习目标
1.通过分析0.9%的生理盐水等典型溶液,了解溶液在工农业生产、生活及科学研究中的广泛应用。
2.通过配制所需的氯化钠溶液,了解配制一定溶质质量分数的溶液的步骤和方法,进一步熟练药品的取用,托盘天平和量筒的使用技能;通过动手实验,对比感知“选量筒的原则”;通过对配制溶液方法的讨论,体会化学实验化繁为简的思想。
3.能关注实验细节,从定量认识溶液组成的角度分析误差形成的原因,培养严谨的科学态度。
溶液的配制
无土栽培 营养液
0.9%的氯化钠溶液
“0.9%”的含义
氯化钠溶液中
溶质和溶剂的质
量比为9:991
100克氯化钠溶液
中含有0.9克氯化钠
你知道生理盐水吗
明确任务
配制50克溶质质量分数为16%的氯化钠溶液
溶液的配制
溶液的配制
农业上常常用16%的
氯化钠溶液选种。
配制50克溶质质量分数为16%的氯化钠溶液
寻找配制方法
实验台上现有试剂(均为足量的)为:
氯化钠固体、25%的氯化钠溶液和蒸馏水
方法一:氯化钠固体和蒸馏水
方法二: 25%的氯化钠溶液和蒸馏水
方法三:氯化钠固体、 25%的氯化钠溶液
和蒸馏水
溶液的配制
方法一:氯化钠固体和蒸馏水
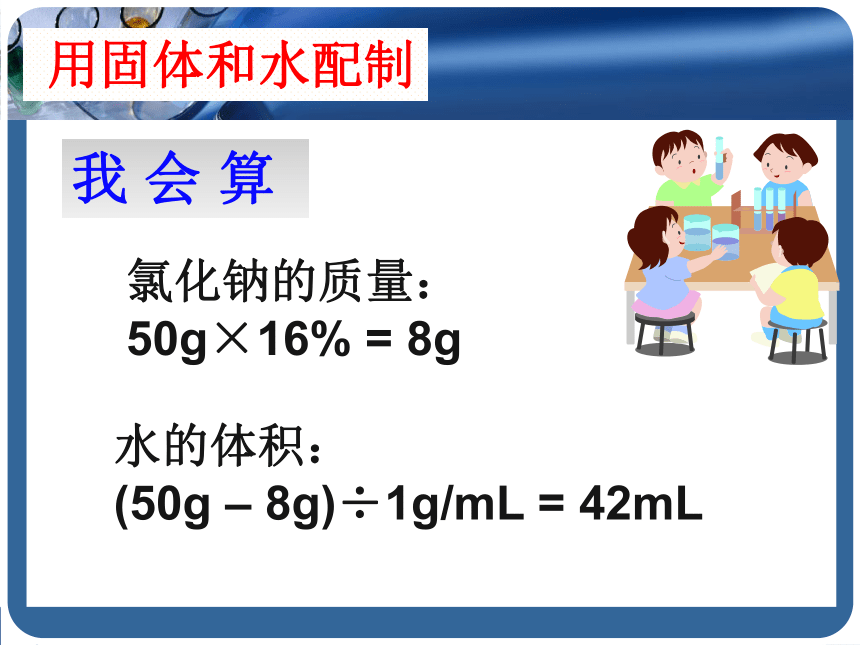
我 会 算
氯化钠的质量:
50g×16% = 8g
水的体积:
(50g – 8g)÷1g/mL = 42mL
用固体和水配制
我会称固体
称8克氯化钠固体
托盘天平、药匙
仪器:
用固体和水配制
托盘天平、药匙
我会称固体
称8克氯化钠固体
一、调节天平平衡
二、在左右托盘中各放一张质量相等的纸
三、在右盘中加5克的砝码,游码拨到刻度3处
四、在左盘中加氯化钠固体至天平平衡
五、取下固体倒入烧杯中,用镊子将砝码放回
砝码盒中,将游码归零
用固体和水配制
我会量水
量取42ml水
量筒、胶头滴管
仪器:
用固体和水配制
量筒、胶头滴管
我会量水
量取42ml水
选择量筒,用左手拿住量筒,使量筒略倾斜,
右手拿试剂瓶,使试剂瓶口紧挨着量筒口,将
水慢慢注入,待注入的量接近42ml时,把量筒
放在平整的桌面上,改用胶头滴管滴加到所需
要的量。读数时视线与凹液面最低处保持水平。
用固体和水配制
我会量水
量取42ml水
分次量取
麻烦且有
误差
为什么不用10ml或100ml的量筒呢?
用固体和水配制
量筒越大,管径越粗,
其精确度越小,由视线
的偏差造成的误差越大。
分次量取
麻烦且有
误差
量筒越大,管径越粗,
其精确度越小,由视线
的偏差造成的误差越大。
我会量水
量取42ml水
体验:用100ml量筒一次量42ml水,
倒入一只50ml量筒中。读数,感知
误差大小
用固体和水配制
我会量水
量取42ml水
选量筒原则:
用固体和水配制
应根据所取液体体积,尽量选用能
一次量取的最小规格的量筒。
我会溶解
用固体和水配制
仪器:
烧杯、玻璃棒
烧杯、玻璃棒
我会溶解
用固体和水配制
搅拌:
玻璃棒要沿着一个方向搅拌,
即一直是顺时针或者一直是
逆时针,以防止方向改变时
液体溅出。搅拌时玻璃棒尽
量不要碰到烧杯内壁。
我会贴标签
用固体和水配制
NaCl溶液
16%
出现下列情况时你是怎样处理的?
1、调平衡时指针向右偏转。
巩固练习
2、称氯化钠时指针向右偏转。
将平衡螺母向左边调整到平衡
向左盘中添加氯化钠到平衡
我会分析
在刚才的实验中,若遇到下列情况,将会对结果是否有影响?有何影响?
①左码右物称量氯化钠。
②称量时选用的砝码少了一个角。
③所用的氯化钠中含有少量杂质。
④溶解用的烧杯使用前不干燥。
⑤用量筒量取水时,俯视读数。
⑥量筒内的水没有全倒入烧杯中。
⑦称量前天平没有调平,且指针向右偏转。
⑧称量时使用的砝码生锈了(比原质量大了)。
⑨好配的溶液向细口瓶中倒时,有少量溅出。
大于16%
小于16%
大于16%
小于16%
小于16%
小于16%
大于16%
大于16%
无影响
误差分析:
用固体和水配制
小于16%的原因:溶质减少或者
溶剂增多。
大于16%的原因:溶质增多或者
溶剂减少。
我会小结
配制50g 16%的NaCl溶液
实验步骤:
⑴ 计算⑵ 称量⑶ 溶解⑷ 装瓶存放
天平、药匙、量筒、胶头滴管、烧杯
玻璃棒 、氯化钠固体、蒸馏水
实验用品:
用固体和水配制
大于16%的可能原因:①称量前天平没有
调平,且指针向右偏转。 ②量筒内的水
没有全倒入烧杯中。③用量筒量取水时,
俯视读数。 ④称量时使用的砝码生锈了
(比原质量大了)等。
误差分析:
用固体和水配制
小于16%的可能原因: ①左码右物称量
氯化钠。②溶解用的烧杯使用前不干燥。
③所用的氯化钠中含有少量杂质等。
溶液组成的定量表示(第二课时)
溶液的配制
鲁教版九年级化学上册
学习目标
1.通过分析0.9%的生理盐水等典型溶液,了解溶液在工农业生产、生活及科学研究中的广泛应用。
2.通过配制所需的氯化钠溶液,了解配制一定溶质质量分数的溶液的步骤和方法,进一步熟练药品的取用,托盘天平和量筒的使用技能;通过动手实验,对比感知“选量筒的原则”;通过对配制溶液方法的讨论,体会化学实验化繁为简的思想。
3.能关注实验细节,从定量认识溶液组成的角度分析误差形成的原因,培养严谨的科学态度。
溶液的配制
无土栽培 营养液
0.9%的氯化钠溶液
“0.9%”的含义
氯化钠溶液中
溶质和溶剂的质
量比为9:991
100克氯化钠溶液
中含有0.9克氯化钠
你知道生理盐水吗
明确任务
配制50克溶质质量分数为16%的氯化钠溶液
溶液的配制
溶液的配制
农业上常常用16%的
氯化钠溶液选种。
配制50克溶质质量分数为16%的氯化钠溶液
寻找配制方法
实验台上现有试剂(均为足量的)为:
氯化钠固体、25%的氯化钠溶液和蒸馏水
方法一:氯化钠固体和蒸馏水
方法二: 25%的氯化钠溶液和蒸馏水
方法三:氯化钠固体、 25%的氯化钠溶液
和蒸馏水
溶液的配制
方法一:氯化钠固体和蒸馏水
我 会 算
氯化钠的质量:
50g×16% = 8g
水的体积:
(50g – 8g)÷1g/mL = 42mL
用固体和水配制
我会称固体
称8克氯化钠固体
托盘天平、药匙
仪器:
用固体和水配制
托盘天平、药匙
我会称固体
称8克氯化钠固体
一、调节天平平衡
二、在左右托盘中各放一张质量相等的纸
三、在右盘中加5克的砝码,游码拨到刻度3处
四、在左盘中加氯化钠固体至天平平衡
五、取下固体倒入烧杯中,用镊子将砝码放回
砝码盒中,将游码归零
用固体和水配制
我会量水
量取42ml水
量筒、胶头滴管
仪器:
用固体和水配制
量筒、胶头滴管
我会量水
量取42ml水
选择量筒,用左手拿住量筒,使量筒略倾斜,
右手拿试剂瓶,使试剂瓶口紧挨着量筒口,将
水慢慢注入,待注入的量接近42ml时,把量筒
放在平整的桌面上,改用胶头滴管滴加到所需
要的量。读数时视线与凹液面最低处保持水平。
用固体和水配制
我会量水
量取42ml水
分次量取
麻烦且有
误差
为什么不用10ml或100ml的量筒呢?
用固体和水配制
量筒越大,管径越粗,
其精确度越小,由视线
的偏差造成的误差越大。
分次量取
麻烦且有
误差
量筒越大,管径越粗,
其精确度越小,由视线
的偏差造成的误差越大。
我会量水
量取42ml水
体验:用100ml量筒一次量42ml水,
倒入一只50ml量筒中。读数,感知
误差大小
用固体和水配制
我会量水
量取42ml水
选量筒原则:
用固体和水配制
应根据所取液体体积,尽量选用能
一次量取的最小规格的量筒。
我会溶解
用固体和水配制
仪器:
烧杯、玻璃棒
烧杯、玻璃棒
我会溶解
用固体和水配制
搅拌:
玻璃棒要沿着一个方向搅拌,
即一直是顺时针或者一直是
逆时针,以防止方向改变时
液体溅出。搅拌时玻璃棒尽
量不要碰到烧杯内壁。
我会贴标签
用固体和水配制
NaCl溶液
16%
出现下列情况时你是怎样处理的?
1、调平衡时指针向右偏转。
巩固练习
2、称氯化钠时指针向右偏转。
将平衡螺母向左边调整到平衡
向左盘中添加氯化钠到平衡
我会分析
在刚才的实验中,若遇到下列情况,将会对结果是否有影响?有何影响?
①左码右物称量氯化钠。
②称量时选用的砝码少了一个角。
③所用的氯化钠中含有少量杂质。
④溶解用的烧杯使用前不干燥。
⑤用量筒量取水时,俯视读数。
⑥量筒内的水没有全倒入烧杯中。
⑦称量前天平没有调平,且指针向右偏转。
⑧称量时使用的砝码生锈了(比原质量大了)。
⑨好配的溶液向细口瓶中倒时,有少量溅出。
大于16%
小于16%
大于16%
小于16%
小于16%
小于16%
大于16%
大于16%
无影响
误差分析:
用固体和水配制
小于16%的原因:溶质减少或者
溶剂增多。
大于16%的原因:溶质增多或者
溶剂减少。
我会小结
配制50g 16%的NaCl溶液
实验步骤:
⑴ 计算⑵ 称量⑶ 溶解⑷ 装瓶存放
天平、药匙、量筒、胶头滴管、烧杯
玻璃棒 、氯化钠固体、蒸馏水
实验用品:
用固体和水配制
大于16%的可能原因:①称量前天平没有
调平,且指针向右偏转。 ②量筒内的水
没有全倒入烧杯中。③用量筒量取水时,
俯视读数。 ④称量时使用的砝码生锈了
(比原质量大了)等。
误差分析:
用固体和水配制
小于16%的可能原因: ①左码右物称量
氯化钠。②溶解用的烧杯使用前不干燥。
③所用的氯化钠中含有少量杂质等。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
