2.3制取氧气同步练习——2021-2022学年人教版九年级化学上册(word版 含解析)
文档属性
| 名称 | 2.3制取氧气同步练习——2021-2022学年人教版九年级化学上册(word版 含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 128.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-20 00:00:00 | ||
图片预览


文档简介
制取氧气
一、单选题
实验室用过氧化氢溶液和二氧化锰粉末制取较纯净的氧气,从如图中选取的装置最佳组合是
A. B. C. D.
下列对催化剂的描述正确的是
A. 二氧化锰可作为各种化学反应的催化剂
B. 在化学反应前后,催化剂本身的质量和所有性质均未改变
C. 并不是所有化学反应都需要催化剂,但分解反应一定需要催化剂
D. 某些化学反应可以有多种催化剂,某些催化剂可催化多个化学反应
有关催化剂的说法不正确的是
A. 在化学反应后其化学性质不发生变化
B. 在化学反应后质量不发生变化
C. 改变了化学反应速率
D. 可增加生成物的质量
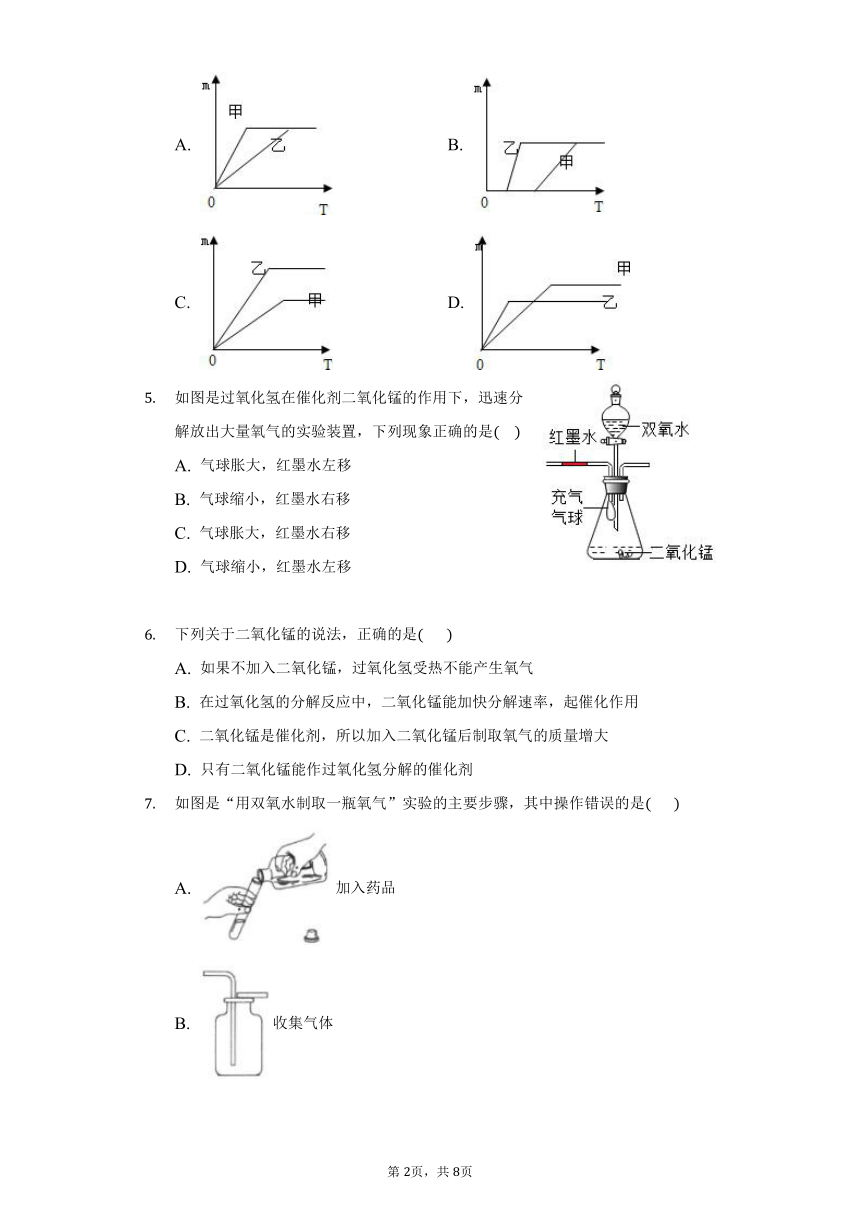
甲同学取12g 的双氧水,乙同学取10g 的双氧水同时做制氧气的实验,乙同学在双氧水中加入2g二氧化锰,则这两位同学所制得的氧气的质量随加热时间的变化曲线为
A. B.
C. D.
如图是过氧化氢在催化剂二氧化锰的作用下,迅速分解放出大量氧气的实验装置,下列现象正确的是
A. 气球胀大,红墨水左移
B. 气球缩小,红墨水右移
C. 气球胀大,红墨水右移
D. 气球缩小,红墨水左移
下列关于二氧化锰的说法,正确的是
A. 如果不加入二氧化锰,过氧化氢受热不能产生氧气
B. 在过氧化氢的分解反应中,二氧化锰能加快分解速率,起催化作用
C. 二氧化锰是催化剂,所以加入二氧化锰后制取氧气的质量增大
D. 只有二氧化锰能作过氧化氢分解的催化剂
如图是“用双氧水制取一瓶氧气”实验的主要步骤,其中操作错误的是
A. 加入药品
B. 收集气体
C. 检查装置气密性
D. 验满
二氧化锰在双氧水分解制取氧气的反应中,所起的作用是
A. 增加氧气的质量 B. 节省双氧水的质量
C. 提高氧气的质量 D. 使双氧水迅速分解放出氧气
在实验室里制取氧气,既可以采用分解过氧化氢的方法,也可以采用分解氯酸钾的方法,上述两种方法的主要共同点有
都需要用二氧化锰作催化剂
反应都需要加热
都是分解反应
实验所需仪器都相同
A. B. C. D.
实验室制取氧气时,必须满足的条件是
A. 必须使用催化剂
B. 必须使用含氧元素的物质作反应物
C. 必须用纯净物制取
D. 必须加热
二、实验题
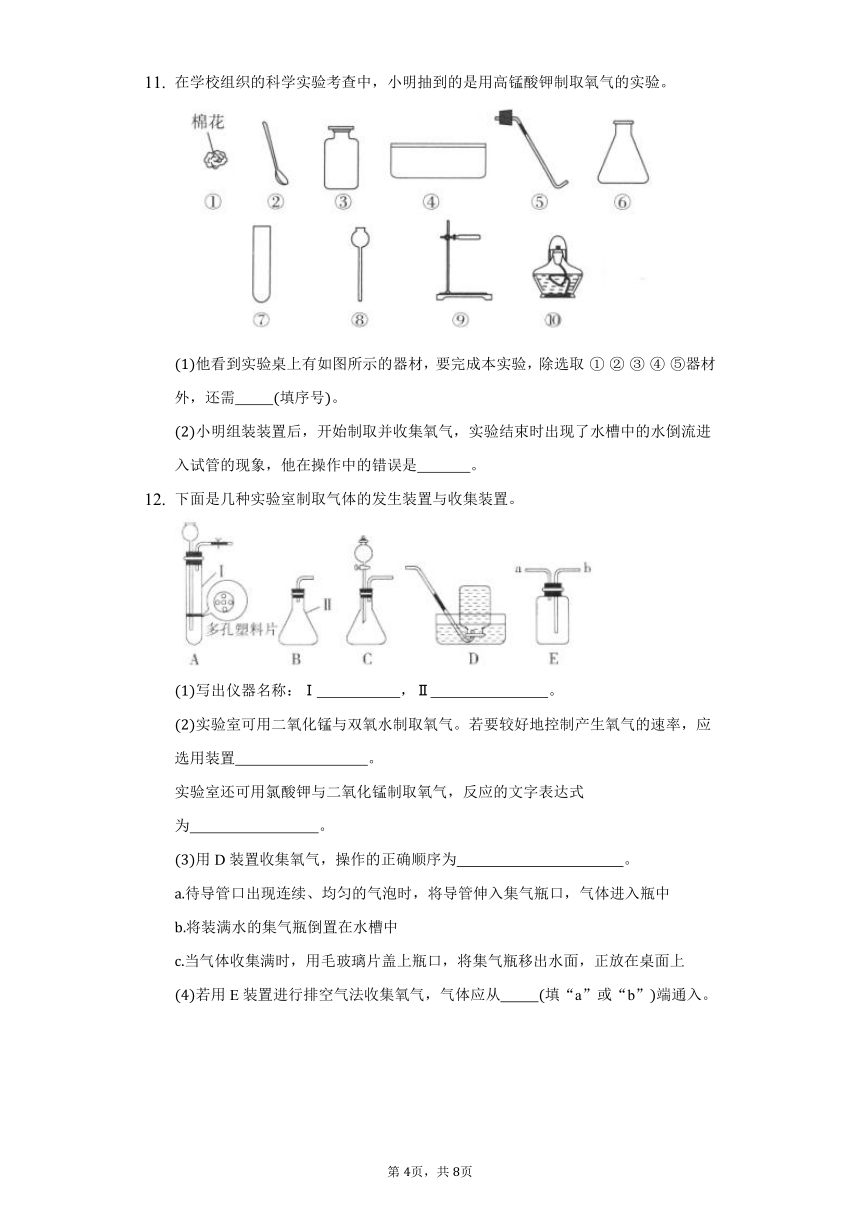
在学校组织的科学实验考查中,小明抽到的是用高锰酸钾制取氧气的实验。
他看到实验桌上有如图所示的器材,要完成本实验,除选取器材外,还需 填序号。
小明组装装置后,开始制取并收集氧气,实验结束时出现了水槽中的水倒流进入试管的现象,他在操作中的错误是 。
下面是几种实验室制取气体的发生装置与收集装置。
写出仪器名称:Ⅰ ,Ⅱ 。
实验室可用二氧化锰与双氧水制取氧气。若要较好地控制产生氧气的速率,应选用装置 。
实验室还可用氯酸钾与二氧化锰制取氧气,反应的文字表达式为 。
用D装置收集氧气,操作的正确顺序为 。
待导管口出现连续、均匀的气泡时,将导管伸入集气瓶口,气体进入瓶中
将装满水的集气瓶倒置在水槽中
当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面,正放在桌面上
若用E装置进行排空气法收集氧气,气体应从 填“a”或“b”端通入。
答案和解析
1.【答案】B
【解析】
【分析】
本考点主要考查了气体的制取装置和收集装置的选择,基础性比较强.
【解答】
气体的制取装置的选择与反应物的状态和反应的条件有关,用双氧水和二氧化锰制氧气为固液混合,不需要加热,选择;
气体的收集装置的选择与气体的密度和溶解性有关,制取较纯净的氧气,应该选用排水法,选择.
故选:B。
2.【答案】D
【解析】解:A、二氧化锰不能作各种化学反应的催化剂,故选项说法错误。
B、在化学反应前后,催化剂本身的质量和化学性质而不是所有性质均未改变,故选项说法错误。
C、并不是所有化学反应都需要催化剂,分解反应不一定需要催化剂,如碳酸分解生成二氧化碳和水,不需要催化剂,故选项说法错误。
D、某些化学反应可以有多种催化剂,如过氧化氢溶液分解催化剂有:二氧化锰、红砖粉末、硫酸铜溶液等;某些催化剂可催化多个化学反应,故选项说法正确。
故选:D。
在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂又叫触媒催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.
本题难度不大,考查对催化剂概念的理解,掌握催化剂的特征“一变二不变”是正确解答本题的关键.
3.【答案】D
【解析】解:A、催化剂反应前后化学性质不变,选项A正确;
B、催化剂反应前后质量不变,选项B正确;
C、催化剂可以改变反应速率,选项C正确;
D、催化剂不能增加生成物质量,选项D错误;
故选:D。
根据催化剂的性质和特点分析回答此题。
在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答。
4.【答案】D
【解析】解:甲同学取12g 的双氧水,乙同学取10g 的双氧水同时做制氧气的实验,甲的过氧化氢的质量大,故生成的氧气的质量多;乙同学在双氧水中加入 2g二氧化锰,则乙同学反应产生氧气的速率大于甲同学反应产生氧气的速率,观察选项,故选D。
根据二氧化锰在过氧化氢分解反应中的作用进行分析解答,催化剂只能改变化学反应的速率,不能改变生成物的质量.
本题考查了二氧化锰对过氧化氢的催化作用,完成此题,可以依据已有的知识进行.
5.【答案】D
【解析】
【分析】
本题考查了二氧化锰在过氧化氢反应中的作用以及压强的知识,完成此题,可以依据已有的知识进行。根据二氧化锰的催化作用以及气体压强的知识进行分析解答即可。
【解答】
过氧化氢在催化剂二氧化锰的作用下,迅速分解放出大量氧气,则瓶内的压强变大,充气的气球缩小,红墨水向左移动。
故选:D。
6.【答案】B
【解析】解:A、如果不加入二氧化锰,过氧化氢受热还是可以产生氧气的,故 A错误;
B、在过氧化氢的分解反应中,二氧化锰能加快分解速率,起催化作用,故B正确;
C、催化剂只能改变化学速率,不能增大或减少生成物的质量,故C错误;
D、一种反应可以有多种物质作催化剂,过氧化氢分解的催化剂不是只有二氧化锰,故D错误;
故选B。
7.【答案】D
【解析】向试管中倾倒液体药品时,瓶塞要倒放,标签要对着手心,瓶口紧挨试管口,试管稍倾斜,A项所示操作正确;氧气密度比空气的大,可用向上排空气法收集,B项所示操作正确;检查装置气密性的方法:把导管的一端浸没在水里,用手紧握容器外壁,若导管口有气泡冒出,则装置不漏气,C项所示操作正确;用向上排空气法收集氧气,检验氧气是否收集满时,应将带火星的木条放在集气瓶口,不能伸入瓶中,D项所示操作错误。
8.【答案】D
【解析】解:二氧化锰在双氧水分解制取氧气的反应中只是加快双氧水的分解速率,而本身的化学性质和质量在化学反应前后都不变,不会增加或提高氧气的质量,也不会节省双氧水的质量。
故选:D。
催化剂在反应中表现出改变反应速率的特性,而本身的化学性质和质量都不变的特点,与参加反应的双氧水的质量及生成氧气的质量多少无关.
此题主要考查能改变反应速率、化学性质不变、质量不变是催化剂在一个反应中表现出来的重要的特征.学生们应熟记催化剂的特征,以便探究其它反应中出现催化剂的题型.
9.【答案】A
【解析】本题运用比较法解答。比较用过氧化氢和用氯酸钾制取氧气的两种方法,发现二者都要用二氧化锰作催化剂,都发生分解反应;不同的是氯酸钾制取氧气需要加热,所用仪器中一定有酒精灯,而用过氧化氢制取氧气不需加热,不用酒精灯。
10.【答案】B
【解析】解:A、实验室用高锰酸钾制取氧气时,只加热即可,不需用催化剂,故错误;
B、根据质量守恒定律,化学反应前后元素的种类不变,要制得氧气,反应物中必须含有氧元素,故正确;
C、实验室制取氧气时,不一定用纯净物制取,故错误;
D、分解过氧化氢溶液制氧气时不需要加热,故错误;
故选B。
11.【答案】
先撤酒精灯,后从水槽中移出导管
【解析】解:完成高锰酸钾制取氧气的实验,,除选取器材外,还需 。
小明组装装置后,开始制取并收集氧气,实验结束时出现了水槽中的水倒流进入试管的现象,他在操作中的错误是先撤酒精灯,后从水槽中移出导管。
12.【答案】试管;锥形瓶;
;氯酸钾氯化钾氧气;
;
【解析】图中仪器Ⅰ为试管,仪器Ⅱ为锥形瓶。
实验室用二氧化锰与双氧水制取氧气,应该选择固液不加热型气体发生装置,若要较好地控制产生氧气的速率,应选择装置C。实验室用氯酸钾与二氧化锰制取氧气,同时还生成氯化钾。
装置为排水法集气装置,操作的正确顺序为将装满水的集气瓶倒置在水槽中;待导管口出现连续、均匀的气泡时,将导管伸入集气瓶口,气体进入瓶中;当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面放置。
因为氧气的密度大于空气,应用向上排空气法收集,若用E装置进行排空气法收集氧气,气体应从b端通入,使瓶内原有空气从a端排出。
第2页,共2页
第1页,共1页
一、单选题
实验室用过氧化氢溶液和二氧化锰粉末制取较纯净的氧气,从如图中选取的装置最佳组合是
A. B. C. D.
下列对催化剂的描述正确的是
A. 二氧化锰可作为各种化学反应的催化剂
B. 在化学反应前后,催化剂本身的质量和所有性质均未改变
C. 并不是所有化学反应都需要催化剂,但分解反应一定需要催化剂
D. 某些化学反应可以有多种催化剂,某些催化剂可催化多个化学反应
有关催化剂的说法不正确的是
A. 在化学反应后其化学性质不发生变化
B. 在化学反应后质量不发生变化
C. 改变了化学反应速率
D. 可增加生成物的质量
甲同学取12g 的双氧水,乙同学取10g 的双氧水同时做制氧气的实验,乙同学在双氧水中加入2g二氧化锰,则这两位同学所制得的氧气的质量随加热时间的变化曲线为
A. B.
C. D.
如图是过氧化氢在催化剂二氧化锰的作用下,迅速分解放出大量氧气的实验装置,下列现象正确的是
A. 气球胀大,红墨水左移
B. 气球缩小,红墨水右移
C. 气球胀大,红墨水右移
D. 气球缩小,红墨水左移
下列关于二氧化锰的说法,正确的是
A. 如果不加入二氧化锰,过氧化氢受热不能产生氧气
B. 在过氧化氢的分解反应中,二氧化锰能加快分解速率,起催化作用
C. 二氧化锰是催化剂,所以加入二氧化锰后制取氧气的质量增大
D. 只有二氧化锰能作过氧化氢分解的催化剂
如图是“用双氧水制取一瓶氧气”实验的主要步骤,其中操作错误的是
A. 加入药品
B. 收集气体
C. 检查装置气密性
D. 验满
二氧化锰在双氧水分解制取氧气的反应中,所起的作用是
A. 增加氧气的质量 B. 节省双氧水的质量
C. 提高氧气的质量 D. 使双氧水迅速分解放出氧气
在实验室里制取氧气,既可以采用分解过氧化氢的方法,也可以采用分解氯酸钾的方法,上述两种方法的主要共同点有
都需要用二氧化锰作催化剂
反应都需要加热
都是分解反应
实验所需仪器都相同
A. B. C. D.
实验室制取氧气时,必须满足的条件是
A. 必须使用催化剂
B. 必须使用含氧元素的物质作反应物
C. 必须用纯净物制取
D. 必须加热
二、实验题
在学校组织的科学实验考查中,小明抽到的是用高锰酸钾制取氧气的实验。
他看到实验桌上有如图所示的器材,要完成本实验,除选取器材外,还需 填序号。
小明组装装置后,开始制取并收集氧气,实验结束时出现了水槽中的水倒流进入试管的现象,他在操作中的错误是 。
下面是几种实验室制取气体的发生装置与收集装置。
写出仪器名称:Ⅰ ,Ⅱ 。
实验室可用二氧化锰与双氧水制取氧气。若要较好地控制产生氧气的速率,应选用装置 。
实验室还可用氯酸钾与二氧化锰制取氧气,反应的文字表达式为 。
用D装置收集氧气,操作的正确顺序为 。
待导管口出现连续、均匀的气泡时,将导管伸入集气瓶口,气体进入瓶中
将装满水的集气瓶倒置在水槽中
当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面,正放在桌面上
若用E装置进行排空气法收集氧气,气体应从 填“a”或“b”端通入。
答案和解析
1.【答案】B
【解析】
【分析】
本考点主要考查了气体的制取装置和收集装置的选择,基础性比较强.
【解答】
气体的制取装置的选择与反应物的状态和反应的条件有关,用双氧水和二氧化锰制氧气为固液混合,不需要加热,选择;
气体的收集装置的选择与气体的密度和溶解性有关,制取较纯净的氧气,应该选用排水法,选择.
故选:B。
2.【答案】D
【解析】解:A、二氧化锰不能作各种化学反应的催化剂,故选项说法错误。
B、在化学反应前后,催化剂本身的质量和化学性质而不是所有性质均未改变,故选项说法错误。
C、并不是所有化学反应都需要催化剂,分解反应不一定需要催化剂,如碳酸分解生成二氧化碳和水,不需要催化剂,故选项说法错误。
D、某些化学反应可以有多种催化剂,如过氧化氢溶液分解催化剂有:二氧化锰、红砖粉末、硫酸铜溶液等;某些催化剂可催化多个化学反应,故选项说法正确。
故选:D。
在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂又叫触媒催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.
本题难度不大,考查对催化剂概念的理解,掌握催化剂的特征“一变二不变”是正确解答本题的关键.
3.【答案】D
【解析】解:A、催化剂反应前后化学性质不变,选项A正确;
B、催化剂反应前后质量不变,选项B正确;
C、催化剂可以改变反应速率,选项C正确;
D、催化剂不能增加生成物质量,选项D错误;
故选:D。
根据催化剂的性质和特点分析回答此题。
在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答。
4.【答案】D
【解析】解:甲同学取12g 的双氧水,乙同学取10g 的双氧水同时做制氧气的实验,甲的过氧化氢的质量大,故生成的氧气的质量多;乙同学在双氧水中加入 2g二氧化锰,则乙同学反应产生氧气的速率大于甲同学反应产生氧气的速率,观察选项,故选D。
根据二氧化锰在过氧化氢分解反应中的作用进行分析解答,催化剂只能改变化学反应的速率,不能改变生成物的质量.
本题考查了二氧化锰对过氧化氢的催化作用,完成此题,可以依据已有的知识进行.
5.【答案】D
【解析】
【分析】
本题考查了二氧化锰在过氧化氢反应中的作用以及压强的知识,完成此题,可以依据已有的知识进行。根据二氧化锰的催化作用以及气体压强的知识进行分析解答即可。
【解答】
过氧化氢在催化剂二氧化锰的作用下,迅速分解放出大量氧气,则瓶内的压强变大,充气的气球缩小,红墨水向左移动。
故选:D。
6.【答案】B
【解析】解:A、如果不加入二氧化锰,过氧化氢受热还是可以产生氧气的,故 A错误;
B、在过氧化氢的分解反应中,二氧化锰能加快分解速率,起催化作用,故B正确;
C、催化剂只能改变化学速率,不能增大或减少生成物的质量,故C错误;
D、一种反应可以有多种物质作催化剂,过氧化氢分解的催化剂不是只有二氧化锰,故D错误;
故选B。
7.【答案】D
【解析】向试管中倾倒液体药品时,瓶塞要倒放,标签要对着手心,瓶口紧挨试管口,试管稍倾斜,A项所示操作正确;氧气密度比空气的大,可用向上排空气法收集,B项所示操作正确;检查装置气密性的方法:把导管的一端浸没在水里,用手紧握容器外壁,若导管口有气泡冒出,则装置不漏气,C项所示操作正确;用向上排空气法收集氧气,检验氧气是否收集满时,应将带火星的木条放在集气瓶口,不能伸入瓶中,D项所示操作错误。
8.【答案】D
【解析】解:二氧化锰在双氧水分解制取氧气的反应中只是加快双氧水的分解速率,而本身的化学性质和质量在化学反应前后都不变,不会增加或提高氧气的质量,也不会节省双氧水的质量。
故选:D。
催化剂在反应中表现出改变反应速率的特性,而本身的化学性质和质量都不变的特点,与参加反应的双氧水的质量及生成氧气的质量多少无关.
此题主要考查能改变反应速率、化学性质不变、质量不变是催化剂在一个反应中表现出来的重要的特征.学生们应熟记催化剂的特征,以便探究其它反应中出现催化剂的题型.
9.【答案】A
【解析】本题运用比较法解答。比较用过氧化氢和用氯酸钾制取氧气的两种方法,发现二者都要用二氧化锰作催化剂,都发生分解反应;不同的是氯酸钾制取氧气需要加热,所用仪器中一定有酒精灯,而用过氧化氢制取氧气不需加热,不用酒精灯。
10.【答案】B
【解析】解:A、实验室用高锰酸钾制取氧气时,只加热即可,不需用催化剂,故错误;
B、根据质量守恒定律,化学反应前后元素的种类不变,要制得氧气,反应物中必须含有氧元素,故正确;
C、实验室制取氧气时,不一定用纯净物制取,故错误;
D、分解过氧化氢溶液制氧气时不需要加热,故错误;
故选B。
11.【答案】
先撤酒精灯,后从水槽中移出导管
【解析】解:完成高锰酸钾制取氧气的实验,,除选取器材外,还需 。
小明组装装置后,开始制取并收集氧气,实验结束时出现了水槽中的水倒流进入试管的现象,他在操作中的错误是先撤酒精灯,后从水槽中移出导管。
12.【答案】试管;锥形瓶;
;氯酸钾氯化钾氧气;
;
【解析】图中仪器Ⅰ为试管,仪器Ⅱ为锥形瓶。
实验室用二氧化锰与双氧水制取氧气,应该选择固液不加热型气体发生装置,若要较好地控制产生氧气的速率,应选择装置C。实验室用氯酸钾与二氧化锰制取氧气,同时还生成氯化钾。
装置为排水法集气装置,操作的正确顺序为将装满水的集气瓶倒置在水槽中;待导管口出现连续、均匀的气泡时,将导管伸入集气瓶口,气体进入瓶中;当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面放置。
因为氧气的密度大于空气,应用向上排空气法收集,若用E装置进行排空气法收集氧气,气体应从b端通入,使瓶内原有空气从a端排出。
第2页,共2页
第1页,共1页
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
