2021-2022学年九年级全册化学鲁教版(五四制)常考实验小练(6)影响铁锈蚀的因素
文档属性
| 名称 | 2021-2022学年九年级全册化学鲁教版(五四制)常考实验小练(6)影响铁锈蚀的因素 |
|
|
| 格式 | doc | ||
| 文件大小 | 390.2KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-20 00:00:00 | ||
图片预览



文档简介
2021-2022学年九年级全册化学鲁教版(五四制)常考实验小练
(6)影响铁锈蚀的因素
一、知识讲解
1、实验目的:通过实验,探究钢铁制品锈蚀的条件。
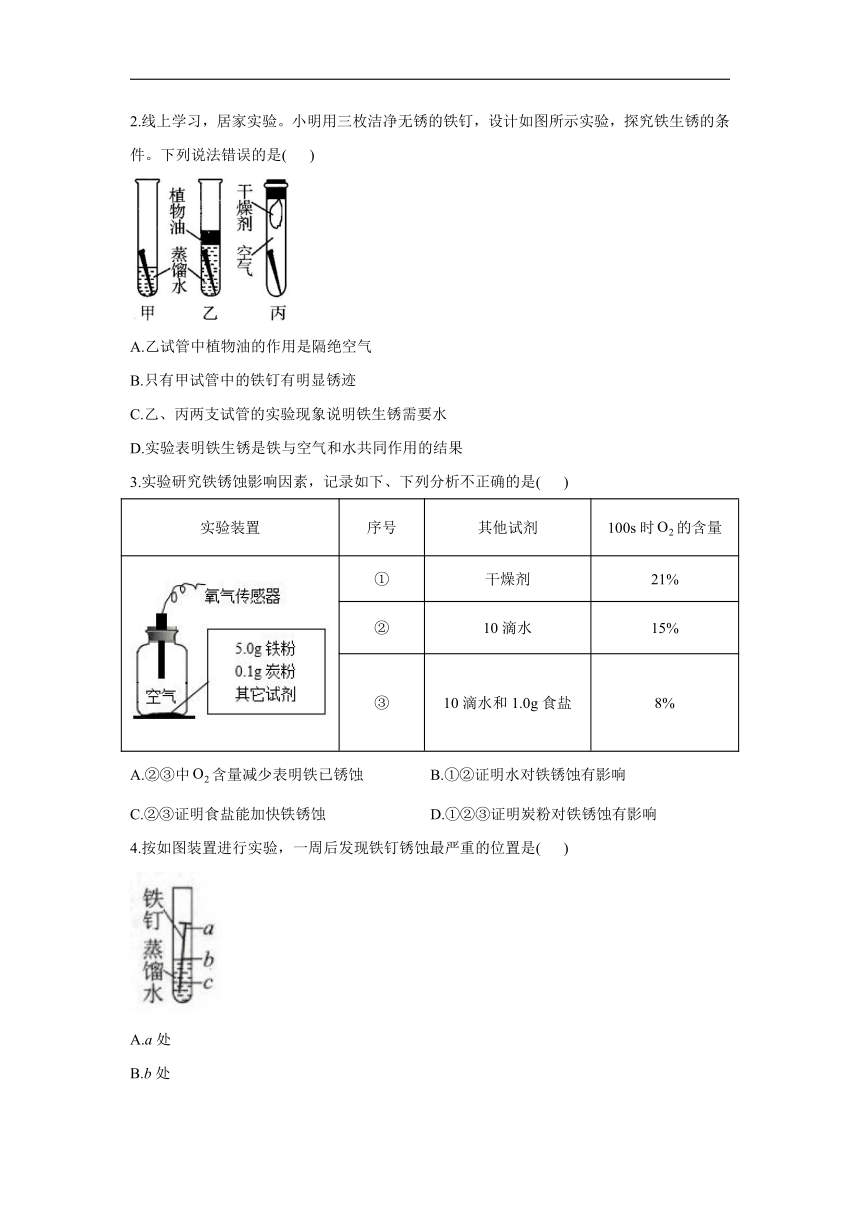
2、实验装置
3、实验现象
观察时间 ① ② ③ ④ ⑤
立即观察 无明显现象 无明显现象 无明显现象 无明显现象 无明显现象
四天后观察 无明显现象 无明显现象 与水面相接触的部分产生较多铁锈,其余部分也出现锈斑 整枚铁钉已严重锈蚀 整枚铁钉已严重锈蚀
4、实验分析
通过试管①、②可知,铁钉在只与氧气或水接触时,不易生锈;对比试管③可知,钢铁锈蚀与氧气和水有关;试管④和试管⑤说明了盐溶液与酸溶液都会影响钢铁的锈蚀。
二、跟踪练习
1.如图是探究铁制品锈蚀的条件时设计的实验。下列对比实验设计与探究的条件,对应关系正确的是( )
A.甲和丁:水 B.乙和丙:空气 C.甲和丙:空气 D.甲和乙:水
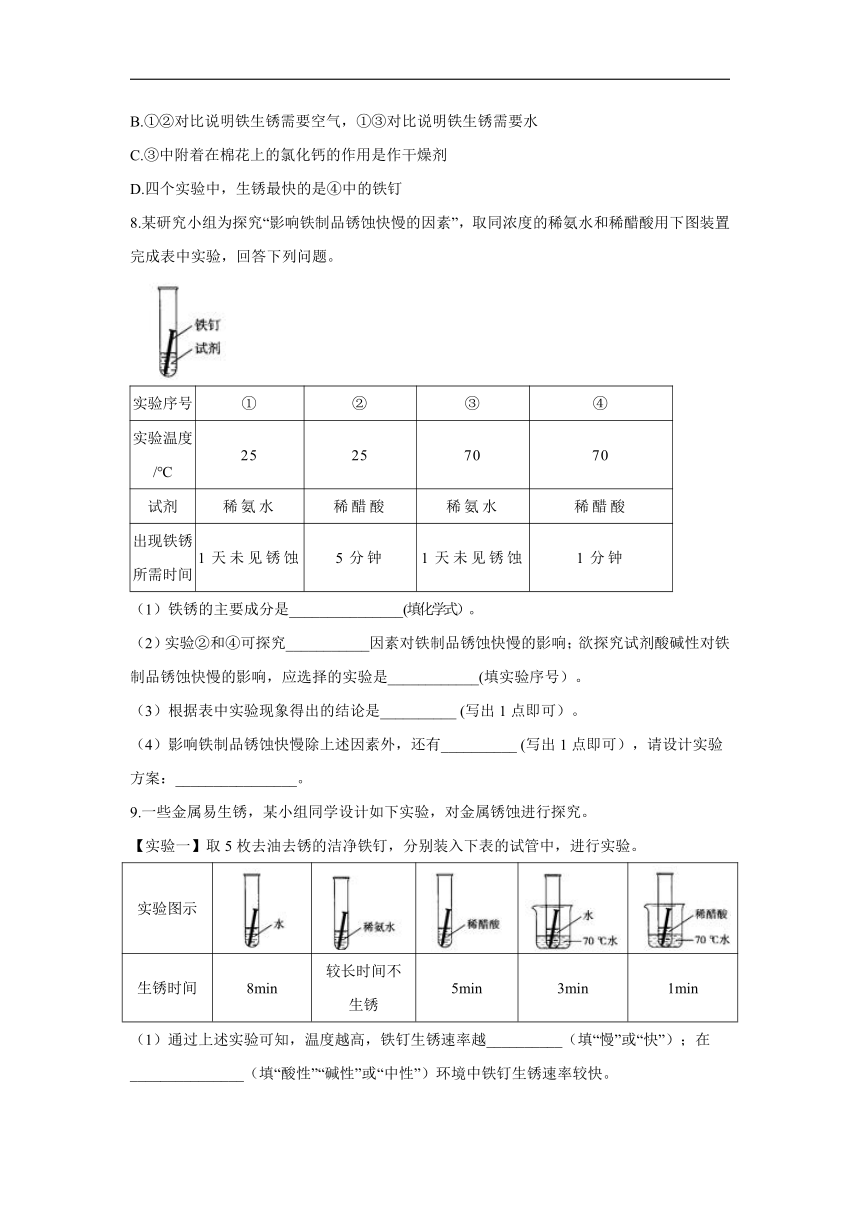
2.线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如图所示实验,探究铁生锈的条件。下列说法错误的是( )
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙、丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
3.实验研究铁锈蚀影响因素,记录如下、下列分析不正确的是( )
实验装置 序号 其他试剂 100s时的含量
① 干燥剂 21%
② 10滴水 15%
③ 10滴水和1.0g食盐 8%
A.②③中含量减少表明铁已锈蚀 B.①②证明水对铁锈蚀有影响
C.②③证明食盐能加快铁锈蚀 D.①②③证明炭粉对铁锈蚀有影响
4.按如图装置进行实验,一周后发现铁钉锈蚀最严重的位置是( )
A.a处
B.b处
C.c处
D.三处同样严重
5. “对比法”是实验探究中常用的一种科学方法。以下铁钉生锈实验的设计(如图所示),得出的结论不正确的是( )
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.保持铁制品表面清洁干燥可以防止铁生锈
6.为了探究铁制品锈蚀的条件,小明用普通铁钉、纯铁钉同时进行下面的四组实验,一段时间后只在实验Ⅰ中观察到了红棕色锈斑,其他均无明显变化。下列说法错误的是( )
A.Ⅰ和Ⅱ说明铁制品锈蚀需要
B.Ⅰ和Ⅲ说明铁制品锈蚀需要
C.Ⅰ和Ⅳ说明和同时存在,铁制品不一定发生锈蚀
D.Ⅲ和Ⅳ说明铁制品锈蚀与铁制品内部结构有关
7.如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是( )
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
8.某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸用下图装置完成表中实验,回答下列问题。
实验序号 ① ② ③ ④
实验温度/℃ 25 25 70 70
试剂 稀氨水 稀醋酸 稀氨水 稀醋酸
出现铁锈 所需时间 1天未见锈蚀 5分钟 1天未见锈蚀 1分钟
(1)铁锈的主要成分是_______________(填化学式)。
(2)实验②和④可探究___________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是____________(填实验序号)。
(3)根据表中实验现象得出的结论是__________ (写出1点即可)。
(4)影响铁制品锈蚀快慢除上述因素外,还有__________ (写出1点即可),请设计实验方案:________________。
9.一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究。
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验。
实验图示
生锈时间 8min 较长时间不生锈 5min 3min 1min
(1)通过上述实验可知,温度越高,铁钉生锈速率越__________(填“慢”或“快”);在_______________(填“酸性”“碱性”或“中性”)环境中铁钉生锈速率较快。
【实验二】为探究铁锈的成分,用图甲所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全)。
【査阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收。
(2)请指出图甲所示实验装置的一个明显缺陷:_____________。
(3)加热前,先通入CO一段时间,目的是_________________。
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有___________元素,从而推断出空气中的__________参加了铁生锈反应。
【实验记录】
质量/g 铁锈样品的质量/g 装置B的质量/g 装置C的质量/g
反应前 23.2 232.4 198.2
反应后 一 239.6 211.4
(5)根据上表数据推算,可确定铁锈的成分,用表示,则=__;若缺少D装置,的值会__________________(填“偏大”“偏小”或“无影响”)。
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图乙所示装置,试管内可选用的物质如下
①
②水
③
④和
⑤和水
⑥和水
⑦、和水
至少需要选用_____________(填数字序号),才能达到探究镁带锈蚀的条件。
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁的化学方程式:________________________。
10.世界上每年因锈蚀而损失大量铁制品。某化学小组设计如下实验探究铁生锈的条件及影响生锈速率的因素。
【进行实验】
实验1:分别取铁钉按如图装置所示,放置一周,结果如下:
序号 1-1 1-2 1-3
实验
现象 无明显现象 无明显现象 铁钉表面有红棕色固体
实验2:分别取铁钉浸于等体积的不同试剂中,放置一周,结果如下:
序号 2-1 2-2 2-3
试剂种类 蒸馏水 3%的NaCl溶液 3%的稀盐酸
U形管左侧液面 上升1.2cm 上升3.7cm 上升5.3cm
【解释与结论】
(1)铁生锈属于_____(填“物理”或“化学”)变化。
(2)铁锈中含有铁、氧、氢元素,从元素守恒角度说明理由:_____。
(3)实验1中,证明铁生锈需要与水接触的现象是_____。
(4)实验2-1中,U形管左侧液面上升的原因是_____。
(5)实验2的目的是_____。
【反思与评价】
(6)结合本实验,对于铁制品的保存,你的一条建议是_____。
答案以及解析
1.答案:A
2.答案:C
解析:乙试管中的铁钉只与蒸馏水接触,丙试管中的铁钉只与空气接触,乙、丙两支试管中的铁钉均不生锈,两试管中现象对比,不能得出铁生锈需要水,C错误。
3.答案:D
解析: ②③中氧气含量减少,说明有氧气参加了反应,铁已锈蚀,A正确;①②对比氧气含量由21%减少至15%,①中放有干燥剂,铁只与氧气接触,没有锈蚀,②中放有10滴水,铁与水、氧气同时接触,发生锈蚀,对比可知水对铁锈蚀有影响,B正确;对比
②③中氧气含量,可知③中铁锈蚀速度快,证明食盐能加快铁锈蚀,C正确;题中炭粉不是变量,无法得出炭粉对铁锈蚀的影响,D不正确。
4.答案:B
解析:本题考查铁的锈蚀条件。铁生锈是铁与氧气水共同作用发生化学反应的结果。图中,a处位于空气中,水比较少,b处位于水与空气的交界处,有充足的氧气和水,c处位于蒸馏水内部,氧气比较少,所以,根据铁生锈所需的条件,b处锈蚀最严重,故选B。
5.答案:B
解析:对比①②可以说明铁生锈一定要有氧气参加,对比①③可以说明铁生锈一定要有水参加,A、C正确;对比②③,变量不唯一,无法获得结论,B错误。防止铁制品生锈的方法之一是保持铁制品表面干燥洁净,D正确。
6.答案:D
解析:实验Ⅲ和Ⅳ存在两个不同的变量,不能互为对照实验,无法说明铁制品锈蚀与铁制品内部结构有关。故选D。
7.答案:A
解析:本题考查铁生锈的条件。铁在氧气、水并存时易生锈,①中甲、乙、丙三处比较,生锈最明显的地方是乙,A项错误;①中的铁钉能与氧气、水充分接触,②中的铁钉只能与水接触,③中的铁钉只能与干燥的空气接触,一段时间后,①中的铁钉生锈,另外两支试管的铁钉没有生锈,①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水,B项正确;氯化钙具有吸水性,③中附着在棉花上的氯化钙的作用是作干燥剂,C项正确;④中铁钉接触到的是纯氧气及水,四个实验中,生锈最快的是④中的铁钉,D项正确。
8.答案:(1)
(2)温度;①②(或③④)
(3)相同条件下,酸性越强,金属生锈越快
(4)酸的浓度;相同条件下,取两份浓度不同的醋酸,分别在25℃时,观察铁钉生锈时间
解析:(1)铁锈的主要成分是氧化铁,铁生锈是铁与空气中的氧气、水共同作用的结果。铁锈的主要成分是。
(2)实验②和④可探究温度因素对铁制品锈蚀快慢的影响,欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是①②或③④。
(3)根据表中实验现象得出的结论是相同条件下,酸性越强,金属生锈越快等。
(4)影响铁制品锈蚀快慢除上述因素外,还有酸的浓度,设计的实验方案是相同条件下,取两份浓度不同的醋酸,分别在25℃时,观察铁钉生锈所用的时间。
9.答案:(1)快;酸性
(2)没有进行尾气处理
(3)排尽装置内的空气,防止发生爆炸
(4)氢;水蒸气
(5)4;偏小
(6)④⑤⑥⑦
(7)
解析:(1)对比实验1和实验4,实验3和实验5可知,温度越高铁钉生锈速率越快;对比实验1、2、3可知,铁钉在酸性环境中锈蚀。
(2)尾气中含有有毒的一氧化碳气体,该装置中没有将其处理。
(3)一氧化碳具有可燃性,不纯时加热或点燃易发生爆炸,所以先通入CO一段时间,排尽装置内的空气。
(4)无水硫酸铜能吸收水而变蓝,将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,这说明了反应后有水生成,说明铁锈中含有氢元素,也就是铁锈蚀的过程中有水蒸气参与。
(5)硬质玻璃管内发生反应的化学方程式为,根据实验数据可知,反应中生成水的质量为(239.6g-232.4g)=7.2g,生成二氧化碳的质量为(211.4g-198.2g)=13.2g。设参加反应的CO的质量为,则
,解得=84g,由质量守恒定律可知,生成铁的质量为23.2g+8.4g-13.2g-7.2g=112g;由于反应前后元素的种类与质量不变,所以23.2g中含铁元素的质量为11.2g;含有“”部分质量为7.2g;则余下的氧元素质量为23.2g-112g-7.2g=4.8g,则,故的化学式为。D装置中的碱石灰既能吸收水也能吸收,防止空气中二氧化碳与水被装置C吸收而造成质量偏大,若没有装置D,则装置C因为吸收了空气中的水蒸气和二氧化碳而质量偏大,由此计算出的二氧化碳质量偏大,导致氧元素的质量偏大,的值偏小。
(6)通过实验探究镁带在空气中锈蚀的条件,应该选择④和;⑤和水;⑥和水;⑦、和水四组实验进行对比。
(7)由镁带在空气中锈蚀,生成碱式碳酸镁[],可以推测是镁与氧气、水和二氧化碳反应生成了碱式碳酸镁。
10.答案:(1)化学
(2)反应物铁氧气和水中含铁、氧、氢元素
(3)1-1中无明显现象,1-3中铁钉表面有红棕色固体产生
(4)铁生锈消耗氧气,装置内气体体积减小,压强减小,低于大气压,大气压将U形管右侧液体压向左侧
(5)探究试剂种类对铁生锈速率的影响
(6)保持铁制品表面干燥(或避免与NaCl及酸性物质接触等)
解析:(2)铁生锈是铁与水、氧气共同作用的结果,根据质量守恒定律化学反应前后,元素种类不变,反应物铁钉中含有铁元素,氧气中含有氧元素,水中含有氢、氧元素,因此铁锈中含有铁、氧、氢元素。
(3)探究铁生锈需要与水接触,需要将水作为变量进行对比实验,实验1-1中没有水,实验1-3中有水,其他实验条件均一致,所以通过实验1-1与1-3的现象可证明铁生锈需要与水接触。
(5)实验2中的变量只是试剂种类,其他实验条件均一致,因此实验2是探究试剂种类对铁生锈速率的影响。
(6)影响铁锈蚀的因素
一、知识讲解
1、实验目的:通过实验,探究钢铁制品锈蚀的条件。
2、实验装置
3、实验现象
观察时间 ① ② ③ ④ ⑤
立即观察 无明显现象 无明显现象 无明显现象 无明显现象 无明显现象
四天后观察 无明显现象 无明显现象 与水面相接触的部分产生较多铁锈,其余部分也出现锈斑 整枚铁钉已严重锈蚀 整枚铁钉已严重锈蚀
4、实验分析
通过试管①、②可知,铁钉在只与氧气或水接触时,不易生锈;对比试管③可知,钢铁锈蚀与氧气和水有关;试管④和试管⑤说明了盐溶液与酸溶液都会影响钢铁的锈蚀。
二、跟踪练习
1.如图是探究铁制品锈蚀的条件时设计的实验。下列对比实验设计与探究的条件,对应关系正确的是( )
A.甲和丁:水 B.乙和丙:空气 C.甲和丙:空气 D.甲和乙:水
2.线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如图所示实验,探究铁生锈的条件。下列说法错误的是( )
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙、丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
3.实验研究铁锈蚀影响因素,记录如下、下列分析不正确的是( )
实验装置 序号 其他试剂 100s时的含量
① 干燥剂 21%
② 10滴水 15%
③ 10滴水和1.0g食盐 8%
A.②③中含量减少表明铁已锈蚀 B.①②证明水对铁锈蚀有影响
C.②③证明食盐能加快铁锈蚀 D.①②③证明炭粉对铁锈蚀有影响
4.按如图装置进行实验,一周后发现铁钉锈蚀最严重的位置是( )
A.a处
B.b处
C.c处
D.三处同样严重
5. “对比法”是实验探究中常用的一种科学方法。以下铁钉生锈实验的设计(如图所示),得出的结论不正确的是( )
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.保持铁制品表面清洁干燥可以防止铁生锈
6.为了探究铁制品锈蚀的条件,小明用普通铁钉、纯铁钉同时进行下面的四组实验,一段时间后只在实验Ⅰ中观察到了红棕色锈斑,其他均无明显变化。下列说法错误的是( )
A.Ⅰ和Ⅱ说明铁制品锈蚀需要
B.Ⅰ和Ⅲ说明铁制品锈蚀需要
C.Ⅰ和Ⅳ说明和同时存在,铁制品不一定发生锈蚀
D.Ⅲ和Ⅳ说明铁制品锈蚀与铁制品内部结构有关
7.如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是( )
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
8.某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸用下图装置完成表中实验,回答下列问题。
实验序号 ① ② ③ ④
实验温度/℃ 25 25 70 70
试剂 稀氨水 稀醋酸 稀氨水 稀醋酸
出现铁锈 所需时间 1天未见锈蚀 5分钟 1天未见锈蚀 1分钟
(1)铁锈的主要成分是_______________(填化学式)。
(2)实验②和④可探究___________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是____________(填实验序号)。
(3)根据表中实验现象得出的结论是__________ (写出1点即可)。
(4)影响铁制品锈蚀快慢除上述因素外,还有__________ (写出1点即可),请设计实验方案:________________。
9.一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究。
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验。
实验图示
生锈时间 8min 较长时间不生锈 5min 3min 1min
(1)通过上述实验可知,温度越高,铁钉生锈速率越__________(填“慢”或“快”);在_______________(填“酸性”“碱性”或“中性”)环境中铁钉生锈速率较快。
【实验二】为探究铁锈的成分,用图甲所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全)。
【査阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收。
(2)请指出图甲所示实验装置的一个明显缺陷:_____________。
(3)加热前,先通入CO一段时间,目的是_________________。
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有___________元素,从而推断出空气中的__________参加了铁生锈反应。
【实验记录】
质量/g 铁锈样品的质量/g 装置B的质量/g 装置C的质量/g
反应前 23.2 232.4 198.2
反应后 一 239.6 211.4
(5)根据上表数据推算,可确定铁锈的成分,用表示,则=__;若缺少D装置,的值会__________________(填“偏大”“偏小”或“无影响”)。
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图乙所示装置,试管内可选用的物质如下
①
②水
③
④和
⑤和水
⑥和水
⑦、和水
至少需要选用_____________(填数字序号),才能达到探究镁带锈蚀的条件。
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁的化学方程式:________________________。
10.世界上每年因锈蚀而损失大量铁制品。某化学小组设计如下实验探究铁生锈的条件及影响生锈速率的因素。
【进行实验】
实验1:分别取铁钉按如图装置所示,放置一周,结果如下:
序号 1-1 1-2 1-3
实验
现象 无明显现象 无明显现象 铁钉表面有红棕色固体
实验2:分别取铁钉浸于等体积的不同试剂中,放置一周,结果如下:
序号 2-1 2-2 2-3
试剂种类 蒸馏水 3%的NaCl溶液 3%的稀盐酸
U形管左侧液面 上升1.2cm 上升3.7cm 上升5.3cm
【解释与结论】
(1)铁生锈属于_____(填“物理”或“化学”)变化。
(2)铁锈中含有铁、氧、氢元素,从元素守恒角度说明理由:_____。
(3)实验1中,证明铁生锈需要与水接触的现象是_____。
(4)实验2-1中,U形管左侧液面上升的原因是_____。
(5)实验2的目的是_____。
【反思与评价】
(6)结合本实验,对于铁制品的保存,你的一条建议是_____。
答案以及解析
1.答案:A
2.答案:C
解析:乙试管中的铁钉只与蒸馏水接触,丙试管中的铁钉只与空气接触,乙、丙两支试管中的铁钉均不生锈,两试管中现象对比,不能得出铁生锈需要水,C错误。
3.答案:D
解析: ②③中氧气含量减少,说明有氧气参加了反应,铁已锈蚀,A正确;①②对比氧气含量由21%减少至15%,①中放有干燥剂,铁只与氧气接触,没有锈蚀,②中放有10滴水,铁与水、氧气同时接触,发生锈蚀,对比可知水对铁锈蚀有影响,B正确;对比
②③中氧气含量,可知③中铁锈蚀速度快,证明食盐能加快铁锈蚀,C正确;题中炭粉不是变量,无法得出炭粉对铁锈蚀的影响,D不正确。
4.答案:B
解析:本题考查铁的锈蚀条件。铁生锈是铁与氧气水共同作用发生化学反应的结果。图中,a处位于空气中,水比较少,b处位于水与空气的交界处,有充足的氧气和水,c处位于蒸馏水内部,氧气比较少,所以,根据铁生锈所需的条件,b处锈蚀最严重,故选B。
5.答案:B
解析:对比①②可以说明铁生锈一定要有氧气参加,对比①③可以说明铁生锈一定要有水参加,A、C正确;对比②③,变量不唯一,无法获得结论,B错误。防止铁制品生锈的方法之一是保持铁制品表面干燥洁净,D正确。
6.答案:D
解析:实验Ⅲ和Ⅳ存在两个不同的变量,不能互为对照实验,无法说明铁制品锈蚀与铁制品内部结构有关。故选D。
7.答案:A
解析:本题考查铁生锈的条件。铁在氧气、水并存时易生锈,①中甲、乙、丙三处比较,生锈最明显的地方是乙,A项错误;①中的铁钉能与氧气、水充分接触,②中的铁钉只能与水接触,③中的铁钉只能与干燥的空气接触,一段时间后,①中的铁钉生锈,另外两支试管的铁钉没有生锈,①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水,B项正确;氯化钙具有吸水性,③中附着在棉花上的氯化钙的作用是作干燥剂,C项正确;④中铁钉接触到的是纯氧气及水,四个实验中,生锈最快的是④中的铁钉,D项正确。
8.答案:(1)
(2)温度;①②(或③④)
(3)相同条件下,酸性越强,金属生锈越快
(4)酸的浓度;相同条件下,取两份浓度不同的醋酸,分别在25℃时,观察铁钉生锈时间
解析:(1)铁锈的主要成分是氧化铁,铁生锈是铁与空气中的氧气、水共同作用的结果。铁锈的主要成分是。
(2)实验②和④可探究温度因素对铁制品锈蚀快慢的影响,欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是①②或③④。
(3)根据表中实验现象得出的结论是相同条件下,酸性越强,金属生锈越快等。
(4)影响铁制品锈蚀快慢除上述因素外,还有酸的浓度,设计的实验方案是相同条件下,取两份浓度不同的醋酸,分别在25℃时,观察铁钉生锈所用的时间。
9.答案:(1)快;酸性
(2)没有进行尾气处理
(3)排尽装置内的空气,防止发生爆炸
(4)氢;水蒸气
(5)4;偏小
(6)④⑤⑥⑦
(7)
解析:(1)对比实验1和实验4,实验3和实验5可知,温度越高铁钉生锈速率越快;对比实验1、2、3可知,铁钉在酸性环境中锈蚀。
(2)尾气中含有有毒的一氧化碳气体,该装置中没有将其处理。
(3)一氧化碳具有可燃性,不纯时加热或点燃易发生爆炸,所以先通入CO一段时间,排尽装置内的空气。
(4)无水硫酸铜能吸收水而变蓝,将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,这说明了反应后有水生成,说明铁锈中含有氢元素,也就是铁锈蚀的过程中有水蒸气参与。
(5)硬质玻璃管内发生反应的化学方程式为,根据实验数据可知,反应中生成水的质量为(239.6g-232.4g)=7.2g,生成二氧化碳的质量为(211.4g-198.2g)=13.2g。设参加反应的CO的质量为,则
,解得=84g,由质量守恒定律可知,生成铁的质量为23.2g+8.4g-13.2g-7.2g=112g;由于反应前后元素的种类与质量不变,所以23.2g中含铁元素的质量为11.2g;含有“”部分质量为7.2g;则余下的氧元素质量为23.2g-112g-7.2g=4.8g,则,故的化学式为。D装置中的碱石灰既能吸收水也能吸收,防止空气中二氧化碳与水被装置C吸收而造成质量偏大,若没有装置D,则装置C因为吸收了空气中的水蒸气和二氧化碳而质量偏大,由此计算出的二氧化碳质量偏大,导致氧元素的质量偏大,的值偏小。
(6)通过实验探究镁带在空气中锈蚀的条件,应该选择④和;⑤和水;⑥和水;⑦、和水四组实验进行对比。
(7)由镁带在空气中锈蚀,生成碱式碳酸镁[],可以推测是镁与氧气、水和二氧化碳反应生成了碱式碳酸镁。
10.答案:(1)化学
(2)反应物铁氧气和水中含铁、氧、氢元素
(3)1-1中无明显现象,1-3中铁钉表面有红棕色固体产生
(4)铁生锈消耗氧气,装置内气体体积减小,压强减小,低于大气压,大气压将U形管右侧液体压向左侧
(5)探究试剂种类对铁生锈速率的影响
(6)保持铁制品表面干燥(或避免与NaCl及酸性物质接触等)
解析:(2)铁生锈是铁与水、氧气共同作用的结果,根据质量守恒定律化学反应前后,元素种类不变,反应物铁钉中含有铁元素,氧气中含有氧元素,水中含有氢、氧元素,因此铁锈中含有铁、氧、氢元素。
(3)探究铁生锈需要与水接触,需要将水作为变量进行对比实验,实验1-1中没有水,实验1-3中有水,其他实验条件均一致,所以通过实验1-1与1-3的现象可证明铁生锈需要与水接触。
(5)实验2中的变量只是试剂种类,其他实验条件均一致,因此实验2是探究试剂种类对铁生锈速率的影响。
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
