2021秋鲁教版九年级化学上册第六单元燃烧与燃料达标检测卷(word版含答案)
文档属性
| 名称 | 2021秋鲁教版九年级化学上册第六单元燃烧与燃料达标检测卷(word版含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 399.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-21 00:00:00 | ||
图片预览




文档简介
第六单元达标检测卷
(100分,60分钟)
题 号 一 二 三 四 总 分
得 分
可能用到的相对原子质量: H—1 C—12 O—16 Cl—35.5 Ca—40
一、选择题(1~10题每题2分,11~15题每题3分,共35分)
1.在汽车加油站见到的油罐车上,所贴的危险化学品图标是( )
2.据《中国环境报》报道,为应对气候变化,落实《巴黎气候变化协定》,国家建立了统一的碳排放权交易市场。按国际惯例,这里的“碳”是指( )
A.二氧化碳 B.单质碳
C.碳元素 D.所有含碳化合物
3.下列关于二氧化碳的说法不正确的是( )
A.二氧化碳有毒 B.二氧化碳常用于灭火
C.干冰可用于人工降雨 D.光合作用会消耗二氧化碳
4.下列四支蜡烛都将熄灭,其中一支熄灭的原因与另外三支不同的是( )
5.燃烧与人类的生活以及社会的发展有着密切的联系。下列有关燃烧和灭火的说法错误的是( )
A.釜底抽薪——移除可燃物
B.电器着火——用水浇灭
C.钻木取火——使温度达到可燃物的着火点
D.架空篝火——使木材与空气有足够大的接触面积
6.燃烧是人类最早利用的化学反应之一。下列说法正确的是( )
A.降低氧气浓度使煤燃烧更充分
B.使温度降到可燃物着火点以下可以灭火
C.物质与氧气发生的反应都是燃烧
D.人类利用的能量都是通过燃烧获得的
7.页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。下列说法错误的是( )
A.页岩气的主要成分是甲烷
B.页岩气是不可再生能源
C.其完全燃烧的化学方程式为2CH4+3O22CO+4H2O
D.页岩气燃烧放出热量
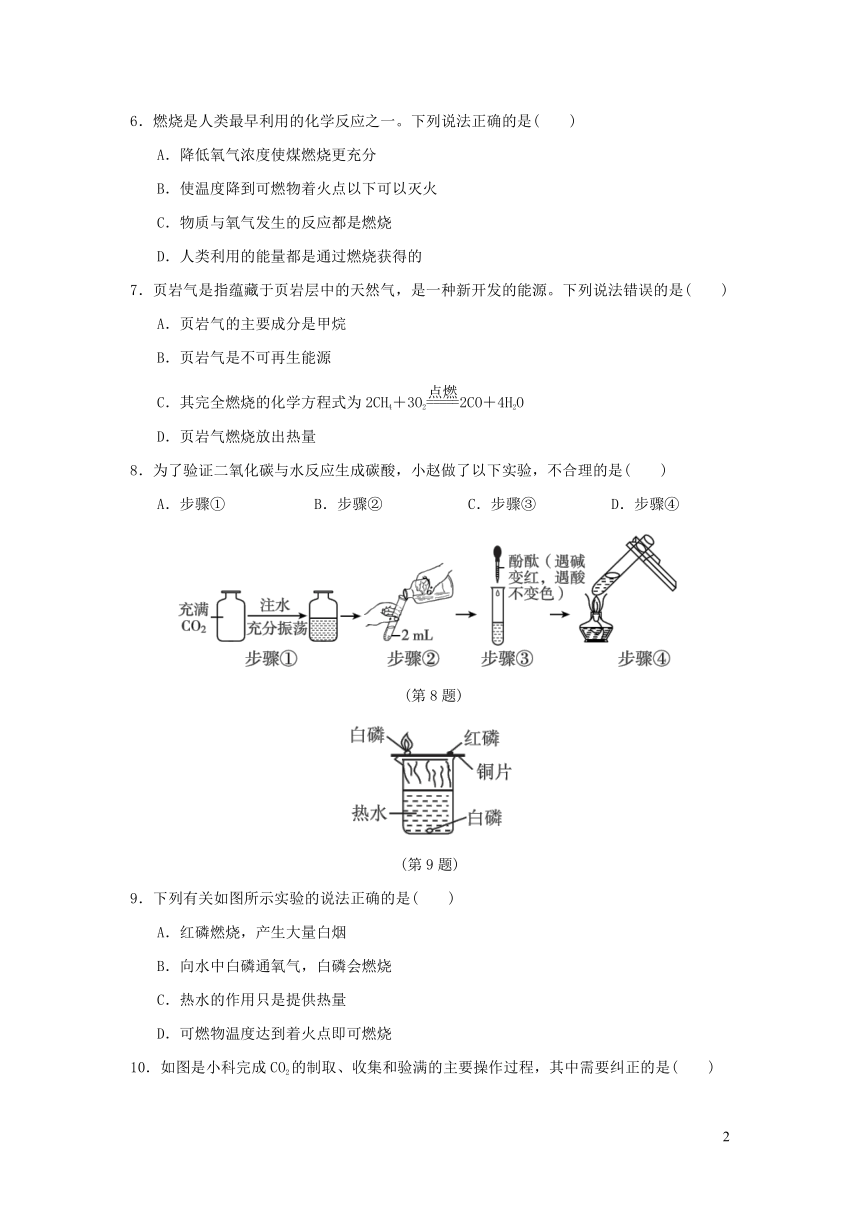
8.为了验证二氧化碳与水反应生成碳酸,小赵做了以下实验,不合理的是( )
A.步骤① B.步骤② C.步骤③ D.步骤④
(第8题)
(第9题)
9.下列有关如图所示实验的说法正确的是( )
A.红磷燃烧,产生大量白烟
B.向水中白磷通氧气,白磷会燃烧
C.热水的作用只是提供热量
D.可燃物温度达到着火点即可燃烧
10.如图是小科完成CO2的制取、收集和验满的主要操作过程,其中需要纠正的是( )
11.关于碳循环和氧循环,下列说法不正确的是( )
A.碳循环和氧循环分别是指二氧化碳和氧气的循环
B.碳循环和氧循环过程中均发生了化学变化
C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环
D.碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
12.2020年6月13日,浙江温岭的槽罐车爆炸事故造成了重大人员伤亡和财产损失。下列有关易燃物和易爆物的生产、运输、使用和贮存的说法正确的是( )
A.生产:面粉加工厂应标有“严禁烟火”字样或图标
B.运输:为方便运输,将烟花厂建在市中心
C.使用:家用天然气泄漏时,用打火机检测泄漏位置
D.贮存:为节约空间,应将易燃物和易爆物紧密堆积
13.下列关于燃料及其利用的相关知识的叙述中错误的是( )
A.可燃性气体点燃前一定要验纯
B.将煤粉制成蜂窝煤,能增大可燃物与空气的接触面积
C.堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点
D.食物的腐烂、动植物的呼吸都属于缓慢氧化
14.科学家发现火星大气层中含有一种称为硫化羰的物质,化学式为COS。已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧。下列有关硫化羰的说法错误的是( )
A.硫化羰是由分子构成的
B.硫化羰可作为理想燃料
C.硫化羰不能用作灭火剂
D.硫化羰完全燃烧会生成CO2和SO2两种氧化物
15.某无色气体可能由H2、CH4、CO、CO2中的几种组成。将该混合气体通过过量的澄清石灰水,出现白色浑浊;将剩余气体导出,经干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成。该混合气体的可能组成是( )
A.H2、CH4 B.H2、CO
C.H2、CH4、CO D.CH4、CO、CO2
二、填空题(46分)
16.(6分)请将下列物质的序号填入相应空格中。
①煤 ②石油 ③天然气 ④氢气 ⑤一氧化碳
⑥二氧化碳 ⑦乙醇
(1)属于化石燃料的是________。
(2)能导致温室效应的气体是________。
(3)点燃前一定要检验纯度的是________。
(4)既能用排水法又能用向下排空气法收集的气体单质是________。
(5)最理想的燃料是________。
(6)能由绿色植物的籽粒发酵制取的是________。
17.(6分)能源利用和环境保护问题一直受到社会的高度关注。
(1)太阳能和石油中,属于可再生能源的是________,属于不可再生能源的是________。
(2)天然气的主要成分是________ (填化学式),天然气燃烧主要是将化学能转化为________能。
(3)中国政府已全面禁止“洋垃圾”入境。无用“洋垃圾”直接露天焚烧会产生许多有毒气体,其中________(填化学式)极易与血液中血红蛋白结合,引起中毒。
18.(8分)科学地利用燃烧反应,对人类生产和生活是非常重要的。
(1)煤的主要成分是碳。请写出碳在空气中充分燃烧的化学方程式_________________________________________________________________。
(2)做饭时,锅底出现黑色物质,需要调________(填“大”或“小”)炉具或灶具的进风口,使燃料充分燃烧。
(3)请写出成语“釜底抽薪”体现的灭火原理:______________________________________。
(4)如果发现火险或遭遇火灾,应采取的应急措施是__________________________________________________________________ (写出一条即可)。
19.(10分)某课外活动小组进行了以下实验。根据实验回答问题:
(1)家庭小实验:将洗净的碎鸡蛋壳(主要成分是碳酸钙)放入小玻璃杯中,然后加入适量的稀盐酸,观察到鸡蛋壳表面__________,该反应的化学方程式是__________________________,立即用蘸有澄清石灰水的玻璃片盖住,一会儿,便可观察到澄清石灰水__________,该反应的化学方程式是_________________________________________________________________。
(2)向盛有紫色石蕊试液的试管中通入适量的CO2,紫色石蕊试液变为 ________色,其反应的化学方程式为____________________________。将反应后的溶液加热,则溶液变成________色,其反应的化学方程式为____________________________________________。
20.(8分)请根据你所学知识,回答有关问题:
(第20题)
(1)用一个空的软塑料瓶收集一瓶二氧化碳气体,在瓶中倒入约1/3容积的水,立即盖紧瓶子并振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是_______________________________________________________________。
(2)如图A,从烧杯的一侧倾倒二氧化碳,观察到的现象是_________________________________________________________________,
该实验说明二氧化碳具有的化学性质是_________________________。
(3)如图B,准备好双孔塞(插有带小气球的短玻璃管和盛有澄清石灰水的分液漏斗),取装满二氧化碳的集气瓶,用双孔塞将集气瓶塞紧。把澄清石灰水放入集气瓶振荡,可观察到的现象是__________________________、_________________,其原因是_____________________(用化学方程式表示)。
(4)如图C所示实验中,a、d为用紫色石蕊试液润湿的棉球,b、c为用石蕊试液染成紫色的干燥棉球,缓慢通入CO2一段时间后观察到:d比a先变红,b、c不变红,此现象说明CO2具有的物理性质是______________,化学性质是_________________________________________________________________。
21.(8分)已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易与血液中血红蛋白结合的有毒气体。它们之间的转化关系如图所示(有些转化关系、反应条件等已略去),试回答:
(第21题)
(1)写出E、F的化学式:E________;F________。
(2)用化学方程式表示以下转化关系:
A→D:__________________________________________;
C→A:__________________________________________;
E→D:__________________________________________。
三、探究实验题(12分)
22.实验室制取气体时要考虑下列问题:
(一)依据原理,确定制取方案。
(1)实验室制取O2时选择的药品在组成上的共同点是_________________。
任写出其中一个反应的化学方程式________________________________________________________________。
(2)下列反应均有CO2生成:①木炭在充足的氧气中燃烧,②大理石与稀盐酸反应,③煅烧石灰石。实验室制取CO2通常选择方法②。不选择①的理由是________________________________________________________________;
不选择③的理由是_______________________________________________。
(二)选择合理的制取装置。
用如图所示装置制取气体,请回答下列问题:
(第22题)
(3)仪器a的名称是________。
(4)用双氧水和二氧化锰制取O2,选择的发生和收集装置的组合是________(写出一种组合,填序号)。
(5)实验室在加热条件下,分解草酸晶体可以制得CO,但是加热时草酸晶体在分解之前先熔化成了液体。如果用这种方法制取CO,你从A、B、C中所选择的发生装置是______(填序号),选择的理由是___________________________________________________________________________________________________________________________________。
四、计算题(7分)
23.实验室用12.5 g含碳酸钙80%的石灰石和一定质量的稀盐酸反应制取二氧化碳(石灰石中的杂质不溶于水,也不与稀盐酸反应),加入稀盐酸的质量与产生气体的质量关系如图所示。试计算该稀盐酸中溶质的质量分数。
(第23题)
答案
一、1.C 2.A 3.A 4.B 5.B
6.B 点拨:增大氧气浓度使煤燃烧更充分,A错误;使温度降到可燃物着火点以下可以灭火,B正确;物质与氧气发生的反应不一定都是燃烧,也可能是缓慢氧化,C错误;人类利用的能量不都是通过燃烧获得的,如利用太阳能、风能等,D错误。
7.C 点拨:页岩气的主要成分是甲烷,甲烷完全燃烧生成二氧化碳和水,化学方程式为CH4+2O2CO2+2H2O。
8.C 点拨:为了验证二氧化碳与水反应生成碳酸,可以借助指示剂,石蕊遇酸性溶液会变红,酚酞遇酸性溶液不变色,所以实验中应用紫色的石蕊试液,不能用无色的酚酞试液,所以步骤③不合理。
9.B 点拨:红磷的着火点为240 ℃,温度没有达到其着火点,不会燃烧,A错误;白磷的着火点为40 ℃,热水中的白磷温度已达到其着火点,再与氧气接触时,白磷会燃烧,B正确;热水中的白磷没有燃烧,此时热水也起到了隔绝氧气的作用,C错误;可燃物燃烧需要与氧气接触且温度达到着火点,D错误。
10.D 点拨:检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,不能伸入瓶中,图D中所示操作错误。
11.A 12.A
13.C 点拨:可燃性气体如果不纯,点燃时可能会发生爆炸,故点燃前一定要验纯,A正确;将煤粉制成“蜂窝煤”是为了增大煤与空气的接触面积,使其燃烧更充分,B正确;水蒸发时吸收热量,可使温度降低到可燃物的着火点以下,从而达到灭火的目的,可燃物的着火点一般是不能改变的,一般不能降低可燃物的着火点,C错误;食物的腐烂、动植物的呼吸是物质与空气中的氧气发生的缓慢氧化,D正确。
14.B 点拨:由硫化羰的化学式COS可知,它是由分子构成的,A正确;由硫化羰的化学式COS可知,它完全燃烧会生成二氧化硫,导致酸雨,故不是理想的燃料,B错误;因为硫化羰具有可燃性,所以不能用作灭火剂,C正确;由硫化羰的化学式COS可知,硫化羰完全燃烧会生成CO2和SO2两种氧化物,D正确。
15.D 方法规律:本题采用现象分析法解答。由实验现象可知,将气体通过过量澄清石灰水,出现白色浑浊,证明气体中一定含有CO2;将剩余气体干燥后点燃,有水生成,证明气体中至少有H2或CH4中的一种。对照选项,含CO2的选项只有D。
二、16.(1)①②③ (2)③⑥
(3)③④⑤ (4)④
(5)④ (6)⑦
17.(1)太阳能;石油 (2)CH4;热 (3)CO
18.(1)C+O2CO2 (2)大 (3)移走可燃物
(4)拨打火警电话119(合理即可)
19.(1)产生气泡;CaCO3+2HCl===CaCl2+CO2↑+H2O;变浑浊;
CO2+Ca(OH)2===CaCO3↓+H2O
(2)红;CO2+H2O===H2CO3;紫;H2CO3CO2↑+H2O
20.(1)二氧化碳能溶于水
(2)蜡烛自下而上依次熄灭;不燃烧也不支持燃烧
(3)气球膨胀;澄清石灰水变浑浊;
CO2+Ca(OH)2===CaCO3↓+H2O
(4)密度比空气大;能与水反应生成碳酸
点拨:(1)二氧化碳能溶于水,故塑料瓶变瘪。(2)蜡烛火焰由下往上依次熄灭,该实验说明二氧化碳密度比空气大的物理性质及不可燃、一般也不助燃的化学性质。(3)二氧化碳与氢氧化钙反应生成碳酸钙和水,装置中压强变小,气球膨胀,把澄清石灰水放入集气瓶振荡,可观察到的现象是气球膨胀, 石灰水变浑浊。(4)缓慢通入CO2一段时间后观察到:d比a先变红,说明CO2密度比空气大,b、c不变红,说明二氧化碳能与水反应生成碳酸。
21.(1)CO;C(或O2)
(2)CaCO3 + 2HCl===CaCl2 + H2O+ CO2↑(或CaCO3CaO+CO2↑);Ca(OH)2+CO2===CaCO3↓+H2O;2CO+O22CO2
三、22.(1)物质中都含有氧元素;2H2O2 2H2O+ O2↑(合理即可)
(2)反应物中有氧气,使生成的二氧化碳不纯,且气体不易收集;反应在高温下进行,操作不方便
(3)酒精灯
(4)D、E(或D、G) (5)C;试管口略向下倾斜,可以防止冷凝水倒流,使试管炸裂,试管底部向下弯曲,可以防止草酸熔化后流到试管口处
点拨:(1)化学反应前后,元素种类不变,所以实验室制取O2时选择的药品在组成上的共同点是物质中都含有氧元素。(2)不选择①的理由是反应物中有氧气,使生成的二氧化碳不纯,且气体不易收集。不选择③的理由是需要高温,操作不方便。(3)仪器a为热源仪器酒精灯。(4)用双氧水和二氧化锰制取O2需选择固液常温型发生装置,用向上排空气法或排水法收集。(5)由于加热时草酸晶体在分解之前先熔化成了液体,故选择C装置,C装置试管口略向下倾斜,可以防止冷凝水倒流,使试管炸裂,试管底部向下弯曲,可以防止草酸熔化后流到试管口处。
四、23.解:设73 g稀盐酸中含氯化氢的质量为x。
碳酸钙质量为12.5 g×80%=10 g。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 73
10 g x
=
x=7.3 g
该稀盐酸中溶质的质量分数为×100%=10%。
答:该稀盐酸中溶质的质量分数是10%。
1
(100分,60分钟)
题 号 一 二 三 四 总 分
得 分
可能用到的相对原子质量: H—1 C—12 O—16 Cl—35.5 Ca—40
一、选择题(1~10题每题2分,11~15题每题3分,共35分)
1.在汽车加油站见到的油罐车上,所贴的危险化学品图标是( )
2.据《中国环境报》报道,为应对气候变化,落实《巴黎气候变化协定》,国家建立了统一的碳排放权交易市场。按国际惯例,这里的“碳”是指( )
A.二氧化碳 B.单质碳
C.碳元素 D.所有含碳化合物
3.下列关于二氧化碳的说法不正确的是( )
A.二氧化碳有毒 B.二氧化碳常用于灭火
C.干冰可用于人工降雨 D.光合作用会消耗二氧化碳
4.下列四支蜡烛都将熄灭,其中一支熄灭的原因与另外三支不同的是( )
5.燃烧与人类的生活以及社会的发展有着密切的联系。下列有关燃烧和灭火的说法错误的是( )
A.釜底抽薪——移除可燃物
B.电器着火——用水浇灭
C.钻木取火——使温度达到可燃物的着火点
D.架空篝火——使木材与空气有足够大的接触面积
6.燃烧是人类最早利用的化学反应之一。下列说法正确的是( )
A.降低氧气浓度使煤燃烧更充分
B.使温度降到可燃物着火点以下可以灭火
C.物质与氧气发生的反应都是燃烧
D.人类利用的能量都是通过燃烧获得的
7.页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。下列说法错误的是( )
A.页岩气的主要成分是甲烷
B.页岩气是不可再生能源
C.其完全燃烧的化学方程式为2CH4+3O22CO+4H2O
D.页岩气燃烧放出热量
8.为了验证二氧化碳与水反应生成碳酸,小赵做了以下实验,不合理的是( )
A.步骤① B.步骤② C.步骤③ D.步骤④
(第8题)
(第9题)
9.下列有关如图所示实验的说法正确的是( )
A.红磷燃烧,产生大量白烟
B.向水中白磷通氧气,白磷会燃烧
C.热水的作用只是提供热量
D.可燃物温度达到着火点即可燃烧
10.如图是小科完成CO2的制取、收集和验满的主要操作过程,其中需要纠正的是( )
11.关于碳循环和氧循环,下列说法不正确的是( )
A.碳循环和氧循环分别是指二氧化碳和氧气的循环
B.碳循环和氧循环过程中均发生了化学变化
C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环
D.碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
12.2020年6月13日,浙江温岭的槽罐车爆炸事故造成了重大人员伤亡和财产损失。下列有关易燃物和易爆物的生产、运输、使用和贮存的说法正确的是( )
A.生产:面粉加工厂应标有“严禁烟火”字样或图标
B.运输:为方便运输,将烟花厂建在市中心
C.使用:家用天然气泄漏时,用打火机检测泄漏位置
D.贮存:为节约空间,应将易燃物和易爆物紧密堆积
13.下列关于燃料及其利用的相关知识的叙述中错误的是( )
A.可燃性气体点燃前一定要验纯
B.将煤粉制成蜂窝煤,能增大可燃物与空气的接触面积
C.堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点
D.食物的腐烂、动植物的呼吸都属于缓慢氧化
14.科学家发现火星大气层中含有一种称为硫化羰的物质,化学式为COS。已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧。下列有关硫化羰的说法错误的是( )
A.硫化羰是由分子构成的
B.硫化羰可作为理想燃料
C.硫化羰不能用作灭火剂
D.硫化羰完全燃烧会生成CO2和SO2两种氧化物
15.某无色气体可能由H2、CH4、CO、CO2中的几种组成。将该混合气体通过过量的澄清石灰水,出现白色浑浊;将剩余气体导出,经干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成。该混合气体的可能组成是( )
A.H2、CH4 B.H2、CO
C.H2、CH4、CO D.CH4、CO、CO2
二、填空题(46分)
16.(6分)请将下列物质的序号填入相应空格中。
①煤 ②石油 ③天然气 ④氢气 ⑤一氧化碳
⑥二氧化碳 ⑦乙醇
(1)属于化石燃料的是________。
(2)能导致温室效应的气体是________。
(3)点燃前一定要检验纯度的是________。
(4)既能用排水法又能用向下排空气法收集的气体单质是________。
(5)最理想的燃料是________。
(6)能由绿色植物的籽粒发酵制取的是________。
17.(6分)能源利用和环境保护问题一直受到社会的高度关注。
(1)太阳能和石油中,属于可再生能源的是________,属于不可再生能源的是________。
(2)天然气的主要成分是________ (填化学式),天然气燃烧主要是将化学能转化为________能。
(3)中国政府已全面禁止“洋垃圾”入境。无用“洋垃圾”直接露天焚烧会产生许多有毒气体,其中________(填化学式)极易与血液中血红蛋白结合,引起中毒。
18.(8分)科学地利用燃烧反应,对人类生产和生活是非常重要的。
(1)煤的主要成分是碳。请写出碳在空气中充分燃烧的化学方程式_________________________________________________________________。
(2)做饭时,锅底出现黑色物质,需要调________(填“大”或“小”)炉具或灶具的进风口,使燃料充分燃烧。
(3)请写出成语“釜底抽薪”体现的灭火原理:______________________________________。
(4)如果发现火险或遭遇火灾,应采取的应急措施是__________________________________________________________________ (写出一条即可)。
19.(10分)某课外活动小组进行了以下实验。根据实验回答问题:
(1)家庭小实验:将洗净的碎鸡蛋壳(主要成分是碳酸钙)放入小玻璃杯中,然后加入适量的稀盐酸,观察到鸡蛋壳表面__________,该反应的化学方程式是__________________________,立即用蘸有澄清石灰水的玻璃片盖住,一会儿,便可观察到澄清石灰水__________,该反应的化学方程式是_________________________________________________________________。
(2)向盛有紫色石蕊试液的试管中通入适量的CO2,紫色石蕊试液变为 ________色,其反应的化学方程式为____________________________。将反应后的溶液加热,则溶液变成________色,其反应的化学方程式为____________________________________________。
20.(8分)请根据你所学知识,回答有关问题:
(第20题)
(1)用一个空的软塑料瓶收集一瓶二氧化碳气体,在瓶中倒入约1/3容积的水,立即盖紧瓶子并振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是_______________________________________________________________。
(2)如图A,从烧杯的一侧倾倒二氧化碳,观察到的现象是_________________________________________________________________,
该实验说明二氧化碳具有的化学性质是_________________________。
(3)如图B,准备好双孔塞(插有带小气球的短玻璃管和盛有澄清石灰水的分液漏斗),取装满二氧化碳的集气瓶,用双孔塞将集气瓶塞紧。把澄清石灰水放入集气瓶振荡,可观察到的现象是__________________________、_________________,其原因是_____________________(用化学方程式表示)。
(4)如图C所示实验中,a、d为用紫色石蕊试液润湿的棉球,b、c为用石蕊试液染成紫色的干燥棉球,缓慢通入CO2一段时间后观察到:d比a先变红,b、c不变红,此现象说明CO2具有的物理性质是______________,化学性质是_________________________________________________________________。
21.(8分)已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易与血液中血红蛋白结合的有毒气体。它们之间的转化关系如图所示(有些转化关系、反应条件等已略去),试回答:
(第21题)
(1)写出E、F的化学式:E________;F________。
(2)用化学方程式表示以下转化关系:
A→D:__________________________________________;
C→A:__________________________________________;
E→D:__________________________________________。
三、探究实验题(12分)
22.实验室制取气体时要考虑下列问题:
(一)依据原理,确定制取方案。
(1)实验室制取O2时选择的药品在组成上的共同点是_________________。
任写出其中一个反应的化学方程式________________________________________________________________。
(2)下列反应均有CO2生成:①木炭在充足的氧气中燃烧,②大理石与稀盐酸反应,③煅烧石灰石。实验室制取CO2通常选择方法②。不选择①的理由是________________________________________________________________;
不选择③的理由是_______________________________________________。
(二)选择合理的制取装置。
用如图所示装置制取气体,请回答下列问题:
(第22题)
(3)仪器a的名称是________。
(4)用双氧水和二氧化锰制取O2,选择的发生和收集装置的组合是________(写出一种组合,填序号)。
(5)实验室在加热条件下,分解草酸晶体可以制得CO,但是加热时草酸晶体在分解之前先熔化成了液体。如果用这种方法制取CO,你从A、B、C中所选择的发生装置是______(填序号),选择的理由是___________________________________________________________________________________________________________________________________。
四、计算题(7分)
23.实验室用12.5 g含碳酸钙80%的石灰石和一定质量的稀盐酸反应制取二氧化碳(石灰石中的杂质不溶于水,也不与稀盐酸反应),加入稀盐酸的质量与产生气体的质量关系如图所示。试计算该稀盐酸中溶质的质量分数。
(第23题)
答案
一、1.C 2.A 3.A 4.B 5.B
6.B 点拨:增大氧气浓度使煤燃烧更充分,A错误;使温度降到可燃物着火点以下可以灭火,B正确;物质与氧气发生的反应不一定都是燃烧,也可能是缓慢氧化,C错误;人类利用的能量不都是通过燃烧获得的,如利用太阳能、风能等,D错误。
7.C 点拨:页岩气的主要成分是甲烷,甲烷完全燃烧生成二氧化碳和水,化学方程式为CH4+2O2CO2+2H2O。
8.C 点拨:为了验证二氧化碳与水反应生成碳酸,可以借助指示剂,石蕊遇酸性溶液会变红,酚酞遇酸性溶液不变色,所以实验中应用紫色的石蕊试液,不能用无色的酚酞试液,所以步骤③不合理。
9.B 点拨:红磷的着火点为240 ℃,温度没有达到其着火点,不会燃烧,A错误;白磷的着火点为40 ℃,热水中的白磷温度已达到其着火点,再与氧气接触时,白磷会燃烧,B正确;热水中的白磷没有燃烧,此时热水也起到了隔绝氧气的作用,C错误;可燃物燃烧需要与氧气接触且温度达到着火点,D错误。
10.D 点拨:检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,不能伸入瓶中,图D中所示操作错误。
11.A 12.A
13.C 点拨:可燃性气体如果不纯,点燃时可能会发生爆炸,故点燃前一定要验纯,A正确;将煤粉制成“蜂窝煤”是为了增大煤与空气的接触面积,使其燃烧更充分,B正确;水蒸发时吸收热量,可使温度降低到可燃物的着火点以下,从而达到灭火的目的,可燃物的着火点一般是不能改变的,一般不能降低可燃物的着火点,C错误;食物的腐烂、动植物的呼吸是物质与空气中的氧气发生的缓慢氧化,D正确。
14.B 点拨:由硫化羰的化学式COS可知,它是由分子构成的,A正确;由硫化羰的化学式COS可知,它完全燃烧会生成二氧化硫,导致酸雨,故不是理想的燃料,B错误;因为硫化羰具有可燃性,所以不能用作灭火剂,C正确;由硫化羰的化学式COS可知,硫化羰完全燃烧会生成CO2和SO2两种氧化物,D正确。
15.D 方法规律:本题采用现象分析法解答。由实验现象可知,将气体通过过量澄清石灰水,出现白色浑浊,证明气体中一定含有CO2;将剩余气体干燥后点燃,有水生成,证明气体中至少有H2或CH4中的一种。对照选项,含CO2的选项只有D。
二、16.(1)①②③ (2)③⑥
(3)③④⑤ (4)④
(5)④ (6)⑦
17.(1)太阳能;石油 (2)CH4;热 (3)CO
18.(1)C+O2CO2 (2)大 (3)移走可燃物
(4)拨打火警电话119(合理即可)
19.(1)产生气泡;CaCO3+2HCl===CaCl2+CO2↑+H2O;变浑浊;
CO2+Ca(OH)2===CaCO3↓+H2O
(2)红;CO2+H2O===H2CO3;紫;H2CO3CO2↑+H2O
20.(1)二氧化碳能溶于水
(2)蜡烛自下而上依次熄灭;不燃烧也不支持燃烧
(3)气球膨胀;澄清石灰水变浑浊;
CO2+Ca(OH)2===CaCO3↓+H2O
(4)密度比空气大;能与水反应生成碳酸
点拨:(1)二氧化碳能溶于水,故塑料瓶变瘪。(2)蜡烛火焰由下往上依次熄灭,该实验说明二氧化碳密度比空气大的物理性质及不可燃、一般也不助燃的化学性质。(3)二氧化碳与氢氧化钙反应生成碳酸钙和水,装置中压强变小,气球膨胀,把澄清石灰水放入集气瓶振荡,可观察到的现象是气球膨胀, 石灰水变浑浊。(4)缓慢通入CO2一段时间后观察到:d比a先变红,说明CO2密度比空气大,b、c不变红,说明二氧化碳能与水反应生成碳酸。
21.(1)CO;C(或O2)
(2)CaCO3 + 2HCl===CaCl2 + H2O+ CO2↑(或CaCO3CaO+CO2↑);Ca(OH)2+CO2===CaCO3↓+H2O;2CO+O22CO2
三、22.(1)物质中都含有氧元素;2H2O2 2H2O+ O2↑(合理即可)
(2)反应物中有氧气,使生成的二氧化碳不纯,且气体不易收集;反应在高温下进行,操作不方便
(3)酒精灯
(4)D、E(或D、G) (5)C;试管口略向下倾斜,可以防止冷凝水倒流,使试管炸裂,试管底部向下弯曲,可以防止草酸熔化后流到试管口处
点拨:(1)化学反应前后,元素种类不变,所以实验室制取O2时选择的药品在组成上的共同点是物质中都含有氧元素。(2)不选择①的理由是反应物中有氧气,使生成的二氧化碳不纯,且气体不易收集。不选择③的理由是需要高温,操作不方便。(3)仪器a为热源仪器酒精灯。(4)用双氧水和二氧化锰制取O2需选择固液常温型发生装置,用向上排空气法或排水法收集。(5)由于加热时草酸晶体在分解之前先熔化成了液体,故选择C装置,C装置试管口略向下倾斜,可以防止冷凝水倒流,使试管炸裂,试管底部向下弯曲,可以防止草酸熔化后流到试管口处。
四、23.解:设73 g稀盐酸中含氯化氢的质量为x。
碳酸钙质量为12.5 g×80%=10 g。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 73
10 g x
=
x=7.3 g
该稀盐酸中溶质的质量分数为×100%=10%。
答:该稀盐酸中溶质的质量分数是10%。
1
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
