2021-2022学年九年级化学人教版上册 4.4 化学式与化合价(共53张PPT含内嵌视频)
文档属性
| 名称 | 2021-2022学年九年级化学人教版上册 4.4 化学式与化合价(共53张PPT含内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 29.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-21 00:00:00 | ||
图片预览







文档简介
(共53张PPT)
新课导入
学习目标
新课讲解
课堂练习
01
02
03
04
目录
课题4 化学式与化合价
人教版九年级上册 第四单元
建
议
2~3
课
时
新课导入
观看视频
学习目标
1.通过复习元素符号的意义,以水的化学式为例分析讨论,能说出化学式及数字的意义。
2.建立科学的物质观,增进对物质宏观微观的认识,能规范使用化学术语。
3.过分类讲解物质化学式的书写和读法,能正确书写和读出物质的化学式,知道一些常见元素和根的化合价,并能利用化合价推求化学式。
4.通过自主阅读课本,能说出相对分子质量的含义,能正确计算相对分子质量、元素质量比和元素质量分数。
BOY
单词
H
H
O
化学式
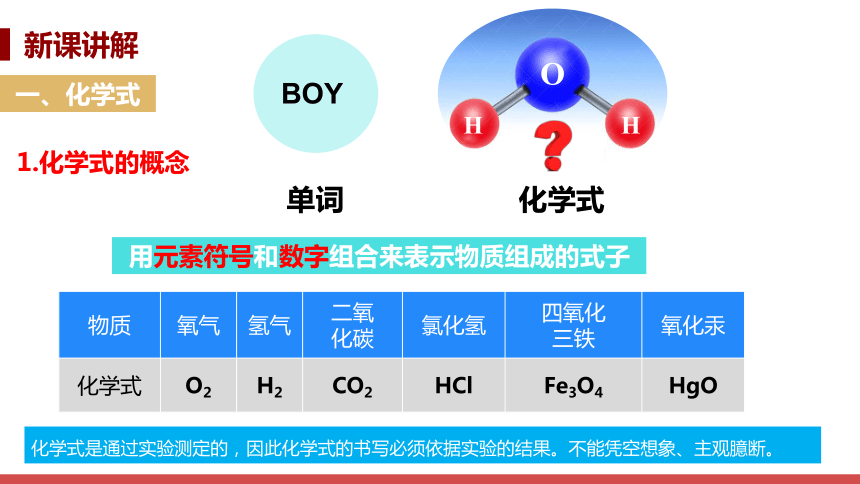
用元素符号和数字组合来表示物质组成的式子
一、化学式
新课讲解
1.化学式的概念
物质 氧气 氢气 二氧 化碳 氯化氢 四氧化 三铁 氧化汞
化学式 O2 H2 CO2 HCl Fe3O4 HgO
化学式是通过实验测定的,因此化学式的书写必须依据实验的结果。不能凭空想象、主观臆断。
……?
化学式可以任意的书写吗?
怎么区分物理变化和化学变化?
思 考
同种物质可以有不同的化学式吗?
新课讲解
新课讲解
物质
混合物
纯净物
没有固定的组成
无化学式
组成固定不变
有并且只有一个化学式
固
液
气
H2O
化学式与物质的状态无关
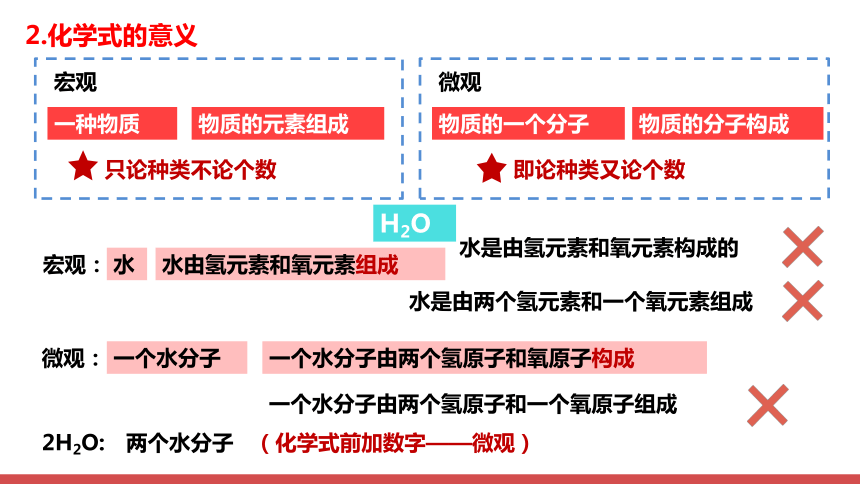
宏观
一种物质
物质的元素组成
微观
物质的一个分子
物质的分子构成
宏观:
微观:
水
水由氢元素和氧元素组成
水是由氢元素和氧元素构成的
水是由两个氢元素和一个氧元素组成
一个水分子
一个水分子由两个氢原子和氧原子构成
一个水分子由两个氢原子和一个氧原子组成
两个水分子
(化学式前加数字——微观)
只论种类不论个数
即论种类又论个数
H2O
2H2O:
2.化学式的意义
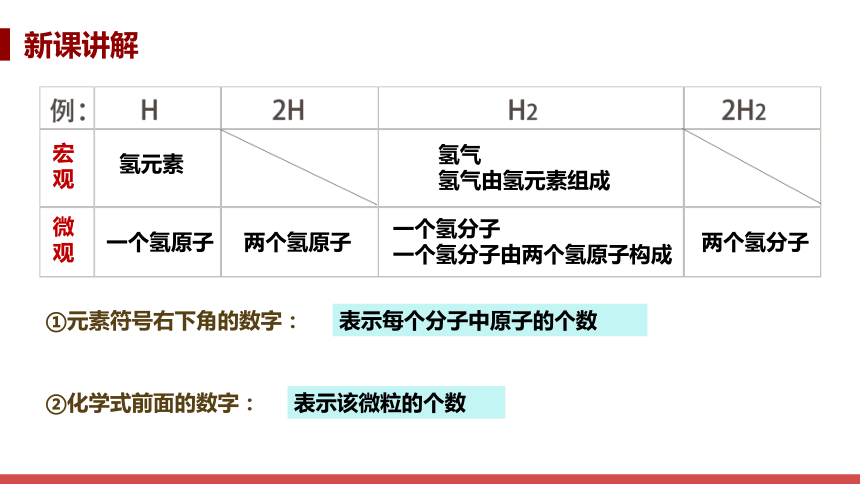
氢元素
一个氢原子
两个氢原子
氢气
氢气由氢元素组成
一个氢分子
一个氢分子由两个氢原子构成
两个氢分子
宏观
微观
①元素符号右下角的数字:
表示每个分子中原子的个数
②化学式前面的数字:
表示该微粒的个数
新课讲解
其他化学符号中各数字的意义
如2Cu表示2个铜原子。
元素符号前的数字:表示原子个数。
离子符号前的数字:表示离子个数。
元素符号右上角的数字:表示该元素的一个离子所带的电荷数。
如2Cu2+表示2个铜离子。
如Cu2+中的“2+”表示1个铜离子带2个单位的正电荷。
新课讲解
微观意义
由分子构成的物质
由原子构成的物质:表示物质的一个原子
表示一种物质
表示该物质的元素组成
宏观意义
表示物质的一个分子
表示物质的分子构成
只论种类不论个数
即论种类又论个数
化学式:一种用元素符号和数字这样的组合来表示物质组成的式子。
新课讲解
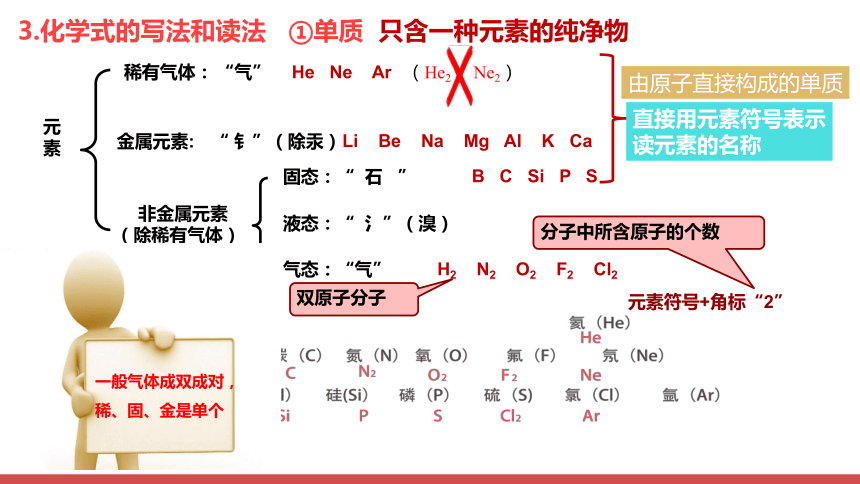
元素
稀有气体:
金属元素:
非金属元素
(除稀有气体)
固态:“ 石 ”
液态:“ 氵”(溴)
气态:“气”
“ 钅”(除汞)
“气”
He Ne Ar (He2 Ne2)
Li Be Na Mg Al K Ca
B C Si P S
由原子直接构成的单质
直接用元素符号表示
读元素的名称
H2 N2 O2 F2 Cl2
分子中所含原子的个数
元素符号+角标“2”
双原子分子
3.化学式的写法和读法 ①单质 只含一种元素的纯净物
一般气体成双成对,稀、固、金是单个
水:
一个水分子是由两个氢原子和一个氧原子构成
H2O1
或
O1H2
H2O
当组成元素原子个数比为1时,1省略不写。
1.氧化物化学式的书写:
一般把氧的元素符号写在右方,另一种元素的符号写在左方。
一氧化碳 二氧化碳 二氧化硫 五氧化二磷 四氧化三铁
CO2
CO
SO2
P2O5
Fe3O4
从后向前读
化学式的读法
②化合物
顺写反读
氯化钠
Cl
Na
NaxCly
2.金属元素和非金属元素组成的化合物:
化学式书写:金属的元素符号写在左方,非金属元素写在右方。
氯化钠 氯化钾 氯化氢 氯化银 氯化钡
KCl
NaCl
HCl
AgCl
BaCl2
从后向前读,某化某
化学式的读法
顺写反读
新课讲解
意义
化学式
读写方法
宏观意义
微观意义
概念
用元素符号和数字的组合表示物质组成的式子。
表示一种物质
表示物质的一个分子
表示该物质的元素组成
表示物质的分子(或原子)构成
课堂小结
通过观察我们可以得出:物质不同,原子个数比可能不同。
Na2O Na2S H2O H2S
个数比为2:1
CaO MgO CO NaCl
个数比为1:1
CaCl2 MgCl2 CO2 SiO2
个数比为1:2
化合物中各元素原子的个数比是由什么来决定的呢?
新课讲解
二、化合价
化合物有固定的组成,即形成化合物的元素有固定的原子个数比。
新课讲解
观看视频
1、 概念:一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质。
2、规定:
(1)在离子构成的化合物中,化合价与离子所带电荷数有关。
Na原子失去一个电子变成Na+,规定Na元素的化合价为+1;
Cl原子得到一个电子变成Cl-,规定Cl元素的化合价为-1。
(2)在分子构成的化合物中,化合价与共用电子对的数目有关。
3、表示方法:
在元素符号或原子团的 用“+/-n”表示。
正上方
+n
-n
H2O中H元素的化合价
H
+1
H2O中O元素的化合价
O
-2
正一价的氢元素
负二价的氧元素
新课讲解
4、基本规律:
(1)化合价有正负之分,在化合物里,
氯化钠
Cl
Na
NaxCly
化合价
通常与对应离子所带电荷数值相等,正负号相同
化合物中,正、负化合价的代数和为0
Na+
Na为+1价
+1
右上角,数字在前,符号在后,1要省略。
正上方,符号在前,数字在后,1不能省略。
Cl-
Cl为-1价
(+1)·x+(-1)·y=0
x:y = 1:1
NaCl
新课讲解
化合价与离子符号的区别
(2)元素的化合价是元素在形成化合物时表现出来的性质,因此单质中元素的化合价为零;
0 0 0 0
O2 N2 H2 Fe
(3)同种元素在不同物质中可显不同的化合价,在同一物质中也可能显不同的化合价。
+3
+2
+7
+6
Fe2O3 FeO KMnO4 K2MnO4
氧化铁
氧化亚铁
高锰酸钾
锰酸钾
新课讲解
(4)在化合物中氢元素通常显+1价,氧元素通常显-2价,常以它们为基准来推算化合物中其他元素的化合价;
HCl H2S H2O
+1
+1
-1
-2
+1
-2
(5)通常,金属元素显正价,非金属元素显负价;
NaCl CaCl2 AlCl3 KCl MgCl2
+1
-1
+1
-1
-1
-1
-1
+2
+2
+3
NH4NO3
-3
+5
元素和根的名称 元素和根的符号 常见化合价 元素和根的名称 元素和根的符号 常见化合价
钾 K +1 氯 Cl -1、+1、+5、+7
钠 Na +1 溴 Br -1
银 Ag +1 氧 O -2
钙 Ca +2 硫 S -2、+4、+6
镁 Mg +2 碳 C +2、+4
钡 Ba +2 硅 Si +4
铜 Cu +1、+2 氮 N -3、+2、+3、+4、+5
铁 Fe +2、+3 磷 P -3、+3、+5
铝 Al +3 氢氧根 OH- -1
锰 Mn +2、+4、+6、+7 硝酸根 NO3- -1
锌 Zn +2 硫酸根 SO42- -2
氢 H +1 碳酸根 CO32- -2
氟 F -1 铵根 NH4+ +1
新课讲解
常见元素和原子团的化合价
钾钠银氢正一价,钙镁钡锌正二价;
铝是正三氧负二,氟氯负价负一价;
硫有负二正四六,正二正三铁可变;
正一二铜二四碳,单质零价永不变。
常见元素化合价的记忆口诀
新课讲解
①、常见元素的化合价(记忆)
观看视频
新课讲解
作为一个整体参加反应的原子集团,原子团也叫作根。
注意:①原子团不能单独存在;②带电荷的原子团也是离子。
SO42-
2个硫酸根
一个硫酸根带两个单位的负电荷
1个硫酸根含有4个氧原子
2
-2
硫酸根显负二价
新课讲解
②、原子团定义及常见化合价
名称 符号 化合价 化合物 读法
氢氧根 OH- -1 NaOH
硝酸根 NO3- -1 KNO3
硫酸根 SO42- -2 CuSO4 碳酸根 CO32- -2 CaCO3 铵根 NH4+ +1 NH4Cl
氢氧化*
*酸*
氯化铵
新课讲解
口诀:
负一硝酸氢氧根,负二碳酸硫酸根,
负三记住磷酸根,正一价的是铵根。
(1)根据化学式求某一元素化合价
原则:化合物里正负化合价的代数和为零。
例 试确定氯酸钾(KClO3)中氯元素的化合价。
解:设氯元素的化合价为x,则
(+1)+ x +(-2)×3=0
所以,在氯酸钾中,氯元素的化合价为+5价
若求原子团中某元素的化合价,则代数和不为零。
5.化合价规律的应用
新课讲解
根据化学式求化合价(氢+1氧-2为标准)
【练习】1.标出画线元素的化合价
Fe2O3(氧化铁) FeO(氧化亚铁)
Fe2+(亚铁离子) Fe3+(铁离子)
KMnO4(高锰酸钾) K2MnO4(锰酸钾)
NH4NO3(硝酸铵) SO42- H2O2
+3
+2
+7
+6
-3
+5
-1
+6
+2
+3
新课讲解
(2)根据元素化合价推出化合物的化学式
1.最小公倍数法:
①写出组成化合物的元素符号,一般正价元素在左,负价元素在右。
②标出有关元素的化合价。
③求两种元素化合价绝对值的最小公倍数。
④确定各元素的原子个数。
⑤把原子个数写在相应元素符号的右下角。
⑥正价总数与负价总数的代数和为0时,化学式正确。
新课讲解
P O
+5 -2
两种元素化合价绝对值的最小公倍数=10
P原子数:10/5=2;
验证: (+5)×2 + (-2)×5=0
【解】
O原子数:10/2=5
答:这种磷的氧化物的化学式P2O5 。
例 已知 P 为 +5 价,O 为 -2 价。写出它们组成物质的化学式。
新课讲解
例 已知 P 为 +5 价,O 为 -2 价。写出它们组成物质的化学式。
①写元素符号,
标化合价
(左+右-)
P
O
②约简
(有公约数,则约简;
无公约数,不约简)
③数字交叉放置在元素符号右下角
④检查
在化合物里,正负化合价的代数和为0
(+5)×2+(-2)×5=0
+5
-2
2
5
P2O5 五氧化二磷
十字
交叉法
2.十字交叉法:
新课讲解
例外:H2O2不用约简
超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料,经研磨烧结后合成一种高温超导物质Y2Ba4Cu6Ox,假设在研磨烧结过程中各元素的化合价均无变化,则x的值为多少?
解:在Y2O3中O为-2价,则由正负化合价的代数和为0,可得Y的化合价为+3价,BaCO3中碳酸根的化合价为-2价,则Ba元素的化合价为+2价,CuO中O为-2价,则Cu元素的化合价为+2价,由在研磨烧结过程中各元素的化合价无变化,则在Y2Ba4Cu6Ox中,Y的化合价为+3价,Ba元素的化合价为+2价,Cu元素的化合价为+2价,O为-2价,根据正负化合价的代数和为0,则有
(+3)×2+(+2)×4+(+2)×6+(-2)×x=0,解得x=13。
新课讲解
综合运用
概念
化合价
在元素的上方写“+”或“-”后面加数值
用来表示原子间化合的数目
表示方法
应用
已知化合价写化学式
已知化学式求化合价
正价、负价、零价
分类
课堂小结
那么,怎样利用化学式进行计算呢?
硝酸铵
净重:50kg
含氮量:≥ 38%
××化肥厂出品
这是一袋硝酸铵
NH4NO3化肥的标签,这袋化肥所标含氮量是否真实?
不真实!该品牌化肥在弄虚作假。可以通过硝酸铵的化学式来算一算其氮元素的含量,就可证实其真假了。
新课讲解
(一)相对分子质量
相对原子质量(Ar) =
某原子的实际质量
碳-12原子×1/12
分子当中各原子的相对原子质量的总和
(Mr)
AmBn
CO2 :
Mr = 12×1+16×2 = 44
KMnO4:
Mr = 39×1+55×1+16×4 = 158
物质中所有C原子的相对原子质量总和
物质中所有O原子的相对原子质量总和
是一个比值,单位为“1”,省略不写。
新课讲解
三、有关相对分子质量的计算
【应用实例】苏丹红一号的相对分子质量为248,其化学式为CxH12N2O,其中x=_____
【相对原子质量:C-12 H-1 N-14 O-16】
计算相对分子质量(写出过程)Cu:64 Cl:35.5
(1)CO2 _______________________________
(2)Ca(OH)2 ___________________________
(3)CaCO3 ____________________________
(4)CuSO4 _____________________________
(5)NH4NO3 ___________________________
(6)2HCl ______________________________
=12+16×2=44
=40+(16+1)×2=74
=40+12+16×3=100
=64+32+16×4=160
=14×2+4×1+16×3=80
=2×(1+35.5)=73
【分析】利用相对分子质量的定义,设未知数,列方程式,求算即可。
【解答】解:12x+12+14×2+16=248 解得x=16
16
新课讲解
新课讲解
2.计算物质组成元素的质量比
化合物中各元素的质量比=“相对原子质量×个数”依次成比例。
说明:
(1)应指明元素的顺序,元素顺序不同,质量比的数值不同;
(2)元素的质量比一般是最简比,计算后应进行约简处理。
CO2 :
中碳元素和氧元素的质量比
KMnO4:
中钾元素和锰元素及氧元素质量比
m(C) : m(O) = (12×1):(16×2)= 3:8
m(K) : m(Mn) : m(O) = (39×1):(55×1):(16×4)= 39 : 55 : 64
2.注意合并相同元素的原子个数,不要漏掉。
如:C6H12O6 中各元素的质量比:
m(C):m(H):m(O)=6:12:6=1:2:1( )
m(C):m(H):m(O)=(6×12):(12×1):(6×16)=6:1:8( )
1.元素质量比 ≠ 原子个数比;
Ca(OH)2 NH4NO3
易错提醒
新课讲解
3、化合物中某元素的质量分数
说明:
化合物中某元素的质量分数= ×100%
= ×100%
该元素的质量
物质的质量
该元素的相对原子质量×原子个数相对分子质量
(1)第一个公式是元素质量分数的定义式;
(2)若已知化合物的化学式,可根据第二个公式进行计算;
(3)元素的质量分数,习惯上用百分数来表示。
新课讲解
【例】计算NH4NO3中氮元素的质量分数
硝酸铵
净重:50kg
含氮量:≥ 38%
××化肥厂出品
解:NH4NO3的相对分子质量=14+1×4+14+16×3=80
N的相对原子质量×N的原子数
NH4NO3的相对分子质量
×100%
=
14×2
80
=35%
×100%
NH4NO3中氮元素的质量分数
=
答:NH4NO3中氮元素的质量分数为35%,标签中写的含氮量是假的。
35%< 38%
新课讲解
这是一袋硝酸铵
NH4NO3化肥的标签,这袋化肥所标含氮量是否真实?
【基础练习】求算:水(H2O)中氢元素的质量分数。【相对原子质量H-1 O-16】
【注意】对于除不尽的数值,应按照题目要求进行取舍,如果没有要求,一般要保留一位小数。
【解答】H2O中氢元素的质量分数= ×100%≈11.1%
1×2
18
【变式训练】计算CO2中碳、氧元素的质量分数。【相对原子质量: C-12 O-16 】
【解答】CO2中碳元素的质量分数= ×100%≈27.3%
12×1
44
CO2中氧元素的质量分数= ×100%≈72.7%
16×2
44
【发现】 CO2中碳元素的质量分数+ CO2中氧元素的质量分数=27.3%+72.7%=100%
在化合物里,所有元素质量分数之和等于1。
新课讲解
【应用实例】某新型胃药的一个分子中含有5个氮原子,其中氮原子的质量分数约为16.5%,则其相对分子质量为多少?【相对原子质量: N-14 】
【解答】解:设该物质的相对分子质量为x。
×100%=16.5%
x=424.2
14×5
x
答:该胃药的相对分子质量为424.2。
新课讲解
公式推导 m(元素) = m(化合物)____C%
m(化合物) = m(元素)____C%
÷
×
某种含硫酸亚铁的药物可用于治疗缺铁性贫血。某贫血患者每天需服用这种含铁元素10%的药物112mg,则每天他服用的这种药物中含硫酸亚铁(FeSO4)的质量是多少?(该药物中其他成分不含铁元素)
解:因药物中只有硫酸亚铁含有铁元素,设硫酸亚铁的质量为x,
根据硫酸亚铁中铁元素的质量等于药物中铁元素的质量,则
x×—————×100%═112mg×10%
解得x═30.4mg
答:每天他服用的这种药物中含硫酸亚铁30.4mg。
56
56+32+16×4
新课讲解
【应用实例】
课堂小结
有关相对分子质量的计算
计算相对分子质量:
相对分子质量=(相对原子质量×原子个数)之和
计算物质组成元素的质量比:
组成元素的质量比=(相对原子质量×原子个数)之比
计算某元素的质量:
某元素的质量=化合物的质量×化合物中该元素的质量分数
计算物质中某元素的质量分数:
某元素的
质量分数
=
该元素的相对原子质量×原子个数
该化合物的相对分子质量
×100%
宏 观 ①
②
微 观 ①
②
一、化学式及其意义
1.用_______________的组合表示_________的式子叫化学式。
元素符号和数字
物质组成
表示二氧化碳这种物质
表示二氧化碳由碳、氧元素组成
表示1个二氧化碳分子
1个二氧化碳分子由1个碳原子和2个氧原子构成
2.意义:以CO2为例
课堂总结
1.化合价标注在元素符号的_________。
2.在化合物中,H通常显_____价,O通常显_____价。金属元素通常显_____价,非金属元素通常显_____价。
3.单质中元素的化合价为_____。
4.一种元素在不同的化合物中可显不同价态。
如:Fe2O3读作__________;FeO读作__________。
5.一种元素在同一种化合物中可显不同价态。如:NH4NO3
6.根据化合价书写化学式所依据的原则为:在化合物里,元素正负化合价代数和为 。
7.化合价与离子符号的相同点: 相等, 相同。
正上方
+1
-2
正
负
0
氧化铁
氧化亚铁
-3
+5
0
数值
正负
课堂总结
1.相对分子质量=化学式中各原子的_____________之和。
2.计算组成物质各元素的质量比
(1)元素质量=相对原子质量×_____________
(2)化学式中原子个数比 元素质量比(= 或 ≠)
3.计算物质中元素的质量分数
(1)元素的质量分数=____________________________
(2)元素质量=__________________________________
(3)物质的相对分子质量=________________________
元素质量÷物质的相对分子质量
物质的相对分子质量×元素的质量分数
元素质量÷元素的质量分数
相对原子质量
原子个数
≠
课堂总结
1.[2021北京昌平区新学道临川学校月考]下列符号能表示两个氢原子的是( )
A.H2 B.2H2 C.2H D.2H+
【解题思路】 A表示一个氢分子或氢气这种物质,B表示两个氢分子,C表示两个氢原子,D表示两个氢离子。
2.[2020山东滨州中考]下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是 ( )
A.O B.N2 C.Cu D.CO2
C
【解题思路】 金属、大多数固体非金属单质等都是由原子直接构成的,故它们的元素符号既能表示一个原子,又能表示一种元素,还能表示一种物质。O可表示氧元素,表示一个氧原子,但不能表示一种物质,A错误。N2可表示氮气,也可表示一个氮分子,但不能表示一种元素,也不能表示一个原子,B错误,同理D错误。
C
课堂练习
3.[2020山东临沂中考]化学用语是学习化学的重要工具,下列表达正确的是 ( )
A.汞元素:hg B.两个磷原子:2P
C.2个铁离子:2Fe2+ D.氧化铝:AlO
【解题思路】 汞元素表示为Hg;2个铁离子表示为2Fe3+;氧化铝表示为Al2O3。
4.[2020 江苏徐州中考改编]元素符号和化学式是国际通用的化学符号。下列叙述正确的是 ( )
A.CO中含有碳元素
B.两个氢分子可表示为2H
C.人体中含量最高的元素是钙
D.铁丝在氧气中燃烧产物的化学式是O4Fe3
B
【解题思路】 一氧化碳中含有碳元素,A正确;两个氢分子可表示为2H2,B错误;人体中含量最高的元素是氧,人体中含量最高的金属元素是钙,C错误;铁丝在氧气中燃烧产物的化学式是Fe3O4,D错误。
A
课堂练习
5.[2021江苏南京江宁区上元中学月考]氧气中氧元素的化合价为 ( )
A.-2 B.0 C.-1 D.+1
【解题思路】 单质中元素的化合价为零。
6.[2020天津中考]氯酸钾(KClO3)是实验室制取氧气常用药品。氯酸钾中氯元素的化合价为 ( )
A.+2 B.+3 C.+4 D.+5
B
【解题思路】 氯酸钾中钾元素的化合价为+1,氧元素的化合价为-2,根据化合物中各元素正负化合价代数和为零的原则,可计算出氯元素的化合价为+5。
D
课堂练习
7.[2021江西九江期中]如图是铁元素和氧元素常见化合价的坐标图,试判断a点上形成化合物的化学式为 ( )
A.Fe
B.FeO
C.Fe2O3
D.Fe3O4
【解题思路】 a点上形成的化合物中,铁元素显+2价,氧元素显-2价,所以a点上形成化合物的化学式为FeO。
8.[2021河南南阳期中]稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化学式为EuCl3,则氧化铕的化学式为(两种化合物中铕元素的化合价相同) ( )
A.EuO B.Eu2O3 C.Eu3O2 D.EuO3
B
【解题思路】 根据氯化铕的化学式EuCl3可以判断,Eu显+3价,所以+3价铕的氧化物的化学式为Eu2O3。
B
9.[2020河南中考]生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是( )
A.双氧水消毒液(H2O2)
B.“84”消毒液(NaClO)
C.酒精消毒液(C2H5OH)
D.过氧乙酸消毒液(C2H4O3)
【解题思路】 纯净物中某元素的质量分数=×100%。过氧化氢(H2O2)中氧元素的质量分数为 ×100%=;次氯酸钠(NaClO)中氧元素的质量分数为 ×100%=;酒精(C2H5OH)中氧元素的质量分数为 ×100%=;过氧乙酸(C2H4O3)中氧元素的质量分数为 ×100%≈。其中过氧化氢中氧元素的质量分数最大。
A
课堂练习
10.[2021广东佛山教研联盟联考]从地沟油中提炼生物柴油是垃圾资源化的方法之一。生物柴油的主要成分是硬脂酸甲酯(C19H38O2),下列有关硬脂酸甲酯的说法正确的是( )
A.C、H、O三种元素的质量比为19∶38∶2
B.相对分子质量为(12×19+1×38+16×2)
C.C、H、O三种原子的个数比为12∶1∶16
D.氧元素的质量分数为×100%
【解题思路】 硬脂酸甲酯中C、H、O三种元素的质量比=(12×19)∶(1×38)∶(16×2)=114∶19∶16,A错误;硬脂酸甲酯分子中C、H、O三种原子的个数比为19∶38∶2,C错误;硬脂酸甲酯中氧元素的质量分数=
×100%,D错误。
B
课堂练习
11.[2021河北邯郸永年区期中节选]如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为144),请回答下列问题:
(1)Na2PO3F中金属元素与氧元素的质量比为 。
(2)若牙膏中的其他成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为 g(结果保留小数点后一位)。
【主要活性成分】单氟磷酸钠
【摩擦剂】碳酸钙
【香 型】清爽薄荷
【氟含量】0.14%
【净含量】200 g
【解题思路】 (1)单氟磷酸钠中钠、氧元素的质量比为(23×2)∶(16×3)=23∶24。
(2)根据标签信息可知,每支这种牙膏中所含氟元素的质量为200 g×0.14%=0.28 g,单氟磷酸钠中氟元素的质量分数为×100%,则每支这种牙膏中含单氟磷酸钠的质量为0.28 g÷(×100%)≈2.1 g。
课堂练习
12.[2021山东微山期中]人体缺乏维生素C易患坏血病。如图所示为某种维生素C说明书的一部分。请回答:
(1)求维生素C的相对分子质量(要有计算过程,下同);
(2)求维生素C中碳元素、氢元素和氧元素的质量比;
(3)若健康成年人每天对维生素C的最低需要量为60 mg。当摄入的维生素C完全来自该维生素C片时,每天至少服用几次
解:(1)维生素C的相对分子质量为12×6+1×8+16×6=176。
(2)维生素C中C、H、O元素的质量比为(12×6)∶(1×8)∶(16×6)=72∶8∶96=9∶1∶12。
(3)已知健康成年人每天对维生素C的最低需要量为60 mg,每片维生素C的质量为100 mg,其中维生素C的含量为10%,每次吃两片,则当摄入的维生素C完全来自该维生素C片时,健康成年人每天至少服用该维生素C片的次数为=3。
课堂练习
新课导入
学习目标
新课讲解
课堂练习
01
02
03
04
目录
课题4 化学式与化合价
人教版九年级上册 第四单元
建
议
2~3
课
时
新课导入
观看视频
学习目标
1.通过复习元素符号的意义,以水的化学式为例分析讨论,能说出化学式及数字的意义。
2.建立科学的物质观,增进对物质宏观微观的认识,能规范使用化学术语。
3.过分类讲解物质化学式的书写和读法,能正确书写和读出物质的化学式,知道一些常见元素和根的化合价,并能利用化合价推求化学式。
4.通过自主阅读课本,能说出相对分子质量的含义,能正确计算相对分子质量、元素质量比和元素质量分数。
BOY
单词
H
H
O
化学式
用元素符号和数字组合来表示物质组成的式子
一、化学式
新课讲解
1.化学式的概念
物质 氧气 氢气 二氧 化碳 氯化氢 四氧化 三铁 氧化汞
化学式 O2 H2 CO2 HCl Fe3O4 HgO
化学式是通过实验测定的,因此化学式的书写必须依据实验的结果。不能凭空想象、主观臆断。
……?
化学式可以任意的书写吗?
怎么区分物理变化和化学变化?
思 考
同种物质可以有不同的化学式吗?
新课讲解
新课讲解
物质
混合物
纯净物
没有固定的组成
无化学式
组成固定不变
有并且只有一个化学式
固
液
气
H2O
化学式与物质的状态无关
宏观
一种物质
物质的元素组成
微观
物质的一个分子
物质的分子构成
宏观:
微观:
水
水由氢元素和氧元素组成
水是由氢元素和氧元素构成的
水是由两个氢元素和一个氧元素组成
一个水分子
一个水分子由两个氢原子和氧原子构成
一个水分子由两个氢原子和一个氧原子组成
两个水分子
(化学式前加数字——微观)
只论种类不论个数
即论种类又论个数
H2O
2H2O:
2.化学式的意义
氢元素
一个氢原子
两个氢原子
氢气
氢气由氢元素组成
一个氢分子
一个氢分子由两个氢原子构成
两个氢分子
宏观
微观
①元素符号右下角的数字:
表示每个分子中原子的个数
②化学式前面的数字:
表示该微粒的个数
新课讲解
其他化学符号中各数字的意义
如2Cu表示2个铜原子。
元素符号前的数字:表示原子个数。
离子符号前的数字:表示离子个数。
元素符号右上角的数字:表示该元素的一个离子所带的电荷数。
如2Cu2+表示2个铜离子。
如Cu2+中的“2+”表示1个铜离子带2个单位的正电荷。
新课讲解
微观意义
由分子构成的物质
由原子构成的物质:表示物质的一个原子
表示一种物质
表示该物质的元素组成
宏观意义
表示物质的一个分子
表示物质的分子构成
只论种类不论个数
即论种类又论个数
化学式:一种用元素符号和数字这样的组合来表示物质组成的式子。
新课讲解
元素
稀有气体:
金属元素:
非金属元素
(除稀有气体)
固态:“ 石 ”
液态:“ 氵”(溴)
气态:“气”
“ 钅”(除汞)
“气”
He Ne Ar (He2 Ne2)
Li Be Na Mg Al K Ca
B C Si P S
由原子直接构成的单质
直接用元素符号表示
读元素的名称
H2 N2 O2 F2 Cl2
分子中所含原子的个数
元素符号+角标“2”
双原子分子
3.化学式的写法和读法 ①单质 只含一种元素的纯净物
一般气体成双成对,稀、固、金是单个
水:
一个水分子是由两个氢原子和一个氧原子构成
H2O1
或
O1H2
H2O
当组成元素原子个数比为1时,1省略不写。
1.氧化物化学式的书写:
一般把氧的元素符号写在右方,另一种元素的符号写在左方。
一氧化碳 二氧化碳 二氧化硫 五氧化二磷 四氧化三铁
CO2
CO
SO2
P2O5
Fe3O4
从后向前读
化学式的读法
②化合物
顺写反读
氯化钠
Cl
Na
NaxCly
2.金属元素和非金属元素组成的化合物:
化学式书写:金属的元素符号写在左方,非金属元素写在右方。
氯化钠 氯化钾 氯化氢 氯化银 氯化钡
KCl
NaCl
HCl
AgCl
BaCl2
从后向前读,某化某
化学式的读法
顺写反读
新课讲解
意义
化学式
读写方法
宏观意义
微观意义
概念
用元素符号和数字的组合表示物质组成的式子。
表示一种物质
表示物质的一个分子
表示该物质的元素组成
表示物质的分子(或原子)构成
课堂小结
通过观察我们可以得出:物质不同,原子个数比可能不同。
Na2O Na2S H2O H2S
个数比为2:1
CaO MgO CO NaCl
个数比为1:1
CaCl2 MgCl2 CO2 SiO2
个数比为1:2
化合物中各元素原子的个数比是由什么来决定的呢?
新课讲解
二、化合价
化合物有固定的组成,即形成化合物的元素有固定的原子个数比。
新课讲解
观看视频
1、 概念:一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质。
2、规定:
(1)在离子构成的化合物中,化合价与离子所带电荷数有关。
Na原子失去一个电子变成Na+,规定Na元素的化合价为+1;
Cl原子得到一个电子变成Cl-,规定Cl元素的化合价为-1。
(2)在分子构成的化合物中,化合价与共用电子对的数目有关。
3、表示方法:
在元素符号或原子团的 用“+/-n”表示。
正上方
+n
-n
H2O中H元素的化合价
H
+1
H2O中O元素的化合价
O
-2
正一价的氢元素
负二价的氧元素
新课讲解
4、基本规律:
(1)化合价有正负之分,在化合物里,
氯化钠
Cl
Na
NaxCly
化合价
通常与对应离子所带电荷数值相等,正负号相同
化合物中,正、负化合价的代数和为0
Na+
Na为+1价
+1
右上角,数字在前,符号在后,1要省略。
正上方,符号在前,数字在后,1不能省略。
Cl-
Cl为-1价
(+1)·x+(-1)·y=0
x:y = 1:1
NaCl
新课讲解
化合价与离子符号的区别
(2)元素的化合价是元素在形成化合物时表现出来的性质,因此单质中元素的化合价为零;
0 0 0 0
O2 N2 H2 Fe
(3)同种元素在不同物质中可显不同的化合价,在同一物质中也可能显不同的化合价。
+3
+2
+7
+6
Fe2O3 FeO KMnO4 K2MnO4
氧化铁
氧化亚铁
高锰酸钾
锰酸钾
新课讲解
(4)在化合物中氢元素通常显+1价,氧元素通常显-2价,常以它们为基准来推算化合物中其他元素的化合价;
HCl H2S H2O
+1
+1
-1
-2
+1
-2
(5)通常,金属元素显正价,非金属元素显负价;
NaCl CaCl2 AlCl3 KCl MgCl2
+1
-1
+1
-1
-1
-1
-1
+2
+2
+3
NH4NO3
-3
+5
元素和根的名称 元素和根的符号 常见化合价 元素和根的名称 元素和根的符号 常见化合价
钾 K +1 氯 Cl -1、+1、+5、+7
钠 Na +1 溴 Br -1
银 Ag +1 氧 O -2
钙 Ca +2 硫 S -2、+4、+6
镁 Mg +2 碳 C +2、+4
钡 Ba +2 硅 Si +4
铜 Cu +1、+2 氮 N -3、+2、+3、+4、+5
铁 Fe +2、+3 磷 P -3、+3、+5
铝 Al +3 氢氧根 OH- -1
锰 Mn +2、+4、+6、+7 硝酸根 NO3- -1
锌 Zn +2 硫酸根 SO42- -2
氢 H +1 碳酸根 CO32- -2
氟 F -1 铵根 NH4+ +1
新课讲解
常见元素和原子团的化合价
钾钠银氢正一价,钙镁钡锌正二价;
铝是正三氧负二,氟氯负价负一价;
硫有负二正四六,正二正三铁可变;
正一二铜二四碳,单质零价永不变。
常见元素化合价的记忆口诀
新课讲解
①、常见元素的化合价(记忆)
观看视频
新课讲解
作为一个整体参加反应的原子集团,原子团也叫作根。
注意:①原子团不能单独存在;②带电荷的原子团也是离子。
SO42-
2个硫酸根
一个硫酸根带两个单位的负电荷
1个硫酸根含有4个氧原子
2
-2
硫酸根显负二价
新课讲解
②、原子团定义及常见化合价
名称 符号 化合价 化合物 读法
氢氧根 OH- -1 NaOH
硝酸根 NO3- -1 KNO3
硫酸根 SO42- -2 CuSO4 碳酸根 CO32- -2 CaCO3 铵根 NH4+ +1 NH4Cl
氢氧化*
*酸*
氯化铵
新课讲解
口诀:
负一硝酸氢氧根,负二碳酸硫酸根,
负三记住磷酸根,正一价的是铵根。
(1)根据化学式求某一元素化合价
原则:化合物里正负化合价的代数和为零。
例 试确定氯酸钾(KClO3)中氯元素的化合价。
解:设氯元素的化合价为x,则
(+1)+ x +(-2)×3=0
所以,在氯酸钾中,氯元素的化合价为+5价
若求原子团中某元素的化合价,则代数和不为零。
5.化合价规律的应用
新课讲解
根据化学式求化合价(氢+1氧-2为标准)
【练习】1.标出画线元素的化合价
Fe2O3(氧化铁) FeO(氧化亚铁)
Fe2+(亚铁离子) Fe3+(铁离子)
KMnO4(高锰酸钾) K2MnO4(锰酸钾)
NH4NO3(硝酸铵) SO42- H2O2
+3
+2
+7
+6
-3
+5
-1
+6
+2
+3
新课讲解
(2)根据元素化合价推出化合物的化学式
1.最小公倍数法:
①写出组成化合物的元素符号,一般正价元素在左,负价元素在右。
②标出有关元素的化合价。
③求两种元素化合价绝对值的最小公倍数。
④确定各元素的原子个数。
⑤把原子个数写在相应元素符号的右下角。
⑥正价总数与负价总数的代数和为0时,化学式正确。
新课讲解
P O
+5 -2
两种元素化合价绝对值的最小公倍数=10
P原子数:10/5=2;
验证: (+5)×2 + (-2)×5=0
【解】
O原子数:10/2=5
答:这种磷的氧化物的化学式P2O5 。
例 已知 P 为 +5 价,O 为 -2 价。写出它们组成物质的化学式。
新课讲解
例 已知 P 为 +5 价,O 为 -2 价。写出它们组成物质的化学式。
①写元素符号,
标化合价
(左+右-)
P
O
②约简
(有公约数,则约简;
无公约数,不约简)
③数字交叉放置在元素符号右下角
④检查
在化合物里,正负化合价的代数和为0
(+5)×2+(-2)×5=0
+5
-2
2
5
P2O5 五氧化二磷
十字
交叉法
2.十字交叉法:
新课讲解
例外:H2O2不用约简
超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料,经研磨烧结后合成一种高温超导物质Y2Ba4Cu6Ox,假设在研磨烧结过程中各元素的化合价均无变化,则x的值为多少?
解:在Y2O3中O为-2价,则由正负化合价的代数和为0,可得Y的化合价为+3价,BaCO3中碳酸根的化合价为-2价,则Ba元素的化合价为+2价,CuO中O为-2价,则Cu元素的化合价为+2价,由在研磨烧结过程中各元素的化合价无变化,则在Y2Ba4Cu6Ox中,Y的化合价为+3价,Ba元素的化合价为+2价,Cu元素的化合价为+2价,O为-2价,根据正负化合价的代数和为0,则有
(+3)×2+(+2)×4+(+2)×6+(-2)×x=0,解得x=13。
新课讲解
综合运用
概念
化合价
在元素的上方写“+”或“-”后面加数值
用来表示原子间化合的数目
表示方法
应用
已知化合价写化学式
已知化学式求化合价
正价、负价、零价
分类
课堂小结
那么,怎样利用化学式进行计算呢?
硝酸铵
净重:50kg
含氮量:≥ 38%
××化肥厂出品
这是一袋硝酸铵
NH4NO3化肥的标签,这袋化肥所标含氮量是否真实?
不真实!该品牌化肥在弄虚作假。可以通过硝酸铵的化学式来算一算其氮元素的含量,就可证实其真假了。
新课讲解
(一)相对分子质量
相对原子质量(Ar) =
某原子的实际质量
碳-12原子×1/12
分子当中各原子的相对原子质量的总和
(Mr)
AmBn
CO2 :
Mr = 12×1+16×2 = 44
KMnO4:
Mr = 39×1+55×1+16×4 = 158
物质中所有C原子的相对原子质量总和
物质中所有O原子的相对原子质量总和
是一个比值,单位为“1”,省略不写。
新课讲解
三、有关相对分子质量的计算
【应用实例】苏丹红一号的相对分子质量为248,其化学式为CxH12N2O,其中x=_____
【相对原子质量:C-12 H-1 N-14 O-16】
计算相对分子质量(写出过程)Cu:64 Cl:35.5
(1)CO2 _______________________________
(2)Ca(OH)2 ___________________________
(3)CaCO3 ____________________________
(4)CuSO4 _____________________________
(5)NH4NO3 ___________________________
(6)2HCl ______________________________
=12+16×2=44
=40+(16+1)×2=74
=40+12+16×3=100
=64+32+16×4=160
=14×2+4×1+16×3=80
=2×(1+35.5)=73
【分析】利用相对分子质量的定义,设未知数,列方程式,求算即可。
【解答】解:12x+12+14×2+16=248 解得x=16
16
新课讲解
新课讲解
2.计算物质组成元素的质量比
化合物中各元素的质量比=“相对原子质量×个数”依次成比例。
说明:
(1)应指明元素的顺序,元素顺序不同,质量比的数值不同;
(2)元素的质量比一般是最简比,计算后应进行约简处理。
CO2 :
中碳元素和氧元素的质量比
KMnO4:
中钾元素和锰元素及氧元素质量比
m(C) : m(O) = (12×1):(16×2)= 3:8
m(K) : m(Mn) : m(O) = (39×1):(55×1):(16×4)= 39 : 55 : 64
2.注意合并相同元素的原子个数,不要漏掉。
如:C6H12O6 中各元素的质量比:
m(C):m(H):m(O)=6:12:6=1:2:1( )
m(C):m(H):m(O)=(6×12):(12×1):(6×16)=6:1:8( )
1.元素质量比 ≠ 原子个数比;
Ca(OH)2 NH4NO3
易错提醒
新课讲解
3、化合物中某元素的质量分数
说明:
化合物中某元素的质量分数= ×100%
= ×100%
该元素的质量
物质的质量
该元素的相对原子质量×原子个数相对分子质量
(1)第一个公式是元素质量分数的定义式;
(2)若已知化合物的化学式,可根据第二个公式进行计算;
(3)元素的质量分数,习惯上用百分数来表示。
新课讲解
【例】计算NH4NO3中氮元素的质量分数
硝酸铵
净重:50kg
含氮量:≥ 38%
××化肥厂出品
解:NH4NO3的相对分子质量=14+1×4+14+16×3=80
N的相对原子质量×N的原子数
NH4NO3的相对分子质量
×100%
=
14×2
80
=35%
×100%
NH4NO3中氮元素的质量分数
=
答:NH4NO3中氮元素的质量分数为35%,标签中写的含氮量是假的。
35%< 38%
新课讲解
这是一袋硝酸铵
NH4NO3化肥的标签,这袋化肥所标含氮量是否真实?
【基础练习】求算:水(H2O)中氢元素的质量分数。【相对原子质量H-1 O-16】
【注意】对于除不尽的数值,应按照题目要求进行取舍,如果没有要求,一般要保留一位小数。
【解答】H2O中氢元素的质量分数= ×100%≈11.1%
1×2
18
【变式训练】计算CO2中碳、氧元素的质量分数。【相对原子质量: C-12 O-16 】
【解答】CO2中碳元素的质量分数= ×100%≈27.3%
12×1
44
CO2中氧元素的质量分数= ×100%≈72.7%
16×2
44
【发现】 CO2中碳元素的质量分数+ CO2中氧元素的质量分数=27.3%+72.7%=100%
在化合物里,所有元素质量分数之和等于1。
新课讲解
【应用实例】某新型胃药的一个分子中含有5个氮原子,其中氮原子的质量分数约为16.5%,则其相对分子质量为多少?【相对原子质量: N-14 】
【解答】解:设该物质的相对分子质量为x。
×100%=16.5%
x=424.2
14×5
x
答:该胃药的相对分子质量为424.2。
新课讲解
公式推导 m(元素) = m(化合物)____C%
m(化合物) = m(元素)____C%
÷
×
某种含硫酸亚铁的药物可用于治疗缺铁性贫血。某贫血患者每天需服用这种含铁元素10%的药物112mg,则每天他服用的这种药物中含硫酸亚铁(FeSO4)的质量是多少?(该药物中其他成分不含铁元素)
解:因药物中只有硫酸亚铁含有铁元素,设硫酸亚铁的质量为x,
根据硫酸亚铁中铁元素的质量等于药物中铁元素的质量,则
x×—————×100%═112mg×10%
解得x═30.4mg
答:每天他服用的这种药物中含硫酸亚铁30.4mg。
56
56+32+16×4
新课讲解
【应用实例】
课堂小结
有关相对分子质量的计算
计算相对分子质量:
相对分子质量=(相对原子质量×原子个数)之和
计算物质组成元素的质量比:
组成元素的质量比=(相对原子质量×原子个数)之比
计算某元素的质量:
某元素的质量=化合物的质量×化合物中该元素的质量分数
计算物质中某元素的质量分数:
某元素的
质量分数
=
该元素的相对原子质量×原子个数
该化合物的相对分子质量
×100%
宏 观 ①
②
微 观 ①
②
一、化学式及其意义
1.用_______________的组合表示_________的式子叫化学式。
元素符号和数字
物质组成
表示二氧化碳这种物质
表示二氧化碳由碳、氧元素组成
表示1个二氧化碳分子
1个二氧化碳分子由1个碳原子和2个氧原子构成
2.意义:以CO2为例
课堂总结
1.化合价标注在元素符号的_________。
2.在化合物中,H通常显_____价,O通常显_____价。金属元素通常显_____价,非金属元素通常显_____价。
3.单质中元素的化合价为_____。
4.一种元素在不同的化合物中可显不同价态。
如:Fe2O3读作__________;FeO读作__________。
5.一种元素在同一种化合物中可显不同价态。如:NH4NO3
6.根据化合价书写化学式所依据的原则为:在化合物里,元素正负化合价代数和为 。
7.化合价与离子符号的相同点: 相等, 相同。
正上方
+1
-2
正
负
0
氧化铁
氧化亚铁
-3
+5
0
数值
正负
课堂总结
1.相对分子质量=化学式中各原子的_____________之和。
2.计算组成物质各元素的质量比
(1)元素质量=相对原子质量×_____________
(2)化学式中原子个数比 元素质量比(= 或 ≠)
3.计算物质中元素的质量分数
(1)元素的质量分数=____________________________
(2)元素质量=__________________________________
(3)物质的相对分子质量=________________________
元素质量÷物质的相对分子质量
物质的相对分子质量×元素的质量分数
元素质量÷元素的质量分数
相对原子质量
原子个数
≠
课堂总结
1.[2021北京昌平区新学道临川学校月考]下列符号能表示两个氢原子的是( )
A.H2 B.2H2 C.2H D.2H+
【解题思路】 A表示一个氢分子或氢气这种物质,B表示两个氢分子,C表示两个氢原子,D表示两个氢离子。
2.[2020山东滨州中考]下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是 ( )
A.O B.N2 C.Cu D.CO2
C
【解题思路】 金属、大多数固体非金属单质等都是由原子直接构成的,故它们的元素符号既能表示一个原子,又能表示一种元素,还能表示一种物质。O可表示氧元素,表示一个氧原子,但不能表示一种物质,A错误。N2可表示氮气,也可表示一个氮分子,但不能表示一种元素,也不能表示一个原子,B错误,同理D错误。
C
课堂练习
3.[2020山东临沂中考]化学用语是学习化学的重要工具,下列表达正确的是 ( )
A.汞元素:hg B.两个磷原子:2P
C.2个铁离子:2Fe2+ D.氧化铝:AlO
【解题思路】 汞元素表示为Hg;2个铁离子表示为2Fe3+;氧化铝表示为Al2O3。
4.[2020 江苏徐州中考改编]元素符号和化学式是国际通用的化学符号。下列叙述正确的是 ( )
A.CO中含有碳元素
B.两个氢分子可表示为2H
C.人体中含量最高的元素是钙
D.铁丝在氧气中燃烧产物的化学式是O4Fe3
B
【解题思路】 一氧化碳中含有碳元素,A正确;两个氢分子可表示为2H2,B错误;人体中含量最高的元素是氧,人体中含量最高的金属元素是钙,C错误;铁丝在氧气中燃烧产物的化学式是Fe3O4,D错误。
A
课堂练习
5.[2021江苏南京江宁区上元中学月考]氧气中氧元素的化合价为 ( )
A.-2 B.0 C.-1 D.+1
【解题思路】 单质中元素的化合价为零。
6.[2020天津中考]氯酸钾(KClO3)是实验室制取氧气常用药品。氯酸钾中氯元素的化合价为 ( )
A.+2 B.+3 C.+4 D.+5
B
【解题思路】 氯酸钾中钾元素的化合价为+1,氧元素的化合价为-2,根据化合物中各元素正负化合价代数和为零的原则,可计算出氯元素的化合价为+5。
D
课堂练习
7.[2021江西九江期中]如图是铁元素和氧元素常见化合价的坐标图,试判断a点上形成化合物的化学式为 ( )
A.Fe
B.FeO
C.Fe2O3
D.Fe3O4
【解题思路】 a点上形成的化合物中,铁元素显+2价,氧元素显-2价,所以a点上形成化合物的化学式为FeO。
8.[2021河南南阳期中]稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化学式为EuCl3,则氧化铕的化学式为(两种化合物中铕元素的化合价相同) ( )
A.EuO B.Eu2O3 C.Eu3O2 D.EuO3
B
【解题思路】 根据氯化铕的化学式EuCl3可以判断,Eu显+3价,所以+3价铕的氧化物的化学式为Eu2O3。
B
9.[2020河南中考]生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是( )
A.双氧水消毒液(H2O2)
B.“84”消毒液(NaClO)
C.酒精消毒液(C2H5OH)
D.过氧乙酸消毒液(C2H4O3)
【解题思路】 纯净物中某元素的质量分数=×100%。过氧化氢(H2O2)中氧元素的质量分数为 ×100%=;次氯酸钠(NaClO)中氧元素的质量分数为 ×100%=;酒精(C2H5OH)中氧元素的质量分数为 ×100%=;过氧乙酸(C2H4O3)中氧元素的质量分数为 ×100%≈。其中过氧化氢中氧元素的质量分数最大。
A
课堂练习
10.[2021广东佛山教研联盟联考]从地沟油中提炼生物柴油是垃圾资源化的方法之一。生物柴油的主要成分是硬脂酸甲酯(C19H38O2),下列有关硬脂酸甲酯的说法正确的是( )
A.C、H、O三种元素的质量比为19∶38∶2
B.相对分子质量为(12×19+1×38+16×2)
C.C、H、O三种原子的个数比为12∶1∶16
D.氧元素的质量分数为×100%
【解题思路】 硬脂酸甲酯中C、H、O三种元素的质量比=(12×19)∶(1×38)∶(16×2)=114∶19∶16,A错误;硬脂酸甲酯分子中C、H、O三种原子的个数比为19∶38∶2,C错误;硬脂酸甲酯中氧元素的质量分数=
×100%,D错误。
B
课堂练习
11.[2021河北邯郸永年区期中节选]如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为144),请回答下列问题:
(1)Na2PO3F中金属元素与氧元素的质量比为 。
(2)若牙膏中的其他成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为 g(结果保留小数点后一位)。
【主要活性成分】单氟磷酸钠
【摩擦剂】碳酸钙
【香 型】清爽薄荷
【氟含量】0.14%
【净含量】200 g
【解题思路】 (1)单氟磷酸钠中钠、氧元素的质量比为(23×2)∶(16×3)=23∶24。
(2)根据标签信息可知,每支这种牙膏中所含氟元素的质量为200 g×0.14%=0.28 g,单氟磷酸钠中氟元素的质量分数为×100%,则每支这种牙膏中含单氟磷酸钠的质量为0.28 g÷(×100%)≈2.1 g。
课堂练习
12.[2021山东微山期中]人体缺乏维生素C易患坏血病。如图所示为某种维生素C说明书的一部分。请回答:
(1)求维生素C的相对分子质量(要有计算过程,下同);
(2)求维生素C中碳元素、氢元素和氧元素的质量比;
(3)若健康成年人每天对维生素C的最低需要量为60 mg。当摄入的维生素C完全来自该维生素C片时,每天至少服用几次
解:(1)维生素C的相对分子质量为12×6+1×8+16×6=176。
(2)维生素C中C、H、O元素的质量比为(12×6)∶(1×8)∶(16×6)=72∶8∶96=9∶1∶12。
(3)已知健康成年人每天对维生素C的最低需要量为60 mg,每片维生素C的质量为100 mg,其中维生素C的含量为10%,每次吃两片,则当摄入的维生素C完全来自该维生素C片时,健康成年人每天至少服用该维生素C片的次数为=3。
课堂练习
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
