人教版(五四学制)九年级化学2.2溶解度同步练习(含解析)
文档属性
| 名称 | 人教版(五四学制)九年级化学2.2溶解度同步练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 74.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-21 00:00:00 | ||
图片预览



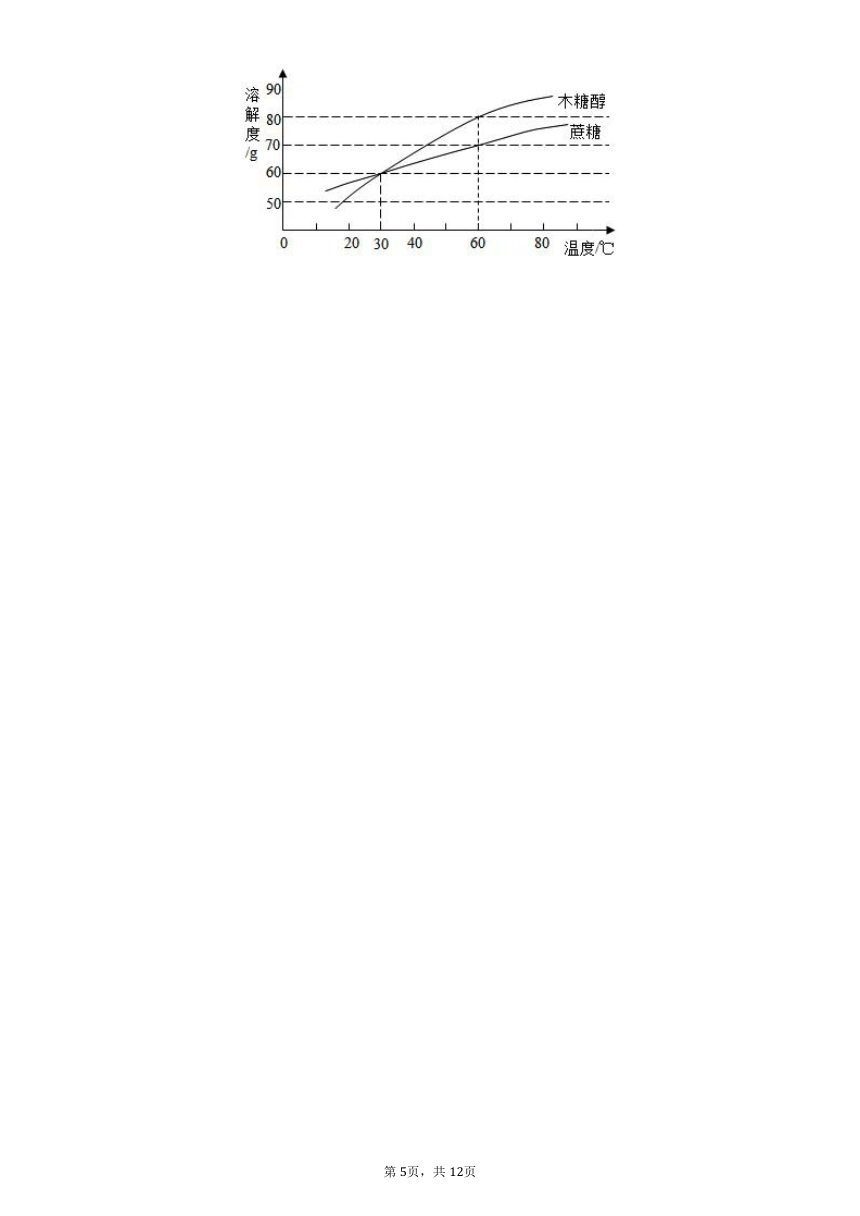
文档简介
溶解度
一、单选题
在时,克食盐溶解在克水中恰好达到饱和,以下关于食盐的溶解度说法正确的是
A. 食盐的溶解度是克 B. 食盐的溶解度是克
C. 时食盐的溶解度是克 D. 时食盐的溶解度是
已知时硝酸钾的溶解度为。下列关于对它的理解正确的是
A. 水中溶解了硝酸钾固体达到饱和
B. 时,硝酸钾固体溶于水形成饱和溶液
C. 时,水中最多能溶解硝酸钾固体
D. 时, 硝酸钾饱和溶液中含 硝酸钾
甲、乙试管中各盛有水,向其中一支中加入固体,另一支中加入固体,按图进行实验和的溶解度曲线如图,下列说法正确的是
A. 甲中加入的固体是
B. 时,甲中溶液可能饱和,乙中溶液一定饱和
C. 中含有少量杂质,可用冷却热饱和溶液的方法提纯
D. 时,若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
在一定温度下,某未饱和溶液蒸发掉克水部分后,析出克晶体不含结晶水;向原溶液投入克溶质晶体后,溶液中还剩下克固体溶质,则此温度下该溶质的溶解度为
A. 克 B. 克 C. 克 D. 克
时,某物质的饱和溶液中,溶质和溶液的质量比为:,则时其溶解度为
A. 克 B. C. 克 D.
在较高温度下,某溶液所含的硝酸钾和氯化钠都已接近饱和,当其冷却至室温时,析出的晶体经检验几乎不含氯化钠,这是因为
A. 氯化钠的溶解度比硝酸钾的大 B. 氯化钠的溶解度比硝酸钾的小
C. 氯化钠的溶解度在室温下更大 D. 氯化钠的溶解度受温度的影响小
根据如图的溶解度曲线,判断下列说法中不正确的是
A. 甲物质的溶解度小于乙物质的溶解度
B. 时,甲物质和乙物质的溶解度相同
C. 将时甲、乙两物质的饱和溶液降温到时都会析出晶体
D. 当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯甲
下列因素中不会影响气体物质溶解度的是
A. 溶剂的量 B. 温度 C. 溶质的种类 D. 压强
甲、乙两物质的溶解度与温度的关系如图所示,下列说法正确的是
A. 时乙的溶解度为
B. 乙的溶解度随温度的升高而降低
C. 时甲的溶解度小于乙的溶解度
D. 点表示时两物质的溶解度相等
时,往克硝酸钾溶液中加入克硝酸钾晶体,充分搅拌后,尚有部分晶体未溶解.稍加热后,晶体全部溶解.下列说法正确的是
A. 搅拌后加热前一定是饱和溶液 B. 搅拌后加热前一定是不饱和溶液
C. 加热后一定是饱和溶液 D. 加热后一定是不饱和溶液
时,四个实验小组分别取不同质量的,逐渐加入到各盛有水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余的质量。记录数据如表:
实验小组 第一组 第二组 第三组 第四组
水的质量
所取的质量
剩余的质量
下列说法错误的是
A. 时,饱和溶液中含有
B. 用蒸发的方法可以使不饱和溶液变成饱和溶液
C. 第二组所得溶液的溶质与溶剂的质量比为:
D. 第三组和第二组溶液溶质质量分数相等
如图是恒温下模拟海水晒盐过程的示意图,下列说法正确的是
A. 四杯溶液中溶质质量分数最大的是丁
B. 四杯溶液中溶质质量分数最小的是甲
C. 四杯溶液中溶质质量分数最小的是乙
D. 在整个过程中,食盐的溶解度发生了变化
二、填空题
甲、乙两种固体物质均不含结晶水的溶解度曲线如图所示。下列说法正确的是 ______
A.时,甲、乙饱和溶液的溶质质量相等
B.时,乙饱和溶液中溶质的质量为
C.时,甲物质可以配制溶质质量分数为的溶液
D.时,向乙饱和溶液中加入 ______水,可得到溶质质量分数为的乙溶液
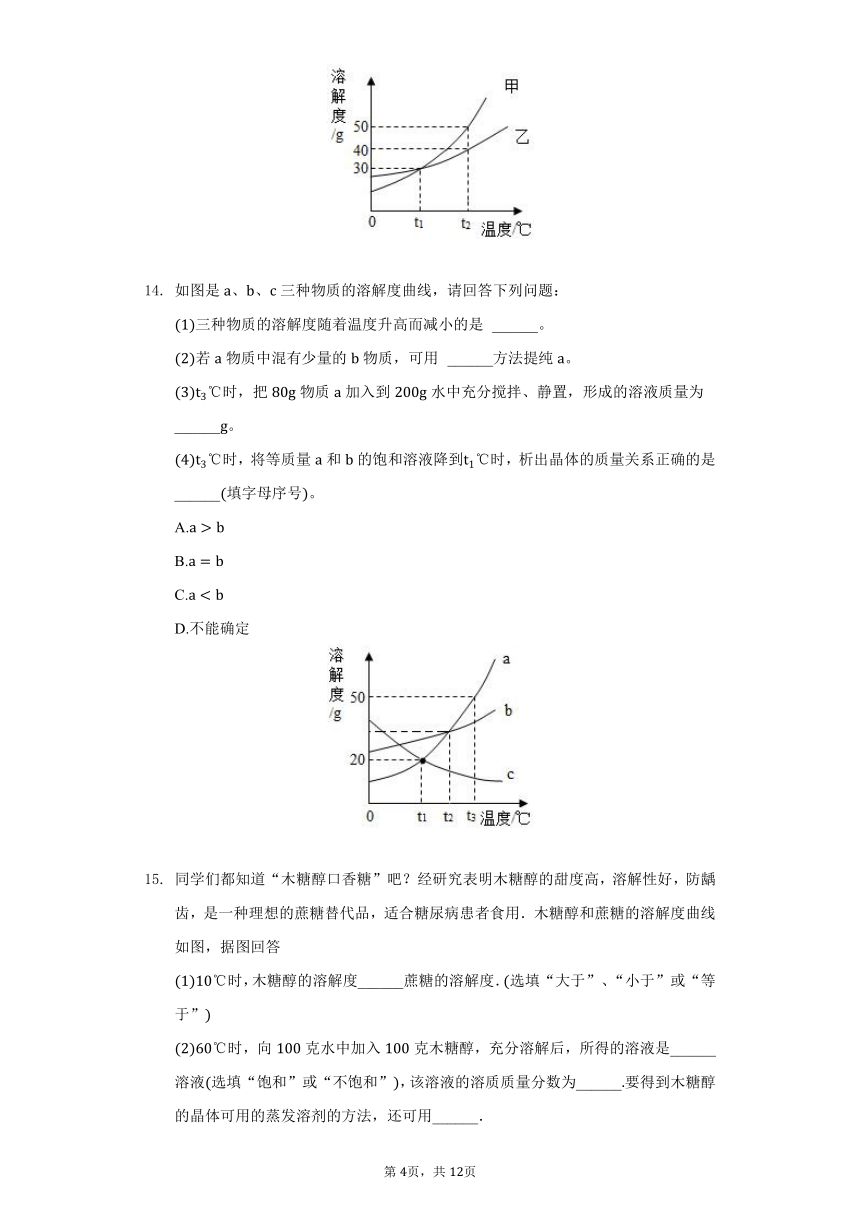
如图是、、三种物质的溶解度曲线,请回答下列问题:
三种物质的溶解度随着温度升高而减小的是 ______。
若物质中混有少量的物质,可用 ______方法提纯。
时,把物质加入到水中充分搅拌、静置,形成的溶液质量为 ______。
时,将等质量和的饱和溶液降到时,析出晶体的质量关系正确的是 ______填字母序号。
A.
B.
C.
D.不能确定
同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.木糖醇和蔗糖的溶解度曲线如图,据图回答
时,木糖醇的溶解度______蔗糖的溶解度.选填“大于”、“小于”或“等于”
时,向克水中加入克木糖醇,充分溶解后,所得的溶液是______溶液选填“饱和”或“不饱和”,该溶液的溶质质量分数为______要得到木糖醇的晶体可用的蒸发溶剂的方法,还可用______.
答案和解析
1.【答案】
【解析】解:、克是溶剂的质量,故A错误;
B、克是饱和溶液中溶质与溶剂的质量之和,故B错误;
C、在时,克食盐溶解在克水中恰好达到饱和,所以时食盐溶解度为克,故C正确;
D、溶解度的单位是克,缺少单位,故D错误;
故选:。
根据溶解度的四要素:一定温度、溶剂、饱和状态、溶解的质量进行分析。
解答本题关键是要熟悉溶解度的四要素:一定温度、溶剂、饱和状态、溶解的质量。
2.【答案】
【解析】解:根据溶解度的概念,时硝酸钾的溶解度为,其含义是时,水中最多溶解硝酸钾,溶液达到饱和状态。
A、选项说法没有指明温度,故选项错误。
B、时,硝酸钾固体溶于水形成饱和溶液,选项说法没有指明水的质量,故选项说法错误。
C、时,水中最多能溶解硝酸钾固体,故选项说法正确。
D、时,水中最多溶解硝酸钾,溶液达到饱和状态,形成饱和溶液,时,硝酸钾饱和溶液中含硝酸钾,故选项说法错误。
故选:。
溶解度是在一定温度下,某固体溶质在溶剂里达到饱和状态所溶解的溶质质量;溶解度定义中的四要素:一定温度、溶剂、溶液达到饱和状态、溶解的质量及单位克。
本题难度不大,理解溶解度的概念,熟记溶解度的四要素温度、溶剂、饱和状态、单位是克是正确解答本题的关键。
3.【答案】
【解析】
【分析】
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
【解答】
A、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,甲、乙试管中各盛有水,向其中一支中加入固体,另一支中加入固体,降温到时,乙中有晶体析出,所以乙中加入的固体是,故A错误;
B、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,的水中可以溶解的氯化钠,乙中有晶体析出,所以时,甲中溶液一定不饱和,乙中溶液一定饱和,故B错误;
C、硝酸钾的溶解度受温度变化影响较大,所以中含有少量杂质,可用冷却热饱和溶液的方法提纯,故C正确;
D、时,硝酸钾的溶解度大于氯化钠的溶解度,所以若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量小于乙中加入对应的溶质质量,故D错误。
故选C。
4.【答案】
【解析】解:根据题意可知,不饱和溶液饱和溶液析出晶体,而根据向原溶液投入克溶质晶体后,溶液中还剩下克固体溶质,说明原溶液在溶解溶质即达到饱和状态,说明这蒸发掉的水若溶解溶质也即达到饱和状态,即每克水中最多溶解溶质,则水中最多溶解溶质,
故选:。
固体的溶解度是指在一定的温度下,某固体物质在溶剂中达到饱和状态时所溶解的质量。
本题难度较大,主要考查了对固体溶解度概念的理解及其应用。
5.【答案】
【解析】解:设则时其溶解度为,,;
故选:。
固体溶解度是指:在一定温度下,某固体物质在克溶剂里达到饱和状态所溶解的质量;固体的溶解度由四个要点:一定温度、溶剂、达到饱和状态、溶解的溶质的质量;根据溶质和溶液的质量比,求溶解度。
本考点考查了固体物质的溶解度,溶解度的概念有四个要点:指明温度;克溶剂;达到饱和状态;质量即单位是克。本考点是中考的一个重要考点,一定要加强记忆,理解应用。
6.【答案】
【解析】解:冷却硝酸钾和氯化钠的热饱和溶液,析出的晶体中几乎不含氯化钠,是因为氯化钠的溶解度受温度变化影响很小,几乎不随温度的降低而降低,故几乎不析出氯化钠晶体;
故选:。
根据课本知识可知,不同物质的溶解度受温度变化影响不同,氯化钠的溶解度受温度变化影响不大,在冷却热饱和溶液时不容易析出晶体.
硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度随温度变化比较小,熟石灰的溶解度随温度的升高而降低.
7.【答案】
【解析】解:、比较溶解度大小须确定温度,温度大于时,甲物质的溶解度大于乙物质的溶解度,故错误;
B、时,甲物质和乙物质的溶解度相同,正确;
C、甲乙的溶解度均随温度的降低而减小,所以将时甲、乙两物质的饱和溶液降温到时都会析出晶体,正确;
D、甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯甲,正确;
故选:。
A、比较溶解度大小须确定温度;
B、溶解度曲线的交点表示该温度下两物质的溶解度相等;
C、甲乙的溶解度均随温度的降低而减小,据此分析解答;
D、据甲乙的溶解度随温度变化情况分析提纯的方法.
解答本题的关键是知道溶解度曲线表示的意义,交点表示的意义,物质从溶液中结晶析出的方法等知识,考查了学生分析、解决问题的能力.
8.【答案】
【解析】解:、溶质质量不会影响气体物质的溶解度,故A符合题意;
B、温度影响气体物质的溶解度,温度越高,气体溶解度越小,故B不合题意;
C、溶质的种类影响气体物质的溶解度,故C不合题意;
D、气压影响气体物质的溶解度,压强越大,气体溶解度越大,故D不合题意。
故选:。
根据已有的知识进行分析解答,影响气体溶解度的因素是温度、压强和气体本身的性质以及溶剂的性质。
本题考查的是影响气体物质的溶解度的因素,完成此题,可以依据已有的知识进行.
9.【答案】
【解析】略
10.【答案】
【解析】解:、时,往硝酸钾溶液中加入硝酸钾晶体,充分搅拌后,尚有部分晶体未溶,搅拌后及加热前一定是饱和的,故A正确;
B、充分搅拌后,尚有部分晶体未溶,搅拌后及加热前一定是饱和的,故B不正确;
C、稍加热后,晶体全部溶解,溶液可能不饱和、可能饱和,故C不正确;
D、稍加热后,晶体全部溶解,溶液可能不饱和、可能饱和,故D不正确。
故选:。
饱和溶液:在一定温度下,一定量的溶剂里,不能继续溶解某溶质的溶液;不饱和溶液:在一定温度下,一定量的溶剂里,还能继续溶解某溶质的溶液.
判断溶液是否饱和不能让题意中的文字叙述迷惑你,一定要根据饱和溶液与不饱和溶液的概念分析作答.
11.【答案】
【解析】解:由表格中的数据分析知,第一组中的在时固体全部溶解,而第二、三、四组的固体,在时均溶解了,所以时,固体的溶解度是,
A、时,水中最多能溶解氯化钠,饱和溶液中含有,故说法错误;
B、用蒸发的方法减少溶剂,可以使不饱和溶液变成饱和溶液,故说法正确;
C、第二组所得溶液的溶质与溶剂的质量比为::,故说法正确;
D、第三组和第二组溶液都是饱和溶液,所以溶质质量分数相等,故说法正确;
故选:。
根据饱和溶液的定义可以判断时,固体的溶解度是,结合溶质质量分数的计算公式和溶液的组成进行分析解答即可。
在判断溶液是否饱和时一定要指明温度,因为溶解度与温度有关。
12.【答案】
【解析】解:、甲为该温度下的不饱和溶液,乙是蒸发一定量溶剂得到的,丙和丁是该温度下的饱和溶液,则四杯溶液中溶质质量分数最大的是丙和丁,故选项说法错误。
B、甲为该温度下的不饱和溶液,乙是蒸发一定量溶剂得到的,丙和丁是该温度下的饱和溶液,则四杯溶液中溶质质量分数最小的是甲,故选项说法正确。
C、甲为该温度下的不饱和溶液,乙是蒸发一定量溶剂得到的,丙和丁是该温度下的饱和溶液,则四杯溶液中溶质质量分数最小的是甲,故选项说法错误。
D、在整个过程中,温度不变,食盐的溶解度不变,故选项说法错误。
故选:。
根据恒温下模拟海水晒盐过程的示意图,乙可能是饱和溶液,也可能是不饱和溶液,丙和丁是该温度下的饱和溶液,进行分析判断。
本题难度不大,明确乙可能是饱和溶液、丙和丁是该温度下的饱和溶液是正确解答本题的关键。
13.【答案】
【解析】解:、时,甲、乙饱和溶液的质量不能确定,所以饱和溶液中的溶质质量也不能确定,故A错误;
B、时,乙物质的溶解度是,所以乙饱和溶液中溶质的质量为,故B正确;
C、时,甲物质的溶解度是,饱和溶液的溶质质量分数为:,所以甲物质不可以配制溶质质量分数为的溶液,故C错误;
D、时,乙物质的溶解度是,所以向乙饱和溶液中加入水,可得到溶质质量分数为的乙溶液,故D正确。
故答案为:,。
根据固体的溶解度曲线,可以查出某物质在一定温度下的溶解度,从而确定饱和溶液中溶质的质量;可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
14.【答案】 降温结晶
【解析】解:通过分析溶解度曲线可知,三种物质的溶解度随着温度升高而减小的是;
物质的溶解度受温度变化影响较大,物质的溶解度受温度变化影响较小,所以若物质中混有少量的物质,可用降温结晶方法提纯;
时,物质的溶解度是,把物质加入到水中充分搅拌、静置,可以全部溶解,形成的溶液质量为;
时,将等质量和的饱和溶液降到时,物质的溶解度受温度变化影响较大,物质的溶解度受温度变化影响较小,所以析出晶体的质量关系正确的是,故选:。
故答案为:;
降温结晶;
;
。
根据固体的溶解度曲线,可以查出某物质在一定温度下的溶解度,从而确定形成溶液的质量;可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小;可以判断物质的溶解度随温度变化的变化情况,从而判断提纯晶体的方法。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
15.【答案】小于 饱和 降温结晶的方法
【解析】解:观察溶解度曲线可知:时木糖醇的溶解度小于蔗糖的溶解度;
时木糖醇的溶解度是,即水中最多溶解的木糖醇,所以将木糖醇放入水中,最多溶解,所得的溶液为饱和溶液,溶质的质量分数是;木糖醇的溶解度随温度升高而减小,所以要得到木糖醇的晶体可用的蒸发溶剂的方法,还可用降温结晶的方法;
故答案为:小于;饱和;;降温结晶的方法.
据溶解度曲线可比较同一温度下物质的溶解度大小;
据 时木糖醇的溶解度分析解答,并据饱和溶液中溶质的质量分数的计算式解答;据木糖醇的溶解度随温度升高而减小分析解答.
本题既考查了学生对溶解度曲线意义的了解,又考查了对知识的应用,分析解决问题的能力,能较好培养学生对知识的掌握和应用.
第2页,共2页
第1页,共1页
一、单选题
在时,克食盐溶解在克水中恰好达到饱和,以下关于食盐的溶解度说法正确的是
A. 食盐的溶解度是克 B. 食盐的溶解度是克
C. 时食盐的溶解度是克 D. 时食盐的溶解度是
已知时硝酸钾的溶解度为。下列关于对它的理解正确的是
A. 水中溶解了硝酸钾固体达到饱和
B. 时,硝酸钾固体溶于水形成饱和溶液
C. 时,水中最多能溶解硝酸钾固体
D. 时, 硝酸钾饱和溶液中含 硝酸钾
甲、乙试管中各盛有水,向其中一支中加入固体,另一支中加入固体,按图进行实验和的溶解度曲线如图,下列说法正确的是
A. 甲中加入的固体是
B. 时,甲中溶液可能饱和,乙中溶液一定饱和
C. 中含有少量杂质,可用冷却热饱和溶液的方法提纯
D. 时,若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
在一定温度下,某未饱和溶液蒸发掉克水部分后,析出克晶体不含结晶水;向原溶液投入克溶质晶体后,溶液中还剩下克固体溶质,则此温度下该溶质的溶解度为
A. 克 B. 克 C. 克 D. 克
时,某物质的饱和溶液中,溶质和溶液的质量比为:,则时其溶解度为
A. 克 B. C. 克 D.
在较高温度下,某溶液所含的硝酸钾和氯化钠都已接近饱和,当其冷却至室温时,析出的晶体经检验几乎不含氯化钠,这是因为
A. 氯化钠的溶解度比硝酸钾的大 B. 氯化钠的溶解度比硝酸钾的小
C. 氯化钠的溶解度在室温下更大 D. 氯化钠的溶解度受温度的影响小
根据如图的溶解度曲线,判断下列说法中不正确的是
A. 甲物质的溶解度小于乙物质的溶解度
B. 时,甲物质和乙物质的溶解度相同
C. 将时甲、乙两物质的饱和溶液降温到时都会析出晶体
D. 当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯甲
下列因素中不会影响气体物质溶解度的是
A. 溶剂的量 B. 温度 C. 溶质的种类 D. 压强
甲、乙两物质的溶解度与温度的关系如图所示,下列说法正确的是
A. 时乙的溶解度为
B. 乙的溶解度随温度的升高而降低
C. 时甲的溶解度小于乙的溶解度
D. 点表示时两物质的溶解度相等
时,往克硝酸钾溶液中加入克硝酸钾晶体,充分搅拌后,尚有部分晶体未溶解.稍加热后,晶体全部溶解.下列说法正确的是
A. 搅拌后加热前一定是饱和溶液 B. 搅拌后加热前一定是不饱和溶液
C. 加热后一定是饱和溶液 D. 加热后一定是不饱和溶液
时,四个实验小组分别取不同质量的,逐渐加入到各盛有水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余的质量。记录数据如表:
实验小组 第一组 第二组 第三组 第四组
水的质量
所取的质量
剩余的质量
下列说法错误的是
A. 时,饱和溶液中含有
B. 用蒸发的方法可以使不饱和溶液变成饱和溶液
C. 第二组所得溶液的溶质与溶剂的质量比为:
D. 第三组和第二组溶液溶质质量分数相等
如图是恒温下模拟海水晒盐过程的示意图,下列说法正确的是
A. 四杯溶液中溶质质量分数最大的是丁
B. 四杯溶液中溶质质量分数最小的是甲
C. 四杯溶液中溶质质量分数最小的是乙
D. 在整个过程中,食盐的溶解度发生了变化
二、填空题
甲、乙两种固体物质均不含结晶水的溶解度曲线如图所示。下列说法正确的是 ______
A.时,甲、乙饱和溶液的溶质质量相等
B.时,乙饱和溶液中溶质的质量为
C.时,甲物质可以配制溶质质量分数为的溶液
D.时,向乙饱和溶液中加入 ______水,可得到溶质质量分数为的乙溶液
如图是、、三种物质的溶解度曲线,请回答下列问题:
三种物质的溶解度随着温度升高而减小的是 ______。
若物质中混有少量的物质,可用 ______方法提纯。
时,把物质加入到水中充分搅拌、静置,形成的溶液质量为 ______。
时,将等质量和的饱和溶液降到时,析出晶体的质量关系正确的是 ______填字母序号。
A.
B.
C.
D.不能确定
同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.木糖醇和蔗糖的溶解度曲线如图,据图回答
时,木糖醇的溶解度______蔗糖的溶解度.选填“大于”、“小于”或“等于”
时,向克水中加入克木糖醇,充分溶解后,所得的溶液是______溶液选填“饱和”或“不饱和”,该溶液的溶质质量分数为______要得到木糖醇的晶体可用的蒸发溶剂的方法,还可用______.
答案和解析
1.【答案】
【解析】解:、克是溶剂的质量,故A错误;
B、克是饱和溶液中溶质与溶剂的质量之和,故B错误;
C、在时,克食盐溶解在克水中恰好达到饱和,所以时食盐溶解度为克,故C正确;
D、溶解度的单位是克,缺少单位,故D错误;
故选:。
根据溶解度的四要素:一定温度、溶剂、饱和状态、溶解的质量进行分析。
解答本题关键是要熟悉溶解度的四要素:一定温度、溶剂、饱和状态、溶解的质量。
2.【答案】
【解析】解:根据溶解度的概念,时硝酸钾的溶解度为,其含义是时,水中最多溶解硝酸钾,溶液达到饱和状态。
A、选项说法没有指明温度,故选项错误。
B、时,硝酸钾固体溶于水形成饱和溶液,选项说法没有指明水的质量,故选项说法错误。
C、时,水中最多能溶解硝酸钾固体,故选项说法正确。
D、时,水中最多溶解硝酸钾,溶液达到饱和状态,形成饱和溶液,时,硝酸钾饱和溶液中含硝酸钾,故选项说法错误。
故选:。
溶解度是在一定温度下,某固体溶质在溶剂里达到饱和状态所溶解的溶质质量;溶解度定义中的四要素:一定温度、溶剂、溶液达到饱和状态、溶解的质量及单位克。
本题难度不大,理解溶解度的概念,熟记溶解度的四要素温度、溶剂、饱和状态、单位是克是正确解答本题的关键。
3.【答案】
【解析】
【分析】
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
【解答】
A、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,甲、乙试管中各盛有水,向其中一支中加入固体,另一支中加入固体,降温到时,乙中有晶体析出,所以乙中加入的固体是,故A错误;
B、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,的水中可以溶解的氯化钠,乙中有晶体析出,所以时,甲中溶液一定不饱和,乙中溶液一定饱和,故B错误;
C、硝酸钾的溶解度受温度变化影响较大,所以中含有少量杂质,可用冷却热饱和溶液的方法提纯,故C正确;
D、时,硝酸钾的溶解度大于氯化钠的溶解度,所以若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量小于乙中加入对应的溶质质量,故D错误。
故选C。
4.【答案】
【解析】解:根据题意可知,不饱和溶液饱和溶液析出晶体,而根据向原溶液投入克溶质晶体后,溶液中还剩下克固体溶质,说明原溶液在溶解溶质即达到饱和状态,说明这蒸发掉的水若溶解溶质也即达到饱和状态,即每克水中最多溶解溶质,则水中最多溶解溶质,
故选:。
固体的溶解度是指在一定的温度下,某固体物质在溶剂中达到饱和状态时所溶解的质量。
本题难度较大,主要考查了对固体溶解度概念的理解及其应用。
5.【答案】
【解析】解:设则时其溶解度为,,;
故选:。
固体溶解度是指:在一定温度下,某固体物质在克溶剂里达到饱和状态所溶解的质量;固体的溶解度由四个要点:一定温度、溶剂、达到饱和状态、溶解的溶质的质量;根据溶质和溶液的质量比,求溶解度。
本考点考查了固体物质的溶解度,溶解度的概念有四个要点:指明温度;克溶剂;达到饱和状态;质量即单位是克。本考点是中考的一个重要考点,一定要加强记忆,理解应用。
6.【答案】
【解析】解:冷却硝酸钾和氯化钠的热饱和溶液,析出的晶体中几乎不含氯化钠,是因为氯化钠的溶解度受温度变化影响很小,几乎不随温度的降低而降低,故几乎不析出氯化钠晶体;
故选:。
根据课本知识可知,不同物质的溶解度受温度变化影响不同,氯化钠的溶解度受温度变化影响不大,在冷却热饱和溶液时不容易析出晶体.
硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度随温度变化比较小,熟石灰的溶解度随温度的升高而降低.
7.【答案】
【解析】解:、比较溶解度大小须确定温度,温度大于时,甲物质的溶解度大于乙物质的溶解度,故错误;
B、时,甲物质和乙物质的溶解度相同,正确;
C、甲乙的溶解度均随温度的降低而减小,所以将时甲、乙两物质的饱和溶液降温到时都会析出晶体,正确;
D、甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯甲,正确;
故选:。
A、比较溶解度大小须确定温度;
B、溶解度曲线的交点表示该温度下两物质的溶解度相等;
C、甲乙的溶解度均随温度的降低而减小,据此分析解答;
D、据甲乙的溶解度随温度变化情况分析提纯的方法.
解答本题的关键是知道溶解度曲线表示的意义,交点表示的意义,物质从溶液中结晶析出的方法等知识,考查了学生分析、解决问题的能力.
8.【答案】
【解析】解:、溶质质量不会影响气体物质的溶解度,故A符合题意;
B、温度影响气体物质的溶解度,温度越高,气体溶解度越小,故B不合题意;
C、溶质的种类影响气体物质的溶解度,故C不合题意;
D、气压影响气体物质的溶解度,压强越大,气体溶解度越大,故D不合题意。
故选:。
根据已有的知识进行分析解答,影响气体溶解度的因素是温度、压强和气体本身的性质以及溶剂的性质。
本题考查的是影响气体物质的溶解度的因素,完成此题,可以依据已有的知识进行.
9.【答案】
【解析】略
10.【答案】
【解析】解:、时,往硝酸钾溶液中加入硝酸钾晶体,充分搅拌后,尚有部分晶体未溶,搅拌后及加热前一定是饱和的,故A正确;
B、充分搅拌后,尚有部分晶体未溶,搅拌后及加热前一定是饱和的,故B不正确;
C、稍加热后,晶体全部溶解,溶液可能不饱和、可能饱和,故C不正确;
D、稍加热后,晶体全部溶解,溶液可能不饱和、可能饱和,故D不正确。
故选:。
饱和溶液:在一定温度下,一定量的溶剂里,不能继续溶解某溶质的溶液;不饱和溶液:在一定温度下,一定量的溶剂里,还能继续溶解某溶质的溶液.
判断溶液是否饱和不能让题意中的文字叙述迷惑你,一定要根据饱和溶液与不饱和溶液的概念分析作答.
11.【答案】
【解析】解:由表格中的数据分析知,第一组中的在时固体全部溶解,而第二、三、四组的固体,在时均溶解了,所以时,固体的溶解度是,
A、时,水中最多能溶解氯化钠,饱和溶液中含有,故说法错误;
B、用蒸发的方法减少溶剂,可以使不饱和溶液变成饱和溶液,故说法正确;
C、第二组所得溶液的溶质与溶剂的质量比为::,故说法正确;
D、第三组和第二组溶液都是饱和溶液,所以溶质质量分数相等,故说法正确;
故选:。
根据饱和溶液的定义可以判断时,固体的溶解度是,结合溶质质量分数的计算公式和溶液的组成进行分析解答即可。
在判断溶液是否饱和时一定要指明温度,因为溶解度与温度有关。
12.【答案】
【解析】解:、甲为该温度下的不饱和溶液,乙是蒸发一定量溶剂得到的,丙和丁是该温度下的饱和溶液,则四杯溶液中溶质质量分数最大的是丙和丁,故选项说法错误。
B、甲为该温度下的不饱和溶液,乙是蒸发一定量溶剂得到的,丙和丁是该温度下的饱和溶液,则四杯溶液中溶质质量分数最小的是甲,故选项说法正确。
C、甲为该温度下的不饱和溶液,乙是蒸发一定量溶剂得到的,丙和丁是该温度下的饱和溶液,则四杯溶液中溶质质量分数最小的是甲,故选项说法错误。
D、在整个过程中,温度不变,食盐的溶解度不变,故选项说法错误。
故选:。
根据恒温下模拟海水晒盐过程的示意图,乙可能是饱和溶液,也可能是不饱和溶液,丙和丁是该温度下的饱和溶液,进行分析判断。
本题难度不大,明确乙可能是饱和溶液、丙和丁是该温度下的饱和溶液是正确解答本题的关键。
13.【答案】
【解析】解:、时,甲、乙饱和溶液的质量不能确定,所以饱和溶液中的溶质质量也不能确定,故A错误;
B、时,乙物质的溶解度是,所以乙饱和溶液中溶质的质量为,故B正确;
C、时,甲物质的溶解度是,饱和溶液的溶质质量分数为:,所以甲物质不可以配制溶质质量分数为的溶液,故C错误;
D、时,乙物质的溶解度是,所以向乙饱和溶液中加入水,可得到溶质质量分数为的乙溶液,故D正确。
故答案为:,。
根据固体的溶解度曲线,可以查出某物质在一定温度下的溶解度,从而确定饱和溶液中溶质的质量;可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
14.【答案】 降温结晶
【解析】解:通过分析溶解度曲线可知,三种物质的溶解度随着温度升高而减小的是;
物质的溶解度受温度变化影响较大,物质的溶解度受温度变化影响较小,所以若物质中混有少量的物质,可用降温结晶方法提纯;
时,物质的溶解度是,把物质加入到水中充分搅拌、静置,可以全部溶解,形成的溶液质量为;
时,将等质量和的饱和溶液降到时,物质的溶解度受温度变化影响较大,物质的溶解度受温度变化影响较小,所以析出晶体的质量关系正确的是,故选:。
故答案为:;
降温结晶;
;
。
根据固体的溶解度曲线,可以查出某物质在一定温度下的溶解度,从而确定形成溶液的质量;可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小;可以判断物质的溶解度随温度变化的变化情况,从而判断提纯晶体的方法。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
15.【答案】小于 饱和 降温结晶的方法
【解析】解:观察溶解度曲线可知:时木糖醇的溶解度小于蔗糖的溶解度;
时木糖醇的溶解度是,即水中最多溶解的木糖醇,所以将木糖醇放入水中,最多溶解,所得的溶液为饱和溶液,溶质的质量分数是;木糖醇的溶解度随温度升高而减小,所以要得到木糖醇的晶体可用的蒸发溶剂的方法,还可用降温结晶的方法;
故答案为:小于;饱和;;降温结晶的方法.
据溶解度曲线可比较同一温度下物质的溶解度大小;
据 时木糖醇的溶解度分析解答,并据饱和溶液中溶质的质量分数的计算式解答;据木糖醇的溶解度随温度升高而减小分析解答.
本题既考查了学生对溶解度曲线意义的了解,又考查了对知识的应用,分析解决问题的能力,能较好培养学生对知识的掌握和应用.
第2页,共2页
第1页,共1页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
