5.2化学反应的表示——2021-2022学年九年级化学鲁教版上册(44张PPT)
文档属性
| 名称 | 5.2化学反应的表示——2021-2022学年九年级化学鲁教版上册(44张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-21 00:00:00 | ||
图片预览








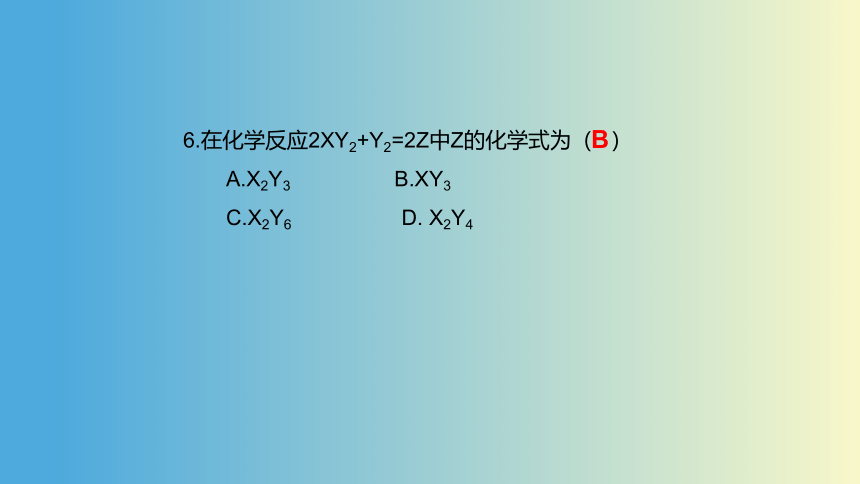
文档简介
(共44张PPT)
5.2.1 化学反应的表示
九年级上册
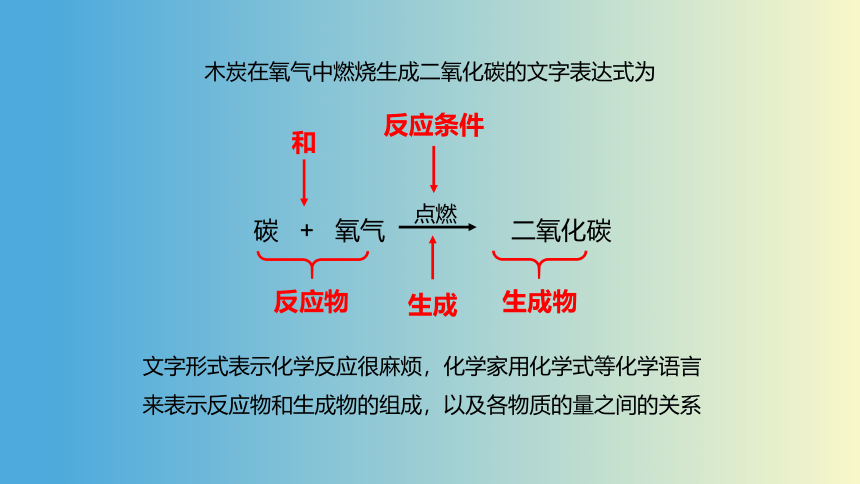
木炭在氧气中燃烧生成二氧化碳的文字表达式为
碳 + 氧气 二氧化碳
点燃
和
反应条件
生成
反应物
生成物
文字形式表示化学反应很麻烦,化学家用化学式等化学语言来表示反应物和生成物的组成,以及各物质的量之间的关系
一、化学方程式
1.定义
用化学式来表示化学反应的式子
2.意义
(1)表示化学反应中的反应物和生成物
(2)表示该化学反应进行的条件
(3)表示各物质之间的质量关系
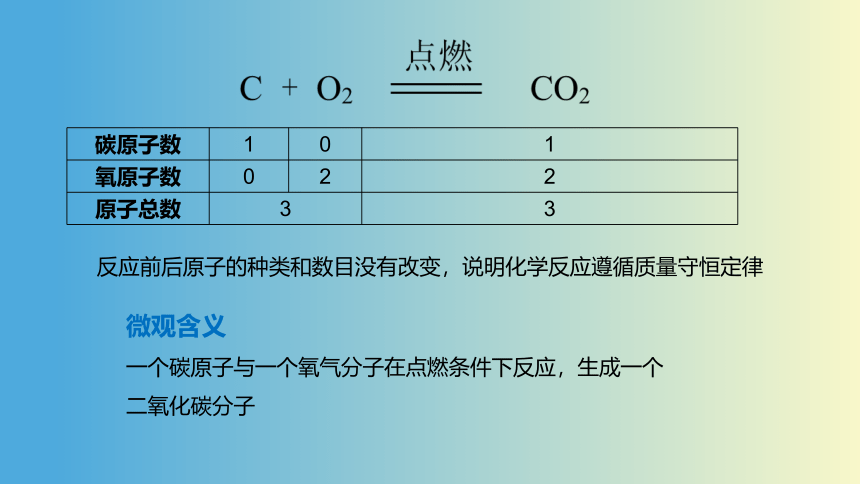
C + O2 CO2
点燃
微观含义
一个碳原子与一个氧气分子在点燃条件下反应,生成一个二氧化碳分子
碳原子数 1 0 1
氧原子数 0 2 2
原子总数 3 3
反应前后原子的种类和数目没有改变,说明化学反应遵循质量守恒定律
相对原子质量 12 : (2×16) : (12+2×16)
质量比 12 : 32 : 44
宏观含义
每12份质量的碳与32份质量的氧气完全反应,生成44份质量的二氧化碳
12+32=44,说明化学反应遵循质量守恒定律
C + O2 CO2
点燃
3.化学方程式的读法:
(1)宏观方面:碳和氧气在点燃条件下反应生成二氧化碳。
(2)微观方面:1个碳原子和1个氧气分子反应生成1个二氧化碳分子。
(3)量的方面:每12份质量的碳和32份质量的氧气完全反应生成44份质量的二氧化碳。
1.根据化学方程式4P+5O2 2P2O5 ,回答下列问题:
这个化学反应的反应物是什么?
反应条件是什么?
反应的生成物是什么?
参加反应的各物质的质量比是多少?
参加反应的各粒子的相对数量?
这个化学方程式有几种读法?
根据下面三个化学方程式,回答上述问题
S+O2 SO2
CuO+H2 Cu+H2O
Fe+CuSO4 = Cu+FeSO4
点燃
点燃
2.煤的汽化是提高煤的利用率、减少环境污染的有效措施之一。煤的汽化过程中发生了化学反应C+H2O==CO+X。请你写出X的化学式 。
H2
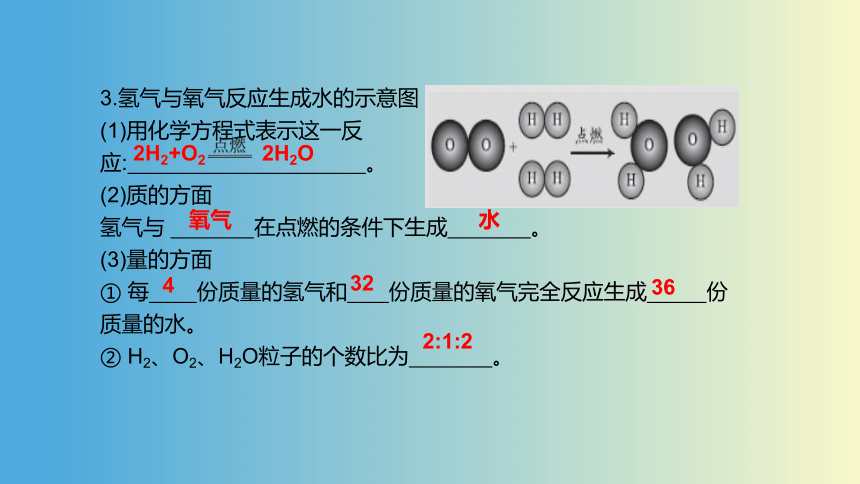
3.氢气与氧气反应生成水的示意图
(1)用化学方程式表示这一反
应: 。
(2)质的方面
氢气与 在点燃的条件下生成 。
(3)量的方面
① 每 份质量的氢气和 份质量的氧气完全反应生成 份质量的水。
② H2、O2、H2O粒子的个数比为 。
2H2+O2 2H2O
氧气
水
4
32
36
2:1:2
4.将25 g氯酸钾和1g二氧化锰的混合物加热至完全分解,得到残余固体质量为14 g,则产生氧气____g
12
5.已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。
C、H
O
6.在化学反应2XY2+Y2=2Z中Z的化学式为( )
A.X2Y3 B.XY3
C.X2Y6 D. X2Y4
B
再 见
5.2.2 化学反应的表示
九年级上册
讨论探究
判断下列化学方程式书写是否正确
1.
2. KClO3KCl + O3↑
都不正确。磷和氧气在燃烧条件下反应,应当生成P2O5,氯酸钾在加热时,应该分解生成氧气。以上两个反应违背了客观事实。
讨论探究
判断下列化学方程式书写是否正确
不正确。反应前后原子的数目不相等,违背了质量守恒定律。
根据以上例子,请说出你认为在书写化学方程式时,应当注意的各种原则
一、化学方程式的书写原则
1.以客观事实为基础
不能臆造事实上不存在的物质和化学反应。不能更改实际物质的化学式
2.遵守质量守恒定律
等号两边各种原子的种类和数目必须相等。
氢原子数 2 0 2
氧原子数 0 2 1
原子总数 4 3
在保证反应物与生成物化学式正确的前提下,我们怎么做才能使等号前后原子个数相等,得到正确的化学方程式呢?
H2+ O2 H2O
×
这样可以吗?为什么?
H2+O2 H2O+O
×
H2+O2 H2O2
×
这样可以吗?为什么?
这样可以吗?为什么?
H2+ O H2O
×
H2+ O2 H2O
×
2
2H2+ O2 2H2O
点燃
√
1.化学计量数
化学式前面的数字叫化学计量数。
2.化学方程式的配平
通过给化学式加上适当的化学计量数,使该化学方程式等号两边的原子种类和数目都相等,这个过程称为化学方程式的配平。
二、化学方程式的配平方法
3.化学方程式的配平方法
(1)最小公倍数法
选择左右只出现一次且个数最多的原子作起点,求其最小公倍数,再以最小公倍数分别除以该原子在不同化学式中的个数作为该化学式的化学计量数,并由此推出其它化学计量数。
P+O2 P2O5
P + 5O2 2P2O5
4P + 5O2 2P2O5
点燃
配平下列化学方程式
(1) C + CO2 CO
(2) Al + O2 Al2O3
(3) CuO + C Cu + CO2
(4)Fe+O2 Fe3O4
点燃
高温
高温
(2)奇数配偶法
当某元素原子出现次数最多,且原子总数在化学式左右两边一奇一偶时,常在奇数个原子对应的化学式前配一个2,再由此推出其它化学计量数
FeS2+ O2 Fe2O3 + SO2
2
4
8
11
点燃
配平下列方程式
H2S + O2 —— SO2 + H2O
KClO3 KCl + O2
MnO2
配平下列化学方程式
C2H5OH+ O2——CO2+ H2O
(3)观察法
①原子团反应前后不变的,将原子团当成一个整体来考虑配平
CuSO4
+
NaOH
Cu(OH)2
+
Na2SO4
2
②反应前后某种原子出现多次的可先观察反应特征再配平
Fe2O3 + CO Fe + CO2
3
3
2
高温
反应前的CO变成反应后的CO2,即每个CO可得到1个O原子,而Fe2O3中有3个O氧原子,因此CO前应配3,其他再相应配平
再 见
5.2.3 化学反应的表示
九年级上册
三、化学方程式的书写步骤
1.写
根据实验事实,左边写出反应物化学式,右边写出生成物的化学式,用短线连接反应物与生成物。反应物或生成物不止一种的,彼此间用“+”号联结。
P + O2 —— P2O5
2.配
配平化学方程式的目的是使“——”两边的原子种类与数目相等,使之遵守质量守恒定律。配平化学方程式后,必须要进行复查。
4P + 5O2 —— 2P2O5
4
2×2=4
2×5=10
5×2=10
左边 右边
磷原子数
氧原子数
3.注
①在短线上注明反应条件
②反应条件常见的有点燃、加热(常用 “△”表示)、高温、催化剂等
③在生成物化学式的右边注明物质状态,气体用“↑”符号,沉淀物质用“↓”符号表示。
4.查
再复查一次配平、书写、条件和物质状态是否有误,无误后把短线改成等号。
5.化学方程式书写注意事项
(1)配平化学方程式时,只能在化学式前面添上适当的化学计量数,不能改动化学式中右下角的数字。
×
√
(2)化学方程式等号两边不能有相同的化学式
(3)化学计量数1可以省略不写,各化学式前的计量数必须是最简整数比
(4)如生成物中有气体,在气体的化学式右边要注“↑”号
反应物和生成物中都有气体,气体生成物就不需注“↑”号
(5)在溶液中进行的反应,如果生成物中有固体,在固体生成物的化学式右边要注“↓”号
在溶液中进行的反应,如果反应物和生成物中都有固体,固体生成物不需注“↓”号
(6)原子团一般作为整体考虑。
2NaOH+H2SO4===Na2SO4+2H2O
Na2CO3+Ca(OH)2===CaCO3+2NaOH
1.指出下列方程式中哪些需要标 符号,并标注出 的位置
S+O2==== SO2
2KMnO4 === K2MnO4 + MnO2 + O2
C+O2==== CO2
2KClO3 === 3O2 + 2KCl
点燃
点燃
MnO2
4P+O2==== 2P2O5
Fe+CuSO4 == FeSO4 + Cu
CuSO4+2NaOH==Na2SO4+Cu(OH)2
点燃
2.指出下列方程式中哪些需要标 符号,并标注出 的位置
3.判断下列化学方程式是否正确
2CO + O2=== 2CO2
点燃
H2 + CuO === Cu + H2O
CO2+Ca(OH)2==== CaCO3 + H2O
再 见
5.2.1 化学反应的表示
九年级上册
木炭在氧气中燃烧生成二氧化碳的文字表达式为
碳 + 氧气 二氧化碳
点燃
和
反应条件
生成
反应物
生成物
文字形式表示化学反应很麻烦,化学家用化学式等化学语言来表示反应物和生成物的组成,以及各物质的量之间的关系
一、化学方程式
1.定义
用化学式来表示化学反应的式子
2.意义
(1)表示化学反应中的反应物和生成物
(2)表示该化学反应进行的条件
(3)表示各物质之间的质量关系
C + O2 CO2
点燃
微观含义
一个碳原子与一个氧气分子在点燃条件下反应,生成一个二氧化碳分子
碳原子数 1 0 1
氧原子数 0 2 2
原子总数 3 3
反应前后原子的种类和数目没有改变,说明化学反应遵循质量守恒定律
相对原子质量 12 : (2×16) : (12+2×16)
质量比 12 : 32 : 44
宏观含义
每12份质量的碳与32份质量的氧气完全反应,生成44份质量的二氧化碳
12+32=44,说明化学反应遵循质量守恒定律
C + O2 CO2
点燃
3.化学方程式的读法:
(1)宏观方面:碳和氧气在点燃条件下反应生成二氧化碳。
(2)微观方面:1个碳原子和1个氧气分子反应生成1个二氧化碳分子。
(3)量的方面:每12份质量的碳和32份质量的氧气完全反应生成44份质量的二氧化碳。
1.根据化学方程式4P+5O2 2P2O5 ,回答下列问题:
这个化学反应的反应物是什么?
反应条件是什么?
反应的生成物是什么?
参加反应的各物质的质量比是多少?
参加反应的各粒子的相对数量?
这个化学方程式有几种读法?
根据下面三个化学方程式,回答上述问题
S+O2 SO2
CuO+H2 Cu+H2O
Fe+CuSO4 = Cu+FeSO4
点燃
点燃
2.煤的汽化是提高煤的利用率、减少环境污染的有效措施之一。煤的汽化过程中发生了化学反应C+H2O==CO+X。请你写出X的化学式 。
H2
3.氢气与氧气反应生成水的示意图
(1)用化学方程式表示这一反
应: 。
(2)质的方面
氢气与 在点燃的条件下生成 。
(3)量的方面
① 每 份质量的氢气和 份质量的氧气完全反应生成 份质量的水。
② H2、O2、H2O粒子的个数比为 。
2H2+O2 2H2O
氧气
水
4
32
36
2:1:2
4.将25 g氯酸钾和1g二氧化锰的混合物加热至完全分解,得到残余固体质量为14 g,则产生氧气____g
12
5.已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。
C、H
O
6.在化学反应2XY2+Y2=2Z中Z的化学式为( )
A.X2Y3 B.XY3
C.X2Y6 D. X2Y4
B
再 见
5.2.2 化学反应的表示
九年级上册
讨论探究
判断下列化学方程式书写是否正确
1.
2. KClO3KCl + O3↑
都不正确。磷和氧气在燃烧条件下反应,应当生成P2O5,氯酸钾在加热时,应该分解生成氧气。以上两个反应违背了客观事实。
讨论探究
判断下列化学方程式书写是否正确
不正确。反应前后原子的数目不相等,违背了质量守恒定律。
根据以上例子,请说出你认为在书写化学方程式时,应当注意的各种原则
一、化学方程式的书写原则
1.以客观事实为基础
不能臆造事实上不存在的物质和化学反应。不能更改实际物质的化学式
2.遵守质量守恒定律
等号两边各种原子的种类和数目必须相等。
氢原子数 2 0 2
氧原子数 0 2 1
原子总数 4 3
在保证反应物与生成物化学式正确的前提下,我们怎么做才能使等号前后原子个数相等,得到正确的化学方程式呢?
H2+ O2 H2O
×
这样可以吗?为什么?
H2+O2 H2O+O
×
H2+O2 H2O2
×
这样可以吗?为什么?
这样可以吗?为什么?
H2+ O H2O
×
H2+ O2 H2O
×
2
2H2+ O2 2H2O
点燃
√
1.化学计量数
化学式前面的数字叫化学计量数。
2.化学方程式的配平
通过给化学式加上适当的化学计量数,使该化学方程式等号两边的原子种类和数目都相等,这个过程称为化学方程式的配平。
二、化学方程式的配平方法
3.化学方程式的配平方法
(1)最小公倍数法
选择左右只出现一次且个数最多的原子作起点,求其最小公倍数,再以最小公倍数分别除以该原子在不同化学式中的个数作为该化学式的化学计量数,并由此推出其它化学计量数。
P+O2 P2O5
P + 5O2 2P2O5
4P + 5O2 2P2O5
点燃
配平下列化学方程式
(1) C + CO2 CO
(2) Al + O2 Al2O3
(3) CuO + C Cu + CO2
(4)Fe+O2 Fe3O4
点燃
高温
高温
(2)奇数配偶法
当某元素原子出现次数最多,且原子总数在化学式左右两边一奇一偶时,常在奇数个原子对应的化学式前配一个2,再由此推出其它化学计量数
FeS2+ O2 Fe2O3 + SO2
2
4
8
11
点燃
配平下列方程式
H2S + O2 —— SO2 + H2O
KClO3 KCl + O2
MnO2
配平下列化学方程式
C2H5OH+ O2——CO2+ H2O
(3)观察法
①原子团反应前后不变的,将原子团当成一个整体来考虑配平
CuSO4
+
NaOH
Cu(OH)2
+
Na2SO4
2
②反应前后某种原子出现多次的可先观察反应特征再配平
Fe2O3 + CO Fe + CO2
3
3
2
高温
反应前的CO变成反应后的CO2,即每个CO可得到1个O原子,而Fe2O3中有3个O氧原子,因此CO前应配3,其他再相应配平
再 见
5.2.3 化学反应的表示
九年级上册
三、化学方程式的书写步骤
1.写
根据实验事实,左边写出反应物化学式,右边写出生成物的化学式,用短线连接反应物与生成物。反应物或生成物不止一种的,彼此间用“+”号联结。
P + O2 —— P2O5
2.配
配平化学方程式的目的是使“——”两边的原子种类与数目相等,使之遵守质量守恒定律。配平化学方程式后,必须要进行复查。
4P + 5O2 —— 2P2O5
4
2×2=4
2×5=10
5×2=10
左边 右边
磷原子数
氧原子数
3.注
①在短线上注明反应条件
②反应条件常见的有点燃、加热(常用 “△”表示)、高温、催化剂等
③在生成物化学式的右边注明物质状态,气体用“↑”符号,沉淀物质用“↓”符号表示。
4.查
再复查一次配平、书写、条件和物质状态是否有误,无误后把短线改成等号。
5.化学方程式书写注意事项
(1)配平化学方程式时,只能在化学式前面添上适当的化学计量数,不能改动化学式中右下角的数字。
×
√
(2)化学方程式等号两边不能有相同的化学式
(3)化学计量数1可以省略不写,各化学式前的计量数必须是最简整数比
(4)如生成物中有气体,在气体的化学式右边要注“↑”号
反应物和生成物中都有气体,气体生成物就不需注“↑”号
(5)在溶液中进行的反应,如果生成物中有固体,在固体生成物的化学式右边要注“↓”号
在溶液中进行的反应,如果反应物和生成物中都有固体,固体生成物不需注“↓”号
(6)原子团一般作为整体考虑。
2NaOH+H2SO4===Na2SO4+2H2O
Na2CO3+Ca(OH)2===CaCO3+2NaOH
1.指出下列方程式中哪些需要标 符号,并标注出 的位置
S+O2==== SO2
2KMnO4 === K2MnO4 + MnO2 + O2
C+O2==== CO2
2KClO3 === 3O2 + 2KCl
点燃
点燃
MnO2
4P+O2==== 2P2O5
Fe+CuSO4 == FeSO4 + Cu
CuSO4+2NaOH==Na2SO4+Cu(OH)2
点燃
2.指出下列方程式中哪些需要标 符号,并标注出 的位置
3.判断下列化学方程式是否正确
2CO + O2=== 2CO2
点燃
H2 + CuO === Cu + H2O
CO2+Ca(OH)2==== CaCO3 + H2O
再 见
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
