第二章 物质转化和材料利用 单元测试卷(含解析)
文档属性
| 名称 | 第二章 物质转化和材料利用 单元测试卷(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 254.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-10-23 00:00:00 | ||
图片预览



文档简介
物质转化和材料利用 单元测试卷
一、选择题
1.超市里买来的饼干、坚果类食品使用铝箔来包装,铝能制作成铝箔,这是利用了铝的( )
A.导电性 B.延展性 C.导热性 D.熔点高
2.我县荣获2019年全省生活垃圾分类工作优秀县,为推进全省垃圾治理作出新贡献。下列生活垃圾应投入可回收垃圾桶的是( )
A.废旧电池 B.过期药品 C.剩饭剩菜 D.铝制易拉罐
3.2020年11月13日开始,龙泉市开展了为期一周的垃圾分类“进商户”专题宣传活动。某商场放着如图所示的三只垃圾桶,下列垃圾应投入可回收垃圾桶的是( )
A.废电池 B.铝制易拉罐 C.剩饭 D.过期药品
4.合金在生活中的应用十分广泛,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是①C+2NiO2Ni+CO2↑;万米深海潜水器“奋斗者”号载人舱外壳材料采用的是钛合金,钛的生产过程中发生的反应之一为:②TiO2+2Cl2+2C = TiCl4+2CO,下列有关这两个反应,说法正确的是( )
A.两个反应都是置换反应 B.①是置换反应,②是复分解反应
C.只有①是置换反应 D.只有①是复分解反应
5.如图所示,U 型管内 a、b 液面相平,当挤压滴管的胶头,使试剂 X 进入锥形瓶内,一段时间后会观察到 a 液面高于 b 液面。则试剂 X、Y 的组合可能是( )
A.水、硝酸铵 B.水、烧碱
C.稀硫酸、铁粉 D.稀盐酸、小苏打
6.下列物质中不能通过金属与硫酸反应得到的是( )
A.FeSO4 B.Al2(SO4)3 C.Fe2(SO4)3 D.ZnSO4
7.化学与生活密切相关。下列生活小窍门正确的是( )
A.小苏打受热分解产生CO2,可用于制作面点
B.烧碱能中和酸,可用于治疗胃酸过多
C.烹调食物时,用工业用盐如亚硝酸钠替换食盐
D.可以用灼烧闻气味的方法区分真丝和纯棉线,有烧焦羽毛味的是纯棉线
8.化学与生活、生产、科技密不可分。下列叙述正确的是( )
A.合金、塑料、玻璃钢属于合成材料
B.用甲醛浸泡过的水产品,可放心食用
C.研制新材料、新能源替代传统能源,减少污染
D.化肥硝酸铵可与碱性物质混合使用,增大肥效
9.如图表示的是纯净物、单质、化合物、含氧化合物、氧化物概念之间的关系,若整个大圆代表纯净物,下列物质应放到C区域的是( )
①澄清的石灰水 ②冰水混合物 ③水银 ④五氧化二磷 ⑤液氧 ⑥高锰酸钾 ⑦氨气
A.②③⑤ B.④⑦ C.②④⑥ D.②④
10.下列关于酸、碱、盐元素组成的说法,正确的是 ( )
A.酸、碱一定含有氢,盐一定不含氢 B.酸、碱、盐可能都不含金属元素
C.碱、盐可能含氧,酸一定含氧 D.盐、碱一定含有金属元素
11.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物—酸—碱—盐”顺序排列的是( )
A.HClO;HCl;Mg(OH)2;MgCl2
B.CO2;H2CO3;CaCO3;Ca(HCO3)2
C.H2O;HNO3;KOH;NH4NO3
D.SO3;NaHSO4;NaOH;Na2SO4
12.绿色化学也称环境友好化学,就是利用化学原理,实现从生产源头减少或消除对环境的污染。某科学小组的同学欲利用单质铜制备硫酸铜,设计了如下甲、乙两个制备实验方案:
甲:CuCuOCuSO4
乙:CuCuSO4[已知:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O]
下列有关甲、乙实验方案的评价合理的是( )
A.铜的活动性排在H前,所以能和浓硫酸发生反应
B.铜和氧气反应属于化合反应,铜和浓硫酸反应属于置换反应
C.取等质量的铜,理论上通过两种不同方案制取的硫酸铜质量不相等
D.甲方案不会产生污染性气体,乙方案产生SO2不符合绿色化学理念
13.某同学设计了四种实验方案,其中理论上正确,操作上可行的是( )
A.CuO CuCl2溶液Cu
B.FeFe2O3 Fe2(SO4)3溶液
C.Zn H2 Cu
D.CaCO3(块状)CO2Na2CO3溶液
14.芯片是电脑“智能家电”的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:
①Si+O2 SiO2
②Si+2NaOH+X=Na2SiO3+2H2↑
③SiO2+2CSi+2CO↑
④SiO2+Na2CO3Na2SiO3+CO2↑
下列说法错误的是( )
A.④属于氧化还原反应
B.Na2SiO3中Si的化合价为+4价
C.②中X的化学式为H2O
D.Si和SiO2在一定条件下可以相互转化
15.24岁的曹原博士发现了让石墨烯实现“高温超导”的方法,令世界瞩目。石墨烯是一种从石墨中剥离出来仅仅由一层碳原子构成的材料,即“魔角石墨烯”。从物质的分类上看,“ 魔角石墨烯”。( )
A.单质 B.化合物 C.混合物 D.氧化物
二、简答题
16.黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品 第1份 第2份 第3份 第4份 第5份
取样品质量(g) 40.0 40.0 40.0 40.0 40.0
取稀硫酸质量(g) 30.0 60.0 90.0 120.0 150.0
产生气体质量(g) 0.3 0.6 0.9 m 1.0
按要求回答下列问题:
(1)根据实验数据分析,表中m的数值为_______;
(2)与40.0g样品恰好完全反应的稀硫酸的质量是_______;
(3)计算加入稀硫酸的溶质质量分数_______。(要求写出计算过程)
(4)计算该黄铜样品中金属锌的质量_______。(要求写出计算过程)
三、探究题
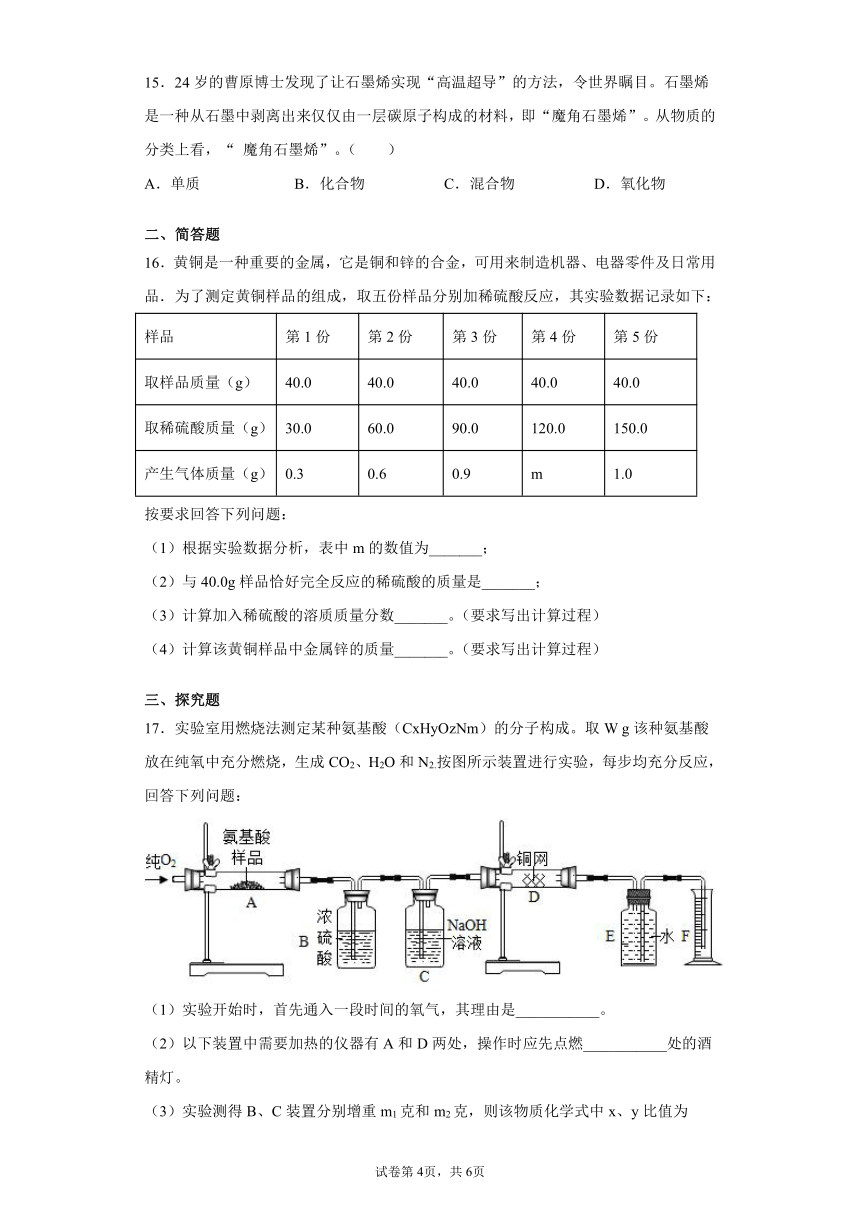
17.实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子构成。取W g该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.按图所示装置进行实验,每步均充分反应,回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是___________。
(2)以下装置中需要加热的仪器有A和D两处,操作时应先点燃___________处的酒精灯。
(3)实验测得B、C装置分别增重m1克和m2克,则该物质化学式中x、y比值为___________。
(4)将B和C装置互换,则测得的氢元素的含量会有偏差。可能的原因是___________。
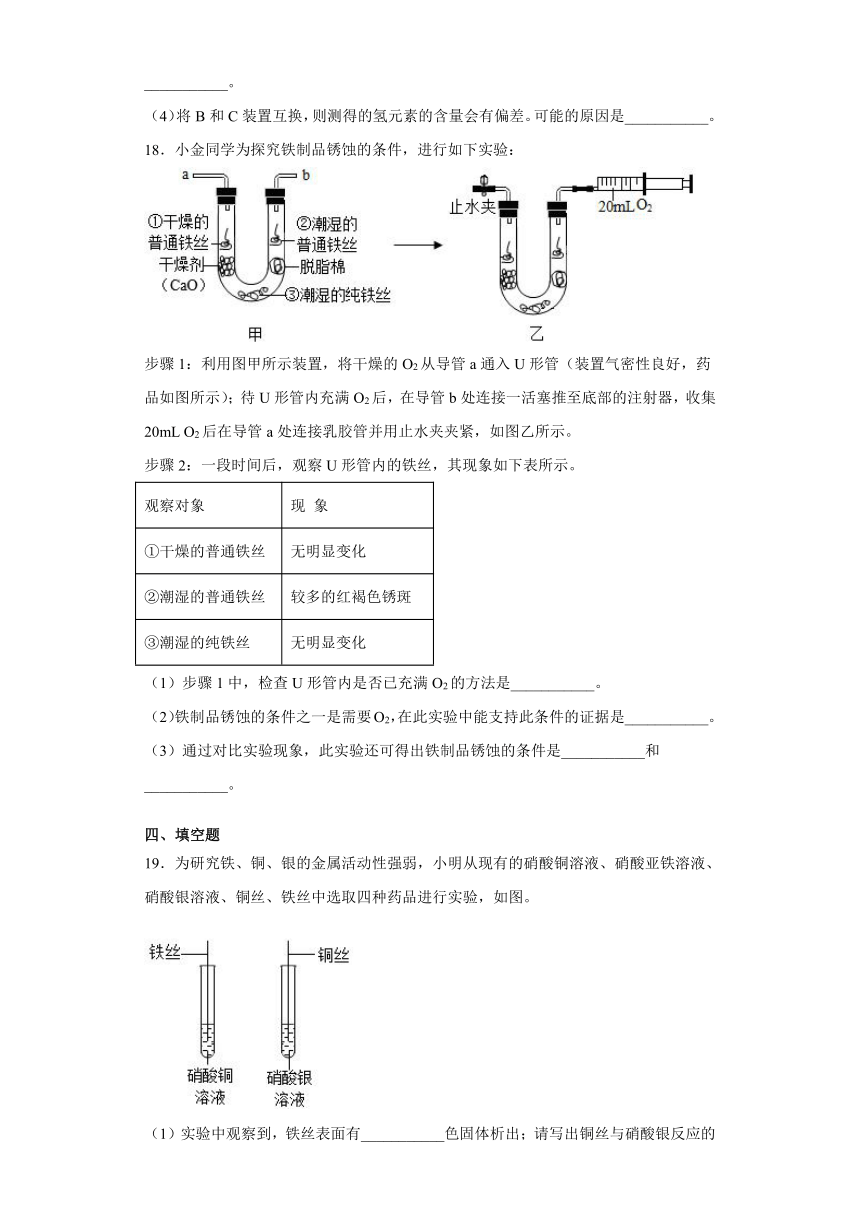
18.小金同学为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mL O2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝,其现象如下表所示。
观察对象 现 象
①干燥的普通铁丝 无明显变化
②潮湿的普通铁丝 较多的红褐色锈斑
③潮湿的纯铁丝 无明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是___________。
(2)铁制品锈蚀的条件之一是需要O2,在此实验中能支持此条件的证据是___________。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是___________和 ___________。
四、填空题
19.为研究铁、铜、银的金属活动性强弱,小明从现有的硝酸铜溶液、硝酸亚铁溶液、硝酸银溶液、铜丝、铁丝中选取四种药品进行实验,如图。
(1)实验中观察到,铁丝表面有___________色固体析出;请写出铜丝与硝酸银反应的化学方程式___________;
(2)上述实验用了四种药品,小金说只要从上述药品中选用三种药品就可以得出三种金属的活动性强弱关系。这三种药品是___________。
20.根据要求回答有关问题:
组别 A B C D
I组 水 氧气 硫酸铜 氯化钾
II组 Fe Na Al Si
(1)从上表Ⅰ组的备选答案中,写出跟“二氧化硫、五氧化二磷、二氧化碳”属于同一 类物质的化学式___________;
(2)小明认为Ⅱ组中的 Si 与其他三种不属于同类物质,你认为其理由是 ___________。
21.某工厂欲从含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
(1)操作Ⅰ的名称是___________;
(2)A物质的化学式是___________;
(3)加入适量H2SO4时发生化学反应的化学方程式是___________。
试卷第1页,共3页
参考答案
1.B
【详解】
物质的性质决定物质的用途,铝能制成铝箔,是利用了铝具有优良的延展性。
故选B。
2.D
【详解】
废铝制易拉罐投入可回收垃圾桶;剩饭剩菜投到厨余桶;废电池和过期的药品投入有害垃圾桶中。故选D。
3.B
【详解】
废铝制易拉罐投入可回收垃圾桶;剩饭剩菜投到厨余桶;废电池和过期的药品投入有害垃圾桶中。故选B。
4.C
【详解】
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,所以①是置换反应,②不是置换反应;
复分解反应是两种化合物成分互换生成另外两种化合物的反应,所以①②都不是复分解反应。
故选C。
5.A
【详解】
A、硝酸铵溶于水吸热,使装置内温度降低,压强减小,在外界大气压的作用下,a液面高于b液面,符合题意。
B、氢氧化钠溶于水放出大量的热,使装置内压强增大,在压强差的作用下,a液面低于b液面,不符合题意。
C、铁与稀硫酸反应生成硫酸亚铁和氢气,装置内压强增大,在压强差的作用下,a液面低于b液面,不符合题意。
D、小苏打是碳酸氢钠的俗称,碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳和水,装置内压强增大,在压强差的作用下,a液面低于b液面,不符合题意。
故选A。
6.C
【详解】
A、铁排在金属活动性顺序表中氢前面,可以与硫酸反应,铁和硫酸发生置换反应时生成硫酸亚铁和氢气,不符合题意。
B、铝在金属活动性顺序中排在氢的前面,能和硫酸反应生成硫酸铝和氢气,不符合题意。
C、铁排在金属活动性顺序表中氢前面,可以与硫酸反应,但铁和硫酸发生置换反应时生成硫酸亚铁,不会生成硫酸铁,符合题意。
D、锌在金属活动性顺序中排在氢的前面,能和硫酸反应生成硫酸锌和氢气,不符合题意。
故选C。
7.A
【详解】
A、小苏打受热分解产生CO2,能使面食疏松多孔,故A正确。
B、烧碱具有强烈的腐蚀性,所以不能用烧碱治疗胃酸过多,故B错误。
C、亚硝酸钠有毒,烹调食物时,不能用工业用盐如亚硝酸钠替换食盐,故C错误。
D、羊毛的主要成分是蛋白质,点燃有烧焦羽毛味,纯棉先点燃有焦味,故D错误。
故选A。
8.C
【详解】
A、合金属于金属材料;塑料属于三大合成材料之一;玻璃钢是玻璃纤维与合成材料塑料复合而成的一种特殊材料,属于复合材料,故选项说法错误。
B、甲醛有毒,能破坏人体蛋白质的结构,使蛋白质变质,用甲醛浸泡过的水产品,会危害人体健康,不能食用,故选项说法错误。
C、研制和开发新能源替代传统能源,能减少环境污染,减少污染,故选项说法正确。
D、铵态氮肥与碱性物质混合后能放出氨气,硝酸铵属于氨态氮肥,与碱性物质混合使用,会降低肥效,故选项说法错误。
故选C。
9.C
【详解】
由图中信息可知,若整个大圆代表纯净物,则A表示单质,B表示化合物,C表示含氧化合物,D表示氧化物。
①澄清的石灰水是氢氧化钙的水溶液,属于混合物;
②冰是水的固体,冰水混合物中只含有一种物质,属于纯净物,且有氢、氧两种元素组成,属于含氧化合物,属于氧化物;
③水银是由一种物质组成的,属于纯净物,且只含有一种元素,属于单质;
④五氧化二磷由一种物质组成的,属于纯净物,且有磷、氧两种元素组成,属于含氧化合物,属于氧化物;
⑤液氧是由一种物质组成的,属于纯净物,且只含有一种元素,属于单质;
⑥高锰酸钾是由一种物质组成的,属于纯净物;且由钾、锰、氧三种元素组成,属于含氧化合物;
⑦氨气是由一种物质组成,且由氮、氢两种元素组成,属于化合物。
C表示含氧化合物,且含氧化合物包含氧化物,所以应放到C区域的是②④⑥。
故选C。
10.B
【详解】
A、由酸、碱的概念可知酸、碱中一定含有氢元素,盐中可能含有氢元素,例如硫酸氢钠属于盐,其中含有氢元素,故A错误。
B、酸不含金属元素,盐中不一定含有金属元素,例如碳酸氢铵属于盐,其中不含有金属元素;碱中可能不含有金属元素,例如一水合氨NH3 H2O属于碱,但不含有金属元素,故B正确。
C、碱中一定含有氧元素,盐中可能含有氧元素,如含氧酸盐与无氧酸盐,酸中不一定含有氧元素,如盐酸HCl,故C错误。
D、盐、碱不一定含有金属元素,如铵盐、一水合氨,酸可能含金属元素,如H2MnO4,故D错误。
故选B。
11.C
【详解】
A、HClO是由氢、氯、氧三种元素组成的化合物,不属于氧化物,不符合排列规律,可排除该选项,故选项错误。
B、二氧化碳是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;H2CO3是由氢离子和碳酸根离子构成的化合物,属于酸;CaCO3是由钙离子和碳酸根离子构成的化合物,属于盐;不符合排列顺序,故选项错误。
C、H2O是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;HNO3是由氢离子和硝酸根离子构成的化合物,属于酸;KOH是由钾离子和氢氧根离子构成的化合物,属于碱;NH4NO3是由铵根离子和硝酸根离子构成的化合物,属于盐;符合排列顺序,故选项正确。
D、SO3是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;NaHSO4是由硫酸氢根离子和钠离子构成的化合物,属于盐;不符合排列顺序,故选项错误。
故选C。
12.D
【详解】
A、铜的活动性排在H后,不符合题意。
B、铜和氧气反应属于化合反应,铜和浓硫酸反应生成物有三种物质,且没有单质,不属于置换反应,不符合题意。
C、由反应前后元素质量不变可知,取等质量的铜,理论上通过两种不同方案制取的硫酸铜质量相等,不符合题意。
D、甲方案不会产生污染性气体,乙方案产生SO2不符合绿色化学理念,符合题意。
故选D。
13.A
【详解】
A、氧化铜会与稀盐酸反应,生成氯化铜(盐)和水,铁可以置换出氯化铜溶液中的铜,故A正确。
B、铁在氧气中燃烧生成四氧化三铁,而不是三氧化二铁,故B错误。
C、氢气能还原氧化铜生成单质铜,但是氢气不能和氢氧化铜反应,故C错误。
D、不能用稀硫酸和块状碳酸钙反应制取二氧化碳,因为反应生成的硫酸钙是微溶的,会覆盖在碳酸钙表面,阻止反应进行,故D错误。
故选A。
14.A
【详解】
A、④中反应前后元素化合价都不变,不属于氧化还原反应,该选项说法不正确。
B、Na2SiO3中钠元素化合价是+1,氧元素化合价是﹣2,根据化合物中元素化合价代数和为零可知,Si的化合价为+4 价,该选项说法正确。
C、②中反应前后硅原子都是1个,钠原子都是2个,反应后氧原子是3个,反应前应该是3个,其中1个包含在X中,反应后氢原子是4个,反应前应该是4个,其中2个包含在X中,X的化学式为H2O,该选项说法正确。
D、由①③可知,Si和SiO2在一定条件下可以相互转化,该选项说法正确。
故选A。
【点睛】
化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础。
15.A
【详解】
只由一种元素组成的纯净物属于单质;由两种或两种以上元素组成的纯净物属于化合物;混合物含有两种或两种以上物质;由两种元素组成,其中一种元素是氧元素的化合物属于氧化物。根据题意,石墨烯是一种从石墨中剥离出来仅仅由一层碳原子构成的材料,即只含有碳元素,有一种元素组成的纯净物属于单质。故石墨烯属于单质。故选A。
16.1.0 100g 由上述分析可知,100g稀硫酸和40g样品恰好完全反应生成气体0.1g,设稀硫酸的溶质质量分数为x,黄铜样品中锌的质量为y
解得:x=49%
y=32.5g
所以稀硫酸的溶质质量分数为49% 由(3)可知,40g黄铜样品中锌的质量为32.5g
【详解】
(1)由第1、2次实验可知,每反应30g稀硫酸,产生气体0.3g,第5次实验加入150g酸,产生气体1.0g,则酸有剩余,说明40g样品完全反应生成气体1.0g。第4次实验,若120g稀硫酸完全反应,应该生成1.2g气体,而40g样品最多生成1.0g气体,所以第4次实验生成气体也为1.0g,所以m的数值为1.0。
(2)40g样品完全反应生成1.0g气体,生成0.3g气体消耗稀硫酸30g,则生成1.0g气体消耗的稀硫酸质量=,所以与40.0g样品恰好完全反应的稀硫酸的质量是100g。
(3)见答案。
(4)见答案。
17.排出装置中的空气,防止影响实验结果 D 实验测得B、C装置分别增重m1g和m2g,说明反应生成水、二氧化碳质量分别是m1g和m2g,碳元素质量为m2g×,氢元素质量为:m1g×。
根据题意有:12x:y= m2g×:m1g×,
解得: 生成的热水蒸汽遇到氢氧化钠溶液会冷凝在其中,或氢氧化钠溶液中的水会以水蒸气的形式随气流逸出C装置等
【详解】
(1)实验开始时,首先通入一段时间的氧气,其理由是排出装置中的空气,防止影响实验结果。
(2)以上装置中需要加热的仪器有A和D两处,操作时应先点燃D处的酒精灯,这是因为先加热D处,能够防止氧气进入E装置,使测定的氮气体积更准确。
(3)见答案。
(4)气体通过溶液会带出水分,如果B和C装置互换,生成的热水蒸汽遇到氢氧化钠溶液会冷凝在其中,则测得的氢元素的含量偏大。
18.在b口放带火星的木条,如果木条复燃则证明装满氧气 注射器中氧气减少 水分 金属的内部结构
【详解】
(1)步骤1中,检查U形管内是否已充满O2的方法是:在b口放带火星的木条,如果木条复燃,则装满氧气。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:注射器中氧气减少。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是:水分和金属的内部结构,因为“潮湿的纯铁丝”和“潮湿的普通铁丝”的变量是“有无碳和其他杂质”。
19.红 Cu+2AgNO3=Cu(NO3)2+2Ag 铜丝、硝酸亚铁溶液、硝酸银溶液
【详解】
(1)铁和硝酸铜反应生成硝酸亚铁和铜,所以实验中观察到铁丝表面有红色的铜析出;铜和硝酸银反应生成硝酸铜和银,化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag。
(2)从上述药品中选用三种药品就可以得出三种金属的活动性强弱关系,这三种药品是铜丝、硝酸亚铁溶液、硝酸银溶液。铜不能与硝酸亚铁溶液反应,所以铜活动性比铁弱,铜能置换出硝酸银溶液中的的银,说明铜的活动性比银强。
20.H2O 硅属于非金属单质,而其他三种属于金属单质
【详解】
(1)氧化物是指由两种元素组成其中一种元素是氧元素的化合物,二氧化硫、五氧化二磷、二氧化碳都属于氧化物,表I组中的水是由氢、氧两种元素组成的化合物,属于氧化物,故填:H2O。
(2)观察所给四种物质,硅属于非金属单质,而铁、钠、铝都属于金属单质。
21.过滤 Fe Fe +H2SO4= FeSO4+H2↑
【详解】
(1)由操作过程可知。操作Ⅰ是将固液分离,操作名称是过滤。
(2)由于铁与硫酸铜反应生成铜和硫酸亚铁,铁与硫酸反应生成了硫酸亚铁和氢气。由题意可知,要回收铜和得到硫酸亚铁,应向废液中加入过量A物质是铁,最后再加入过量的B应是稀硫酸,将过量的铁除去,所以A的化学式是Fe。
(3)由上述分析可知,加入适量硫酸时反应的化学方程式是:Fe+H2SO4═FeSO4+H2↑。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.超市里买来的饼干、坚果类食品使用铝箔来包装,铝能制作成铝箔,这是利用了铝的( )
A.导电性 B.延展性 C.导热性 D.熔点高
2.我县荣获2019年全省生活垃圾分类工作优秀县,为推进全省垃圾治理作出新贡献。下列生活垃圾应投入可回收垃圾桶的是( )
A.废旧电池 B.过期药品 C.剩饭剩菜 D.铝制易拉罐
3.2020年11月13日开始,龙泉市开展了为期一周的垃圾分类“进商户”专题宣传活动。某商场放着如图所示的三只垃圾桶,下列垃圾应投入可回收垃圾桶的是( )
A.废电池 B.铝制易拉罐 C.剩饭 D.过期药品
4.合金在生活中的应用十分广泛,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是①C+2NiO2Ni+CO2↑;万米深海潜水器“奋斗者”号载人舱外壳材料采用的是钛合金,钛的生产过程中发生的反应之一为:②TiO2+2Cl2+2C = TiCl4+2CO,下列有关这两个反应,说法正确的是( )
A.两个反应都是置换反应 B.①是置换反应,②是复分解反应
C.只有①是置换反应 D.只有①是复分解反应
5.如图所示,U 型管内 a、b 液面相平,当挤压滴管的胶头,使试剂 X 进入锥形瓶内,一段时间后会观察到 a 液面高于 b 液面。则试剂 X、Y 的组合可能是( )
A.水、硝酸铵 B.水、烧碱
C.稀硫酸、铁粉 D.稀盐酸、小苏打
6.下列物质中不能通过金属与硫酸反应得到的是( )
A.FeSO4 B.Al2(SO4)3 C.Fe2(SO4)3 D.ZnSO4
7.化学与生活密切相关。下列生活小窍门正确的是( )
A.小苏打受热分解产生CO2,可用于制作面点
B.烧碱能中和酸,可用于治疗胃酸过多
C.烹调食物时,用工业用盐如亚硝酸钠替换食盐
D.可以用灼烧闻气味的方法区分真丝和纯棉线,有烧焦羽毛味的是纯棉线
8.化学与生活、生产、科技密不可分。下列叙述正确的是( )
A.合金、塑料、玻璃钢属于合成材料
B.用甲醛浸泡过的水产品,可放心食用
C.研制新材料、新能源替代传统能源,减少污染
D.化肥硝酸铵可与碱性物质混合使用,增大肥效
9.如图表示的是纯净物、单质、化合物、含氧化合物、氧化物概念之间的关系,若整个大圆代表纯净物,下列物质应放到C区域的是( )
①澄清的石灰水 ②冰水混合物 ③水银 ④五氧化二磷 ⑤液氧 ⑥高锰酸钾 ⑦氨气
A.②③⑤ B.④⑦ C.②④⑥ D.②④
10.下列关于酸、碱、盐元素组成的说法,正确的是 ( )
A.酸、碱一定含有氢,盐一定不含氢 B.酸、碱、盐可能都不含金属元素
C.碱、盐可能含氧,酸一定含氧 D.盐、碱一定含有金属元素
11.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物—酸—碱—盐”顺序排列的是( )
A.HClO;HCl;Mg(OH)2;MgCl2
B.CO2;H2CO3;CaCO3;Ca(HCO3)2
C.H2O;HNO3;KOH;NH4NO3
D.SO3;NaHSO4;NaOH;Na2SO4
12.绿色化学也称环境友好化学,就是利用化学原理,实现从生产源头减少或消除对环境的污染。某科学小组的同学欲利用单质铜制备硫酸铜,设计了如下甲、乙两个制备实验方案:
甲:CuCuOCuSO4
乙:CuCuSO4[已知:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O]
下列有关甲、乙实验方案的评价合理的是( )
A.铜的活动性排在H前,所以能和浓硫酸发生反应
B.铜和氧气反应属于化合反应,铜和浓硫酸反应属于置换反应
C.取等质量的铜,理论上通过两种不同方案制取的硫酸铜质量不相等
D.甲方案不会产生污染性气体,乙方案产生SO2不符合绿色化学理念
13.某同学设计了四种实验方案,其中理论上正确,操作上可行的是( )
A.CuO CuCl2溶液Cu
B.FeFe2O3 Fe2(SO4)3溶液
C.Zn H2 Cu
D.CaCO3(块状)CO2Na2CO3溶液
14.芯片是电脑“智能家电”的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:
①Si+O2 SiO2
②Si+2NaOH+X=Na2SiO3+2H2↑
③SiO2+2CSi+2CO↑
④SiO2+Na2CO3Na2SiO3+CO2↑
下列说法错误的是( )
A.④属于氧化还原反应
B.Na2SiO3中Si的化合价为+4价
C.②中X的化学式为H2O
D.Si和SiO2在一定条件下可以相互转化
15.24岁的曹原博士发现了让石墨烯实现“高温超导”的方法,令世界瞩目。石墨烯是一种从石墨中剥离出来仅仅由一层碳原子构成的材料,即“魔角石墨烯”。从物质的分类上看,“ 魔角石墨烯”。( )
A.单质 B.化合物 C.混合物 D.氧化物
二、简答题
16.黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品 第1份 第2份 第3份 第4份 第5份
取样品质量(g) 40.0 40.0 40.0 40.0 40.0
取稀硫酸质量(g) 30.0 60.0 90.0 120.0 150.0
产生气体质量(g) 0.3 0.6 0.9 m 1.0
按要求回答下列问题:
(1)根据实验数据分析,表中m的数值为_______;
(2)与40.0g样品恰好完全反应的稀硫酸的质量是_______;
(3)计算加入稀硫酸的溶质质量分数_______。(要求写出计算过程)
(4)计算该黄铜样品中金属锌的质量_______。(要求写出计算过程)
三、探究题
17.实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子构成。取W g该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.按图所示装置进行实验,每步均充分反应,回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是___________。
(2)以下装置中需要加热的仪器有A和D两处,操作时应先点燃___________处的酒精灯。
(3)实验测得B、C装置分别增重m1克和m2克,则该物质化学式中x、y比值为___________。
(4)将B和C装置互换,则测得的氢元素的含量会有偏差。可能的原因是___________。
18.小金同学为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mL O2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝,其现象如下表所示。
观察对象 现 象
①干燥的普通铁丝 无明显变化
②潮湿的普通铁丝 较多的红褐色锈斑
③潮湿的纯铁丝 无明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是___________。
(2)铁制品锈蚀的条件之一是需要O2,在此实验中能支持此条件的证据是___________。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是___________和 ___________。
四、填空题
19.为研究铁、铜、银的金属活动性强弱,小明从现有的硝酸铜溶液、硝酸亚铁溶液、硝酸银溶液、铜丝、铁丝中选取四种药品进行实验,如图。
(1)实验中观察到,铁丝表面有___________色固体析出;请写出铜丝与硝酸银反应的化学方程式___________;
(2)上述实验用了四种药品,小金说只要从上述药品中选用三种药品就可以得出三种金属的活动性强弱关系。这三种药品是___________。
20.根据要求回答有关问题:
组别 A B C D
I组 水 氧气 硫酸铜 氯化钾
II组 Fe Na Al Si
(1)从上表Ⅰ组的备选答案中,写出跟“二氧化硫、五氧化二磷、二氧化碳”属于同一 类物质的化学式___________;
(2)小明认为Ⅱ组中的 Si 与其他三种不属于同类物质,你认为其理由是 ___________。
21.某工厂欲从含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
(1)操作Ⅰ的名称是___________;
(2)A物质的化学式是___________;
(3)加入适量H2SO4时发生化学反应的化学方程式是___________。
试卷第1页,共3页
参考答案
1.B
【详解】
物质的性质决定物质的用途,铝能制成铝箔,是利用了铝具有优良的延展性。
故选B。
2.D
【详解】
废铝制易拉罐投入可回收垃圾桶;剩饭剩菜投到厨余桶;废电池和过期的药品投入有害垃圾桶中。故选D。
3.B
【详解】
废铝制易拉罐投入可回收垃圾桶;剩饭剩菜投到厨余桶;废电池和过期的药品投入有害垃圾桶中。故选B。
4.C
【详解】
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,所以①是置换反应,②不是置换反应;
复分解反应是两种化合物成分互换生成另外两种化合物的反应,所以①②都不是复分解反应。
故选C。
5.A
【详解】
A、硝酸铵溶于水吸热,使装置内温度降低,压强减小,在外界大气压的作用下,a液面高于b液面,符合题意。
B、氢氧化钠溶于水放出大量的热,使装置内压强增大,在压强差的作用下,a液面低于b液面,不符合题意。
C、铁与稀硫酸反应生成硫酸亚铁和氢气,装置内压强增大,在压强差的作用下,a液面低于b液面,不符合题意。
D、小苏打是碳酸氢钠的俗称,碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳和水,装置内压强增大,在压强差的作用下,a液面低于b液面,不符合题意。
故选A。
6.C
【详解】
A、铁排在金属活动性顺序表中氢前面,可以与硫酸反应,铁和硫酸发生置换反应时生成硫酸亚铁和氢气,不符合题意。
B、铝在金属活动性顺序中排在氢的前面,能和硫酸反应生成硫酸铝和氢气,不符合题意。
C、铁排在金属活动性顺序表中氢前面,可以与硫酸反应,但铁和硫酸发生置换反应时生成硫酸亚铁,不会生成硫酸铁,符合题意。
D、锌在金属活动性顺序中排在氢的前面,能和硫酸反应生成硫酸锌和氢气,不符合题意。
故选C。
7.A
【详解】
A、小苏打受热分解产生CO2,能使面食疏松多孔,故A正确。
B、烧碱具有强烈的腐蚀性,所以不能用烧碱治疗胃酸过多,故B错误。
C、亚硝酸钠有毒,烹调食物时,不能用工业用盐如亚硝酸钠替换食盐,故C错误。
D、羊毛的主要成分是蛋白质,点燃有烧焦羽毛味,纯棉先点燃有焦味,故D错误。
故选A。
8.C
【详解】
A、合金属于金属材料;塑料属于三大合成材料之一;玻璃钢是玻璃纤维与合成材料塑料复合而成的一种特殊材料,属于复合材料,故选项说法错误。
B、甲醛有毒,能破坏人体蛋白质的结构,使蛋白质变质,用甲醛浸泡过的水产品,会危害人体健康,不能食用,故选项说法错误。
C、研制和开发新能源替代传统能源,能减少环境污染,减少污染,故选项说法正确。
D、铵态氮肥与碱性物质混合后能放出氨气,硝酸铵属于氨态氮肥,与碱性物质混合使用,会降低肥效,故选项说法错误。
故选C。
9.C
【详解】
由图中信息可知,若整个大圆代表纯净物,则A表示单质,B表示化合物,C表示含氧化合物,D表示氧化物。
①澄清的石灰水是氢氧化钙的水溶液,属于混合物;
②冰是水的固体,冰水混合物中只含有一种物质,属于纯净物,且有氢、氧两种元素组成,属于含氧化合物,属于氧化物;
③水银是由一种物质组成的,属于纯净物,且只含有一种元素,属于单质;
④五氧化二磷由一种物质组成的,属于纯净物,且有磷、氧两种元素组成,属于含氧化合物,属于氧化物;
⑤液氧是由一种物质组成的,属于纯净物,且只含有一种元素,属于单质;
⑥高锰酸钾是由一种物质组成的,属于纯净物;且由钾、锰、氧三种元素组成,属于含氧化合物;
⑦氨气是由一种物质组成,且由氮、氢两种元素组成,属于化合物。
C表示含氧化合物,且含氧化合物包含氧化物,所以应放到C区域的是②④⑥。
故选C。
10.B
【详解】
A、由酸、碱的概念可知酸、碱中一定含有氢元素,盐中可能含有氢元素,例如硫酸氢钠属于盐,其中含有氢元素,故A错误。
B、酸不含金属元素,盐中不一定含有金属元素,例如碳酸氢铵属于盐,其中不含有金属元素;碱中可能不含有金属元素,例如一水合氨NH3 H2O属于碱,但不含有金属元素,故B正确。
C、碱中一定含有氧元素,盐中可能含有氧元素,如含氧酸盐与无氧酸盐,酸中不一定含有氧元素,如盐酸HCl,故C错误。
D、盐、碱不一定含有金属元素,如铵盐、一水合氨,酸可能含金属元素,如H2MnO4,故D错误。
故选B。
11.C
【详解】
A、HClO是由氢、氯、氧三种元素组成的化合物,不属于氧化物,不符合排列规律,可排除该选项,故选项错误。
B、二氧化碳是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;H2CO3是由氢离子和碳酸根离子构成的化合物,属于酸;CaCO3是由钙离子和碳酸根离子构成的化合物,属于盐;不符合排列顺序,故选项错误。
C、H2O是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;HNO3是由氢离子和硝酸根离子构成的化合物,属于酸;KOH是由钾离子和氢氧根离子构成的化合物,属于碱;NH4NO3是由铵根离子和硝酸根离子构成的化合物,属于盐;符合排列顺序,故选项正确。
D、SO3是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;NaHSO4是由硫酸氢根离子和钠离子构成的化合物,属于盐;不符合排列顺序,故选项错误。
故选C。
12.D
【详解】
A、铜的活动性排在H后,不符合题意。
B、铜和氧气反应属于化合反应,铜和浓硫酸反应生成物有三种物质,且没有单质,不属于置换反应,不符合题意。
C、由反应前后元素质量不变可知,取等质量的铜,理论上通过两种不同方案制取的硫酸铜质量相等,不符合题意。
D、甲方案不会产生污染性气体,乙方案产生SO2不符合绿色化学理念,符合题意。
故选D。
13.A
【详解】
A、氧化铜会与稀盐酸反应,生成氯化铜(盐)和水,铁可以置换出氯化铜溶液中的铜,故A正确。
B、铁在氧气中燃烧生成四氧化三铁,而不是三氧化二铁,故B错误。
C、氢气能还原氧化铜生成单质铜,但是氢气不能和氢氧化铜反应,故C错误。
D、不能用稀硫酸和块状碳酸钙反应制取二氧化碳,因为反应生成的硫酸钙是微溶的,会覆盖在碳酸钙表面,阻止反应进行,故D错误。
故选A。
14.A
【详解】
A、④中反应前后元素化合价都不变,不属于氧化还原反应,该选项说法不正确。
B、Na2SiO3中钠元素化合价是+1,氧元素化合价是﹣2,根据化合物中元素化合价代数和为零可知,Si的化合价为+4 价,该选项说法正确。
C、②中反应前后硅原子都是1个,钠原子都是2个,反应后氧原子是3个,反应前应该是3个,其中1个包含在X中,反应后氢原子是4个,反应前应该是4个,其中2个包含在X中,X的化学式为H2O,该选项说法正确。
D、由①③可知,Si和SiO2在一定条件下可以相互转化,该选项说法正确。
故选A。
【点睛】
化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础。
15.A
【详解】
只由一种元素组成的纯净物属于单质;由两种或两种以上元素组成的纯净物属于化合物;混合物含有两种或两种以上物质;由两种元素组成,其中一种元素是氧元素的化合物属于氧化物。根据题意,石墨烯是一种从石墨中剥离出来仅仅由一层碳原子构成的材料,即只含有碳元素,有一种元素组成的纯净物属于单质。故石墨烯属于单质。故选A。
16.1.0 100g 由上述分析可知,100g稀硫酸和40g样品恰好完全反应生成气体0.1g,设稀硫酸的溶质质量分数为x,黄铜样品中锌的质量为y
解得:x=49%
y=32.5g
所以稀硫酸的溶质质量分数为49% 由(3)可知,40g黄铜样品中锌的质量为32.5g
【详解】
(1)由第1、2次实验可知,每反应30g稀硫酸,产生气体0.3g,第5次实验加入150g酸,产生气体1.0g,则酸有剩余,说明40g样品完全反应生成气体1.0g。第4次实验,若120g稀硫酸完全反应,应该生成1.2g气体,而40g样品最多生成1.0g气体,所以第4次实验生成气体也为1.0g,所以m的数值为1.0。
(2)40g样品完全反应生成1.0g气体,生成0.3g气体消耗稀硫酸30g,则生成1.0g气体消耗的稀硫酸质量=,所以与40.0g样品恰好完全反应的稀硫酸的质量是100g。
(3)见答案。
(4)见答案。
17.排出装置中的空气,防止影响实验结果 D 实验测得B、C装置分别增重m1g和m2g,说明反应生成水、二氧化碳质量分别是m1g和m2g,碳元素质量为m2g×,氢元素质量为:m1g×。
根据题意有:12x:y= m2g×:m1g×,
解得: 生成的热水蒸汽遇到氢氧化钠溶液会冷凝在其中,或氢氧化钠溶液中的水会以水蒸气的形式随气流逸出C装置等
【详解】
(1)实验开始时,首先通入一段时间的氧气,其理由是排出装置中的空气,防止影响实验结果。
(2)以上装置中需要加热的仪器有A和D两处,操作时应先点燃D处的酒精灯,这是因为先加热D处,能够防止氧气进入E装置,使测定的氮气体积更准确。
(3)见答案。
(4)气体通过溶液会带出水分,如果B和C装置互换,生成的热水蒸汽遇到氢氧化钠溶液会冷凝在其中,则测得的氢元素的含量偏大。
18.在b口放带火星的木条,如果木条复燃则证明装满氧气 注射器中氧气减少 水分 金属的内部结构
【详解】
(1)步骤1中,检查U形管内是否已充满O2的方法是:在b口放带火星的木条,如果木条复燃,则装满氧气。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:注射器中氧气减少。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是:水分和金属的内部结构,因为“潮湿的纯铁丝”和“潮湿的普通铁丝”的变量是“有无碳和其他杂质”。
19.红 Cu+2AgNO3=Cu(NO3)2+2Ag 铜丝、硝酸亚铁溶液、硝酸银溶液
【详解】
(1)铁和硝酸铜反应生成硝酸亚铁和铜,所以实验中观察到铁丝表面有红色的铜析出;铜和硝酸银反应生成硝酸铜和银,化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag。
(2)从上述药品中选用三种药品就可以得出三种金属的活动性强弱关系,这三种药品是铜丝、硝酸亚铁溶液、硝酸银溶液。铜不能与硝酸亚铁溶液反应,所以铜活动性比铁弱,铜能置换出硝酸银溶液中的的银,说明铜的活动性比银强。
20.H2O 硅属于非金属单质,而其他三种属于金属单质
【详解】
(1)氧化物是指由两种元素组成其中一种元素是氧元素的化合物,二氧化硫、五氧化二磷、二氧化碳都属于氧化物,表I组中的水是由氢、氧两种元素组成的化合物,属于氧化物,故填:H2O。
(2)观察所给四种物质,硅属于非金属单质,而铁、钠、铝都属于金属单质。
21.过滤 Fe Fe +H2SO4= FeSO4+H2↑
【详解】
(1)由操作过程可知。操作Ⅰ是将固液分离,操作名称是过滤。
(2)由于铁与硫酸铜反应生成铜和硫酸亚铁,铁与硫酸反应生成了硫酸亚铁和氢气。由题意可知,要回收铜和得到硫酸亚铁,应向废液中加入过量A物质是铁,最后再加入过量的B应是稀硫酸,将过量的铁除去,所以A的化学式是Fe。
(3)由上述分析可知,加入适量硫酸时反应的化学方程式是:Fe+H2SO4═FeSO4+H2↑。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
