人教版五四制九年级化学3.2酸和碱的中和反应同步练习(word 含解析)
文档属性
| 名称 | 人教版五四制九年级化学3.2酸和碱的中和反应同步练习(word 含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 84.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-22 00:00:00 | ||
图片预览




文档简介
酸和碱的中和反应
一、单选题
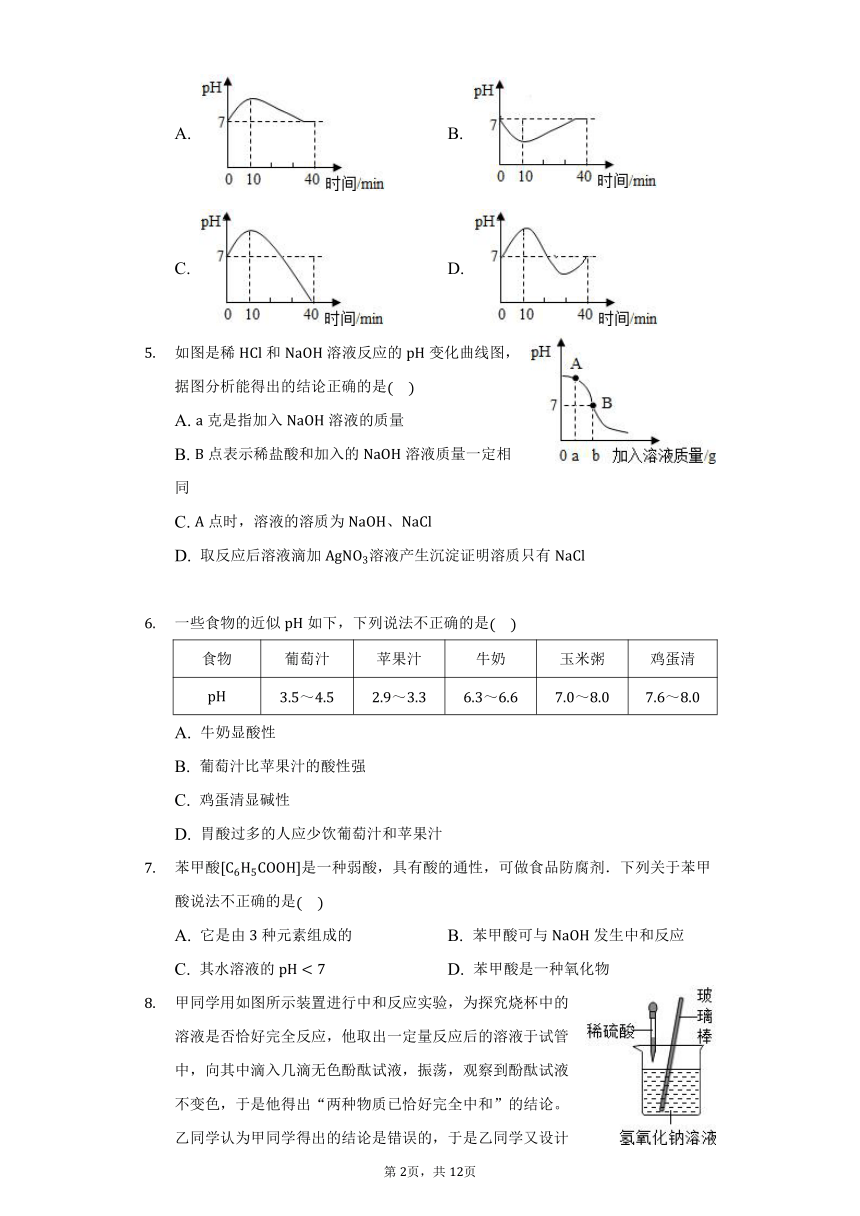
下列操作不正确的是
A. 加热液体 B. 稀释浓硫酸
C. 取固体粉末 D. 检查气密性
下列实验现象描述正确的是
A. 把碘放入水中:碘很快溶解到水中形成棕色溶液
B. 一氧化碳在空气中燃烧:产生淡蓝色火焰,放出大量的热
C. 铁钉放在硫酸铜溶液中:银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
D. 打开浓盐酸的试剂瓶盖,瓶口会出现白色烟雾
如图模型分别表示生成氯化钠的不同化学反应,相关叙述正确的是
A. 图甲反应的实质是氢离子和氢氧根离子结合生成水分子
B. 紫色石蕊试液、铁、硝酸银溶液都能验证图甲反应中物质恰好完全反应
C. 图乙表示的反应中所涉及种物质,其中属于氧化物的有两种
D. 图乙表示的反应属于置换反应
医生在给病人看病时,可以通过人体口腔内唾液的约为来判断病情的程度,如下是医生对某病人口腔内唾液的进行的实验:在进食过程的最初分钟,酸性逐渐增强,之后酸性逐渐减弱,至分钟趋于正常。与上述事实最接近的图象是
A. B.
C. D.
如图是稀和溶液反应的变化曲线图,据图分析能得出的结论正确的是
A. 克是指加入溶液的质量
B. 点表示稀盐酸和加入的溶液质量一定相同
C. 点时,溶液的溶质为、
D. 取反应后溶液滴加溶液产生沉淀证明溶质只有
一些食物的近似如下,下列说法不正确的是
食物 葡萄汁 苹果汁 牛奶 玉米粥 鸡蛋清
A. 牛奶显酸性
B. 葡萄汁比苹果汁的酸性强
C. 鸡蛋清显碱性
D. 胃酸过多的人应少饮葡萄汁和苹果汁
苯甲酸是一种弱酸,具有酸的通性,可做食品防腐剂.下列关于苯甲酸说法不正确的是
A. 它是由种元素组成的 B. 苯甲酸可与发生中和反应
C. 其水溶液的 D. 苯甲酸是一种氧化物
甲同学用如图所示装置进行中和反应实验,为探究烧杯中的溶液是否恰好完全反应,他取出一定量反应后的溶液于试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论。乙同学认为甲同学得出的结论是错误的,于是乙同学又设计了下列实验方案,其中还不能证明氢氧化钠和稀硫酸恰好完全中和的是
A. 从烧杯中取样于试管中,滴加碳酸钠溶液,无气泡产生
B. 从烧杯中取样于试管中,加入粒,无气泡产生
C. 从烧杯中取样于试管中,加入氯化钡溶液,有白色沉淀产生
D. 从烧杯中取样于试管中,滴加紫色石蕊试液,试液不变色
某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液的变化,其图象如图所示,下列说法正确的是
A. 图中点所示溶液呈碱性
B. 图中点所示溶液中,含有的微粒是、
C. 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D. 由点到点的变化过程证明酸和碱发生了化学反应
下列关于中和反应的说法,正确的是
A. 碱性物质和稀盐酸混合发生的反应一定是中和反应
B. 有盐和水生成的反应一定是中和反应
C. 工厂废水中含有的硫酸可用氨水中和
D. 可用氢氧化钠固体与稀盐酸反应验证中和反应放热
二、填空题
在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.
该反应的化学方程式为:______.
该实验操作是将 ______滴加到另一种溶液中.
当加入溶液的质量为时,所得溶液中的溶质为写化学式 ______.
当加入溶液的质量为时,向所得溶液中滴加酚酞溶液,溶液呈 ______色.若加入酚酞后溶液颜色为无色时 ______填能或不能说明恰好完全反应.
某市初中化学实验操作考查内容为“溶液酸碱性的检验”。请根据实验回答下列问题。
测得碳酸饮料的 ______填“”“”或“”。
若用水润湿试纸测得稀盐酸的酸碱度,测得值将会 ______填偏大或偏小或不变。
下列使用试纸的方法中,正确的是 ______填字母。
A.将试纸剪成几段使用
B.将试纸直接插入待测液中
C.将试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在试纸上
D.将试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在试纸上
E.读数时,在秒内将试纸呈现的颜色与标准比色卡对照
下表列出生活中一些液体的;
液体 雨水 蒸馏水 厨房清洁剂 厕所清洁剂
上述液体中,酸性最强的是______,能使酚酞试液变红的是______.
厨房清洁剂与厕所清洁剂不能混合使用,其原因是______.
化学就在身边,为了应用所学知识,小明取刚降到地面的雨水进行研究。
若用酸碱指示剂检验该雨水的酸碱性,方法是__________________________________________。
若用计每隔几分钟测一次该雨水的,数据如下表:
测定时刻
该雨水是否为酸雨?________填“是”或“不是”。
上表数据的能否用试纸测得?________填“能”或“不能”。
从上表数据中,你还能得出该雨水的一个结论是______________________________________________________________________________。
可用于检验该雨水是否为硬水的物质是____________。
答案和解析
1.【答案】
【解析】解:、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的,图中所示操作正确。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散;一定不能把水注入浓硫酸中;图中所示操作错误。
C、取用粉末状药品,试管横放,用药匙或纸槽把药品送到试管底部,图中所示操作正确。
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确。
故选:。
A、根据给试管中的液体加热的方法进行分析判断。
B、根据浓硫酸的稀释方法酸入水,沿器壁,慢慢倒,不断搅进行分析判断。
C、根据向试管中装粉末状固体药品的方法“一斜、二送、三直立”进行分析判断。
D、根据检查装置气密性的方法进行分析判断。
本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.【答案】
【解析】解:、碘难溶于水,把碘放入水中,几乎不溶解,故选项说法错误。
B、一氧化碳在空气中燃烧,产生蓝色火焰,放出大量的热,故选项说法错误。
C、铁钉放在硫酸铜溶液中生成硫酸亚铁溶液和铜,银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色,故选项说法正确。
D、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气接触形成盐酸小液滴,瓶口上方有白雾产生,而不是白色烟雾,故选项说法错误。
故选:。
A、根据碘难溶于水,进行分析判断。
B、根据一氧化碳在空气中燃烧的现象,进行分析判断。
C、根据金属的化学性质,进行分析判断。
D、根据浓盐酸具有挥发性,进行分析判断。
本题难度不大,掌握浓盐酸具有挥发性、金属的化学性质、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾的区别、物质颜色的变化。
3.【答案】
【解析】解:、图甲反应是盐酸和氢氧化钠反应生成氯化钠和水,属于中和反应,反应的实质是氢离子和氢氧根离子结合生成水分子,故选项说法正确。
B、紫色石蕊试液、铁都能通过与酸的反应,验证图甲反应中物质恰好完全反应,氯化钠、盐酸均能与硝酸银溶液反应生成氯化银沉淀,不能验证图甲反应中物质恰好完全反应,故选项说法错误。
C、图乙表示的反应中所涉及种物质,反应物是和,生成物是和,属于氧化物的有一种,故选项说法错误。
D、图乙表示的反应生成物均为化合物,不属于置换反应,故选项说法错误。
故选:。
A、根据图甲反应是盐酸和氢氧化钠反应生成氯化钠和水,进行分析判断。
B、根据酸的化学性质,进行分析判断。
C、根据氧化物是只含有两种元素且其中一种元素是氧元素的化合物,进行分析判断。
D、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。
本题难度不大,掌握中和反应的实质、氧化物的特征、置换反应的特征等是正确解答本题的关键。
4.【答案】
【解析】解:在进食过程的最初分钟,酸性逐渐增强,溶液的应该减小,之后酸性逐渐减弱,溶液的应该增大,因此图中的曲线变化符合这一情况。
故选:。
当溶液的小于时,随着的减小酸性增强,随着的增大酸性减弱。
解答本题要掌握溶液的酸碱性与溶液大小之间的关系,只有这样才能对相关方面的问题做出正确的判断。
5.【答案】
【解析】解:、由图象可知,值是开始时大于逐渐的减小到然后小于,可知原溶液显碱性,然后不断的加入酸性溶液,使减小,说明是把稀盐酸滴加到氢氧化钠溶液中,克是指加入稀盐酸的质量,故选项说法错误。
B、由于不知道稀盐酸和氢氧化钠溶液的溶质质量分数,无法确定稀盐酸和氢氧化钠溶液的质量,故选项说法错误。
C、点时溶液的大于,溶液显碱性,说明氢氧化钠过量,所得溶液中的溶质为、,故选项说法正确。
D、稀盐酸与氯化钠均能与硝酸银溶液反应生成氯化银沉淀,不能确定证明溶质只有,故选项说法错误。
故选:。
A、根据图象中值的变化是从大于逐渐的减小到小于,进行分析判断。
B、根据不知道稀盐酸和氢氧化钠溶液的溶质质量分数,进行分析判断。
C、根据点时溶液的大于,进行分析判断。
D、根据稀盐酸与氯化钠均能与硝酸银溶液反应生成氯化银沉淀,进行分析判断。
本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键。
6.【答案】
【解析】解:、牛奶的小于,显酸性,故说法正确;
B.苹果汁、葡萄汁的都小于,都显酸性,但苹果汁的更小,酸性更强,故说法错误;
C.鸡蛋清的大于,显碱性,故说法正确;
D.对于胃酸过多的人比较适宜食用的食物是接近中性或偏碱性的食物,而不适宜吃酸性食物,葡萄汁和苹果汁显酸性,所以应少吃,故说法正确。
故选:。
当溶液的等于时,呈中性;当溶液的大于时,呈碱性;当溶液的小于时,呈酸性。当溶液的小于时,随着的减小酸性增强。
解答本题要掌握溶液的酸碱性和溶液大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论。
7.【答案】
【解析】解:、苯甲酸由、、三种元素组成,故A说法正确;
B、苯甲酸属于酸可与发生中和反应生成盐和水,故B说法正确;
C、苯甲酸属于酸,水溶液的,故C说法正确;
D、氧化物必须由两种元素组成,一种元素是氧元素,而苯甲酸由、、三种元素组成,故D说法错误。
故选:。
A、根据物质的元素组成考虑;、根据酸的化学性质考虑;、根据酸的考虑;、根据氧化物的特点考虑.
解答本题关键是知道物质的元素组成,知道中和反应的实质,知道氧化物的特点.
8.【答案】
【解析】解:、从烧杯中取样于试管中,滴加碳酸钠溶液,无气泡产生,说明反应后的溶液中不含稀硫酸,说明氢氧化钠和稀硫酸恰好完全中和,故选项不符合题意;
、从烧杯中取样于试管中,加入粒,无气泡产生,说明反应后的溶液中不含稀硫酸,说明氢氧化钠和稀硫酸恰好完全中和,故选项不符合题意;
、从烧杯中取样于试管中,加入氯化钡溶液,硫酸钠、硫酸均能与氯化钡溶液反应生成硫酸钡白色沉淀,不能说明氢氧化钠和稀硫酸恰好完全中和,故选项符合题意;
D、从烧杯中取样于试管中,滴加紫色石蕊试液,试液不变色,说明溶液显中性,说明氢氧化钠和稀硫酸恰好完全中和,故选项不符合题意;
故选:。
根据探究酸是否过量的方法,如可选用指示剂或能与酸反应有明显现象的物质,如碳酸盐,活泼金属等进行分析。
解答本题关键是要知道酸的化学性质及反应的明显现象。
9.【答案】
【解析】解:、点时溶液的小于,溶液显酸性,故选项说法错误;
、点时溶液的等于,溶液显中性,含有的溶质是,溶剂是水,所以含有的微粒有:、、;故选项说法错误;
、由图象可知,值是开始时大于逐渐的减小到然后小于,可知原溶液显碱性,然后不断的加入酸性溶液,使减小,说明是把稀硫酸滴加到氢氧化钠溶液中,故选项说法错误;
、由点到点的变化过程,碱性逐渐变弱,说明酸和碱发生了中和反应,故选项说法正确;
故选:。
A、根据 点时溶液的小于,进行分析判断;
、根据点时溶液的,进行分析判断;
、根据图象中值的变化是从大于逐渐的减小到小于,进行分析判断;
、根据点时溶液的小于,进行分析判断。
本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液 大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键。
10.【答案】
【解析】解:、碱性物质和稀盐酸混合发生的反应不一定是中和反应,如碳酸钠属于盐,其水溶液呈碱性,碳酸钠能够与稀盐酸反应生成氯化钠、水和二氧化碳,是盐与酸的反应,不属于中和反应,故A错误;
B、有盐和水生成的反应不一定是中和反应,如氢氧化钠与二氧化碳反应生成碳酸钠和水,也生成盐和水,但该反应不属于中和反应,故B错误;
、氮水是一种碱,能够中和工厂废水中含有的硫酸生成硫酸铵和水,故D正确;
、氢氧化钠固体溶于水放出热量,所以用氢氧化钠固体与稀盐酸反应不能验证中和反应放热,故D错误;
故选:。
A、根据纯碱是盐,其水溶液呈碱性进行分析;
B、根据反应物可以是非金属氧化物和碱反应进行分析;
C、根据氨水是碱,可以用来中和含有硫酸的废水进行分析;
D、根据氢氧化钠固体溶于水放热进行分析。
本题考查的是中和反应,解题关键是掌握中和反应的定义及应用;中和反应是酸和碱反应生成盐和水。
11.【答案】 氢氧化钠溶液 红 不能
【解析】解:稀盐酸和氢氧化钠溶液反应的化学方程式为:
由图象可知,值是开始时小于逐渐的增大到然后大于,可知原溶液显酸性,然后不断的加入碱性溶液,使升高,说明是把氢氧化钠溶液滴加到稀盐酸中.
当加入溶液的质量为时显酸性,盐酸过量,溶液中含有氯化氢,所以有两钟溶质:氯化钠和氯化氢;
当加入溶液的质量为时,溶液的大于,溶液显碱性,说明氢氧化钠溶液过量,滴加酚酞试液变红色;酚酞在酸性和中性的溶液中都为无色.若加入酚酞后溶液颜色为无色时不能说明恰好完全反应.
故答案为:;氢氧化钠溶液; ;红;不能.
氢氧化钠和盐酸反应能生成氯化钠和水;盐酸显酸性,小于,氢氧化钠溶液显碱性,大于;当盐酸过量时,盐酸和氢氧化钠反应后的溶液中含有氯化氢、氯化钠;显碱性的溶液能使酚酞试液变红色,氢氧化钠过量时反应后的溶液中含有氢氧化钠和氯化钠.
本题以图象的形式考查了酸碱中和反应时溶液的变化,以及物质间的质量关系,完成此题,可以依据已有的知识进行.
12.【答案】 偏大
【解析】解:碳酸显酸性,;
若用水润湿试纸测得稀盐酸的酸碱度,相当于酸性溶液用水稀释,则碱性减弱,测得的会偏答,
、可将试纸剪成几段使用,故说法正确。
B、不能将试纸直接插入待测液中,以免污染待测液,故说法错误。
C、将试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在试纸上,故说法正确。
D、不能将试纸润湿后放在表面皿上,若溶液显酸性或碱性,则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,故说法错误。
E、读数时,在内将试纸呈现的颜色与标准比色卡对照,故说法正确。
故答案为:
;
偏大;
。
根据碳酸显酸性分析溶液的;
根据实验操作的注意事项分析实验错误;
根据用试纸测定溶液的的方法,进行分析判断。
本题难度不大,掌握用试纸测定未知溶液的的方法、注意事项不能浸入待测液、不能用水润湿是正确解答本题的关键。
13.【答案】厕所清洁剂 厨房清洁剂 酸与碱发生中和反应
【解析】解:厕所清洁剂、雨水的都小于,显酸性,厕所清洁剂的小于雨水的,酸性更强.故填:厕所清洁剂.
厨房清洁剂的大于,显碱性,能使酚酞试液变红色.故填:厨房清洁剂.
厨房清洁剂与厕所清洁剂不能混合使用,其原因是厨房清洁剂和厕所清洁剂能够发生酸碱中和反应.故填:酸与碱发生中和反应.
当溶液的等于时,呈中性.当溶液的大于时,呈碱性.当溶液的小于时,呈酸性.
当溶液的小于时,随着的减小酸性增强;
酚酞试液遇酸性溶液不变色,遇碱性溶液变红,遇中性溶液不变色.
解答本题要掌握溶液的酸碱性和溶液大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.
14.【答案】取少量雨水放入试管,滴加紫色石蕊试液,若变红,雨水呈酸性;若变蓝,雨水呈碱性;若不变色,雨水呈中性;
是;不能;雨水的小于,属于酸雨,且越来越小,酸性逐渐增强;
肥皂水。
【解析】解:
用酸碱指示剂检验该雨水的酸碱性,方法是取少量雨水放入试管,滴加紫色石蕊试液,若变红,雨水呈酸性;若变蓝,雨水呈碱性;若不变色,雨水呈中性。
因为酸雨的小于,从检查的结果看,所有时间的雨水的都小于,是酸雨;
用试纸测溶液的酸碱度,数值为整数,不能用试纸测;
根据表格可知,雨水的小于,属于酸雨,且越来越小,酸性逐渐增强;
可用于检验该雨水是否为硬水的物质是肥皂水。
故答案为:
取少量雨水放入试管,滴加紫色石蕊试液,若变红,雨水呈酸性;若变蓝,雨水呈碱性;若不变色,雨水呈中性;
是;不能;雨水的小于,属于酸雨,且越来越小,酸性逐渐增强;
肥皂水。
本题考查酸雨及其成因,酸雨对自然界的危害极大,是人们很关注的问题,同时也是较为热门的考点之一。
第2页,共2页
第1页,共1页
一、单选题
下列操作不正确的是
A. 加热液体 B. 稀释浓硫酸
C. 取固体粉末 D. 检查气密性
下列实验现象描述正确的是
A. 把碘放入水中:碘很快溶解到水中形成棕色溶液
B. 一氧化碳在空气中燃烧:产生淡蓝色火焰,放出大量的热
C. 铁钉放在硫酸铜溶液中:银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
D. 打开浓盐酸的试剂瓶盖,瓶口会出现白色烟雾
如图模型分别表示生成氯化钠的不同化学反应,相关叙述正确的是
A. 图甲反应的实质是氢离子和氢氧根离子结合生成水分子
B. 紫色石蕊试液、铁、硝酸银溶液都能验证图甲反应中物质恰好完全反应
C. 图乙表示的反应中所涉及种物质,其中属于氧化物的有两种
D. 图乙表示的反应属于置换反应
医生在给病人看病时,可以通过人体口腔内唾液的约为来判断病情的程度,如下是医生对某病人口腔内唾液的进行的实验:在进食过程的最初分钟,酸性逐渐增强,之后酸性逐渐减弱,至分钟趋于正常。与上述事实最接近的图象是
A. B.
C. D.
如图是稀和溶液反应的变化曲线图,据图分析能得出的结论正确的是
A. 克是指加入溶液的质量
B. 点表示稀盐酸和加入的溶液质量一定相同
C. 点时,溶液的溶质为、
D. 取反应后溶液滴加溶液产生沉淀证明溶质只有
一些食物的近似如下,下列说法不正确的是
食物 葡萄汁 苹果汁 牛奶 玉米粥 鸡蛋清
A. 牛奶显酸性
B. 葡萄汁比苹果汁的酸性强
C. 鸡蛋清显碱性
D. 胃酸过多的人应少饮葡萄汁和苹果汁
苯甲酸是一种弱酸,具有酸的通性,可做食品防腐剂.下列关于苯甲酸说法不正确的是
A. 它是由种元素组成的 B. 苯甲酸可与发生中和反应
C. 其水溶液的 D. 苯甲酸是一种氧化物
甲同学用如图所示装置进行中和反应实验,为探究烧杯中的溶液是否恰好完全反应,他取出一定量反应后的溶液于试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论。乙同学认为甲同学得出的结论是错误的,于是乙同学又设计了下列实验方案,其中还不能证明氢氧化钠和稀硫酸恰好完全中和的是
A. 从烧杯中取样于试管中,滴加碳酸钠溶液,无气泡产生
B. 从烧杯中取样于试管中,加入粒,无气泡产生
C. 从烧杯中取样于试管中,加入氯化钡溶液,有白色沉淀产生
D. 从烧杯中取样于试管中,滴加紫色石蕊试液,试液不变色
某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液的变化,其图象如图所示,下列说法正确的是
A. 图中点所示溶液呈碱性
B. 图中点所示溶液中,含有的微粒是、
C. 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D. 由点到点的变化过程证明酸和碱发生了化学反应
下列关于中和反应的说法,正确的是
A. 碱性物质和稀盐酸混合发生的反应一定是中和反应
B. 有盐和水生成的反应一定是中和反应
C. 工厂废水中含有的硫酸可用氨水中和
D. 可用氢氧化钠固体与稀盐酸反应验证中和反应放热
二、填空题
在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.
该反应的化学方程式为:______.
该实验操作是将 ______滴加到另一种溶液中.
当加入溶液的质量为时,所得溶液中的溶质为写化学式 ______.
当加入溶液的质量为时,向所得溶液中滴加酚酞溶液,溶液呈 ______色.若加入酚酞后溶液颜色为无色时 ______填能或不能说明恰好完全反应.
某市初中化学实验操作考查内容为“溶液酸碱性的检验”。请根据实验回答下列问题。
测得碳酸饮料的 ______填“”“”或“”。
若用水润湿试纸测得稀盐酸的酸碱度,测得值将会 ______填偏大或偏小或不变。
下列使用试纸的方法中,正确的是 ______填字母。
A.将试纸剪成几段使用
B.将试纸直接插入待测液中
C.将试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在试纸上
D.将试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在试纸上
E.读数时,在秒内将试纸呈现的颜色与标准比色卡对照
下表列出生活中一些液体的;
液体 雨水 蒸馏水 厨房清洁剂 厕所清洁剂
上述液体中,酸性最强的是______,能使酚酞试液变红的是______.
厨房清洁剂与厕所清洁剂不能混合使用,其原因是______.
化学就在身边,为了应用所学知识,小明取刚降到地面的雨水进行研究。
若用酸碱指示剂检验该雨水的酸碱性,方法是__________________________________________。
若用计每隔几分钟测一次该雨水的,数据如下表:
测定时刻
该雨水是否为酸雨?________填“是”或“不是”。
上表数据的能否用试纸测得?________填“能”或“不能”。
从上表数据中,你还能得出该雨水的一个结论是______________________________________________________________________________。
可用于检验该雨水是否为硬水的物质是____________。
答案和解析
1.【答案】
【解析】解:、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的,图中所示操作正确。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散;一定不能把水注入浓硫酸中;图中所示操作错误。
C、取用粉末状药品,试管横放,用药匙或纸槽把药品送到试管底部,图中所示操作正确。
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确。
故选:。
A、根据给试管中的液体加热的方法进行分析判断。
B、根据浓硫酸的稀释方法酸入水,沿器壁,慢慢倒,不断搅进行分析判断。
C、根据向试管中装粉末状固体药品的方法“一斜、二送、三直立”进行分析判断。
D、根据检查装置气密性的方法进行分析判断。
本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.【答案】
【解析】解:、碘难溶于水,把碘放入水中,几乎不溶解,故选项说法错误。
B、一氧化碳在空气中燃烧,产生蓝色火焰,放出大量的热,故选项说法错误。
C、铁钉放在硫酸铜溶液中生成硫酸亚铁溶液和铜,银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色,故选项说法正确。
D、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气接触形成盐酸小液滴,瓶口上方有白雾产生,而不是白色烟雾,故选项说法错误。
故选:。
A、根据碘难溶于水,进行分析判断。
B、根据一氧化碳在空气中燃烧的现象,进行分析判断。
C、根据金属的化学性质,进行分析判断。
D、根据浓盐酸具有挥发性,进行分析判断。
本题难度不大,掌握浓盐酸具有挥发性、金属的化学性质、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾的区别、物质颜色的变化。
3.【答案】
【解析】解:、图甲反应是盐酸和氢氧化钠反应生成氯化钠和水,属于中和反应,反应的实质是氢离子和氢氧根离子结合生成水分子,故选项说法正确。
B、紫色石蕊试液、铁都能通过与酸的反应,验证图甲反应中物质恰好完全反应,氯化钠、盐酸均能与硝酸银溶液反应生成氯化银沉淀,不能验证图甲反应中物质恰好完全反应,故选项说法错误。
C、图乙表示的反应中所涉及种物质,反应物是和,生成物是和,属于氧化物的有一种,故选项说法错误。
D、图乙表示的反应生成物均为化合物,不属于置换反应,故选项说法错误。
故选:。
A、根据图甲反应是盐酸和氢氧化钠反应生成氯化钠和水,进行分析判断。
B、根据酸的化学性质,进行分析判断。
C、根据氧化物是只含有两种元素且其中一种元素是氧元素的化合物,进行分析判断。
D、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。
本题难度不大,掌握中和反应的实质、氧化物的特征、置换反应的特征等是正确解答本题的关键。
4.【答案】
【解析】解:在进食过程的最初分钟,酸性逐渐增强,溶液的应该减小,之后酸性逐渐减弱,溶液的应该增大,因此图中的曲线变化符合这一情况。
故选:。
当溶液的小于时,随着的减小酸性增强,随着的增大酸性减弱。
解答本题要掌握溶液的酸碱性与溶液大小之间的关系,只有这样才能对相关方面的问题做出正确的判断。
5.【答案】
【解析】解:、由图象可知,值是开始时大于逐渐的减小到然后小于,可知原溶液显碱性,然后不断的加入酸性溶液,使减小,说明是把稀盐酸滴加到氢氧化钠溶液中,克是指加入稀盐酸的质量,故选项说法错误。
B、由于不知道稀盐酸和氢氧化钠溶液的溶质质量分数,无法确定稀盐酸和氢氧化钠溶液的质量,故选项说法错误。
C、点时溶液的大于,溶液显碱性,说明氢氧化钠过量,所得溶液中的溶质为、,故选项说法正确。
D、稀盐酸与氯化钠均能与硝酸银溶液反应生成氯化银沉淀,不能确定证明溶质只有,故选项说法错误。
故选:。
A、根据图象中值的变化是从大于逐渐的减小到小于,进行分析判断。
B、根据不知道稀盐酸和氢氧化钠溶液的溶质质量分数,进行分析判断。
C、根据点时溶液的大于,进行分析判断。
D、根据稀盐酸与氯化钠均能与硝酸银溶液反应生成氯化银沉淀,进行分析判断。
本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键。
6.【答案】
【解析】解:、牛奶的小于,显酸性,故说法正确;
B.苹果汁、葡萄汁的都小于,都显酸性,但苹果汁的更小,酸性更强,故说法错误;
C.鸡蛋清的大于,显碱性,故说法正确;
D.对于胃酸过多的人比较适宜食用的食物是接近中性或偏碱性的食物,而不适宜吃酸性食物,葡萄汁和苹果汁显酸性,所以应少吃,故说法正确。
故选:。
当溶液的等于时,呈中性;当溶液的大于时,呈碱性;当溶液的小于时,呈酸性。当溶液的小于时,随着的减小酸性增强。
解答本题要掌握溶液的酸碱性和溶液大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论。
7.【答案】
【解析】解:、苯甲酸由、、三种元素组成,故A说法正确;
B、苯甲酸属于酸可与发生中和反应生成盐和水,故B说法正确;
C、苯甲酸属于酸,水溶液的,故C说法正确;
D、氧化物必须由两种元素组成,一种元素是氧元素,而苯甲酸由、、三种元素组成,故D说法错误。
故选:。
A、根据物质的元素组成考虑;、根据酸的化学性质考虑;、根据酸的考虑;、根据氧化物的特点考虑.
解答本题关键是知道物质的元素组成,知道中和反应的实质,知道氧化物的特点.
8.【答案】
【解析】解:、从烧杯中取样于试管中,滴加碳酸钠溶液,无气泡产生,说明反应后的溶液中不含稀硫酸,说明氢氧化钠和稀硫酸恰好完全中和,故选项不符合题意;
、从烧杯中取样于试管中,加入粒,无气泡产生,说明反应后的溶液中不含稀硫酸,说明氢氧化钠和稀硫酸恰好完全中和,故选项不符合题意;
、从烧杯中取样于试管中,加入氯化钡溶液,硫酸钠、硫酸均能与氯化钡溶液反应生成硫酸钡白色沉淀,不能说明氢氧化钠和稀硫酸恰好完全中和,故选项符合题意;
D、从烧杯中取样于试管中,滴加紫色石蕊试液,试液不变色,说明溶液显中性,说明氢氧化钠和稀硫酸恰好完全中和,故选项不符合题意;
故选:。
根据探究酸是否过量的方法,如可选用指示剂或能与酸反应有明显现象的物质,如碳酸盐,活泼金属等进行分析。
解答本题关键是要知道酸的化学性质及反应的明显现象。
9.【答案】
【解析】解:、点时溶液的小于,溶液显酸性,故选项说法错误;
、点时溶液的等于,溶液显中性,含有的溶质是,溶剂是水,所以含有的微粒有:、、;故选项说法错误;
、由图象可知,值是开始时大于逐渐的减小到然后小于,可知原溶液显碱性,然后不断的加入酸性溶液,使减小,说明是把稀硫酸滴加到氢氧化钠溶液中,故选项说法错误;
、由点到点的变化过程,碱性逐渐变弱,说明酸和碱发生了中和反应,故选项说法正确;
故选:。
A、根据 点时溶液的小于,进行分析判断;
、根据点时溶液的,进行分析判断;
、根据图象中值的变化是从大于逐渐的减小到小于,进行分析判断;
、根据点时溶液的小于,进行分析判断。
本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液 大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键。
10.【答案】
【解析】解:、碱性物质和稀盐酸混合发生的反应不一定是中和反应,如碳酸钠属于盐,其水溶液呈碱性,碳酸钠能够与稀盐酸反应生成氯化钠、水和二氧化碳,是盐与酸的反应,不属于中和反应,故A错误;
B、有盐和水生成的反应不一定是中和反应,如氢氧化钠与二氧化碳反应生成碳酸钠和水,也生成盐和水,但该反应不属于中和反应,故B错误;
、氮水是一种碱,能够中和工厂废水中含有的硫酸生成硫酸铵和水,故D正确;
、氢氧化钠固体溶于水放出热量,所以用氢氧化钠固体与稀盐酸反应不能验证中和反应放热,故D错误;
故选:。
A、根据纯碱是盐,其水溶液呈碱性进行分析;
B、根据反应物可以是非金属氧化物和碱反应进行分析;
C、根据氨水是碱,可以用来中和含有硫酸的废水进行分析;
D、根据氢氧化钠固体溶于水放热进行分析。
本题考查的是中和反应,解题关键是掌握中和反应的定义及应用;中和反应是酸和碱反应生成盐和水。
11.【答案】 氢氧化钠溶液 红 不能
【解析】解:稀盐酸和氢氧化钠溶液反应的化学方程式为:
由图象可知,值是开始时小于逐渐的增大到然后大于,可知原溶液显酸性,然后不断的加入碱性溶液,使升高,说明是把氢氧化钠溶液滴加到稀盐酸中.
当加入溶液的质量为时显酸性,盐酸过量,溶液中含有氯化氢,所以有两钟溶质:氯化钠和氯化氢;
当加入溶液的质量为时,溶液的大于,溶液显碱性,说明氢氧化钠溶液过量,滴加酚酞试液变红色;酚酞在酸性和中性的溶液中都为无色.若加入酚酞后溶液颜色为无色时不能说明恰好完全反应.
故答案为:;氢氧化钠溶液; ;红;不能.
氢氧化钠和盐酸反应能生成氯化钠和水;盐酸显酸性,小于,氢氧化钠溶液显碱性,大于;当盐酸过量时,盐酸和氢氧化钠反应后的溶液中含有氯化氢、氯化钠;显碱性的溶液能使酚酞试液变红色,氢氧化钠过量时反应后的溶液中含有氢氧化钠和氯化钠.
本题以图象的形式考查了酸碱中和反应时溶液的变化,以及物质间的质量关系,完成此题,可以依据已有的知识进行.
12.【答案】 偏大
【解析】解:碳酸显酸性,;
若用水润湿试纸测得稀盐酸的酸碱度,相当于酸性溶液用水稀释,则碱性减弱,测得的会偏答,
、可将试纸剪成几段使用,故说法正确。
B、不能将试纸直接插入待测液中,以免污染待测液,故说法错误。
C、将试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在试纸上,故说法正确。
D、不能将试纸润湿后放在表面皿上,若溶液显酸性或碱性,则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,故说法错误。
E、读数时,在内将试纸呈现的颜色与标准比色卡对照,故说法正确。
故答案为:
;
偏大;
。
根据碳酸显酸性分析溶液的;
根据实验操作的注意事项分析实验错误;
根据用试纸测定溶液的的方法,进行分析判断。
本题难度不大,掌握用试纸测定未知溶液的的方法、注意事项不能浸入待测液、不能用水润湿是正确解答本题的关键。
13.【答案】厕所清洁剂 厨房清洁剂 酸与碱发生中和反应
【解析】解:厕所清洁剂、雨水的都小于,显酸性,厕所清洁剂的小于雨水的,酸性更强.故填:厕所清洁剂.
厨房清洁剂的大于,显碱性,能使酚酞试液变红色.故填:厨房清洁剂.
厨房清洁剂与厕所清洁剂不能混合使用,其原因是厨房清洁剂和厕所清洁剂能够发生酸碱中和反应.故填:酸与碱发生中和反应.
当溶液的等于时,呈中性.当溶液的大于时,呈碱性.当溶液的小于时,呈酸性.
当溶液的小于时,随着的减小酸性增强;
酚酞试液遇酸性溶液不变色,遇碱性溶液变红,遇中性溶液不变色.
解答本题要掌握溶液的酸碱性和溶液大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.
14.【答案】取少量雨水放入试管,滴加紫色石蕊试液,若变红,雨水呈酸性;若变蓝,雨水呈碱性;若不变色,雨水呈中性;
是;不能;雨水的小于,属于酸雨,且越来越小,酸性逐渐增强;
肥皂水。
【解析】解:
用酸碱指示剂检验该雨水的酸碱性,方法是取少量雨水放入试管,滴加紫色石蕊试液,若变红,雨水呈酸性;若变蓝,雨水呈碱性;若不变色,雨水呈中性。
因为酸雨的小于,从检查的结果看,所有时间的雨水的都小于,是酸雨;
用试纸测溶液的酸碱度,数值为整数,不能用试纸测;
根据表格可知,雨水的小于,属于酸雨,且越来越小,酸性逐渐增强;
可用于检验该雨水是否为硬水的物质是肥皂水。
故答案为:
取少量雨水放入试管,滴加紫色石蕊试液,若变红,雨水呈酸性;若变蓝,雨水呈碱性;若不变色,雨水呈中性;
是;不能;雨水的小于,属于酸雨,且越来越小,酸性逐渐增强;
肥皂水。
本题考查酸雨及其成因,酸雨对自然界的危害极大,是人们很关注的问题,同时也是较为热门的考点之一。
第2页,共2页
第1页,共1页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
