4.3质量守恒定律课后培优练习-2021-2022学年九年级化学科粤版(2012)上册(有答案)
文档属性
| 名称 | 4.3质量守恒定律课后培优练习-2021-2022学年九年级化学科粤版(2012)上册(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 129.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-22 00:00:00 | ||
图片预览



文档简介
第四章4.3质量守恒定律课后培优2021_2022学年粤教版初中化学九年级上册
一、单选题(共19题)
1.构建化学基本观念是学好化学的基础,下列对化学基本观念的认识错误的是( )
A. 微粒观:保持C60化学性质的最小微粒是碳原子
B. 元素观:H2O是H、O元素组成的化合物,金刚石和石墨都是碳元素组成的单质
C. 变化观:石墨在一定条件下转化为金刚石,属于化学变化
D. 守恒观:6gC和16gO2充分反应后,一定生成22gCO2
2.2018年10月28日,我国首艘国产航母第三次试海成功,用到的金属钛主要通过下列反应制得:①2FeTio+6C+7C12=2X+2TiCl4+6CO,②TiCl4+2Mg=Ti+MgCl2 , X的化学式为()
A. FeCl3 B. FeCl2 C. Fe2O3 D. FeO
3.工业制漂白粉的化学方程式为:2Ca(OH)2+2Cl2═X+CaCl2+2H2O,则X为()
A. CaClO B. Ca(ClO)2 C. Ca(ClO)3 D. Ca(ClO)4
4.我国科学家寻找到新型催化剂,使低温工业产氢取得突破,反应过程如图所示,相关说法正确的是( )
A. 有利于氢能源的经济推广 B. 反应前后原子数目发生变化
C. 反应前后分子数目发生变化的法。证化 D. 反应前后催化剂化学性质发生改变
5.一定条件下密闭容器内发生某反应,反应过程中各物质的质量变化见下表。
物质 甲 乙 丙 丁
反应前 46g 100g 2g 0
反应中 23g 52g 46g m1
反应后 m2 4g m3 m4
其中未知数据错误的是( )
A. m1为29g B. m2为0g C. m3为90g D. m4为54g
6.在密闭容器里放入四种物质,使其在一定条件下充分反应,数据如表,下列表述正确的是( )
四种物质 甲 乙 丙 丁
反应前质量/g 25 15 1 5
反应后质量/g 11 未测 1 22
A. 未测值为3g B. 乙全部发生了反应 C. 甲与乙反应的质量比为14:3 D. 丙一定是催化剂
7.某纯净物R常温下即可分解,生成H2O和CO2 , 根据这一事实,下列的推理中,错误的是( )
A. R中一定含有碳元素 B. R一定为化合物 C. R中一定含有水 D. R的化学性质不稳定
8.能够直接用于验证质量守恒定律的实验是( )
A. B. C. D.
9.通常情况下铜不与稀硫酸反应,但将一小块铜片加入装有过量稀硫酸的烧杯中,在不断通入O2并加热的条件下,可以发生如下反应:2Cu+2H2SO4(稀)+O2 2CuSO4+2X,下列说法正确的是( )
A. 反应后烧杯中的物质只含有CuSO4和H2O B. 生成物X的化学式是H2O2
C. 反应后溶液由无色变为蓝色 D. 反应前后烧杯内液体的质量不变
10.A,B两种物质,在一定条件下只能发生下式所示化学反应A+B=C,现将agA和bgB在此条件下充分反应,分析得知剩余物为混合物,则生成C物质的质量为( )
A. 等于(a+b)g B. 小于(a+b)g C. 大于(a+b)g D. 以上答案都不符合题意
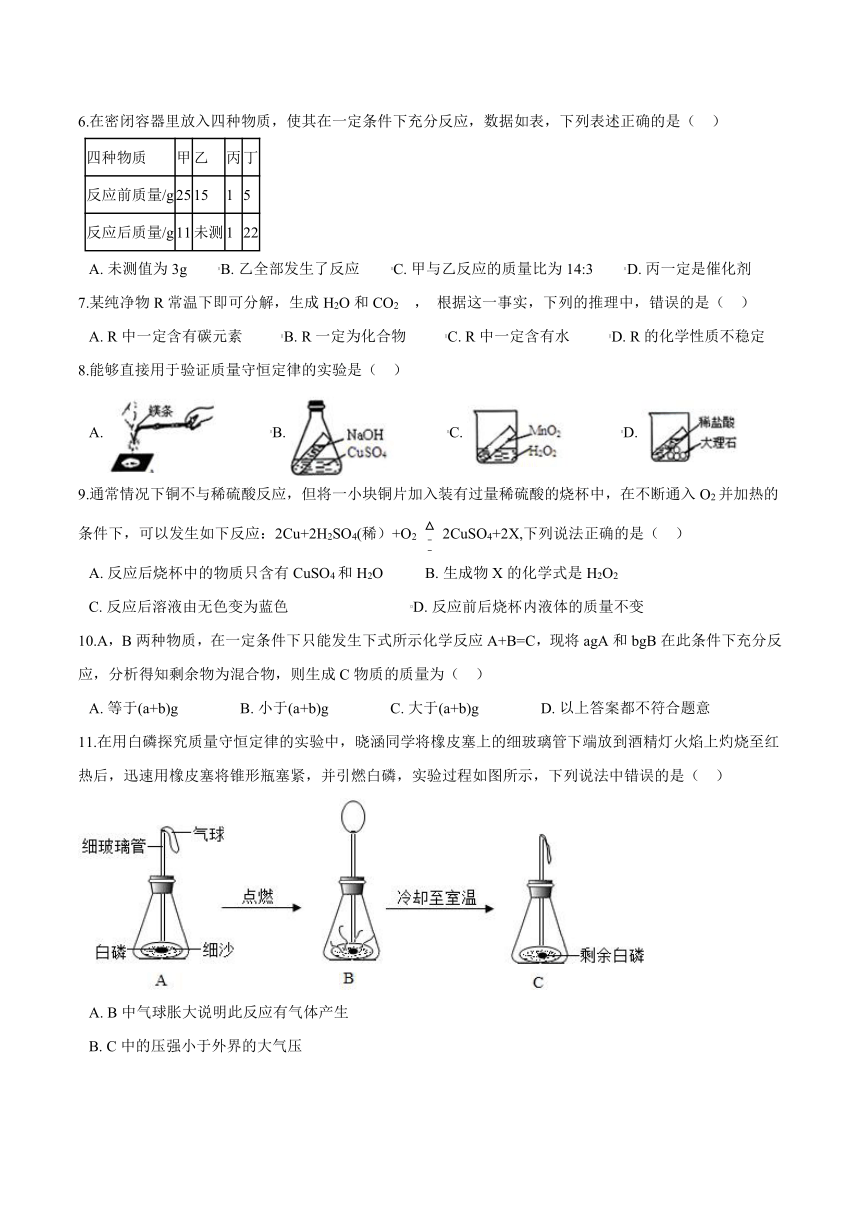
11.在用白磷探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如图所示,下列说法中错误的是( )
A. B中气球胀大说明此反应有气体产生
B. C中的压强小于外界的大气压
C. 此反应符合质量守恒定律
D. 用天平称量A系统的质量,天平保持平衡后,换成B系统,指针向右偏转
12.某化工厂进行电解食盐水生产,电解食盐水不能得到的是()
A. NaOH B. HNO3 C. H2 D. Cl2
13.把15.8g高锰酸钾装入试管中加热一段时间后,试管中锰元素质量为5.5g,则高锰酸钾的分解程度是()
A. 没有分解 B. 部分分解 C. 全部分解 D. 无法确定
14.在一个密闭的容器内有四种物质,在一定条件下充分反应测得反应前后各物质的质量如下表:下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 4 10 0 25
反应后质量/g X 21 5 9
A. 甲物质一定是催化剂。 B. 该反应属于分解反应。
C. 丁中一定包含了甲、乙、丙中所有的元素。 D. 反应中,丙与丁发生变化的质量比为5:9。
15.华为公司研发了一种以甲醇CH3OH为原料的新型手机电池,可连续使用1个月才充一次电,其电池反应原理为:2CH3OH+3X+4NaOH═2Na2CO3+6H2O,X的化学式是( )
A. O2 B. CO2 C. CH4 D. H2O
16.2017年4月20日,我国天舟一号货运飞船成功抵达空间站。 此次发射所使用的燃料为液氧和煤油,而四氧化二氮、偏二甲肼作为燃料因毒性较大已较少使用,其燃烧的反应 ,其中X的化学式为( )
A. C2H4 B. N2 C. NO D. NH3
17.现有C4H8、CnH2n组成的可燃性混合物140 g,完全燃烧后生成CO2的质量是( )
A. 120 g B. 360 g C. 440 g D. 560 g
18.某纯净物R常温下即可分解,生成NH3、H2O和CO2。根据这一事实,下列的推理中,错误的是( )
A. R中一定含有氮元素 B. R中一定含有水 C. R一定为化合物 D. R的化学性质不稳定
19.在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法错误的是( )
物质 甲 乙 丙 丁
反应前物质的质量(g) 8 32 5 4
反应后物质的质量(g) 16 X 5 24
A. 该反应为分解反应 B. 丙可能是该反应的催化剂
C. 反应的生成物是甲和丁 D. X的值为28
二、综合题(共4题;共15分)
20.从宏观和微观上理解质量守恒定律可归纳为五个“不变”、两个“一定变”和一个“可能变”.请按要求填写正确选项的序号.
①物质的种类 ②元素的种类 ③原子的种类 ④原子的质量 ⑤原子的数目 ⑥分子的种类 ⑦分子的数目 ⑧反应物和生成物的总质量
(1).五个“不变”:从宏观上看, 和 不变;从微观上看, 、 和 不变.
(2).两个“一定变”:从宏观上看, 一定变;从微观上看, 一定变.
(3).一个“可能变”: 可能变.
21.可用甲醇(CH3OH)直接制得用作汽车燃料的氢气,其原理示意图如下:
(1)从元素守恒角度解释甲醇能产生氢气的原因:________。
(2)从微观角度分析,一定量常压氢气经过压缩机后,改变的是________。
22.H2O2 是一种重要的化学品,其早期制备方法如下图所示。
(1)反应 I 的化学方程式为 2Ba(NO3)2=2BaO + O 2 ↑ +4________↑。请补齐生成物。
(2)Ba(NO3)2 中氮元素的化合价为________。
(3)减压能够降低蒸馏温度。从 H2O2 的化学性质角度说明 IV 中采用减压蒸馏的原因:________。
23.工业上用高温煅烧氢氧化铝制备氧化铝。氢氧化铝在回转窑经高温煅烧,反应过程中产生烟气的主要成分是氧化铝、氮氧化物等。回收氧化铝、降低氮氧化物排放的烟气净化流程如下图所示。
(1)旋风分离器和金属滤袋除尘器的作用是分离并得到烟气中的氧化铝,该过程发生的变化是________(填“物理”、“化学”)变化。
(2)SCR工艺中反应的化学方程式为6NO2+8NH3 7X+12H2O,其中X是________(填化学式)。
答案部分
一、单选题
1.【答案】 A
2.【答案】 A
3.【答案】 B
4.【答案】 A
5.【答案】 A
6.【答案】 C
7.【答案】 C
8.【答案】 B
9.【答案】 C
10.【答案】 B
11.【答案】 A
12.【答案】 B
13.【答案】 D
14.【答案】 B
15.【答案】 A
16.【答案】 B
17.【答案】 C
18.【答案】 B
19.【答案】 D
二、综合题
20.【答案】 (1)②;⑧;③;④;⑤
(2)①;⑥
(3)⑦
21.【答案】 (1)化学反应前后元素种类不变,氢气中只含有氢元素,甲醇中含有氢元素,
(2)分子间隔
22.【答案】 (1)NO2
(2)+5
(3)因为H2O2受热易分解,减压蒸馏能降低温度,减少H2O2分解
(
…………○…………外…………○…………装…………○…………订…………○…………线…………○…………
) (
※※请※※不※※要※※在※※装※※订※※线※※内※※答※※题※※
) (
…………○…………内…………○…………装…………○…………订…………○…………线…………○…………
)
23.【答案】 (1)物理
(2)N2
一、单选题(共19题)
1.构建化学基本观念是学好化学的基础,下列对化学基本观念的认识错误的是( )
A. 微粒观:保持C60化学性质的最小微粒是碳原子
B. 元素观:H2O是H、O元素组成的化合物,金刚石和石墨都是碳元素组成的单质
C. 变化观:石墨在一定条件下转化为金刚石,属于化学变化
D. 守恒观:6gC和16gO2充分反应后,一定生成22gCO2
2.2018年10月28日,我国首艘国产航母第三次试海成功,用到的金属钛主要通过下列反应制得:①2FeTio+6C+7C12=2X+2TiCl4+6CO,②TiCl4+2Mg=Ti+MgCl2 , X的化学式为()
A. FeCl3 B. FeCl2 C. Fe2O3 D. FeO
3.工业制漂白粉的化学方程式为:2Ca(OH)2+2Cl2═X+CaCl2+2H2O,则X为()
A. CaClO B. Ca(ClO)2 C. Ca(ClO)3 D. Ca(ClO)4
4.我国科学家寻找到新型催化剂,使低温工业产氢取得突破,反应过程如图所示,相关说法正确的是( )
A. 有利于氢能源的经济推广 B. 反应前后原子数目发生变化
C. 反应前后分子数目发生变化的法。证化 D. 反应前后催化剂化学性质发生改变
5.一定条件下密闭容器内发生某反应,反应过程中各物质的质量变化见下表。
物质 甲 乙 丙 丁
反应前 46g 100g 2g 0
反应中 23g 52g 46g m1
反应后 m2 4g m3 m4
其中未知数据错误的是( )
A. m1为29g B. m2为0g C. m3为90g D. m4为54g
6.在密闭容器里放入四种物质,使其在一定条件下充分反应,数据如表,下列表述正确的是( )
四种物质 甲 乙 丙 丁
反应前质量/g 25 15 1 5
反应后质量/g 11 未测 1 22
A. 未测值为3g B. 乙全部发生了反应 C. 甲与乙反应的质量比为14:3 D. 丙一定是催化剂
7.某纯净物R常温下即可分解,生成H2O和CO2 , 根据这一事实,下列的推理中,错误的是( )
A. R中一定含有碳元素 B. R一定为化合物 C. R中一定含有水 D. R的化学性质不稳定
8.能够直接用于验证质量守恒定律的实验是( )
A. B. C. D.
9.通常情况下铜不与稀硫酸反应,但将一小块铜片加入装有过量稀硫酸的烧杯中,在不断通入O2并加热的条件下,可以发生如下反应:2Cu+2H2SO4(稀)+O2 2CuSO4+2X,下列说法正确的是( )
A. 反应后烧杯中的物质只含有CuSO4和H2O B. 生成物X的化学式是H2O2
C. 反应后溶液由无色变为蓝色 D. 反应前后烧杯内液体的质量不变
10.A,B两种物质,在一定条件下只能发生下式所示化学反应A+B=C,现将agA和bgB在此条件下充分反应,分析得知剩余物为混合物,则生成C物质的质量为( )
A. 等于(a+b)g B. 小于(a+b)g C. 大于(a+b)g D. 以上答案都不符合题意
11.在用白磷探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如图所示,下列说法中错误的是( )
A. B中气球胀大说明此反应有气体产生
B. C中的压强小于外界的大气压
C. 此反应符合质量守恒定律
D. 用天平称量A系统的质量,天平保持平衡后,换成B系统,指针向右偏转
12.某化工厂进行电解食盐水生产,电解食盐水不能得到的是()
A. NaOH B. HNO3 C. H2 D. Cl2
13.把15.8g高锰酸钾装入试管中加热一段时间后,试管中锰元素质量为5.5g,则高锰酸钾的分解程度是()
A. 没有分解 B. 部分分解 C. 全部分解 D. 无法确定
14.在一个密闭的容器内有四种物质,在一定条件下充分反应测得反应前后各物质的质量如下表:下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 4 10 0 25
反应后质量/g X 21 5 9
A. 甲物质一定是催化剂。 B. 该反应属于分解反应。
C. 丁中一定包含了甲、乙、丙中所有的元素。 D. 反应中,丙与丁发生变化的质量比为5:9。
15.华为公司研发了一种以甲醇CH3OH为原料的新型手机电池,可连续使用1个月才充一次电,其电池反应原理为:2CH3OH+3X+4NaOH═2Na2CO3+6H2O,X的化学式是( )
A. O2 B. CO2 C. CH4 D. H2O
16.2017年4月20日,我国天舟一号货运飞船成功抵达空间站。 此次发射所使用的燃料为液氧和煤油,而四氧化二氮、偏二甲肼作为燃料因毒性较大已较少使用,其燃烧的反应 ,其中X的化学式为( )
A. C2H4 B. N2 C. NO D. NH3
17.现有C4H8、CnH2n组成的可燃性混合物140 g,完全燃烧后生成CO2的质量是( )
A. 120 g B. 360 g C. 440 g D. 560 g
18.某纯净物R常温下即可分解,生成NH3、H2O和CO2。根据这一事实,下列的推理中,错误的是( )
A. R中一定含有氮元素 B. R中一定含有水 C. R一定为化合物 D. R的化学性质不稳定
19.在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法错误的是( )
物质 甲 乙 丙 丁
反应前物质的质量(g) 8 32 5 4
反应后物质的质量(g) 16 X 5 24
A. 该反应为分解反应 B. 丙可能是该反应的催化剂
C. 反应的生成物是甲和丁 D. X的值为28
二、综合题(共4题;共15分)
20.从宏观和微观上理解质量守恒定律可归纳为五个“不变”、两个“一定变”和一个“可能变”.请按要求填写正确选项的序号.
①物质的种类 ②元素的种类 ③原子的种类 ④原子的质量 ⑤原子的数目 ⑥分子的种类 ⑦分子的数目 ⑧反应物和生成物的总质量
(1).五个“不变”:从宏观上看, 和 不变;从微观上看, 、 和 不变.
(2).两个“一定变”:从宏观上看, 一定变;从微观上看, 一定变.
(3).一个“可能变”: 可能变.
21.可用甲醇(CH3OH)直接制得用作汽车燃料的氢气,其原理示意图如下:
(1)从元素守恒角度解释甲醇能产生氢气的原因:________。
(2)从微观角度分析,一定量常压氢气经过压缩机后,改变的是________。
22.H2O2 是一种重要的化学品,其早期制备方法如下图所示。
(1)反应 I 的化学方程式为 2Ba(NO3)2=2BaO + O 2 ↑ +4________↑。请补齐生成物。
(2)Ba(NO3)2 中氮元素的化合价为________。
(3)减压能够降低蒸馏温度。从 H2O2 的化学性质角度说明 IV 中采用减压蒸馏的原因:________。
23.工业上用高温煅烧氢氧化铝制备氧化铝。氢氧化铝在回转窑经高温煅烧,反应过程中产生烟气的主要成分是氧化铝、氮氧化物等。回收氧化铝、降低氮氧化物排放的烟气净化流程如下图所示。
(1)旋风分离器和金属滤袋除尘器的作用是分离并得到烟气中的氧化铝,该过程发生的变化是________(填“物理”、“化学”)变化。
(2)SCR工艺中反应的化学方程式为6NO2+8NH3 7X+12H2O,其中X是________(填化学式)。
答案部分
一、单选题
1.【答案】 A
2.【答案】 A
3.【答案】 B
4.【答案】 A
5.【答案】 A
6.【答案】 C
7.【答案】 C
8.【答案】 B
9.【答案】 C
10.【答案】 B
11.【答案】 A
12.【答案】 B
13.【答案】 D
14.【答案】 B
15.【答案】 A
16.【答案】 B
17.【答案】 C
18.【答案】 B
19.【答案】 D
二、综合题
20.【答案】 (1)②;⑧;③;④;⑤
(2)①;⑥
(3)⑦
21.【答案】 (1)化学反应前后元素种类不变,氢气中只含有氢元素,甲醇中含有氢元素,
(2)分子间隔
22.【答案】 (1)NO2
(2)+5
(3)因为H2O2受热易分解,减压蒸馏能降低温度,减少H2O2分解
(
…………○…………外…………○…………装…………○…………订…………○…………线…………○…………
) (
※※请※※不※※要※※在※※装※※订※※线※※内※※答※※题※※
) (
…………○…………内…………○…………装…………○…………订…………○…………线…………○…………
)
23.【答案】 (1)物理
(2)N2
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
