7.4结晶现象 同步训练-2021-2022学年科粤版化学九年级下册(有答案)
文档属性
| 名称 | 7.4结晶现象 同步训练-2021-2022学年科粤版化学九年级下册(有答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 157.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-22 00:00:00 | ||
图片预览



文档简介
7.4结晶现象同步训练
副标题
学校:___________姓名:___________班级:___________考号:___________
一、单选题(本大题共12小题,共24.0分)
实验室在进行过滤的操作实验时,没有使用的实验仪器是( )
A. 烧杯 B. 漏斗 C. 铁架台 D. 天平
下列关于海水晒盐原理的说法正确的是()
A. 日晒风吹使海水中的氯化钠蒸发
B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发、晶体析出
D. 日晒风吹使氯化钠的溶解度变小
下列实验基本操作中,正确的是( )
A. 熄灭酒精灯 B. 倾倒液体
C. 气体验满 D. 液体过滤
下列说法不正确的是( )
A. 工业废水处理达标后再排放
B. 矿泉水是纯净物
C. 生活中可用煮沸的方法降低水的硬度
D. 过滤时玻璃棒的作用是引流
下列关于过滤的实验操作错误的是( )
A. 过滤时玻璃棒斜靠在三层滤纸一边
B. 过滤时漏斗下端管口紧靠烧杯内壁
C. 过滤时,若流速慢可用玻璃棒在漏斗内搅拌使流速加快
D. 过滤时用玻璃棒引流
水是重要资源,下列说法正确的是( )
A. 活性炭的吸附作用可使海水转化为淡水
B. 水中的Ca2+、Mg2+可用过滤的方法除去
C. 电解水得到的H2和O2,质量比为2:1
D. 液态水变成水蒸气,分子间间隔增大
下列变化过程中,与其他变化不是同一类型的是()
A. 过氧乙酸溶液杀菌 B. 铁块拉制成铁丝
C. 过滤除去海水中的泥沙 D. 试管因受热不均匀炸裂
下列实验操作和分析都正确的是( )
操作 分析
A 用燃着的木条伸入集气瓶底部来检验CO2是否收集满 因为CO2的密度比空气大
B 过滤操作时,用玻璃棒 目的是搅拌,加快过滤速度
C 木炭还原三氧化二铁时,试管口向下倾斜 目的是防止冷凝水回流到热的试管底部,炸裂试管
D 将燃着的木条伸入装有空气和呼出气体的集气瓶中 目的是证明呼出气体中二氧化碳的含量比空气中多
A. A B. B C. C D. D
如表是KCl固体在不同温度时的溶解度。下列说法错误的是( )
温度/℃ 0 20 40 60 80
溶解度/g 27.6 34.0 40.0 45.5 51.1
A. KCl固体的溶解度随温度的升高而增大
B. 60℃的KCl饱和溶液降温后会有晶体析出
C. 80℃时,KCl固体的溶解度是51.1g
D. 20℃时,KCl饱和溶液的溶质质量分数为34.0%
20℃某物质的溶解度是40g,现将20℃、1kg该物质的饱和溶液蒸发掉15克水后,析出晶体(不含结晶水)的质量是( )
A. 12克 B. 4.3克 C. 6克 D. 5克
如图是恒温下模拟海水晒盐过程的示意图,下列说法正确的是( )
A. 四杯溶液中溶质质量分数最大的是丁
B. 四杯溶液中溶质质量分数最小的是甲
C. 四杯溶液中溶质质量分数最小的是乙
D. 在整个过程中,食盐的溶解度发生了变化
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A. 随温度升高,a、b、c三种物质的溶解度均增大
B. t2℃时 ,把50 g a放入50 g 水中,可得到100 g a的饱和溶液
C. 将t2℃时等质量的 a、b饱和溶液降温到t1℃ ,析出晶体的质量a大于b
D. t1℃时 ,a、c的溶解度相等,则两溶液的溶质质量分数也相等
二、填空题(本大题共3小题,共24.0分)
请从下列选项中选择适当的物质填空(填字母序号)。
A.氯化钠 B.氮气 C.石墨 D.镁 E.氧气 F.红磷
(1)可用于制铅笔芯 ______;
(2)重要的调味品 ______;
(3)常用作保护气 ______;
(4)用于急救病人的是 ______;
(5)可制作照明弹的是 ______;
(6)可制用作烟幕弹的是 ______。
提高节水意识,培养良好的用水习惯,是我们每个公民的义务和责任,请根据所学知识回答下列问题:
(1)矿泉水、海水、蒸馏水、雨水都是生活中常见的“水”,其中属于纯净物的是 ______。海水中含有大量的氯化钠(NaCl),氯化钠是由 ______(填离子符号)和Cl-构成的。
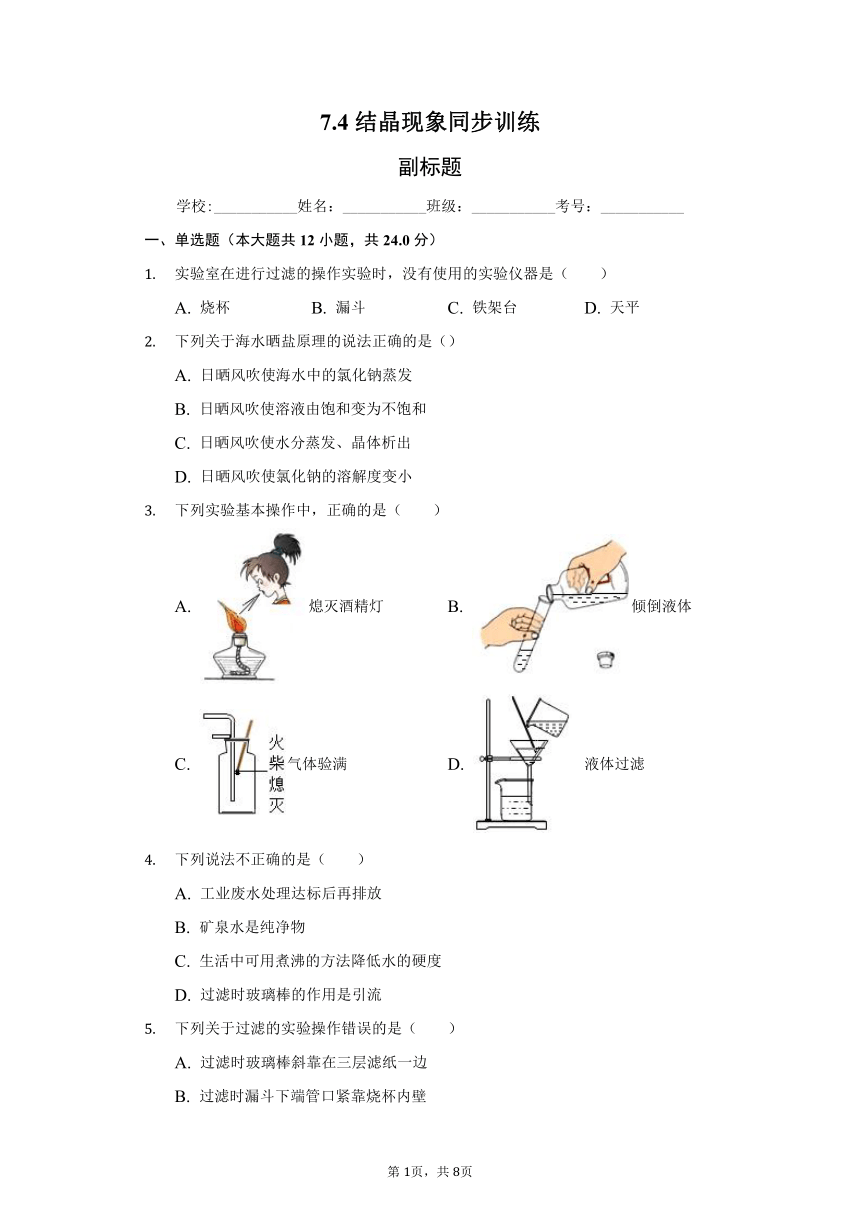
(2)“生命吸管”是一种可以随身携带的小型水净化器,主要处理步骤与自来水的净化过程相似,其简要流程如图所示。
滤网的作用相当于过滤操作,实验室进行该操作时,用到的玻璃仪器有玻璃棒、烧杯、______,其中玻璃棒的作用是 ______,检查此“生命吸管”净化后的水属于硬水还是软水,可向净化后的水样中加入 ______。
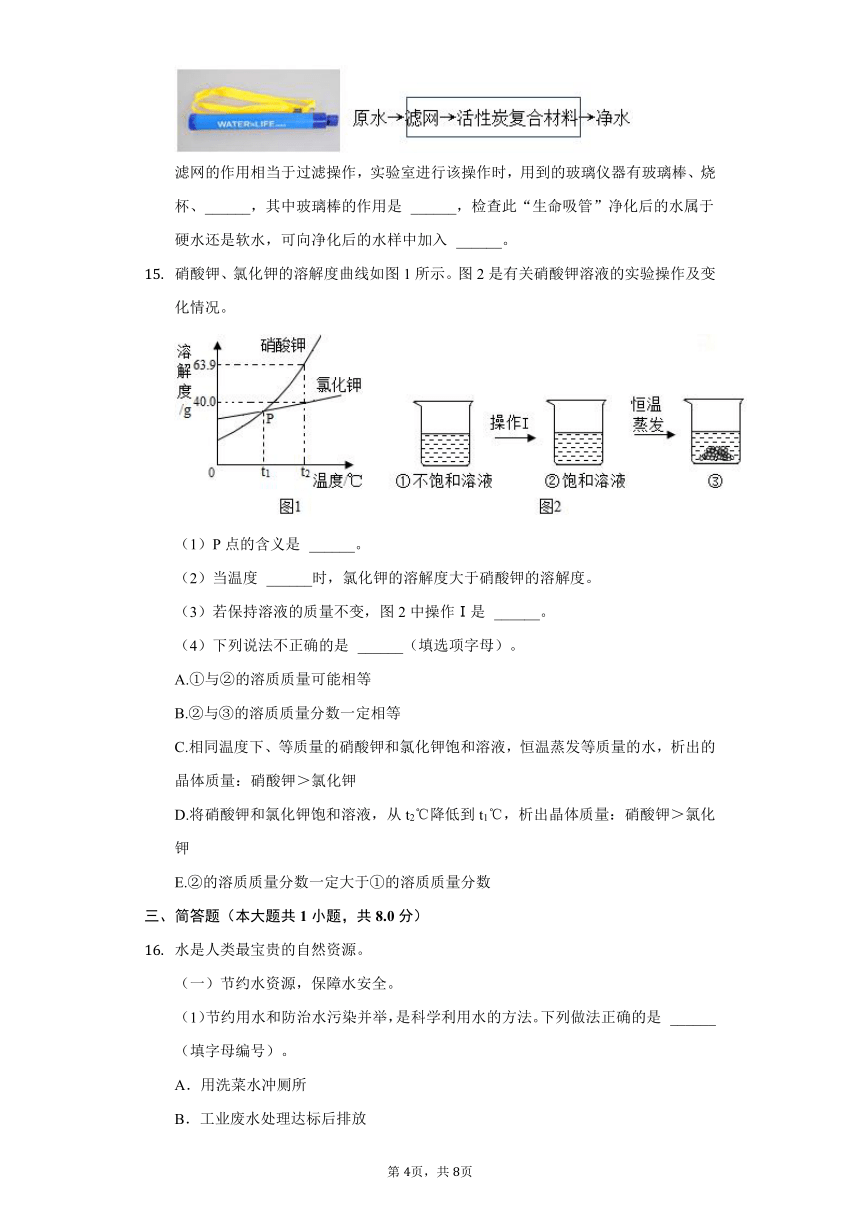
硝酸钾、氯化钾的溶解度曲线如图1所示。图2是有关硝酸钾溶液的实验操作及变化情况。
(1)P点的含义是 ______。
(2)当温度 ______时,氯化钾的溶解度大于硝酸钾的溶解度。
(3)若保持溶液的质量不变,图2中操作Ⅰ是 ______。
(4)下列说法不正确的是 ______(填选项字母)。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.相同温度下、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.将硝酸钾和氯化钾饱和溶液,从t2℃降低到t1℃,析出晶体质量:硝酸钾>氯化钾
E.②的溶质质量分数一定大于①的溶质质量分数
三、简答题(本大题共1小题,共8.0分)
水是人类最宝贵的自然资源。
(一)节约水资源,保障水安全。
(1)节约用水和防治水污染并举,是科学利用水的方法。下列做法正确的是 ______(填字母编号)。
A.用洗菜水冲厕所
B.工业废水处理达标后排放
C.生活污水任意排放
(2)自然界中的水一般要净化后才能使用。吸附、过滤、蒸馏等三种净化水的操作中,单一操作相对净化程度最高的是 ______。
(二)小明收集到一瓶浑浊的长江水,他模拟自来水厂的净水过程,最终制成自来水。其实验过程如图所示。
请回答以下问题:
(1)通过操作①可除去水样中的不溶性杂质,操作①的名称是 ______,该操作中玻璃棒的作用是______,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 ______(填字母编号)。
A.漏斗内的滤纸有破损
B.漏斗下端未靠在烧杯内壁
C.漏斗内液面高于滤纸的边缘
(2)生活中常用 ______的方法将硬水软化。
(3)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这是水壶中出现水垢的原因之一。试写出Ca(HCO3)2受热分解的化学方程式______。
四、实验题(本大题共1小题,共10.0分)
某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:
(1)操作①、②、③依次为图中的(填字母)______、b、______.
(2)若NaCl的产率偏低(产率=×100%),则可能的原因是(填字母)______.
A.过滤时滤纸有破损 B.蒸发时有固体溅出 C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5%NaCl溶液50.0g,需称取NaCl______g,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、______.
1.【答案】D
2.【答案】C
3.【答案】D
4.【答案】B
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】C
9.【答案】D
10.【答案】C
11.【答案】B
12.【答案】C
13.【答案】C A B E D F
14.【答案】蒸馏水 Na+ 漏斗 引流 肥皂水
15.【答案】t1℃时,硝酸钾和氯化钾的溶解度相等 小于t1℃ 降低温度 CDE
16.【答案】AB 蒸馏 过滤 引流 AC 煮沸 Ca(HCO3)2CaCO3↓+H2O+CO2↑
17.【答案】(1)c;a;
(2)BC;
(3)2.5;量筒
第2页,共2页
第1页,共1页
副标题
学校:___________姓名:___________班级:___________考号:___________
一、单选题(本大题共12小题,共24.0分)
实验室在进行过滤的操作实验时,没有使用的实验仪器是( )
A. 烧杯 B. 漏斗 C. 铁架台 D. 天平
下列关于海水晒盐原理的说法正确的是()
A. 日晒风吹使海水中的氯化钠蒸发
B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发、晶体析出
D. 日晒风吹使氯化钠的溶解度变小
下列实验基本操作中,正确的是( )
A. 熄灭酒精灯 B. 倾倒液体
C. 气体验满 D. 液体过滤
下列说法不正确的是( )
A. 工业废水处理达标后再排放
B. 矿泉水是纯净物
C. 生活中可用煮沸的方法降低水的硬度
D. 过滤时玻璃棒的作用是引流
下列关于过滤的实验操作错误的是( )
A. 过滤时玻璃棒斜靠在三层滤纸一边
B. 过滤时漏斗下端管口紧靠烧杯内壁
C. 过滤时,若流速慢可用玻璃棒在漏斗内搅拌使流速加快
D. 过滤时用玻璃棒引流
水是重要资源,下列说法正确的是( )
A. 活性炭的吸附作用可使海水转化为淡水
B. 水中的Ca2+、Mg2+可用过滤的方法除去
C. 电解水得到的H2和O2,质量比为2:1
D. 液态水变成水蒸气,分子间间隔增大
下列变化过程中,与其他变化不是同一类型的是()
A. 过氧乙酸溶液杀菌 B. 铁块拉制成铁丝
C. 过滤除去海水中的泥沙 D. 试管因受热不均匀炸裂
下列实验操作和分析都正确的是( )
操作 分析
A 用燃着的木条伸入集气瓶底部来检验CO2是否收集满 因为CO2的密度比空气大
B 过滤操作时,用玻璃棒 目的是搅拌,加快过滤速度
C 木炭还原三氧化二铁时,试管口向下倾斜 目的是防止冷凝水回流到热的试管底部,炸裂试管
D 将燃着的木条伸入装有空气和呼出气体的集气瓶中 目的是证明呼出气体中二氧化碳的含量比空气中多
A. A B. B C. C D. D
如表是KCl固体在不同温度时的溶解度。下列说法错误的是( )
温度/℃ 0 20 40 60 80
溶解度/g 27.6 34.0 40.0 45.5 51.1
A. KCl固体的溶解度随温度的升高而增大
B. 60℃的KCl饱和溶液降温后会有晶体析出
C. 80℃时,KCl固体的溶解度是51.1g
D. 20℃时,KCl饱和溶液的溶质质量分数为34.0%
20℃某物质的溶解度是40g,现将20℃、1kg该物质的饱和溶液蒸发掉15克水后,析出晶体(不含结晶水)的质量是( )
A. 12克 B. 4.3克 C. 6克 D. 5克
如图是恒温下模拟海水晒盐过程的示意图,下列说法正确的是( )
A. 四杯溶液中溶质质量分数最大的是丁
B. 四杯溶液中溶质质量分数最小的是甲
C. 四杯溶液中溶质质量分数最小的是乙
D. 在整个过程中,食盐的溶解度发生了变化
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A. 随温度升高,a、b、c三种物质的溶解度均增大
B. t2℃时 ,把50 g a放入50 g 水中,可得到100 g a的饱和溶液
C. 将t2℃时等质量的 a、b饱和溶液降温到t1℃ ,析出晶体的质量a大于b
D. t1℃时 ,a、c的溶解度相等,则两溶液的溶质质量分数也相等
二、填空题(本大题共3小题,共24.0分)
请从下列选项中选择适当的物质填空(填字母序号)。
A.氯化钠 B.氮气 C.石墨 D.镁 E.氧气 F.红磷
(1)可用于制铅笔芯 ______;
(2)重要的调味品 ______;
(3)常用作保护气 ______;
(4)用于急救病人的是 ______;
(5)可制作照明弹的是 ______;
(6)可制用作烟幕弹的是 ______。
提高节水意识,培养良好的用水习惯,是我们每个公民的义务和责任,请根据所学知识回答下列问题:
(1)矿泉水、海水、蒸馏水、雨水都是生活中常见的“水”,其中属于纯净物的是 ______。海水中含有大量的氯化钠(NaCl),氯化钠是由 ______(填离子符号)和Cl-构成的。
(2)“生命吸管”是一种可以随身携带的小型水净化器,主要处理步骤与自来水的净化过程相似,其简要流程如图所示。
滤网的作用相当于过滤操作,实验室进行该操作时,用到的玻璃仪器有玻璃棒、烧杯、______,其中玻璃棒的作用是 ______,检查此“生命吸管”净化后的水属于硬水还是软水,可向净化后的水样中加入 ______。
硝酸钾、氯化钾的溶解度曲线如图1所示。图2是有关硝酸钾溶液的实验操作及变化情况。
(1)P点的含义是 ______。
(2)当温度 ______时,氯化钾的溶解度大于硝酸钾的溶解度。
(3)若保持溶液的质量不变,图2中操作Ⅰ是 ______。
(4)下列说法不正确的是 ______(填选项字母)。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.相同温度下、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.将硝酸钾和氯化钾饱和溶液,从t2℃降低到t1℃,析出晶体质量:硝酸钾>氯化钾
E.②的溶质质量分数一定大于①的溶质质量分数
三、简答题(本大题共1小题,共8.0分)
水是人类最宝贵的自然资源。
(一)节约水资源,保障水安全。
(1)节约用水和防治水污染并举,是科学利用水的方法。下列做法正确的是 ______(填字母编号)。
A.用洗菜水冲厕所
B.工业废水处理达标后排放
C.生活污水任意排放
(2)自然界中的水一般要净化后才能使用。吸附、过滤、蒸馏等三种净化水的操作中,单一操作相对净化程度最高的是 ______。
(二)小明收集到一瓶浑浊的长江水,他模拟自来水厂的净水过程,最终制成自来水。其实验过程如图所示。
请回答以下问题:
(1)通过操作①可除去水样中的不溶性杂质,操作①的名称是 ______,该操作中玻璃棒的作用是______,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 ______(填字母编号)。
A.漏斗内的滤纸有破损
B.漏斗下端未靠在烧杯内壁
C.漏斗内液面高于滤纸的边缘
(2)生活中常用 ______的方法将硬水软化。
(3)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这是水壶中出现水垢的原因之一。试写出Ca(HCO3)2受热分解的化学方程式______。
四、实验题(本大题共1小题,共10.0分)
某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:
(1)操作①、②、③依次为图中的(填字母)______、b、______.
(2)若NaCl的产率偏低(产率=×100%),则可能的原因是(填字母)______.
A.过滤时滤纸有破损 B.蒸发时有固体溅出 C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5%NaCl溶液50.0g,需称取NaCl______g,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、______.
1.【答案】D
2.【答案】C
3.【答案】D
4.【答案】B
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】C
9.【答案】D
10.【答案】C
11.【答案】B
12.【答案】C
13.【答案】C A B E D F
14.【答案】蒸馏水 Na+ 漏斗 引流 肥皂水
15.【答案】t1℃时,硝酸钾和氯化钾的溶解度相等 小于t1℃ 降低温度 CDE
16.【答案】AB 蒸馏 过滤 引流 AC 煮沸 Ca(HCO3)2CaCO3↓+H2O+CO2↑
17.【答案】(1)c;a;
(2)BC;
(3)2.5;量筒
第2页,共2页
第1页,共1页
