10.1常见的酸和碱第2课时同步练习-2020-2021学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 10.1常见的酸和碱第2课时同步练习-2020-2021学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 216.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-23 00:00:00 | ||
图片预览


文档简介
10.1 常见的酸和碱(第2课时)
【基础练习】
1. 日常生活中的下列物质能使紫色石蕊溶液变红的是( )
A.蒸馏水 B.食盐水
C.白醋 D.石灰水
2. 下列物质中,不能与稀盐酸发生反应的是 ( )
A.Fe2O3 B.CaCO3
C.CO2 D.Mg
3. 下列关于H2SO4性质的描述中,不属于酸的通性的是 ( )
A.使紫色石蕊溶液变红
B.稀硫酸与氧化铜反应
C.浓硫酸滴到白纸上使纸变黑
D.稀硫酸与铁反应放出氢气
4. 白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易被蚁酸腐蚀的是( )
A.镀锌水管
B.铜制塑像
C.大理石栏杆
D.铝合金门窗
5. 食醋里通常含有3%~5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列说法不正确的是 ( )
A.产生的气体是二氧化碳
B.醋酸可以使酚酞溶液变红
C.可用食醋除去暖水瓶中的水垢
D.不宜用铝制容器盛装食醋
6. 下列物质的变化中,只有加酸才能一步实现的是 ( )
将生锈的铁钉投入过量的稀盐酸中,首先观察到的现象是 ,发生反应的化学方程式为 ;反应一段时间后,又观察到有气泡产生,发生反应的化学方程式为 。
8. 某同学在实验室中看到铁钉表面附着红色物质,分不出是铁锈还是铜,为证明红色物质的成分,将其“刮”下来,放入 溶液中进行验证。
(1)若固体溶解,则该物质为铁锈;铁锈是铁与 反应生成的。
(2)若固体不溶,则该物质为铜;铜可能是铁与 溶液反应生成的。
9. 酸溶液有相似的化学性质。
(1)酸溶液能使紫色石蕊溶液 ,无色酚酞溶液遇酸 。
(2)酸能与某些金属反应,下列金属与酸中,能反应的写出化学方程式,不能反应的说明理由。
①铝与稀盐酸 。
②锌与稀硫酸 。
③铜与稀硫酸 。
(3)酸能与某些金属氧化物反应,写出稀盐酸、稀硫酸利用此性质的一个用途 。
①盐酸和氧化铝反应的化学方程式为 。
②稀硫酸与氧化铜反应的化学方程式为 ,反应的现象为 。
实验室制取二氧化碳的原料是 ,相关反应的化学方程式是 。
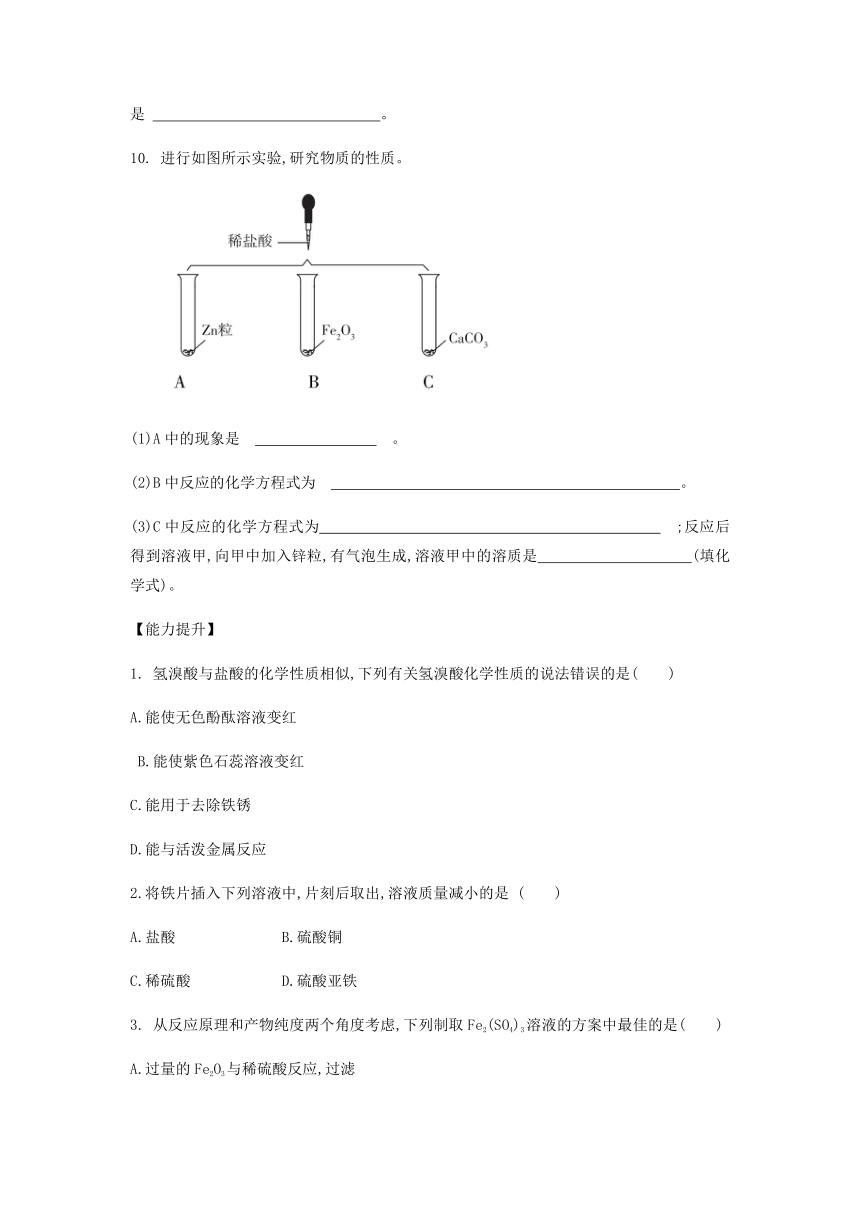
10. 进行如图所示实验,研究物质的性质。
(1)A中的现象是 。
(2)B中反应的化学方程式为 。
(3)C中反应的化学方程式为 ;反应后得到溶液甲,向甲中加入锌粒,有气泡生成,溶液甲中的溶质是 (填化学式)。
【能力提升】
1. 氢溴酸与盐酸的化学性质相似,下列有关氢溴酸化学性质的说法错误的是( )
A.能使无色酚酞溶液变红
B.能使紫色石蕊溶液变红
C.能用于去除铁锈
D.能与活泼金属反应
2.将铁片插入下列溶液中,片刻后取出,溶液质量减小的是 ( )
A.盐酸 B.硫酸铜
C.稀硫酸 D.硫酸亚铁
3. 从反应原理和产物纯度两个角度考虑,下列制取Fe2(SO4)3溶液的方案中最佳的是( )
A.过量的Fe2O3与稀硫酸反应,过滤
B.过量的Fe粉与稀硫酸反应,过滤
C.过量的稀硫酸与Fe2O3反应
D.过量的Fe粉与CuSO4溶液反应,过滤
4. 如图表示化学反应中溶液的颜色变化。下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊溶液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
5. 请结合图示分析,下列说法正确的是 ( )
(图中“—”表示相连的物质可以发生反应;“→”表示一种物质可以转化成另一种物质)
A.能实现转化①的金属也一定能和稀硫酸反应
B.转化②只能通过铁与硫酸铜溶液反应实现
C.通过与C或CO发生置换反应可实现转化③
D.反应④中能观察到溶液变为浅绿色
6. 盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观角度分析该变化过程中改变的是 。
(2)在盐酸中加入过量的铁粉,使其充分反应。
①可以看到的现象是 。
②下图表示该反应前后溶液中存在的主要离子, 请写出每种图形代表的离子(填离子符号):
③下列能与盐酸发生类似反应的金属是 (填序号)。
A.Cu B.Mg C.Zn D.Ag
7. 小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200 mL的软透明塑料瓶、白醋、鸡蛋壳、紫罗兰花、生锈铁钉、蒸馏水、熟石灰[Ca(OH)2]、小玻璃杯、吸管等。
【提出问题】白醋是否具有酸的性质
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为CH3COOH;
(2)紫罗兰花遇酸变为红色;
(3)醋酸盐中除银盐和汞盐外都易溶于水。
【实验探究】
实验序号 实验操作 实验现象 实验结论
① 将白醋滴在紫罗兰花上 紫罗兰花 白醋显酸性
② 将生锈铁钉放在小玻璃杯中,加入白醋 刚开始时 ,一段时间后,有气泡冒出 白醋能与铁锈反应;
③ 向软塑料瓶中加入10 mL白醋,将瓶捏瘪,加入约5 g鸡蛋壳,拧紧瓶盖 瓶中有气泡冒出,瘪塑料瓶逐渐鼓起 白醋能与碳酸钙反应生成CO2
【反思与评价】上述实验③的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,实验步骤为 ,现象是 ;发生反应的化学方程式是 。
答案
【基础练习】
1-6 CCCBDC
8.【参考答案】 稀盐酸(或稀硫酸)
(1)氧气、水
(2)硫酸铜(或氯化铜,或硝酸铜)
【能力提升】
1-5 ABACA
6.【参考答案】 (1)氯化氢分子间的间隔
(2)①固体逐渐减少,有气泡产生,溶液由无色变为浅绿色
②H+ Cl- Fe2+ ③BC
7.【参考答案】 【探究与验证】①变红 ②铁钉表面的红棕色物质慢慢消失,溶液变为黄色 白醋能与铁反应
【反思与评价】将产生的气体通入澄清石灰水中 澄清石灰水变浑浊 Ca(OH)2+CO2 CaCO3↓+H2O
【基础练习】
1. 日常生活中的下列物质能使紫色石蕊溶液变红的是( )
A.蒸馏水 B.食盐水
C.白醋 D.石灰水
2. 下列物质中,不能与稀盐酸发生反应的是 ( )
A.Fe2O3 B.CaCO3
C.CO2 D.Mg
3. 下列关于H2SO4性质的描述中,不属于酸的通性的是 ( )
A.使紫色石蕊溶液变红
B.稀硫酸与氧化铜反应
C.浓硫酸滴到白纸上使纸变黑
D.稀硫酸与铁反应放出氢气
4. 白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易被蚁酸腐蚀的是( )
A.镀锌水管
B.铜制塑像
C.大理石栏杆
D.铝合金门窗
5. 食醋里通常含有3%~5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列说法不正确的是 ( )
A.产生的气体是二氧化碳
B.醋酸可以使酚酞溶液变红
C.可用食醋除去暖水瓶中的水垢
D.不宜用铝制容器盛装食醋
6. 下列物质的变化中,只有加酸才能一步实现的是 ( )
将生锈的铁钉投入过量的稀盐酸中,首先观察到的现象是 ,发生反应的化学方程式为 ;反应一段时间后,又观察到有气泡产生,发生反应的化学方程式为 。
8. 某同学在实验室中看到铁钉表面附着红色物质,分不出是铁锈还是铜,为证明红色物质的成分,将其“刮”下来,放入 溶液中进行验证。
(1)若固体溶解,则该物质为铁锈;铁锈是铁与 反应生成的。
(2)若固体不溶,则该物质为铜;铜可能是铁与 溶液反应生成的。
9. 酸溶液有相似的化学性质。
(1)酸溶液能使紫色石蕊溶液 ,无色酚酞溶液遇酸 。
(2)酸能与某些金属反应,下列金属与酸中,能反应的写出化学方程式,不能反应的说明理由。
①铝与稀盐酸 。
②锌与稀硫酸 。
③铜与稀硫酸 。
(3)酸能与某些金属氧化物反应,写出稀盐酸、稀硫酸利用此性质的一个用途 。
①盐酸和氧化铝反应的化学方程式为 。
②稀硫酸与氧化铜反应的化学方程式为 ,反应的现象为 。
实验室制取二氧化碳的原料是 ,相关反应的化学方程式是 。
10. 进行如图所示实验,研究物质的性质。
(1)A中的现象是 。
(2)B中反应的化学方程式为 。
(3)C中反应的化学方程式为 ;反应后得到溶液甲,向甲中加入锌粒,有气泡生成,溶液甲中的溶质是 (填化学式)。
【能力提升】
1. 氢溴酸与盐酸的化学性质相似,下列有关氢溴酸化学性质的说法错误的是( )
A.能使无色酚酞溶液变红
B.能使紫色石蕊溶液变红
C.能用于去除铁锈
D.能与活泼金属反应
2.将铁片插入下列溶液中,片刻后取出,溶液质量减小的是 ( )
A.盐酸 B.硫酸铜
C.稀硫酸 D.硫酸亚铁
3. 从反应原理和产物纯度两个角度考虑,下列制取Fe2(SO4)3溶液的方案中最佳的是( )
A.过量的Fe2O3与稀硫酸反应,过滤
B.过量的Fe粉与稀硫酸反应,过滤
C.过量的稀硫酸与Fe2O3反应
D.过量的Fe粉与CuSO4溶液反应,过滤
4. 如图表示化学反应中溶液的颜色变化。下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊溶液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
5. 请结合图示分析,下列说法正确的是 ( )
(图中“—”表示相连的物质可以发生反应;“→”表示一种物质可以转化成另一种物质)
A.能实现转化①的金属也一定能和稀硫酸反应
B.转化②只能通过铁与硫酸铜溶液反应实现
C.通过与C或CO发生置换反应可实现转化③
D.反应④中能观察到溶液变为浅绿色
6. 盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观角度分析该变化过程中改变的是 。
(2)在盐酸中加入过量的铁粉,使其充分反应。
①可以看到的现象是 。
②下图表示该反应前后溶液中存在的主要离子, 请写出每种图形代表的离子(填离子符号):
③下列能与盐酸发生类似反应的金属是 (填序号)。
A.Cu B.Mg C.Zn D.Ag
7. 小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200 mL的软透明塑料瓶、白醋、鸡蛋壳、紫罗兰花、生锈铁钉、蒸馏水、熟石灰[Ca(OH)2]、小玻璃杯、吸管等。
【提出问题】白醋是否具有酸的性质
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为CH3COOH;
(2)紫罗兰花遇酸变为红色;
(3)醋酸盐中除银盐和汞盐外都易溶于水。
【实验探究】
实验序号 实验操作 实验现象 实验结论
① 将白醋滴在紫罗兰花上 紫罗兰花 白醋显酸性
② 将生锈铁钉放在小玻璃杯中,加入白醋 刚开始时 ,一段时间后,有气泡冒出 白醋能与铁锈反应;
③ 向软塑料瓶中加入10 mL白醋,将瓶捏瘪,加入约5 g鸡蛋壳,拧紧瓶盖 瓶中有气泡冒出,瘪塑料瓶逐渐鼓起 白醋能与碳酸钙反应生成CO2
【反思与评价】上述实验③的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,实验步骤为 ,现象是 ;发生反应的化学方程式是 。
答案
【基础练习】
1-6 CCCBDC
8.【参考答案】 稀盐酸(或稀硫酸)
(1)氧气、水
(2)硫酸铜(或氯化铜,或硝酸铜)
【能力提升】
1-5 ABACA
6.【参考答案】 (1)氯化氢分子间的间隔
(2)①固体逐渐减少,有气泡产生,溶液由无色变为浅绿色
②H+ Cl- Fe2+ ③BC
7.【参考答案】 【探究与验证】①变红 ②铁钉表面的红棕色物质慢慢消失,溶液变为黄色 白醋能与铁反应
【反思与评价】将产生的气体通入澄清石灰水中 澄清石灰水变浑浊 Ca(OH)2+CO2 CaCO3↓+H2O
同课章节目录
