第四单元课题4化学式与化合价同步练习题-2021-2022学年九年级化学人教版上册(word版 含答案)
文档属性
| 名称 | 第四单元课题4化学式与化合价同步练习题-2021-2022学年九年级化学人教版上册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 125.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-23 00:00:00 | ||
图片预览



文档简介
2021——2022学年度人教版九年级化学 第四单元 自然界的水 课题4化学式与化合价 同步练习题
一、选择题
1.下列化学式正确的是
A.SFe B.Al(OH)3 C.MgO2 D.K(OH)
2.下列计算正确的是
A.H2O的相对分子质量=1×2×16=32
B.Mg(OH)2的相对分子质量= 24 +(16 + 1)×2 = 58
C.NH4NO3中氮元素的质量分数=×100% = 17.5%
D.SO2中硫元素与氧元素的质量比=1:2
3.下列有关微粒的说法错误的是
A.水分子由氢分子和氧原子组成 B.镁原子失去两个电子形成镁离子
C.构成物质的微粒是在不停地运动 D.原子、分子、离子都是构成物质的微粒
4.高氯酸钾(KClO4)可用于制备火箭燃料。有关KClO4的说法正确的是
A.含4种元素 B.属于混合物
C.氯元素的化合价为+6 D.钾、氯元素的质量比为78:71
5.下列化学用语中“2”所表示的意义正确的是
A.CO2:二氧化碳分子中含有两个氧原子
B.2Al:两个氯原子
C.Fe2+:每个铁离子带两个单位的正电荷
D. :在氧化镁中,镁元素的化合价为+2价
6.蓝莓中含有丰富的花青素(化学式为C15H11O6)。下列有关花青素的说法中正确的是
A.花青素的相对分子质量是287g B.花青素中氧元素的质量分数最小
C.花青素分子中含有氧气分子 D.一个花青素分子中碳、氢原子个数比为15:1l
7.下列说法错误的是
A.铁(Fe)是由铁原子构成
B.水(H2O)是由氢元素和氧元素组成的
C.氯化钠(NaCl)是由氯化钠离子构成的
D.每个二氧化碳(CO2)分子是由一个碳原子和两个氧原子构成的
8.成熟的枇杷味道鲜美,营养颇丰。枇杷中富含的维生素A1具有预防夜盲症、抗衰老和促进骨骼生长等功效,其化学式为C20H30O。下列说法正确的是
A.维生素A1中碳元素的质量分数最大
B.维生素A1由20个碳原子、30个氢原子和1个氧原子组成
C.维生素A1中碳、氢、氧元素的质量比为20:30:1
D.维生素A1的相对分子质量为286g
9.根据粒子结构示意图给出的信息,下列说法正确的是
A.①②③表示的是同种原子
B.②易与③结合,形成稳定的化合物
C.①②③都是原子失去电子后形成的粒子
D.①②③表示的粒子都不是相对稳定结构
10.下列叙述、对应的表达式、所属基本反应类型均正确的是
A.细铁丝在空气中燃烧 化合反应
B.实验室测定空气中氧气含量 化合反应
C.实验室用过氧化氢溶液制氧气 分解反应
D.电解水 分解反应
11.人尿中氮元素的质量分数为0.91%。假定人尿中只含尿素[CO(NH2)2]而不含其他含氮物质,则人尿中尿素的质量分数为
A.0.91% B.1.95% C.23% D.46%
12.胡萝卜中富含的维生素A1具有预防夜盲症、抗衰老和促进骨髓生长等功效,其化学式为C20H30O。下列说法正确的是
A.维生素A1属于化合物
B.维生素A1中氢元素的质量分数最大
C.维生素A1分子是由碳、氢、氧元素组成
D.维生素A1是由20个碳原子,30个氢原子和1个氧原子构成
13.某气体可能由CO、CO2、O2三种气体中一种或多种组成,经测定其中只含有碳、氧两种元素,且碳、氧两种元素的质量比为3:5,则关于该气体的说法不正确的是.
A.一定含有CO B.一定是CO与CO2组成的混合物
C.该气体最多有3种组成情况 D.可能是由CO与CO2组成的混合物
14.《我不是药神》是一部关于白血病和印度药的电影作品。药品“甲磺酸伊马替尼片”用于治疗慢性髓性白血病和恶性胃肠道间质肿瘤,原理是融合基因,使BCR-ABL蛋白得不到磷酸,不能活化,就发不出指令,细胞的增殖态势得到抑制。甲磺酸伊马替尼的化学式为C29H31N7OCH4SO3,关于甲磺酸伊马替尼的说法正确的是
A.甲磺酸伊马替尼是8种元素组成的化合物
B.甲磺酸伊马替尼分子由77个原子构成
C.甲磺酸伊马替尼中碳、氢、氧元素的质量比为30:35:4
D.甲磺酸伊马替尼的相对分子质量是589
二、填空题
15.化学用语是学习化学的重要工具,写出下列微粒的化学符号:
(1)三个氮原子___________。
(2)五氧化二磷___________。
(3)地壳中含量最多的金属元素___________。
(4)保持水的化学性质的最小粒子___________。
(5)某微粒的结构示意图为,该微粒的符号是___________。
16.标出下列各组物质中加点元素的化合价:
(1)H2S_______;S_______;SO2_______;Na2SO3_______;H2SO4_______。
(2)MnO2_______;MnCl2_______;Mn_______;CaMnO4_______;KMnO4_______。
17.薄荷香牙膏上的抗牙腐蚀的药物的化学式为Na2FPO3,其中Na2FPO3 中含有________种元素,每个分子中含有________个原子,其相对分子质量为:________。
18.人体缺乏维生素C(简写“VC”)就会患坏血病,哥伦布探险时的许多船员就因此而死亡。如图所示为某种“维生素C”说明书的一部分。请你回答:
(1)“VC”中含有种元素,VC的相对分子质量__________它的分子中碳、氢、氧原子的个数比__________。 “VC”中碳、氢、氧元素的质量比__________。
(2)若正常成人每天对“VC”的最低需要量为60mg。当“VC”完全来自右图的“维生素C”,则每天至少服用________次;
(3)①维生素C中碳元素的质量分数__________;
②__________克维生素C与66克二氧化碳所含氧元素质量相等。
19.比较、归纳和总结是化学学习常用的方法,请结合所学知识填空:
(1)有下列三组物质:Ⅰ组O2 O3 Ⅱ组MnO2 CO2 P2O5 Ⅲ组KClO3 Ca(OH)2 CuSO4
①这些物质含有相同的元素,该元素是_______。
②Ⅰ组和Ⅱ、Ⅲ组的物质相比较,从组成上看不同之处在于_______。
③请补充一种属于Ⅱ组物质的化学式_______。
(2)找规律,填空
①化合价:HNO3、NO2、NaNO2、NO、_______(写一氧化物的化学式)。
②已知物质间转化关系:H2O2→H2O→_______(填化学式)→P2O5。
③物质的组成:CH4(甲烷)、C2H6(乙烷)、C3H8(丙烷)、C4H10、_______、_______(戊烷)。
20.计算下列物质中各元素的质量比及原子个数比:
(1)H2O中氢元素与氧元素的质量比为______,原子个数比为_________ ;
(2)H2SO4中氢元素、硫元素与氧元素的质量比为________,原子个数比为_______;
(3)NH4HCO3中氮元素、氢元素、碳元素与氧元素的质量比为___,原子个数比为___。
三、简答题
21.水是生命之源
(1)1滴水(以20滴水为1mL计)中大约含有1.67×1021个水_____(用“分子”、“原子“或“离子”填空)水中氢、氧元素的质量比为_____。
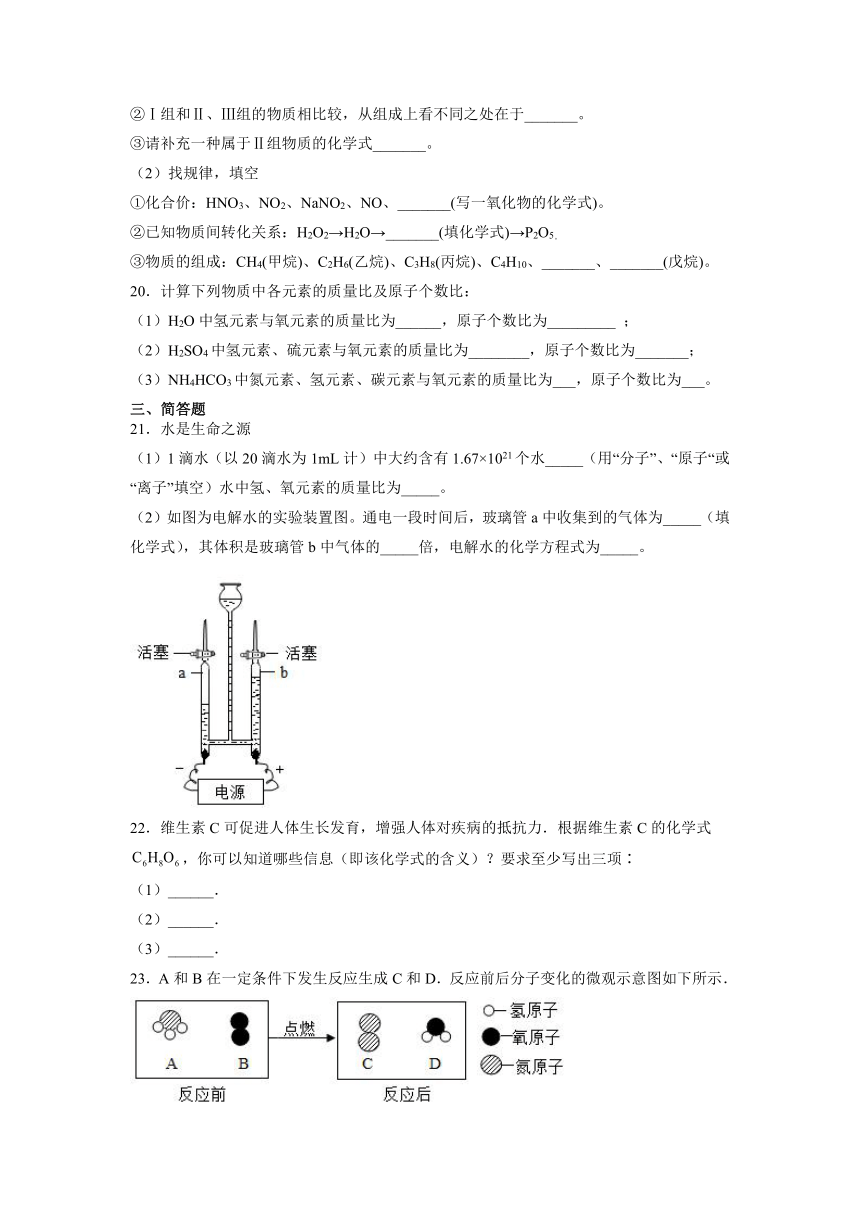
(2)如图为电解水的实验装置图。通电一段时间后,玻璃管a中收集到的气体为_____(填化学式),其体积是玻璃管b中气体的_____倍,电解水的化学方程式为_____。
22.维生素C可促进人体生长发育,增强人体对疾病的抵抗力.根据维生素C的化学式,你可以知道哪些信息(即该化学式的含义)?要求至少写出三项∶
(1)______.
(2)______.
(3)______.
23.A和B在一定条件下发生反应生成C和D.反应前后分子变化的微观示意图如下所示.
(1)A中氮元素和氢元素的质量比为 _________ .
(2)4种物质中,属于化合物的是 _________ (填图中字母).
(3)该反应的基本反应类型为 _________ 反应.
24.如图为A、B、C、D四种粒子的结构示意图以及硒元素在元素周期表中的信息,请按要求填空
(1)A、B、C、D四种粒子中,属于同种元素的是 _____ (填序号)A粒子的符号为 _____ 。
(2)由B元素和C元素形成的化合物的化学式为 _____ 。
(3)该硒原子的中子数是 _____ 。
(4)不同元素的原子中,下列各项肯定不相同的是 _____ 。(填序号)
①中子数②质子数③电子层数④核外电子总数⑤最外层电子数⑥核电荷数
四、综合应用题
25.实验小组的同学们对过氧化氢溶液制氧气的实验进行了如下拓展探究。
(探究一)甲组同学探究催化剂种类对过氧化氢溶液分解速率的影响(实验中催化剂均为 0.4g,过氧化氢 溶液浓度均为 6%,以收集 10mL 气体为准),该小组采用了下图所示装置进行实验,具体数据如下表:
催化剂种类 时间(s)
CuO 0.07
MnO2 0.03
活性炭 0.12
(1)C 处应补全的装置是______(填“C1”或“C2”)。
(2)原装置中的空气对实验结果是否有影响?______(填“是”或“否”)。
(3)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为______。
(4)为完成此探究,实验时需要测定的数据是______。
(5)当 C 处量筒中收集到 10mL 水时,过氧化氢溶液分解出的氧气体积______10mL(填“大于”、“等于”或“小于”)。
(探究二)乙组同学探究过氧化氢溶液浓度对分解速率的影响(水浴池温度控制在 21℃,二氧化锰均为 0.5g,过氧化氢溶液均为 5mL,三颈瓶容积为 250mL),该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制图乙的图像:
(6)实验中,用水浴池加热比用酒精灯直接加热的优点是______(任填一点)。
(7)图 1 说明过氧化氢溶液浓度越高,反应速率越______(填“快”或“慢”),以 10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是______。
(8)图 2 说明从温度看,过氧化氢溶液浓度越高,反应越______(填“剧烈”或“平稳”)。
(9)丙同学根据下图过氧化氢分解的微观图,另取 25g 过氧化氢溶液,完全分解共生成氧气 1.6 g,计算 此过氧化氢溶液中过氧化氢的质量分数______(写出计算过程)。
(查阅资料)反应前后元素的种类和各元素的质量都不变。
【参考答案】
1.B 2.B 3.A 4.D 5.D 6.D 7.C 8.A 9.B 10.C 11.B 12.A 13.B 14.D
15.(1)3N(2)P2O5(3)Al(4)H2O(5)O2-
16.(1)
(2)
17.4##四 7 144
18.(1) 176 3:4:3 9:1:12 (2)3(3) 40.9%
解:设与66克二氧化碳所含氧元素质量相等的维生素C的质量为x。
66g×=x×,x=88g。
19.
(1) 氧元素 组成的元素种类不同,第Ⅰ组物质由一种元素组成,Ⅱ、Ⅲ组物质由不同元素组成 H2O
(2) N2O O2 丁烷 C5H12
20.(1) 1:8 2:1 (2) 1:16:32 2:1:4 (3) 14:5:12:48 1:5:1:3
21.分子 1:8(或2:16) H2 2
22.维生素C是有机物(或化合物) 维生素C是由碳、氢、氧三种元素组成的 维生素C分子是由碳、氢、氧三种原子构成的
23.14:3 A和D 置换反应
24.AD; S2﹣ Al2O3 45 ②④⑥
25.(1)C2(2)否(3)MnO2>CuO>活性炭(4)收集10mL气体所用的时间(5)小于(6)受热均匀、温度可控(任填一点)(7) 快 反应结束后,气体温度降低,气压减小 (合理均给分) (8)剧烈(9)H2O2的质量= 过氧化氢溶液中,H2O2的质量分数=
一、选择题
1.下列化学式正确的是
A.SFe B.Al(OH)3 C.MgO2 D.K(OH)
2.下列计算正确的是
A.H2O的相对分子质量=1×2×16=32
B.Mg(OH)2的相对分子质量= 24 +(16 + 1)×2 = 58
C.NH4NO3中氮元素的质量分数=×100% = 17.5%
D.SO2中硫元素与氧元素的质量比=1:2
3.下列有关微粒的说法错误的是
A.水分子由氢分子和氧原子组成 B.镁原子失去两个电子形成镁离子
C.构成物质的微粒是在不停地运动 D.原子、分子、离子都是构成物质的微粒
4.高氯酸钾(KClO4)可用于制备火箭燃料。有关KClO4的说法正确的是
A.含4种元素 B.属于混合物
C.氯元素的化合价为+6 D.钾、氯元素的质量比为78:71
5.下列化学用语中“2”所表示的意义正确的是
A.CO2:二氧化碳分子中含有两个氧原子
B.2Al:两个氯原子
C.Fe2+:每个铁离子带两个单位的正电荷
D. :在氧化镁中,镁元素的化合价为+2价
6.蓝莓中含有丰富的花青素(化学式为C15H11O6)。下列有关花青素的说法中正确的是
A.花青素的相对分子质量是287g B.花青素中氧元素的质量分数最小
C.花青素分子中含有氧气分子 D.一个花青素分子中碳、氢原子个数比为15:1l
7.下列说法错误的是
A.铁(Fe)是由铁原子构成
B.水(H2O)是由氢元素和氧元素组成的
C.氯化钠(NaCl)是由氯化钠离子构成的
D.每个二氧化碳(CO2)分子是由一个碳原子和两个氧原子构成的
8.成熟的枇杷味道鲜美,营养颇丰。枇杷中富含的维生素A1具有预防夜盲症、抗衰老和促进骨骼生长等功效,其化学式为C20H30O。下列说法正确的是
A.维生素A1中碳元素的质量分数最大
B.维生素A1由20个碳原子、30个氢原子和1个氧原子组成
C.维生素A1中碳、氢、氧元素的质量比为20:30:1
D.维生素A1的相对分子质量为286g
9.根据粒子结构示意图给出的信息,下列说法正确的是
A.①②③表示的是同种原子
B.②易与③结合,形成稳定的化合物
C.①②③都是原子失去电子后形成的粒子
D.①②③表示的粒子都不是相对稳定结构
10.下列叙述、对应的表达式、所属基本反应类型均正确的是
A.细铁丝在空气中燃烧 化合反应
B.实验室测定空气中氧气含量 化合反应
C.实验室用过氧化氢溶液制氧气 分解反应
D.电解水 分解反应
11.人尿中氮元素的质量分数为0.91%。假定人尿中只含尿素[CO(NH2)2]而不含其他含氮物质,则人尿中尿素的质量分数为
A.0.91% B.1.95% C.23% D.46%
12.胡萝卜中富含的维生素A1具有预防夜盲症、抗衰老和促进骨髓生长等功效,其化学式为C20H30O。下列说法正确的是
A.维生素A1属于化合物
B.维生素A1中氢元素的质量分数最大
C.维生素A1分子是由碳、氢、氧元素组成
D.维生素A1是由20个碳原子,30个氢原子和1个氧原子构成
13.某气体可能由CO、CO2、O2三种气体中一种或多种组成,经测定其中只含有碳、氧两种元素,且碳、氧两种元素的质量比为3:5,则关于该气体的说法不正确的是.
A.一定含有CO B.一定是CO与CO2组成的混合物
C.该气体最多有3种组成情况 D.可能是由CO与CO2组成的混合物
14.《我不是药神》是一部关于白血病和印度药的电影作品。药品“甲磺酸伊马替尼片”用于治疗慢性髓性白血病和恶性胃肠道间质肿瘤,原理是融合基因,使BCR-ABL蛋白得不到磷酸,不能活化,就发不出指令,细胞的增殖态势得到抑制。甲磺酸伊马替尼的化学式为C29H31N7OCH4SO3,关于甲磺酸伊马替尼的说法正确的是
A.甲磺酸伊马替尼是8种元素组成的化合物
B.甲磺酸伊马替尼分子由77个原子构成
C.甲磺酸伊马替尼中碳、氢、氧元素的质量比为30:35:4
D.甲磺酸伊马替尼的相对分子质量是589
二、填空题
15.化学用语是学习化学的重要工具,写出下列微粒的化学符号:
(1)三个氮原子___________。
(2)五氧化二磷___________。
(3)地壳中含量最多的金属元素___________。
(4)保持水的化学性质的最小粒子___________。
(5)某微粒的结构示意图为,该微粒的符号是___________。
16.标出下列各组物质中加点元素的化合价:
(1)H2S_______;S_______;SO2_______;Na2SO3_______;H2SO4_______。
(2)MnO2_______;MnCl2_______;Mn_______;CaMnO4_______;KMnO4_______。
17.薄荷香牙膏上的抗牙腐蚀的药物的化学式为Na2FPO3,其中Na2FPO3 中含有________种元素,每个分子中含有________个原子,其相对分子质量为:________。
18.人体缺乏维生素C(简写“VC”)就会患坏血病,哥伦布探险时的许多船员就因此而死亡。如图所示为某种“维生素C”说明书的一部分。请你回答:
(1)“VC”中含有种元素,VC的相对分子质量__________它的分子中碳、氢、氧原子的个数比__________。 “VC”中碳、氢、氧元素的质量比__________。
(2)若正常成人每天对“VC”的最低需要量为60mg。当“VC”完全来自右图的“维生素C”,则每天至少服用________次;
(3)①维生素C中碳元素的质量分数__________;
②__________克维生素C与66克二氧化碳所含氧元素质量相等。
19.比较、归纳和总结是化学学习常用的方法,请结合所学知识填空:
(1)有下列三组物质:Ⅰ组O2 O3 Ⅱ组MnO2 CO2 P2O5 Ⅲ组KClO3 Ca(OH)2 CuSO4
①这些物质含有相同的元素,该元素是_______。
②Ⅰ组和Ⅱ、Ⅲ组的物质相比较,从组成上看不同之处在于_______。
③请补充一种属于Ⅱ组物质的化学式_______。
(2)找规律,填空
①化合价:HNO3、NO2、NaNO2、NO、_______(写一氧化物的化学式)。
②已知物质间转化关系:H2O2→H2O→_______(填化学式)→P2O5。
③物质的组成:CH4(甲烷)、C2H6(乙烷)、C3H8(丙烷)、C4H10、_______、_______(戊烷)。
20.计算下列物质中各元素的质量比及原子个数比:
(1)H2O中氢元素与氧元素的质量比为______,原子个数比为_________ ;
(2)H2SO4中氢元素、硫元素与氧元素的质量比为________,原子个数比为_______;
(3)NH4HCO3中氮元素、氢元素、碳元素与氧元素的质量比为___,原子个数比为___。
三、简答题
21.水是生命之源
(1)1滴水(以20滴水为1mL计)中大约含有1.67×1021个水_____(用“分子”、“原子“或“离子”填空)水中氢、氧元素的质量比为_____。
(2)如图为电解水的实验装置图。通电一段时间后,玻璃管a中收集到的气体为_____(填化学式),其体积是玻璃管b中气体的_____倍,电解水的化学方程式为_____。
22.维生素C可促进人体生长发育,增强人体对疾病的抵抗力.根据维生素C的化学式,你可以知道哪些信息(即该化学式的含义)?要求至少写出三项∶
(1)______.
(2)______.
(3)______.
23.A和B在一定条件下发生反应生成C和D.反应前后分子变化的微观示意图如下所示.
(1)A中氮元素和氢元素的质量比为 _________ .
(2)4种物质中,属于化合物的是 _________ (填图中字母).
(3)该反应的基本反应类型为 _________ 反应.
24.如图为A、B、C、D四种粒子的结构示意图以及硒元素在元素周期表中的信息,请按要求填空
(1)A、B、C、D四种粒子中,属于同种元素的是 _____ (填序号)A粒子的符号为 _____ 。
(2)由B元素和C元素形成的化合物的化学式为 _____ 。
(3)该硒原子的中子数是 _____ 。
(4)不同元素的原子中,下列各项肯定不相同的是 _____ 。(填序号)
①中子数②质子数③电子层数④核外电子总数⑤最外层电子数⑥核电荷数
四、综合应用题
25.实验小组的同学们对过氧化氢溶液制氧气的实验进行了如下拓展探究。
(探究一)甲组同学探究催化剂种类对过氧化氢溶液分解速率的影响(实验中催化剂均为 0.4g,过氧化氢 溶液浓度均为 6%,以收集 10mL 气体为准),该小组采用了下图所示装置进行实验,具体数据如下表:
催化剂种类 时间(s)
CuO 0.07
MnO2 0.03
活性炭 0.12
(1)C 处应补全的装置是______(填“C1”或“C2”)。
(2)原装置中的空气对实验结果是否有影响?______(填“是”或“否”)。
(3)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为______。
(4)为完成此探究,实验时需要测定的数据是______。
(5)当 C 处量筒中收集到 10mL 水时,过氧化氢溶液分解出的氧气体积______10mL(填“大于”、“等于”或“小于”)。
(探究二)乙组同学探究过氧化氢溶液浓度对分解速率的影响(水浴池温度控制在 21℃,二氧化锰均为 0.5g,过氧化氢溶液均为 5mL,三颈瓶容积为 250mL),该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制图乙的图像:
(6)实验中,用水浴池加热比用酒精灯直接加热的优点是______(任填一点)。
(7)图 1 说明过氧化氢溶液浓度越高,反应速率越______(填“快”或“慢”),以 10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是______。
(8)图 2 说明从温度看,过氧化氢溶液浓度越高,反应越______(填“剧烈”或“平稳”)。
(9)丙同学根据下图过氧化氢分解的微观图,另取 25g 过氧化氢溶液,完全分解共生成氧气 1.6 g,计算 此过氧化氢溶液中过氧化氢的质量分数______(写出计算过程)。
(查阅资料)反应前后元素的种类和各元素的质量都不变。
【参考答案】
1.B 2.B 3.A 4.D 5.D 6.D 7.C 8.A 9.B 10.C 11.B 12.A 13.B 14.D
15.(1)3N(2)P2O5(3)Al(4)H2O(5)O2-
16.(1)
(2)
17.4##四 7 144
18.(1) 176 3:4:3 9:1:12 (2)3(3) 40.9%
解:设与66克二氧化碳所含氧元素质量相等的维生素C的质量为x。
66g×=x×,x=88g。
19.
(1) 氧元素 组成的元素种类不同,第Ⅰ组物质由一种元素组成,Ⅱ、Ⅲ组物质由不同元素组成 H2O
(2) N2O O2 丁烷 C5H12
20.(1) 1:8 2:1 (2) 1:16:32 2:1:4 (3) 14:5:12:48 1:5:1:3
21.分子 1:8(或2:16) H2 2
22.维生素C是有机物(或化合物) 维生素C是由碳、氢、氧三种元素组成的 维生素C分子是由碳、氢、氧三种原子构成的
23.14:3 A和D 置换反应
24.AD; S2﹣ Al2O3 45 ②④⑥
25.(1)C2(2)否(3)MnO2>CuO>活性炭(4)收集10mL气体所用的时间(5)小于(6)受热均匀、温度可控(任填一点)(7) 快 反应结束后,气体温度降低,气压减小 (合理均给分) (8)剧烈(9)H2O2的质量= 过氧化氢溶液中,H2O2的质量分数=
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
