2021年河南省中考化学命题信息原创卷(一)(word版 含答案)
文档属性
| 名称 | 2021年河南省中考化学命题信息原创卷(一)(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 251.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-23 00:00:00 | ||
图片预览




文档简介
2021年河南省中考命题信息原创卷(一)
(满分50分,考试时间50分钟)
相对原子质量 H:1 C:12 N:14 O:16 Na:23 Mg:24 S:32 Cl:35.5
Ca:40 Fe:56 Cu:64 Zn:65 Ag:108 Ba:137
选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
大米是中国人的主食之一,其中富含的营养物质是( )
糖类 B.蛋白质 C.维生素 D.油脂
下列物质的用途中,主要体现了物质的化学性质的是( )
用汽油除去油污 B.用氮气做保护气
用浓硫酸做干燥剂 D.用干冰进行人工降雨
“垃圾分类益处多,环境保护靠你我”。下列标志属于可回收标志的是( )
A B C D
下列空气的成分中,可用于霓虹灯的是( )
氮气 B.氧气 C.二氧化碳 D.稀有气体
5.2021年3月22日是第二十九届“世界水日”。世界水日的宗旨是唤起公众的节水意识,加强水资源保护。下列有关水的说法正确的是( )
明矾净水是为了降低水的硬度
水是由氢原子和氧原子构成的
长期饮用蒸馏水无益身体健康
过滤可以除去水中所有的杂质
6.下列各组物质中,都由离子构成的一组是( )
A.氯化钾、硝酸铵 B.氯化氢、硫酸镁
C.甲烷、干冰 D.钠、钾
7.下列图示的实验操作中正确的是( )
A.量取液体 B.干燥氧气 C.测溶液的pH D.称量固体
下列化学方程式中,符合题意且书写正确的是( )
稀盐酸与氧化铁反应:2HCl+FeO===FeCl2+H2O
实验室制取氢气:Cu+H2SO4===CuSO4+H2↑
除去CO2中含有的少量CO:2CO+O22CO2
正常雨水呈弱酸性的原因是:H2O+CO2===H2CO3
氯化钠是重要的化工原料,是氯碱工业的基础。电解饱和食盐水一定不能得到的物质是( )
A.H2 B.Cl2 C.Na2CO3 D.NaOH
10.分类、归纳是化学学习的重要方法。下列有关说法正确的是( )
A.甲烷、乙醇和干冰都属于有机化合物
B.尿素、硝酸钾、磷酸二氢铵都是复合肥料
C.蚕丝、羊毛、塑料都属于有机高分子材料
D.二氧化硫、二氧化氮和二氧化碳都是空气污染物
11.下列区分物质所用的方法或试剂不正确的是( )
A.硬水和软水——肥皂水
B.氮气和二氧化碳——燃着的木条
C.硝酸铵和硝酸钾固体——水
D.碳酸钠溶液和硫酸钠溶液——酚酞溶液
12.经测定,某溶液中含有大量的Na+、SO42-、Cl-、X四种离子,且四种离子个数比为1:1:1:1,则X可能是( )
A.K+ B.Cu2+ C.Ba2+ D.Al3+
13.下列图像分别与选项中的操作相对应,其中合理的是( )
A B C D
向一定量澄清石灰水中不断加入水
向盛有一定量铁粉的试管中不断滴加硫酸铜溶液
向两份完全相同的稀盐酸中分别加入足量锌、镁
用向上排空气法收集氧气时集气瓶内氧气的质量
现有40.0g氯化钡和氯化钙的固体混合物,加足量蒸馏水使之完全溶解,再加入足量碳酸钠溶液充分反应,将反应后的混合物过滤、洗涤、干燥,得到滤渣37.8g。则反应生成的氯化钠的质量为( )
A.5.85g B.11.70g C.23.4g D.35.1g
二、填空题(本题包括6个小题,每空1分,共16分)
15.焙制糕点所用发酵粉的主要成分之一是 (填化学式,下同);已知相同元素可以组成不同物质,则生物体中含量居前两位的元素形成的化合物为 。
16.为预防新型冠状病毒感染,在人员密集的场所需要佩戴口罩,医用口罩阻隔病毒的原理类似化学基本实验中的 操作;活性炭口罩能有效防止空气中的苯和甲醛等气体对人体的伤害,其原因是 ;下图是活性炭中碳原子的结构示意图,据图分析可知碳元素与硅元素的化学性质相似,原因是它们原子的 相同。
17.汽车已逐渐成为生活中重要的代步工具,使用乙醇汽油可以减少污染物的排放,乙醇充分燃烧的化学方程式为 ;你心目中最理想的汽车燃料是 ,原因是 。
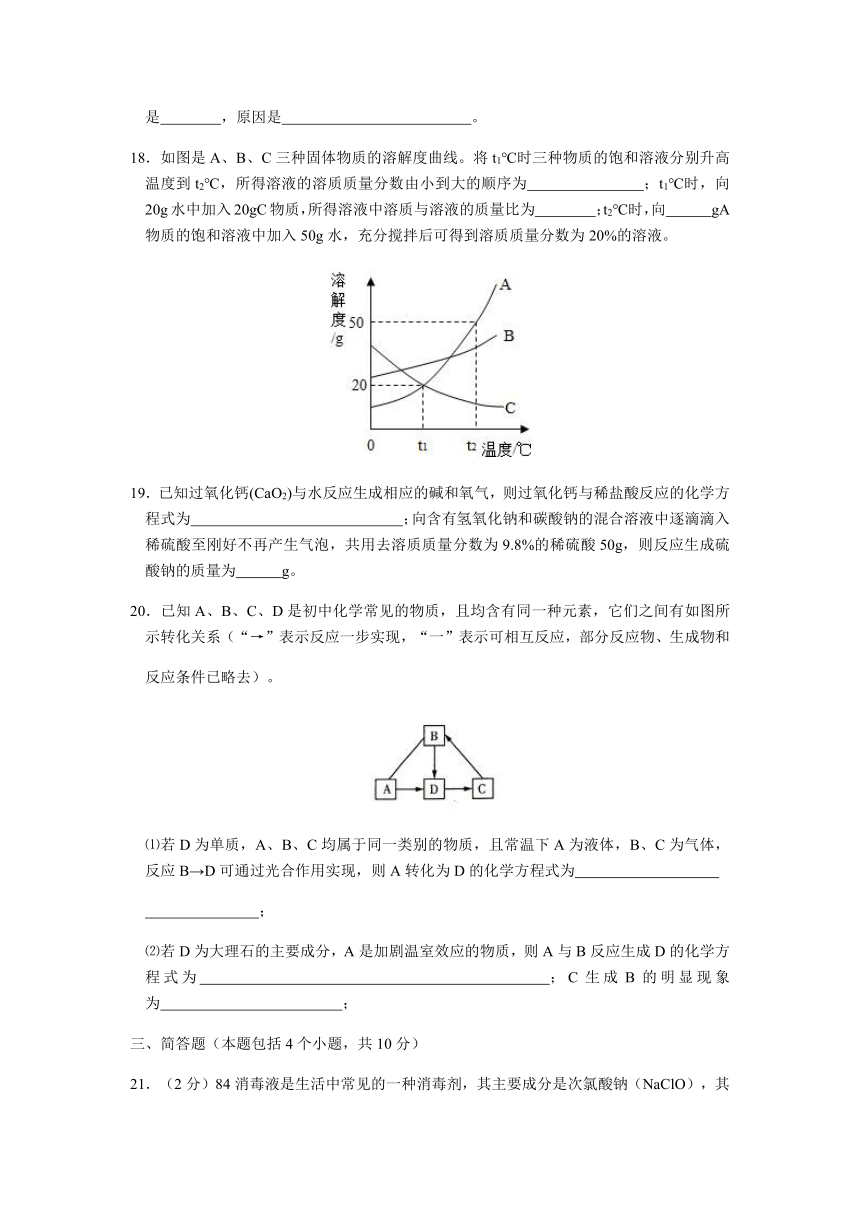
18.如图是A、B、C三种固体物质的溶解度曲线。将t1℃时三种物质的饱和溶液分别升高温度到t2℃,所得溶液的溶质质量分数由小到大的顺序为 ;t1℃时,向20g水中加入20gC物质,所得溶液中溶质与溶液的质量比为 ;t2℃时,向 gA物质的饱和溶液中加入50g水,充分搅拌后可得到溶质质量分数为20%的溶液。
19.已知过氧化钙(CaO2)与水反应生成相应的碱和氧气,则过氧化钙与稀盐酸反应的化学方程式为 ;向含有氢氧化钠和碳酸钠的混合溶液中逐滴滴入稀硫酸至刚好不再产生气泡,共用去溶质质量分数为9.8%的稀硫酸50g,则反应生成硫酸钠的质量为 g。
20.已知A、B、C、D是初中化学常见的物质,且均含有同一种元素,它们之间有如图所示转化关系(“→”表示反应一步实现,“一”表示可相互反应,部分反应物、生成物和
反应条件已略去)。
⑴若D为单质,A、B、C均属于同一类别的物质,且常温下A为液体,B、C为气体,反应B→D可通过光合作用实现,则A转化为D的化学方程式为
;
⑵若D为大理石的主要成分,A是加剧温室效应的物质,则A与B反应生成D的化学方程式为 ;C生成B的明显现象为 ;
三、简答题(本题包括4个小题,共10分)
21.(2分)84消毒液是生活中常见的一种消毒剂,其主要成分是次氯酸钠(NaClO),其消毒原理为2NaClO+CO2+X===Na2CO3+2HClO,生成的次氯酸(HClO)具有杀菌作用。
⑴写出X的化学式。
⑵根据消毒原理可知,在贮存84消毒液时应注意什么
22.(2分)下图是某化学反应的微观示意图。
⑴写出反应后生成C、D的分子个数比。
⑵写出该反应前后化合价一定发生变化的元素的符号。
23.(2分)患有胃酸过多症的人可服用碳酸氢钠片或铝碳酸镁片[主要成分为Al2Mg6(OH)16CO3]进行治疗,某兴趣小组的同学对这两种药物开展了如下探究。
⑴写出碳酸氢钠片与人体中的胃酸反应的化学方程式。
⑵如图是小组同学利用数字化实验装置分别模拟碳酸氢钠片、铝碳酸镁片与胃酸的反应(碳酸氢钠片与铝碳酸镁片规格相同,“胃酸”体积相同),探究两种药物中和酸的能力强弱的曲线图。分析图像可知,服用铝碳酸镁片治疗胃酸过多症的效果更好,请说明理由。
24.(4分)如图是实验室制取二氧化碳并验证其化学性质的部分装置。
⑴图A是实验室制取二氧化碳的发生装置,写出实验室制取二氧化碳的化学方程式,并将该装置补画完整。
⑵B中胶头滴管和水槽中均为氢氧化钠溶液,将胶头滴管中的溶液挤入烧瓶后,可观察到什么现象
⑶实验结束后,若要确定烧瓶内溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。
四、综合应用题(共10分)
25.酸、碱、盐、氧化物是九年级化学学习的重要知识。
⑴酸、碱、盐、氧化物之间发生复分解反应,一定会生成的物质是 (填字母序号)
a.酸 b.碱 c.盐 d.氧化物
⑵如图是氢氧化钠溶液与稀盐酸反应的实验操作和溶液pH变化示意图
①该反应的化学方程式为 ;
②当滴入溶液的体积为15mL时,溶液中的溶质为 。
⑶已知甲酸是一种具有挥发性的酸,在热的浓硫酸作用下分解生成H2O和CO。某化学兴趣小组利用甲酸分解产生的CO还原Fe2O3,并检验气体生成物,设计了下图所示实验装置。
①B装置的作用是什么
②写出C处玻璃管中发生反应的化学方程式。
⑷向盛有硝酸铜溶液的烧杯中,加入一定量锌粉和铁粉的混合物,充分反应后过滤,得到滤渣和滤液。
①若滤液呈无色,请分析滤渣的成分。
②所得滤液的质量与反应前溶液的质量相比,可能增大,其原因是什么
⑸实验室有一瓶标签破损的硝酸银溶液,为测定其溶质质量分数,取50.00g该硝酸银液,向其中加入足量的氯化钠溶液,充分反应后,过滤、洗涤、烘干,称得所得沉淀的质量为2.87g,则该硝酸银溶液的溶质质量分数是多少
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A B C D C A B D C C B B D C
NaHCO3 CO和CO2(答全才得分)
过滤 活性炭具有吸附性 最外层电子数
C2H5OH+3O22CO2+3H2O 氢气(或H2) 燃烧热值高(或产物无污染,合理即可)
C2CaO2+4HCl===2CaCl2+2H2O+O2↑ 7.1
⑴2H2O2H2↑+O2↑
⑵Ca(OH)2+CO2===CaCO3↓+H2O 放出大量热
⑴H2O(1分) ⑵密封保存。(1分)
⑴1:3(1分) ⑵N、O(写全才得分,1分)
⑴NaHCO3+HCl===NaCl+H2O+CO2↑(1分)
⑵相同时间内铝碳酸镁片使pH增大的程度更大。(1分)
24.⑴CaCO3+ 2HCl===CaCl2+H2O+CO2↑(1分)
见右图(长颈漏斗下端必须画到液面以下,1分)
⑵可观察到水槽中的氢氧化钠溶液迅速经导管进入烧瓶内,形成喷泉。(合理即可,1分)
⑶取少量烧瓶中的溶液于试管中,加入足量的CaCl2(或BaCl2等)溶液,有白色沉淀生成,说明溶质有Na2CO3,静置,向上层清液中滴加无色酚酞溶液,若溶液变红,则溶液中的溶质为Na2CO3和NaOH,若溶液不变红,则溶液中的溶质为Na2CO3。(1分)
25.⑴c(1分)
⑵①HCl+NaOH===NaCl+H2O(1分)
②NaOH和NaCl(1分)
⑶①吸收挥发出的甲酸,防止干扰气体生成物的检验。(合理即可,1分)
②Fe2O3+3CO2Fe+3CO2(1分)
⑷①一定有Cu、Fe,可能有Zn。(答全才得分,1分)
②Zn与Cu(NO3)2溶液反应,溶液质量增大;Fe与Cu(NO3)2溶液反应,溶液质量减小。当增大的质量大于减小的质量时,溶液质量增大。(1分)
⑸解:设50.00g该硝酸银溶液中AgNO3的质量为x。
AgNO3+NaCl===AgCl↓+NaNO3
170 143.5
x 2.87g
=
x=3.40g
该硝酸银溶液的溶质质量分数为×100%=6.8%
答:该硝酸银溶液的溶质质量分数为6.8%
(满分50分,考试时间50分钟)
相对原子质量 H:1 C:12 N:14 O:16 Na:23 Mg:24 S:32 Cl:35.5
Ca:40 Fe:56 Cu:64 Zn:65 Ag:108 Ba:137
选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
大米是中国人的主食之一,其中富含的营养物质是( )
糖类 B.蛋白质 C.维生素 D.油脂
下列物质的用途中,主要体现了物质的化学性质的是( )
用汽油除去油污 B.用氮气做保护气
用浓硫酸做干燥剂 D.用干冰进行人工降雨
“垃圾分类益处多,环境保护靠你我”。下列标志属于可回收标志的是( )
A B C D
下列空气的成分中,可用于霓虹灯的是( )
氮气 B.氧气 C.二氧化碳 D.稀有气体
5.2021年3月22日是第二十九届“世界水日”。世界水日的宗旨是唤起公众的节水意识,加强水资源保护。下列有关水的说法正确的是( )
明矾净水是为了降低水的硬度
水是由氢原子和氧原子构成的
长期饮用蒸馏水无益身体健康
过滤可以除去水中所有的杂质
6.下列各组物质中,都由离子构成的一组是( )
A.氯化钾、硝酸铵 B.氯化氢、硫酸镁
C.甲烷、干冰 D.钠、钾
7.下列图示的实验操作中正确的是( )
A.量取液体 B.干燥氧气 C.测溶液的pH D.称量固体
下列化学方程式中,符合题意且书写正确的是( )
稀盐酸与氧化铁反应:2HCl+FeO===FeCl2+H2O
实验室制取氢气:Cu+H2SO4===CuSO4+H2↑
除去CO2中含有的少量CO:2CO+O22CO2
正常雨水呈弱酸性的原因是:H2O+CO2===H2CO3
氯化钠是重要的化工原料,是氯碱工业的基础。电解饱和食盐水一定不能得到的物质是( )
A.H2 B.Cl2 C.Na2CO3 D.NaOH
10.分类、归纳是化学学习的重要方法。下列有关说法正确的是( )
A.甲烷、乙醇和干冰都属于有机化合物
B.尿素、硝酸钾、磷酸二氢铵都是复合肥料
C.蚕丝、羊毛、塑料都属于有机高分子材料
D.二氧化硫、二氧化氮和二氧化碳都是空气污染物
11.下列区分物质所用的方法或试剂不正确的是( )
A.硬水和软水——肥皂水
B.氮气和二氧化碳——燃着的木条
C.硝酸铵和硝酸钾固体——水
D.碳酸钠溶液和硫酸钠溶液——酚酞溶液
12.经测定,某溶液中含有大量的Na+、SO42-、Cl-、X四种离子,且四种离子个数比为1:1:1:1,则X可能是( )
A.K+ B.Cu2+ C.Ba2+ D.Al3+
13.下列图像分别与选项中的操作相对应,其中合理的是( )
A B C D
向一定量澄清石灰水中不断加入水
向盛有一定量铁粉的试管中不断滴加硫酸铜溶液
向两份完全相同的稀盐酸中分别加入足量锌、镁
用向上排空气法收集氧气时集气瓶内氧气的质量
现有40.0g氯化钡和氯化钙的固体混合物,加足量蒸馏水使之完全溶解,再加入足量碳酸钠溶液充分反应,将反应后的混合物过滤、洗涤、干燥,得到滤渣37.8g。则反应生成的氯化钠的质量为( )
A.5.85g B.11.70g C.23.4g D.35.1g
二、填空题(本题包括6个小题,每空1分,共16分)
15.焙制糕点所用发酵粉的主要成分之一是 (填化学式,下同);已知相同元素可以组成不同物质,则生物体中含量居前两位的元素形成的化合物为 。
16.为预防新型冠状病毒感染,在人员密集的场所需要佩戴口罩,医用口罩阻隔病毒的原理类似化学基本实验中的 操作;活性炭口罩能有效防止空气中的苯和甲醛等气体对人体的伤害,其原因是 ;下图是活性炭中碳原子的结构示意图,据图分析可知碳元素与硅元素的化学性质相似,原因是它们原子的 相同。
17.汽车已逐渐成为生活中重要的代步工具,使用乙醇汽油可以减少污染物的排放,乙醇充分燃烧的化学方程式为 ;你心目中最理想的汽车燃料是 ,原因是 。
18.如图是A、B、C三种固体物质的溶解度曲线。将t1℃时三种物质的饱和溶液分别升高温度到t2℃,所得溶液的溶质质量分数由小到大的顺序为 ;t1℃时,向20g水中加入20gC物质,所得溶液中溶质与溶液的质量比为 ;t2℃时,向 gA物质的饱和溶液中加入50g水,充分搅拌后可得到溶质质量分数为20%的溶液。
19.已知过氧化钙(CaO2)与水反应生成相应的碱和氧气,则过氧化钙与稀盐酸反应的化学方程式为 ;向含有氢氧化钠和碳酸钠的混合溶液中逐滴滴入稀硫酸至刚好不再产生气泡,共用去溶质质量分数为9.8%的稀硫酸50g,则反应生成硫酸钠的质量为 g。
20.已知A、B、C、D是初中化学常见的物质,且均含有同一种元素,它们之间有如图所示转化关系(“→”表示反应一步实现,“一”表示可相互反应,部分反应物、生成物和
反应条件已略去)。
⑴若D为单质,A、B、C均属于同一类别的物质,且常温下A为液体,B、C为气体,反应B→D可通过光合作用实现,则A转化为D的化学方程式为
;
⑵若D为大理石的主要成分,A是加剧温室效应的物质,则A与B反应生成D的化学方程式为 ;C生成B的明显现象为 ;
三、简答题(本题包括4个小题,共10分)
21.(2分)84消毒液是生活中常见的一种消毒剂,其主要成分是次氯酸钠(NaClO),其消毒原理为2NaClO+CO2+X===Na2CO3+2HClO,生成的次氯酸(HClO)具有杀菌作用。
⑴写出X的化学式。
⑵根据消毒原理可知,在贮存84消毒液时应注意什么
22.(2分)下图是某化学反应的微观示意图。
⑴写出反应后生成C、D的分子个数比。
⑵写出该反应前后化合价一定发生变化的元素的符号。
23.(2分)患有胃酸过多症的人可服用碳酸氢钠片或铝碳酸镁片[主要成分为Al2Mg6(OH)16CO3]进行治疗,某兴趣小组的同学对这两种药物开展了如下探究。
⑴写出碳酸氢钠片与人体中的胃酸反应的化学方程式。
⑵如图是小组同学利用数字化实验装置分别模拟碳酸氢钠片、铝碳酸镁片与胃酸的反应(碳酸氢钠片与铝碳酸镁片规格相同,“胃酸”体积相同),探究两种药物中和酸的能力强弱的曲线图。分析图像可知,服用铝碳酸镁片治疗胃酸过多症的效果更好,请说明理由。
24.(4分)如图是实验室制取二氧化碳并验证其化学性质的部分装置。
⑴图A是实验室制取二氧化碳的发生装置,写出实验室制取二氧化碳的化学方程式,并将该装置补画完整。
⑵B中胶头滴管和水槽中均为氢氧化钠溶液,将胶头滴管中的溶液挤入烧瓶后,可观察到什么现象
⑶实验结束后,若要确定烧瓶内溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。
四、综合应用题(共10分)
25.酸、碱、盐、氧化物是九年级化学学习的重要知识。
⑴酸、碱、盐、氧化物之间发生复分解反应,一定会生成的物质是 (填字母序号)
a.酸 b.碱 c.盐 d.氧化物
⑵如图是氢氧化钠溶液与稀盐酸反应的实验操作和溶液pH变化示意图
①该反应的化学方程式为 ;
②当滴入溶液的体积为15mL时,溶液中的溶质为 。
⑶已知甲酸是一种具有挥发性的酸,在热的浓硫酸作用下分解生成H2O和CO。某化学兴趣小组利用甲酸分解产生的CO还原Fe2O3,并检验气体生成物,设计了下图所示实验装置。
①B装置的作用是什么
②写出C处玻璃管中发生反应的化学方程式。
⑷向盛有硝酸铜溶液的烧杯中,加入一定量锌粉和铁粉的混合物,充分反应后过滤,得到滤渣和滤液。
①若滤液呈无色,请分析滤渣的成分。
②所得滤液的质量与反应前溶液的质量相比,可能增大,其原因是什么
⑸实验室有一瓶标签破损的硝酸银溶液,为测定其溶质质量分数,取50.00g该硝酸银液,向其中加入足量的氯化钠溶液,充分反应后,过滤、洗涤、烘干,称得所得沉淀的质量为2.87g,则该硝酸银溶液的溶质质量分数是多少
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A B C D C A B D C C B B D C
NaHCO3 CO和CO2(答全才得分)
过滤 活性炭具有吸附性 最外层电子数
C2H5OH+3O22CO2+3H2O 氢气(或H2) 燃烧热值高(或产物无污染,合理即可)
C
⑴2H2O2H2↑+O2↑
⑵Ca(OH)2+CO2===CaCO3↓+H2O 放出大量热
⑴H2O(1分) ⑵密封保存。(1分)
⑴1:3(1分) ⑵N、O(写全才得分,1分)
⑴NaHCO3+HCl===NaCl+H2O+CO2↑(1分)
⑵相同时间内铝碳酸镁片使pH增大的程度更大。(1分)
24.⑴CaCO3+ 2HCl===CaCl2+H2O+CO2↑(1分)
见右图(长颈漏斗下端必须画到液面以下,1分)
⑵可观察到水槽中的氢氧化钠溶液迅速经导管进入烧瓶内,形成喷泉。(合理即可,1分)
⑶取少量烧瓶中的溶液于试管中,加入足量的CaCl2(或BaCl2等)溶液,有白色沉淀生成,说明溶质有Na2CO3,静置,向上层清液中滴加无色酚酞溶液,若溶液变红,则溶液中的溶质为Na2CO3和NaOH,若溶液不变红,则溶液中的溶质为Na2CO3。(1分)
25.⑴c(1分)
⑵①HCl+NaOH===NaCl+H2O(1分)
②NaOH和NaCl(1分)
⑶①吸收挥发出的甲酸,防止干扰气体生成物的检验。(合理即可,1分)
②Fe2O3+3CO2Fe+3CO2(1分)
⑷①一定有Cu、Fe,可能有Zn。(答全才得分,1分)
②Zn与Cu(NO3)2溶液反应,溶液质量增大;Fe与Cu(NO3)2溶液反应,溶液质量减小。当增大的质量大于减小的质量时,溶液质量增大。(1分)
⑸解:设50.00g该硝酸银溶液中AgNO3的质量为x。
AgNO3+NaCl===AgCl↓+NaNO3
170 143.5
x 2.87g
=
x=3.40g
该硝酸银溶液的溶质质量分数为×100%=6.8%
答:该硝酸银溶液的溶质质量分数为6.8%
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
