铁和铜及其化合物的应用1
图片预览






文档简介
(共24张PPT)
铁和铜及其化合物的应用
在含有Fe3+的溶液中加入硫氰化钾(KSCN)溶液,溶液变成血红色
Fe3++3SCN- Fe(SCN)3
请你设计实验方案:用不同的方法鉴别待检液A、B。
实验室提供以下试剂:
待检液A、待检液B(FeCl3或FeCl2)0.5moL/LNaOH溶液、KSCN溶液
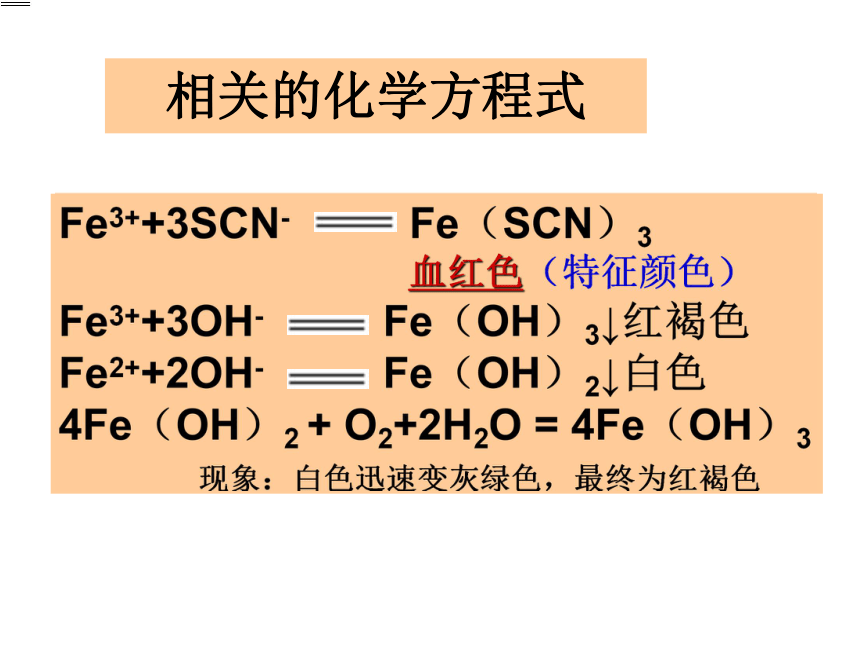
相关的化学方程式
Fe3++3SCN- Fe(SCN)3
血红色(特征颜色)
Fe3++3OH- Fe(OH)3↓红褐色
Fe2++2OH- Fe(OH)2↓白色
4Fe(OH)2 + O2+2H2O = 4Fe(OH)3
现象:白色迅速变灰绿色,最终为红褐色
实验员小王的困惑
昨日配置的硫酸亚铁溶液的怎么变成了浅黄色呢 这是怎么回事呢?该怎么办呢?
实验目的:找出一种强氧化剂,将FeCl2转变成FeCl3,并验证这一转变
实验室提供以下试剂:
0.1mol/L FeCl3溶液(A溶液)、
0.1mol/L FeCl2溶液(B溶液)、 KSCN溶液、还原铁粉、新制氯水、淀粉KI试纸
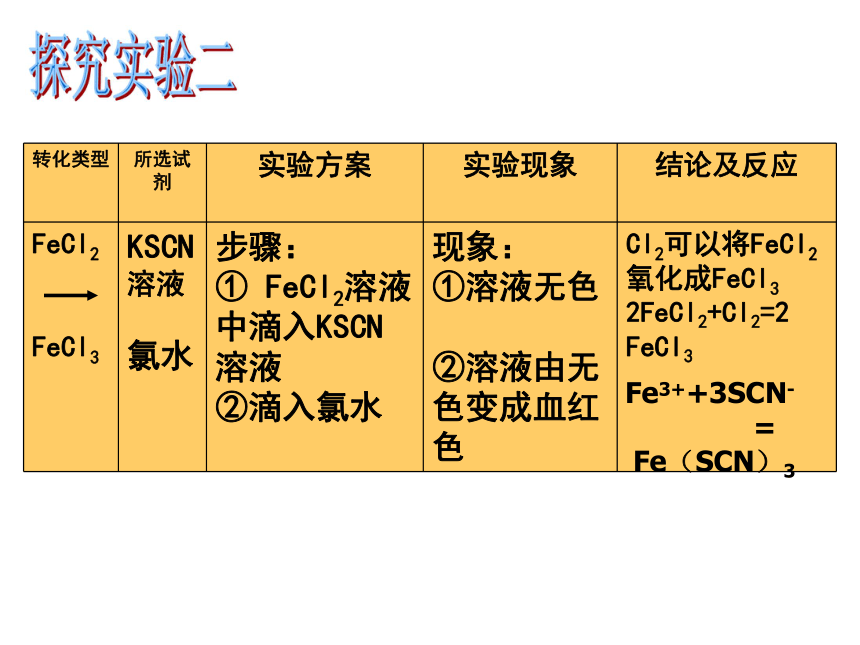
转化类型 所选试剂 实验方案 实验现象 结论及反应
FeCl2
FeCl3 KSCN溶液
氯水 步骤:
① FeCl2溶液中滴入KSCN溶液
②滴入氯水 现象:
①溶液无色
②溶液由无色变成血红色 Cl2可以将FeCl2氧化成FeCl3
2FeCl2+Cl2=2 FeCl3
Fe3++3SCN-
=
Fe(SCN)3
实验目的:找出一种还原剂,将FeCl3转变成FeCl2,并验证这一转变
实验室提供以下试剂:
0.1mol/L FeCl3溶液(A溶液)、
0.1mol/L FeCl2溶液(B溶液)、
KSCN溶液、还原铁粉、新制氯水、淀粉KI试纸
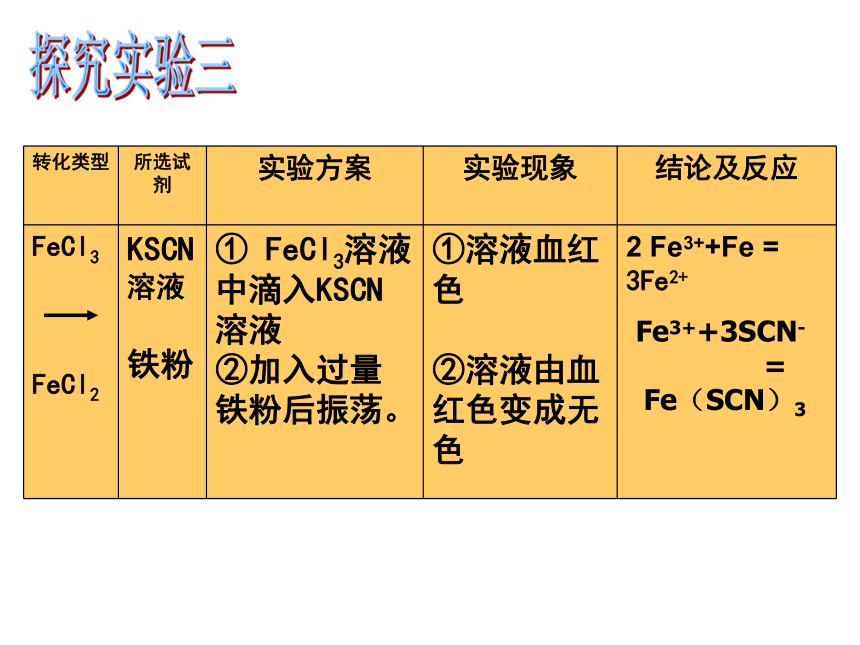
转化类型 所选试剂 实验方案 实验现象 结论及反应
FeCl3
FeCl2 KSCN溶液
铁粉 ① FeCl3溶液中滴入KSCN溶液
②加入过量铁粉后振荡。 ①溶液血红色
②溶液由血红色变成无色 2 Fe3++Fe = 3Fe2+
Fe3++3SCN-
=
Fe(SCN)3
电路板
三、铁及铜的化合物的应用
1、铁的化合物
①Fe2O3作颜料
②氯化铁、硫酸亚铁可作净水剂
③作磁性材料
④维持生命的微量元素
2、铜的化合物:
铜盐可杀菌,CuSO4溶液杀灭寄生虫,治疗皮肤病。
1.如何除去杂质,提纯下列各物质
混合物成分 提纯所用试剂
(1)FeCl2中含少量FeCl3
(2)FeCl3中含少量FeCl2
(3)FeSO4中含少量CuSO4
讨论与思考
足量铁粉
足量Cl2或氯水
足量铁粉
2、苹果汁是人们喜爱的饮料,由于此饮料中含有,现榨的苹果汁在空气中会由浅绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
氧化性 B. 还原性 C. 碱性 D. 酸性
B
讨论与思考
3、将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是( )
A.硫酸 B.氯水
C.硫酸锌 D.氯化铜
B
讨论与思考
4、在配置Fe2+溶液时,常常需要向溶液中加入少量铁粉,
原因是 ;
离子方程式 。
讨论与思考
5.某化工厂为消除所排出的废气中Cl2对环境的污染,
将含Cl2的废气通过含铁单质的FeCl2溶液中即可有效
地除去Cl2,这一处理过程可用化学方程式表示为:
。
处理过程中需要定期添加的原料是 。
①2FeCl2+Cl2=2FeCl3 ② 2FeCl3+Fe=3FeCl2
Fe
讨论与思考
6、请将适量的铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是 。
2∶3
讨论与思考
小结
Fe
2+
Fe
3+
与
的鉴别
一、
Fe
2+
Fe
3+
与
的相互转化
二、
三、铁及铜的化合物的应用
练习:
3、为什么说制备Fe(OH)2要用新制的的硫酸亚铁溶液?
原因:硫酸亚铁易被空气中的氧气氧化而影响效果。
4、怎样才能使Fe2+溶液长时间保存?
在配制溶液时,要加入铁钉或少量铁粉防止氧化,加入少量对应酸抑制水解。
练习:
[5]用FeCl3溶液腐蚀印刷线路板(铜)。请写出离子方程式
,若想从废液中回收铜,应如何操作: 。将适量的铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是 。
加入过量的铁粉后过滤,用磁铁吸取铁得到铜或用酸洗后水洗干燥
1、要证明某溶液中不含
练习:
Fe
3+
Fe
2+
而可能含有
,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4
③加入少量KSCN溶液
( )
①③ B. ③② C. ③① D. ①②③
C
2、要证明某溶液中不含
练习:
Fe
3+
Fe
2+
而可能含有
,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4 ③加入少量KSCN溶液
( )
A. ①③ B. ③② C. ③① D. ①②③
C
1、向某溶液中加入含
Fe
2+
的溶液后,无明显变化,当再滴加几滴新制氯水后,
混合液变成血红色,则下列结论中错误的是 ( )
A.该溶液中一定含有SCN
-
Fe
3+
B.氧化性: >Cl2
Fe
2+
SCN
-
与 不能形成红色物质
C.
D.
Fe
2+
Fe
3+
被氯水氧化为
B
用毛笔蘸取少量30%FeCl3溶液,在铜片上画一个十字,放置片刻后,用少量水将铜片上的溶液冲到小烧杯中。有什么现象?方程式?
Cu + 2Fe3+= Cu2+ + 2Fe2+
铜与Fe3+反应:
活动与探究
一、Fe2+与 Fe3+的鉴别
鉴别方法 Fe2+ Fe3+
1
2
3
观察溶液颜色
与KSCN反应
溶液变为血红色
无明显现象
与NaOH反应
白色沉淀迅速变灰
绿色最后呈红褐色
立即产生红
褐色沉淀
浅绿色
棕黄色
铁和铜及其化合物的应用
在含有Fe3+的溶液中加入硫氰化钾(KSCN)溶液,溶液变成血红色
Fe3++3SCN- Fe(SCN)3
请你设计实验方案:用不同的方法鉴别待检液A、B。
实验室提供以下试剂:
待检液A、待检液B(FeCl3或FeCl2)0.5moL/LNaOH溶液、KSCN溶液
相关的化学方程式
Fe3++3SCN- Fe(SCN)3
血红色(特征颜色)
Fe3++3OH- Fe(OH)3↓红褐色
Fe2++2OH- Fe(OH)2↓白色
4Fe(OH)2 + O2+2H2O = 4Fe(OH)3
现象:白色迅速变灰绿色,最终为红褐色
实验员小王的困惑
昨日配置的硫酸亚铁溶液的怎么变成了浅黄色呢 这是怎么回事呢?该怎么办呢?
实验目的:找出一种强氧化剂,将FeCl2转变成FeCl3,并验证这一转变
实验室提供以下试剂:
0.1mol/L FeCl3溶液(A溶液)、
0.1mol/L FeCl2溶液(B溶液)、 KSCN溶液、还原铁粉、新制氯水、淀粉KI试纸
转化类型 所选试剂 实验方案 实验现象 结论及反应
FeCl2
FeCl3 KSCN溶液
氯水 步骤:
① FeCl2溶液中滴入KSCN溶液
②滴入氯水 现象:
①溶液无色
②溶液由无色变成血红色 Cl2可以将FeCl2氧化成FeCl3
2FeCl2+Cl2=2 FeCl3
Fe3++3SCN-
=
Fe(SCN)3
实验目的:找出一种还原剂,将FeCl3转变成FeCl2,并验证这一转变
实验室提供以下试剂:
0.1mol/L FeCl3溶液(A溶液)、
0.1mol/L FeCl2溶液(B溶液)、
KSCN溶液、还原铁粉、新制氯水、淀粉KI试纸
转化类型 所选试剂 实验方案 实验现象 结论及反应
FeCl3
FeCl2 KSCN溶液
铁粉 ① FeCl3溶液中滴入KSCN溶液
②加入过量铁粉后振荡。 ①溶液血红色
②溶液由血红色变成无色 2 Fe3++Fe = 3Fe2+
Fe3++3SCN-
=
Fe(SCN)3
电路板
三、铁及铜的化合物的应用
1、铁的化合物
①Fe2O3作颜料
②氯化铁、硫酸亚铁可作净水剂
③作磁性材料
④维持生命的微量元素
2、铜的化合物:
铜盐可杀菌,CuSO4溶液杀灭寄生虫,治疗皮肤病。
1.如何除去杂质,提纯下列各物质
混合物成分 提纯所用试剂
(1)FeCl2中含少量FeCl3
(2)FeCl3中含少量FeCl2
(3)FeSO4中含少量CuSO4
讨论与思考
足量铁粉
足量Cl2或氯水
足量铁粉
2、苹果汁是人们喜爱的饮料,由于此饮料中含有,现榨的苹果汁在空气中会由浅绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
氧化性 B. 还原性 C. 碱性 D. 酸性
B
讨论与思考
3、将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是( )
A.硫酸 B.氯水
C.硫酸锌 D.氯化铜
B
讨论与思考
4、在配置Fe2+溶液时,常常需要向溶液中加入少量铁粉,
原因是 ;
离子方程式 。
讨论与思考
5.某化工厂为消除所排出的废气中Cl2对环境的污染,
将含Cl2的废气通过含铁单质的FeCl2溶液中即可有效
地除去Cl2,这一处理过程可用化学方程式表示为:
。
处理过程中需要定期添加的原料是 。
①2FeCl2+Cl2=2FeCl3 ② 2FeCl3+Fe=3FeCl2
Fe
讨论与思考
6、请将适量的铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是 。
2∶3
讨论与思考
小结
Fe
2+
Fe
3+
与
的鉴别
一、
Fe
2+
Fe
3+
与
的相互转化
二、
三、铁及铜的化合物的应用
练习:
3、为什么说制备Fe(OH)2要用新制的的硫酸亚铁溶液?
原因:硫酸亚铁易被空气中的氧气氧化而影响效果。
4、怎样才能使Fe2+溶液长时间保存?
在配制溶液时,要加入铁钉或少量铁粉防止氧化,加入少量对应酸抑制水解。
练习:
[5]用FeCl3溶液腐蚀印刷线路板(铜)。请写出离子方程式
,若想从废液中回收铜,应如何操作: 。将适量的铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是 。
加入过量的铁粉后过滤,用磁铁吸取铁得到铜或用酸洗后水洗干燥
1、要证明某溶液中不含
练习:
Fe
3+
Fe
2+
而可能含有
,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4
③加入少量KSCN溶液
( )
①③ B. ③② C. ③① D. ①②③
C
2、要证明某溶液中不含
练习:
Fe
3+
Fe
2+
而可能含有
,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4 ③加入少量KSCN溶液
( )
A. ①③ B. ③② C. ③① D. ①②③
C
1、向某溶液中加入含
Fe
2+
的溶液后,无明显变化,当再滴加几滴新制氯水后,
混合液变成血红色,则下列结论中错误的是 ( )
A.该溶液中一定含有SCN
-
Fe
3+
B.氧化性: >Cl2
Fe
2+
SCN
-
与 不能形成红色物质
C.
D.
Fe
2+
Fe
3+
被氯水氧化为
B
用毛笔蘸取少量30%FeCl3溶液,在铜片上画一个十字,放置片刻后,用少量水将铜片上的溶液冲到小烧杯中。有什么现象?方程式?
Cu + 2Fe3+= Cu2+ + 2Fe2+
铜与Fe3+反应:
活动与探究
一、Fe2+与 Fe3+的鉴别
鉴别方法 Fe2+ Fe3+
1
2
3
观察溶液颜色
与KSCN反应
溶液变为血红色
无明显现象
与NaOH反应
白色沉淀迅速变灰
绿色最后呈红褐色
立即产生红
褐色沉淀
浅绿色
棕黄色
