第二章 空气、物质的构成测试卷-2021-2022学年九年级化学上册科粤版(含答案)
文档属性
| 名称 | 第二章 空气、物质的构成测试卷-2021-2022学年九年级化学上册科粤版(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 395.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-26 20:22:45 | ||
图片预览


文档简介
第二章 空气、物质的构成测试卷
(时间:40分钟 满分:100分)
一、选择题(每小题只有一个选项符合题意。每小题3分,共45分)
1.下列符号中,既有宏观意义,又有微观意义的是( )
A.Fe B.Fe2+ C.Fe3+ D.2Fe
2.下列物质由原子构成的是( )
A.蒸馏水 B.金刚石 C.氯化钠 D.五氧化二磷
3.下列情况中不会造成环境污染的是( )
A,垃圾的燃烧
B.汽车尾气的排放
C.鞭炮的燃放
D.绿色植物的光合作用
4.下列空气的成分中按体积分数由多到少顺序排列的是( )
①氧气 ②二氧化碳 ③氮气 ④稀有气体
A.①②③④ B.①③②④ C.③①④② D. ③①②④
5.如图装置常用来测定空气中氧气的含量。下列对该实验认识正确的是( )
A.红磷燃烧产生大量白
B.该实验可说明氮气难溶于水
C.燃烧结束后立刻打开止水夹
D.红磷的量不足会导致进人集气瓶中水的体积大于1/5
6.同学们积极参与“我们的呼吸作用”实验探究活动,但得到的结论却大不相同。下列结论正确的是( )
A.我们呼出的气体极易溶于水 B.我们吸入的气体全部是氧气
C.我们呼出的气体里含有水蒸气 D.我们呼出的气体全部为二氧化碳
7.下列有关原子的叙述不正确的是( )
A.原子在化学变化中能够再分 B.原子的质子数等于核外电子数
C.原子的质量主要集中在原子核上 D.符号“〇”可以代表一个氧原子
8.下列有关物质的构成与原子、分子的关系中,正确的是( )
9.用分子的观点对下列事实进行解释,错误的是( )
A.在花园中可闻到花香——分子在不断地运动
B.用肉眼不能直接观察到CO2分子——CO2分子很小
C.冰受热变为水,水受热变为水蒸气——分子可以再分
D.50 mL水与50 mL乙醇混合,态译枳小于100 ml——分子之间有间隔
10.影响元素化学性质的最主要因素是( )
A.原子的最外层电子数 B.原子的电子层数
C.原子的质子数 D.组成某种物质的原子个数
11.如图是某微粒X的结构示意图,下列说法正确的是( )
涝
A.X是金属元素 B.该微粒可表示为X+
C.该微粒的核电荷数为18 D.该微粒最外层电子已达到稳定结构
12.下列说法中正确的是( )
A.原子失去电子后变成阴离子 B.金属都是由原子直接构成的
C.分子是化学变化中的最小微粒 D.元素间最本质的区别是中子数不同
13.下列“○”“”“●”分别表示氢、氯、氧三种不同元素的原子,其中表示氧化物的是( )
14.下列事实不能作为相应观点的证据的是( )
A.尘土飞扬,说明分子总是在不断地运动着
B.水蒸发属于物理变化,说明水蒸发过程中分子种类没有改变
C.气体被压缩后体积发生了较大变化,说明气体分子间的距离大
D.将两个干净平整的铅柱紧压在一起会结合起来,说明分子间存在引力
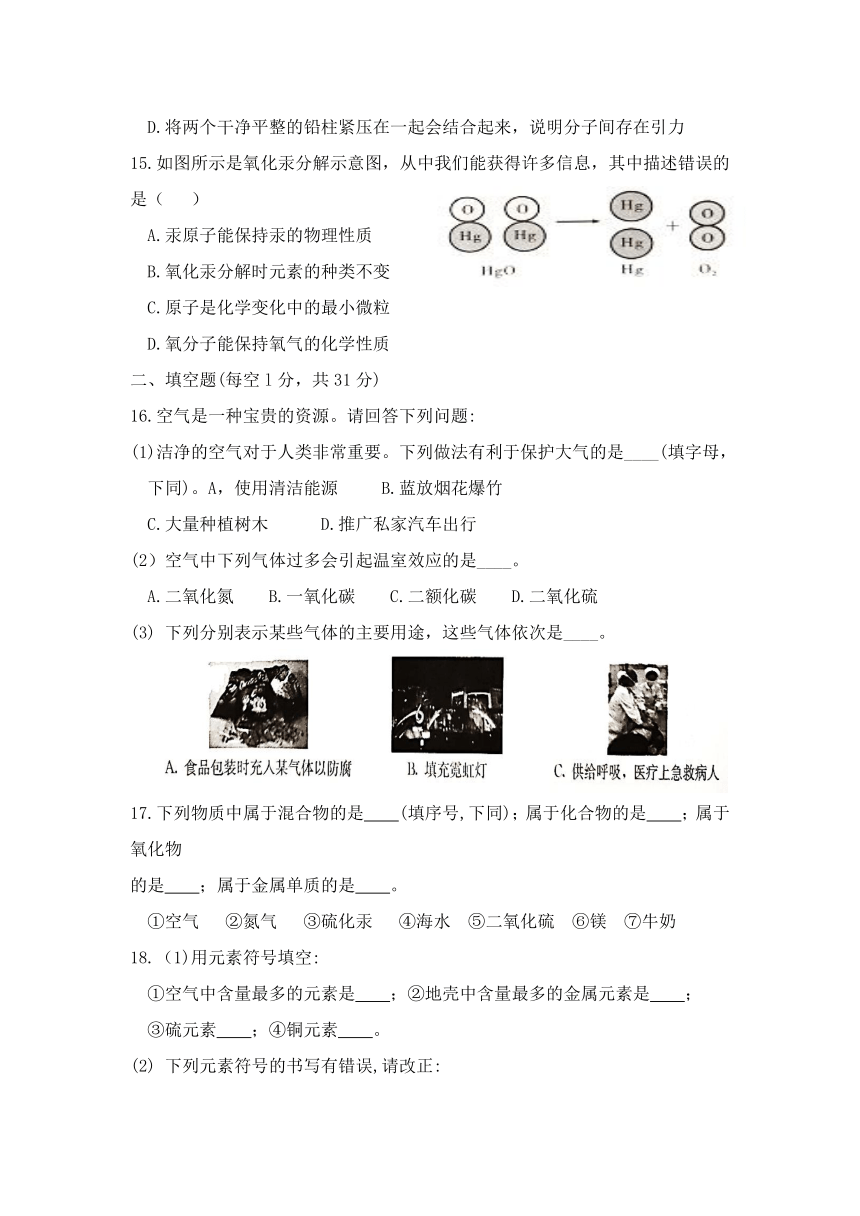
15.如图所示是氧化汞分解示意图,从中我们能获得许多信息,其中描述错误的是( )
A.汞原子能保持汞的物理性质
B.氧化汞分解时元素的种类不变
C.原子是化学变化中的最小微粒
D.氧分子能保持氧气的化学性质
二、填空题(每空l分,共31分)
16.空气是一种宝贵的资源。请回答下列问题:
(1)洁净的空气对于人类非常重要。下列做法有利于保护大气的是____(填字母,下同)。A,使用清洁能源 B.蓝放烟花爆竹
C.大量种植树木 D.推广私家汽车出行
(2)空气中下列气体过多会引起温室效应的是____。
A.二氧化氮 B.一氧化碳 C.二额化碳 D.二氧化硫
(3) 下列分别表示某些气体的主要用途,这些气体依次是____。
17.下列物质中属于混合物的是 (填序号,下同);属于化合物的是 ;属于氧化物
的是 ;属于金属单质的是 。
①空气 ②氮气 ③硫化汞 ④海水 ⑤二氧化硫 ⑥镁 ⑦牛奶
18.(1)用元素符号填空:
①空气中含量最多的元素是 ;②地壳中含量最多的金属元素是 ;
③硫元素 ;④铜元素 。
(2) 下列元素符号的书写有错误,请改正:
①氦N ;②汞Ag ;③氯cl ;④锰MN ;⑤送mG 。
19.用原子、分子的观点回答下列问题:
(1)化学变化中的最小微粒是 。
(2)氧化汞在分解成汞和氧气的过程中,不变的微粒是 。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是 。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是 。
20.图4是钠元素和氯元素在元素周期表中的信息和3种微粒的结构示意图。请回答下列问题:
(1)氯原子的核电荷数是 ,钠原子与氯原子最本质的区别是 。
(2)氯化钠由 和 构成。在钠和氯气生成氯化钠的反应中,得到电子的是 。
(3)图4中表示钠离子结构示意图的是 (填字母,下同),表示同种元素的是 。
21.下表列出了几种原子中的质子、中子、电子的数目,以及各种原子的相对原子质量。
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
铁 26 30 26 56
铀 92 146 92 238
通过此表,除了可以总结出“在原子中质子数等于核外电子数”,还能总结出:
(1) ;
(2) ;
(3) ;
(4) 。
三、实验探究题(每空2分,共24 分)
22.某校化学兴趣小组就空气中氧气的含量进行实验探究。
【小组讨论】(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择 (填字母),为了充分消耗容器中的氧气,药品的用量应保证 。
a.蜡烛 b.红磷 c.硫 d.木炭
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是 (填字母)。为了确保实验的成功,在装药品之前应 。
【小组实验】在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下。(注:集气瓶容积为100 mL)
组别 1 2 3 4 5 6
进人集气瓶中水的体积/ml 20 21 19 20 22 19
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 。
通过实验还可以推断集气瓶中剩余气体的主要成分是 ,该气体具有 。的性质。
23.如图中Ⅰ是研究温度对微粒运动速率影响的实验,实验时同学们闻到了氨气强烈的刺激性气味。小明查阅资料得知氨气极易溶于水,他做了如图Ⅱ所示的改进实验,过程如下:
【实验操作】步骤一:向B、D、F三支试管中分别加入5 mL蒸馏水,各滴人1~2滴无色酚酞溶液,振荡,观察溶液颜色。
步骤二:向A、E试管中分别加入2mL浓氨水,立即用带有橡皮塞的导管按图Ⅱ连接好,并将E试管放在盛有热水的烧杯中,观察几分钟。
【分析讨论】(1)Ⅰ实验中能观察到湿润的酚酞试纸变 色。
(2)改进后的实验中使用了F试管,其作用是 。
(3)步骤二中将E试管放置在盛有热水的烧杯中,最先可观察到的现象是E中试管内冒气泡,然后可观察到B、D试管中先出现颜色变化的是_____试管,由此可得出结论_____。
(4)与Ⅰ实验相比,改进后的实验的一个主要优点是_____。
第二章 空气、物质的构成测试卷
参考答案
一、选择题(每小题只有一个选项符合题意。每小题3分,共45分)
1.A 2.B 3.D 4.C 5.B 6.C 7.A 8.D
9.C 10.A 11.D 12.B 13.C 14.A 15.A
二、填空题(每空l分,共31分)
16.(1)AC(2)C(3)氮气、稀有气体、氧气
17.④⑦、③⑤、⑤、②⑥
18.(1)①N ②Al ③s ④Cu (2)①He ②Hg ③CI ④Mn ⑤Mg
19.(1)原子(2)汞原子和氧原子(3)水分子在不断地运动(4)温度降低,分子之间的间隔变小了
20.(1)17质子数不同(2)钠离子氯离子氯原子(3)AA、B
21.(1)相对原子质量=质子数+中子数(2)原子核内不一定有中子(3)质子数不同,元素种类就不同(4)原子核内质子数不一定等于中子数(答案合理即可)
三、实验探究题(每空2分,共24 分)
22.(1)b足量(或过量)(2)A检查装置的气密性(3)1/5氮气难溶于水.(或化学性质不活泼等)
23.(1)红(2)做对比实验(3)D 温度越高,分子运动速率越快(4)能尽量防止氨气逸出污染空气
(时间:40分钟 满分:100分)
一、选择题(每小题只有一个选项符合题意。每小题3分,共45分)
1.下列符号中,既有宏观意义,又有微观意义的是( )
A.Fe B.Fe2+ C.Fe3+ D.2Fe
2.下列物质由原子构成的是( )
A.蒸馏水 B.金刚石 C.氯化钠 D.五氧化二磷
3.下列情况中不会造成环境污染的是( )
A,垃圾的燃烧
B.汽车尾气的排放
C.鞭炮的燃放
D.绿色植物的光合作用
4.下列空气的成分中按体积分数由多到少顺序排列的是( )
①氧气 ②二氧化碳 ③氮气 ④稀有气体
A.①②③④ B.①③②④ C.③①④② D. ③①②④
5.如图装置常用来测定空气中氧气的含量。下列对该实验认识正确的是( )
A.红磷燃烧产生大量白
B.该实验可说明氮气难溶于水
C.燃烧结束后立刻打开止水夹
D.红磷的量不足会导致进人集气瓶中水的体积大于1/5
6.同学们积极参与“我们的呼吸作用”实验探究活动,但得到的结论却大不相同。下列结论正确的是( )
A.我们呼出的气体极易溶于水 B.我们吸入的气体全部是氧气
C.我们呼出的气体里含有水蒸气 D.我们呼出的气体全部为二氧化碳
7.下列有关原子的叙述不正确的是( )
A.原子在化学变化中能够再分 B.原子的质子数等于核外电子数
C.原子的质量主要集中在原子核上 D.符号“〇”可以代表一个氧原子
8.下列有关物质的构成与原子、分子的关系中,正确的是( )
9.用分子的观点对下列事实进行解释,错误的是( )
A.在花园中可闻到花香——分子在不断地运动
B.用肉眼不能直接观察到CO2分子——CO2分子很小
C.冰受热变为水,水受热变为水蒸气——分子可以再分
D.50 mL水与50 mL乙醇混合,态译枳小于100 ml——分子之间有间隔
10.影响元素化学性质的最主要因素是( )
A.原子的最外层电子数 B.原子的电子层数
C.原子的质子数 D.组成某种物质的原子个数
11.如图是某微粒X的结构示意图,下列说法正确的是( )
涝
A.X是金属元素 B.该微粒可表示为X+
C.该微粒的核电荷数为18 D.该微粒最外层电子已达到稳定结构
12.下列说法中正确的是( )
A.原子失去电子后变成阴离子 B.金属都是由原子直接构成的
C.分子是化学变化中的最小微粒 D.元素间最本质的区别是中子数不同
13.下列“○”“”“●”分别表示氢、氯、氧三种不同元素的原子,其中表示氧化物的是( )
14.下列事实不能作为相应观点的证据的是( )
A.尘土飞扬,说明分子总是在不断地运动着
B.水蒸发属于物理变化,说明水蒸发过程中分子种类没有改变
C.气体被压缩后体积发生了较大变化,说明气体分子间的距离大
D.将两个干净平整的铅柱紧压在一起会结合起来,说明分子间存在引力
15.如图所示是氧化汞分解示意图,从中我们能获得许多信息,其中描述错误的是( )
A.汞原子能保持汞的物理性质
B.氧化汞分解时元素的种类不变
C.原子是化学变化中的最小微粒
D.氧分子能保持氧气的化学性质
二、填空题(每空l分,共31分)
16.空气是一种宝贵的资源。请回答下列问题:
(1)洁净的空气对于人类非常重要。下列做法有利于保护大气的是____(填字母,下同)。A,使用清洁能源 B.蓝放烟花爆竹
C.大量种植树木 D.推广私家汽车出行
(2)空气中下列气体过多会引起温室效应的是____。
A.二氧化氮 B.一氧化碳 C.二额化碳 D.二氧化硫
(3) 下列分别表示某些气体的主要用途,这些气体依次是____。
17.下列物质中属于混合物的是 (填序号,下同);属于化合物的是 ;属于氧化物
的是 ;属于金属单质的是 。
①空气 ②氮气 ③硫化汞 ④海水 ⑤二氧化硫 ⑥镁 ⑦牛奶
18.(1)用元素符号填空:
①空气中含量最多的元素是 ;②地壳中含量最多的金属元素是 ;
③硫元素 ;④铜元素 。
(2) 下列元素符号的书写有错误,请改正:
①氦N ;②汞Ag ;③氯cl ;④锰MN ;⑤送mG 。
19.用原子、分子的观点回答下列问题:
(1)化学变化中的最小微粒是 。
(2)氧化汞在分解成汞和氧气的过程中,不变的微粒是 。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是 。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是 。
20.图4是钠元素和氯元素在元素周期表中的信息和3种微粒的结构示意图。请回答下列问题:
(1)氯原子的核电荷数是 ,钠原子与氯原子最本质的区别是 。
(2)氯化钠由 和 构成。在钠和氯气生成氯化钠的反应中,得到电子的是 。
(3)图4中表示钠离子结构示意图的是 (填字母,下同),表示同种元素的是 。
21.下表列出了几种原子中的质子、中子、电子的数目,以及各种原子的相对原子质量。
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
铁 26 30 26 56
铀 92 146 92 238
通过此表,除了可以总结出“在原子中质子数等于核外电子数”,还能总结出:
(1) ;
(2) ;
(3) ;
(4) 。
三、实验探究题(每空2分,共24 分)
22.某校化学兴趣小组就空气中氧气的含量进行实验探究。
【小组讨论】(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择 (填字母),为了充分消耗容器中的氧气,药品的用量应保证 。
a.蜡烛 b.红磷 c.硫 d.木炭
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是 (填字母)。为了确保实验的成功,在装药品之前应 。
【小组实验】在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下。(注:集气瓶容积为100 mL)
组别 1 2 3 4 5 6
进人集气瓶中水的体积/ml 20 21 19 20 22 19
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 。
通过实验还可以推断集气瓶中剩余气体的主要成分是 ,该气体具有 。的性质。
23.如图中Ⅰ是研究温度对微粒运动速率影响的实验,实验时同学们闻到了氨气强烈的刺激性气味。小明查阅资料得知氨气极易溶于水,他做了如图Ⅱ所示的改进实验,过程如下:
【实验操作】步骤一:向B、D、F三支试管中分别加入5 mL蒸馏水,各滴人1~2滴无色酚酞溶液,振荡,观察溶液颜色。
步骤二:向A、E试管中分别加入2mL浓氨水,立即用带有橡皮塞的导管按图Ⅱ连接好,并将E试管放在盛有热水的烧杯中,观察几分钟。
【分析讨论】(1)Ⅰ实验中能观察到湿润的酚酞试纸变 色。
(2)改进后的实验中使用了F试管,其作用是 。
(3)步骤二中将E试管放置在盛有热水的烧杯中,最先可观察到的现象是E中试管内冒气泡,然后可观察到B、D试管中先出现颜色变化的是_____试管,由此可得出结论_____。
(4)与Ⅰ实验相比,改进后的实验的一个主要优点是_____。
第二章 空气、物质的构成测试卷
参考答案
一、选择题(每小题只有一个选项符合题意。每小题3分,共45分)
1.A 2.B 3.D 4.C 5.B 6.C 7.A 8.D
9.C 10.A 11.D 12.B 13.C 14.A 15.A
二、填空题(每空l分,共31分)
16.(1)AC(2)C(3)氮气、稀有气体、氧气
17.④⑦、③⑤、⑤、②⑥
18.(1)①N ②Al ③s ④Cu (2)①He ②Hg ③CI ④Mn ⑤Mg
19.(1)原子(2)汞原子和氧原子(3)水分子在不断地运动(4)温度降低,分子之间的间隔变小了
20.(1)17质子数不同(2)钠离子氯离子氯原子(3)AA、B
21.(1)相对原子质量=质子数+中子数(2)原子核内不一定有中子(3)质子数不同,元素种类就不同(4)原子核内质子数不一定等于中子数(答案合理即可)
三、实验探究题(每空2分,共24 分)
22.(1)b足量(或过量)(2)A检查装置的气密性(3)1/5氮气难溶于水.(或化学性质不活泼等)
23.(1)红(2)做对比实验(3)D 温度越高,分子运动速率越快(4)能尽量防止氨气逸出污染空气
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
