1.6物质的分离 同步练习(含解析)
图片预览


文档简介
物质的分离
一、单选题
1. 水是宝贵的自然资源,下列净化水的方法中,净化程度最高的是( )
A. 蒸馏 B. 沉淀 C. 过滤 D. 吸附
2. 为了除去粗盐中的Ca2+、Mg2+、SO42﹣等离子,可将粗盐溶于水后进行如下操作:①加入适量盐酸,②加过量NaOH溶液,③加过量Na2CO3溶液,④加过量BaCl2溶液,⑤过滤.下列操作顺序合理的是( )
A. ②③④⑤① B. ②④③⑤① C. ④②③①⑤ D. ④③②①⑤
3. 下列净化水的方法中,净化程度最高的是( )
A. 吸附 B. 沉降 C. 过滤 D. 蒸馏
4. 如图是甲、乙两种固体物质的溶解度曲线.下列说法错误的是( )
A. t℃时甲和乙的溶解度相等 B. t℃时30g乙加到100g水中形成饱和溶液
C. 从甲的饱和溶液中得到甲可用降温结晶的方法 D. 甲的溶解度大于乙的溶解度
5. 自来水厂的净水过程中没有涉及到的净水方法是( )
A. 沉淀 B. 吸附 C. 过滤 D. 蒸馏
6. 2015年4月25日,尼泊尔发生8.1级强震.震后灾区人民须将河水净化成生活用水,常见的净水操作有①过滤、②加明矾吸附、③蒸馏、④消毒杀菌.应选用的净化顺序为( )
A. ①②③④ B. ②④①③ C. ②①④ D. ①③④
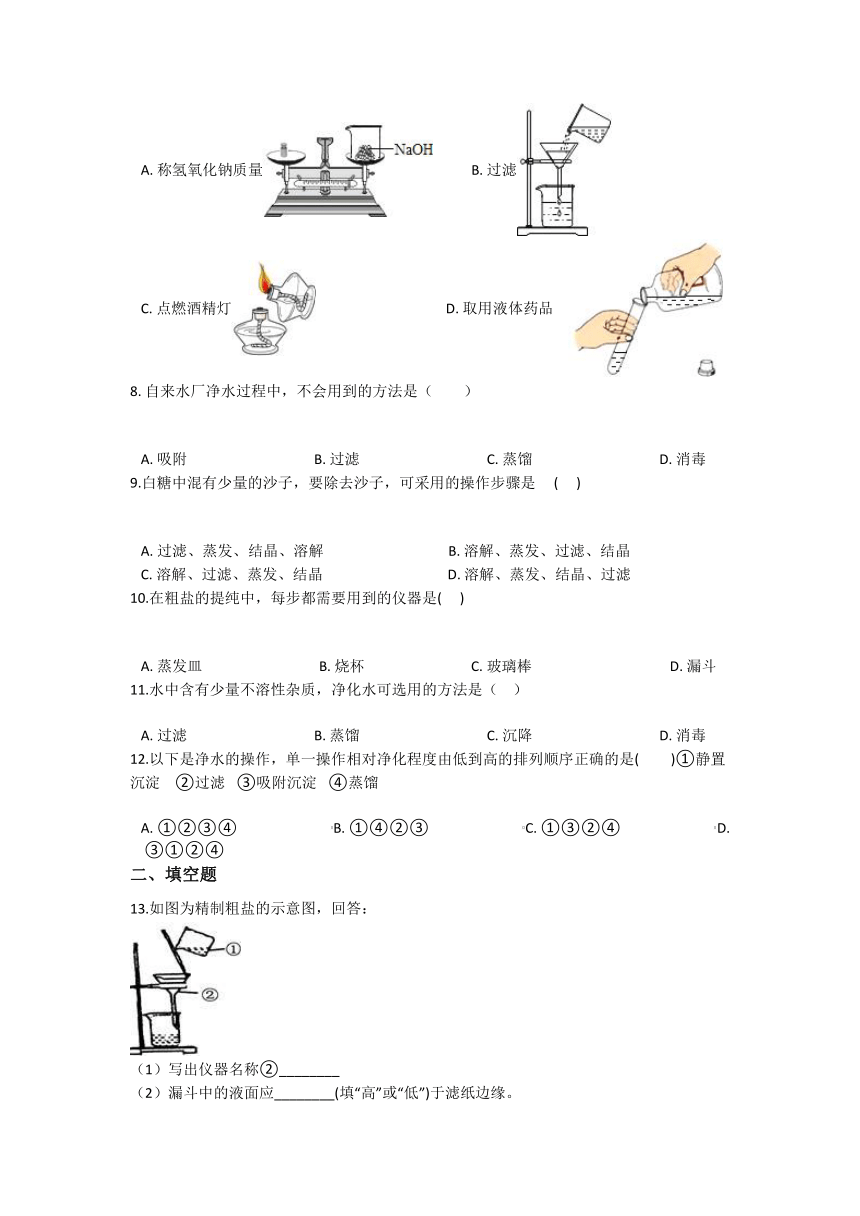
7. 如图的实验基本操作正确的是( )
A. 称氢氧化钠质量 B. 过滤
C. 点燃酒精灯 D. 取用液体药品
8. 自来水厂净水过程中,不会用到的方法是( )
A. 吸附 B. 过滤 C. 蒸馏 D. 消毒
9.白糖中混有少量的沙子,要除去沙子,可采用的操作步骤是 ( )
A. 过滤、蒸发、结晶、溶解 B. 溶解、蒸发、过滤、结晶
C. 溶解、过滤、蒸发、结晶 D. 溶解、蒸发、结晶、过滤
10.在粗盐的提纯中,每步都需要用到的仪器是( )
A. 蒸发皿 B. 烧杯 C. 玻璃棒 D. 漏斗
11.水中含有少量不溶性杂质,净化水可选用的方法是( )
A. 过滤 B. 蒸馏 C. 沉降 D. 消毒
12.以下是净水的操作,单一操作相对净化程度由低到高的排列顺序正确的是( )①静置沉淀 ②过滤 ③吸附沉淀 ④蒸馏
A. ①②③④ B. ①④②③ C. ①③②④ D. ③①②④
二、填空题
13.如图为精制粗盐的示意图,回答:
(1)写出仪器名称②________
(2)漏斗中的液面应________(填“高”或“低”)于滤纸边缘。
14.下图是粗盐提纯实验的部分操作,请回答相关问题。
(1)上图所示操作中,有错误的是________(填字母)。
(2)粗盐提纯的正确操作顺序为________(填字母)。
(3)操作B中,玻璃棒的作用是________。
三、解答题
15.在我国北方有一个盐碱湖,当地居民“夏日晒盐(NaCl),冬天捞碱(Na 2CO3 10H2O)”.你能说明它的原理吗?
答案解析部分
一、单选题
1.【答案】 A
【解析】【解答】蒸馏得到的水中不含有其他的杂质,是净化程度最高的净水方法,观察选项.
故选A.
【分析】根据已有的知识进行分析,蒸馏得到的水中不含有其他的杂质,是净化程度最高的净水方法.
2.【答案】 B
【解析】【解答】解:除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,得到纯净的NaCl,可以先加入过量的氢氧化钠溶液除去镁离子,再加入过量的氯化钡溶液除去硫酸根离子,然后加入过量的碳酸钠溶液除去钙离子和多余的氯化钡,过滤将生成的沉淀除去,此时溶液中含有过量的氢氧化钠溶液和碳酸钠溶液,可以加入适量的盐酸,调节呈中性;氢氧化钠溶液也可以调整顺序,因此顺序可以为:②④③⑤①;或④②③⑤①或④③②⑤①;观察选项.
故选B.
【分析】氢氧化钠可以除去镁离子,碳酸钠可以除去钙离子,氯化钡可以除去硫酸根离子;过滤可以除去不溶于水的物质;稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳;注意要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠进行分析排序.
3.【答案】 D
【解析】【解答】解:A、吸附只会除去水中的异味和色素,不会除去其他可溶性的杂质;
B、沉降只会除去颗粒较大的杂质,不会除去其他的杂质;
C、过滤可以除去不溶性颗粒较小的杂质,不会除去细菌和可溶性的杂质;
D、蒸馏可以将水转化成水蒸气,然后再液化的一种操作,得到纯净的水;
综上所述,净化程度最高的净水方法是蒸馏;故选:D.
【分析】A、根据吸附会除去异味和杂质解答;
B、根据沉降会除去颗粒较大的杂质解答;
C、根据过滤操作的原理进行分析;
D、根据蒸馏可以将水转化成水蒸气,然后再液化得到纯净的水解答.
4.【答案】 D
【解析】【解答】解:A、通过溶解度曲线可知,甲、乙两物质的溶解度曲线在t℃时相较于一点,所以溶解度相等,故A正确;
B、t℃时,乙物质的溶解度时30g,所以30g乙加到100g水中形成饱和溶液,故B正确;
C、甲物质的溶解度随温度的升高而增大,所以从甲的饱和溶液中得到甲可用降温结晶的方法,故C正确;
D、固体物质的溶解度受温度影响较大,所以要比较物质的溶解度,需要指明温度,故D错误.
故选:D.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
5.【答案】 D
【解析】【解答】解:生产自来水的净水方法有沉淀、吸附、过滤、消毒等,不涉及到蒸馏.
答案:D.
【分析】根据已有的知识进行分析,生产自来水的净水方法有沉淀、吸附、过滤、消毒等解答.
6.【答案】 C
【解析】【解答】净化河水时,要先加明矾吸附沉降,使水中的悬浮物沉淀下来,再通过过滤把不溶于水的物质除去,最后通过消毒杀菌可以将河水净化成生活用水.将河水净化成生活用水时一般不用蒸馏的方法.所以C正确.
故选C.
【分析】根据净化水的方法、原理分析排序.
7.【答案】 D
【解析】【解答】A、托盘天平的使用要遵循“左物右码”的原则,氢氧化钠具有腐蚀性必须放在玻璃器皿中称量,故A错;
B、过滤液体时,要注意“一贴、二低、三靠”的原则,图中漏斗的下端没有紧靠烧杯壁,没有用玻璃棒引流,故B错;
C、点燃酒精灯时要用火柴点燃,不能用酒精灯引燃,容易发生火灾,故C错;
D、取用液体药时,瓶塞应倒放,试管应略倾斜,标签应向着手心,瓶口应紧挨着试管口,故D正确.
故选:D.
【分析】A、根据托盘天平的使用要遵循“左物右码”的原则进行分析;
B、过滤液体时,要注意“一贴、二低、三靠”的原则;
C、根据酒精灯的点燃方法考虑;
D、根据取用液体药的注意事项进行分析.
8.【答案】 C
【解析】【解答】生产自来水的净水方法有沉淀、吸附、过滤、消毒等,不涉及到蒸馏.
答案:C.
【分析】根据已有的知识进行分析,生产自来水的净水方法有沉淀、吸附、过滤、消毒等解答.
9.【答案】 C
【解析】
【分析】根据白糖易溶于水,泥沙不溶于水,两种固体物质的溶解性不同,可采用“溶解、过滤、蒸发”的步骤进行分离,据此进行分析判断。
【解答】白糖易溶于水,泥沙不溶于水,两种固体物质的溶解性不同,故除去混在白糖中的少量泥沙,可采用溶解(白糖溶于水,泥沙不溶于水)、过滤(将泥沙除去)、蒸发(除去水分)的方法进行分离。
故选:C
10.【答案】 C
【解析】
【分析】溶解需要烧杯、玻璃棒;过滤需要铁架台、漏斗、烧杯、玻璃棒;蒸发需要铁架台、酒精灯、玻璃棒,以此来解答。
【解答】提纯混有泥沙的食盐,主要操作有溶解、过滤、蒸发,均使用的仪器为玻璃棒,作用分别为搅拌、引流、搅拌(防止局部温度过高)。
故选C
11.【答案】 A
【解析】【解答】将不溶于液体的固体和液体分离的方法是过滤,故选A.
【分析】根据过滤除去的杂质属于不溶于液体的固体。
12.【答案】 C
【解析】【解答】静置沉淀净化程度最低,吸附沉淀比静置沉淀净化程度高,再通过过滤将沉淀除掉,所以过滤要比吸附沉淀净化程度高;蒸馏净化程度最高.
【分析】先沉淀再过滤再蒸馏,净化程度依次升高,沉淀又分为自然沉淀和吸附沉淀。
二、填空题
13.【答案】 (1)漏斗
(2)低
【解析】【分析】(1)根据仪器的名称解答;
(2)如果液面高于滤纸的边缘,那么液体可能会从滤纸和漏斗的接缝中直接流出,从而起不到过滤作用,因此液体的表面必须低于滤纸的边缘。
【解答】(1)根据图片可知,仪器①为漏斗;
(2)漏斗中的液面应该低于滤纸的边缘。
14.【答案】 (1)C
(2)DACB
(3)搅拌,防止液体飞溅
【解析】【分析】(1)在过滤操作时,溶液不能直接倒入漏斗,应该使用玻璃棒引流,防止液体飞溅;
(2)粗盐提纯的基本步骤为:称量、溶解、过滤和蒸发结晶;、
(3)在蒸发结晶时,用玻璃棒不断搅拌,使液体均匀受热,防止液体飞溅。
【解答】(1)在过滤操作时,溶液不能直接倒入漏斗,应该使用玻璃棒引流,因此 上图所示操作中,有错误的C;
(2) 粗盐提纯的正确操作顺序为 称量、溶解、过滤和蒸发结晶,即 DACB ;
(3)操作B中,玻璃棒的作用是搅拌,防止液体飞溅。
三、解答题
15.【答案】 “夏天晒盐”的原理是食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;
“冬天捞碱”的原理是纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
【解析】【解答】“夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
故答案为:“夏天晒盐”的原理是食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;“冬天捞碱”的原理是纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
【分析】根据溶解度受影响的大小,选择结晶的操作方法﹣﹣蒸发结晶或降温结晶法;溶解度受温度影响不大的物质结晶时一般采取蒸发结晶的方法,溶解度受温度影响较大的物质结晶时一般采取降温结晶的方法.
一、单选题
1. 水是宝贵的自然资源,下列净化水的方法中,净化程度最高的是( )
A. 蒸馏 B. 沉淀 C. 过滤 D. 吸附
2. 为了除去粗盐中的Ca2+、Mg2+、SO42﹣等离子,可将粗盐溶于水后进行如下操作:①加入适量盐酸,②加过量NaOH溶液,③加过量Na2CO3溶液,④加过量BaCl2溶液,⑤过滤.下列操作顺序合理的是( )
A. ②③④⑤① B. ②④③⑤① C. ④②③①⑤ D. ④③②①⑤
3. 下列净化水的方法中,净化程度最高的是( )
A. 吸附 B. 沉降 C. 过滤 D. 蒸馏
4. 如图是甲、乙两种固体物质的溶解度曲线.下列说法错误的是( )
A. t℃时甲和乙的溶解度相等 B. t℃时30g乙加到100g水中形成饱和溶液
C. 从甲的饱和溶液中得到甲可用降温结晶的方法 D. 甲的溶解度大于乙的溶解度
5. 自来水厂的净水过程中没有涉及到的净水方法是( )
A. 沉淀 B. 吸附 C. 过滤 D. 蒸馏
6. 2015年4月25日,尼泊尔发生8.1级强震.震后灾区人民须将河水净化成生活用水,常见的净水操作有①过滤、②加明矾吸附、③蒸馏、④消毒杀菌.应选用的净化顺序为( )
A. ①②③④ B. ②④①③ C. ②①④ D. ①③④
7. 如图的实验基本操作正确的是( )
A. 称氢氧化钠质量 B. 过滤
C. 点燃酒精灯 D. 取用液体药品
8. 自来水厂净水过程中,不会用到的方法是( )
A. 吸附 B. 过滤 C. 蒸馏 D. 消毒
9.白糖中混有少量的沙子,要除去沙子,可采用的操作步骤是 ( )
A. 过滤、蒸发、结晶、溶解 B. 溶解、蒸发、过滤、结晶
C. 溶解、过滤、蒸发、结晶 D. 溶解、蒸发、结晶、过滤
10.在粗盐的提纯中,每步都需要用到的仪器是( )
A. 蒸发皿 B. 烧杯 C. 玻璃棒 D. 漏斗
11.水中含有少量不溶性杂质,净化水可选用的方法是( )
A. 过滤 B. 蒸馏 C. 沉降 D. 消毒
12.以下是净水的操作,单一操作相对净化程度由低到高的排列顺序正确的是( )①静置沉淀 ②过滤 ③吸附沉淀 ④蒸馏
A. ①②③④ B. ①④②③ C. ①③②④ D. ③①②④
二、填空题
13.如图为精制粗盐的示意图,回答:
(1)写出仪器名称②________
(2)漏斗中的液面应________(填“高”或“低”)于滤纸边缘。
14.下图是粗盐提纯实验的部分操作,请回答相关问题。
(1)上图所示操作中,有错误的是________(填字母)。
(2)粗盐提纯的正确操作顺序为________(填字母)。
(3)操作B中,玻璃棒的作用是________。
三、解答题
15.在我国北方有一个盐碱湖,当地居民“夏日晒盐(NaCl),冬天捞碱(Na 2CO3 10H2O)”.你能说明它的原理吗?
答案解析部分
一、单选题
1.【答案】 A
【解析】【解答】蒸馏得到的水中不含有其他的杂质,是净化程度最高的净水方法,观察选项.
故选A.
【分析】根据已有的知识进行分析,蒸馏得到的水中不含有其他的杂质,是净化程度最高的净水方法.
2.【答案】 B
【解析】【解答】解:除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,得到纯净的NaCl,可以先加入过量的氢氧化钠溶液除去镁离子,再加入过量的氯化钡溶液除去硫酸根离子,然后加入过量的碳酸钠溶液除去钙离子和多余的氯化钡,过滤将生成的沉淀除去,此时溶液中含有过量的氢氧化钠溶液和碳酸钠溶液,可以加入适量的盐酸,调节呈中性;氢氧化钠溶液也可以调整顺序,因此顺序可以为:②④③⑤①;或④②③⑤①或④③②⑤①;观察选项.
故选B.
【分析】氢氧化钠可以除去镁离子,碳酸钠可以除去钙离子,氯化钡可以除去硫酸根离子;过滤可以除去不溶于水的物质;稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳;注意要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠进行分析排序.
3.【答案】 D
【解析】【解答】解:A、吸附只会除去水中的异味和色素,不会除去其他可溶性的杂质;
B、沉降只会除去颗粒较大的杂质,不会除去其他的杂质;
C、过滤可以除去不溶性颗粒较小的杂质,不会除去细菌和可溶性的杂质;
D、蒸馏可以将水转化成水蒸气,然后再液化的一种操作,得到纯净的水;
综上所述,净化程度最高的净水方法是蒸馏;故选:D.
【分析】A、根据吸附会除去异味和杂质解答;
B、根据沉降会除去颗粒较大的杂质解答;
C、根据过滤操作的原理进行分析;
D、根据蒸馏可以将水转化成水蒸气,然后再液化得到纯净的水解答.
4.【答案】 D
【解析】【解答】解:A、通过溶解度曲线可知,甲、乙两物质的溶解度曲线在t℃时相较于一点,所以溶解度相等,故A正确;
B、t℃时,乙物质的溶解度时30g,所以30g乙加到100g水中形成饱和溶液,故B正确;
C、甲物质的溶解度随温度的升高而增大,所以从甲的饱和溶液中得到甲可用降温结晶的方法,故C正确;
D、固体物质的溶解度受温度影响较大,所以要比较物质的溶解度,需要指明温度,故D错误.
故选:D.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
5.【答案】 D
【解析】【解答】解:生产自来水的净水方法有沉淀、吸附、过滤、消毒等,不涉及到蒸馏.
答案:D.
【分析】根据已有的知识进行分析,生产自来水的净水方法有沉淀、吸附、过滤、消毒等解答.
6.【答案】 C
【解析】【解答】净化河水时,要先加明矾吸附沉降,使水中的悬浮物沉淀下来,再通过过滤把不溶于水的物质除去,最后通过消毒杀菌可以将河水净化成生活用水.将河水净化成生活用水时一般不用蒸馏的方法.所以C正确.
故选C.
【分析】根据净化水的方法、原理分析排序.
7.【答案】 D
【解析】【解答】A、托盘天平的使用要遵循“左物右码”的原则,氢氧化钠具有腐蚀性必须放在玻璃器皿中称量,故A错;
B、过滤液体时,要注意“一贴、二低、三靠”的原则,图中漏斗的下端没有紧靠烧杯壁,没有用玻璃棒引流,故B错;
C、点燃酒精灯时要用火柴点燃,不能用酒精灯引燃,容易发生火灾,故C错;
D、取用液体药时,瓶塞应倒放,试管应略倾斜,标签应向着手心,瓶口应紧挨着试管口,故D正确.
故选:D.
【分析】A、根据托盘天平的使用要遵循“左物右码”的原则进行分析;
B、过滤液体时,要注意“一贴、二低、三靠”的原则;
C、根据酒精灯的点燃方法考虑;
D、根据取用液体药的注意事项进行分析.
8.【答案】 C
【解析】【解答】生产自来水的净水方法有沉淀、吸附、过滤、消毒等,不涉及到蒸馏.
答案:C.
【分析】根据已有的知识进行分析,生产自来水的净水方法有沉淀、吸附、过滤、消毒等解答.
9.【答案】 C
【解析】
【分析】根据白糖易溶于水,泥沙不溶于水,两种固体物质的溶解性不同,可采用“溶解、过滤、蒸发”的步骤进行分离,据此进行分析判断。
【解答】白糖易溶于水,泥沙不溶于水,两种固体物质的溶解性不同,故除去混在白糖中的少量泥沙,可采用溶解(白糖溶于水,泥沙不溶于水)、过滤(将泥沙除去)、蒸发(除去水分)的方法进行分离。
故选:C
10.【答案】 C
【解析】
【分析】溶解需要烧杯、玻璃棒;过滤需要铁架台、漏斗、烧杯、玻璃棒;蒸发需要铁架台、酒精灯、玻璃棒,以此来解答。
【解答】提纯混有泥沙的食盐,主要操作有溶解、过滤、蒸发,均使用的仪器为玻璃棒,作用分别为搅拌、引流、搅拌(防止局部温度过高)。
故选C
11.【答案】 A
【解析】【解答】将不溶于液体的固体和液体分离的方法是过滤,故选A.
【分析】根据过滤除去的杂质属于不溶于液体的固体。
12.【答案】 C
【解析】【解答】静置沉淀净化程度最低,吸附沉淀比静置沉淀净化程度高,再通过过滤将沉淀除掉,所以过滤要比吸附沉淀净化程度高;蒸馏净化程度最高.
【分析】先沉淀再过滤再蒸馏,净化程度依次升高,沉淀又分为自然沉淀和吸附沉淀。
二、填空题
13.【答案】 (1)漏斗
(2)低
【解析】【分析】(1)根据仪器的名称解答;
(2)如果液面高于滤纸的边缘,那么液体可能会从滤纸和漏斗的接缝中直接流出,从而起不到过滤作用,因此液体的表面必须低于滤纸的边缘。
【解答】(1)根据图片可知,仪器①为漏斗;
(2)漏斗中的液面应该低于滤纸的边缘。
14.【答案】 (1)C
(2)DACB
(3)搅拌,防止液体飞溅
【解析】【分析】(1)在过滤操作时,溶液不能直接倒入漏斗,应该使用玻璃棒引流,防止液体飞溅;
(2)粗盐提纯的基本步骤为:称量、溶解、过滤和蒸发结晶;、
(3)在蒸发结晶时,用玻璃棒不断搅拌,使液体均匀受热,防止液体飞溅。
【解答】(1)在过滤操作时,溶液不能直接倒入漏斗,应该使用玻璃棒引流,因此 上图所示操作中,有错误的C;
(2) 粗盐提纯的正确操作顺序为 称量、溶解、过滤和蒸发结晶,即 DACB ;
(3)操作B中,玻璃棒的作用是搅拌,防止液体飞溅。
三、解答题
15.【答案】 “夏天晒盐”的原理是食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;
“冬天捞碱”的原理是纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
【解析】【解答】“夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
故答案为:“夏天晒盐”的原理是食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;“冬天捞碱”的原理是纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
【分析】根据溶解度受影响的大小,选择结晶的操作方法﹣﹣蒸发结晶或降温结晶法;溶解度受温度影响不大的物质结晶时一般采取蒸发结晶的方法,溶解度受温度影响较大的物质结晶时一般采取降温结晶的方法.
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
