期中复习卷4-2021-2022学年九年级化学沪教版(试用本)上册(word版有答案)
文档属性
| 名称 | 期中复习卷4-2021-2022学年九年级化学沪教版(试用本)上册(word版有答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 356.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-28 00:00:00 | ||
图片预览


文档简介
期中复习卷(四)
(满分60分,考试时间40分钟)
本卷可能用到的相对原子质量:H—1 C—12 O—16 Mg-24 S—32 Cl—35.5 K--39
选择题(共20分)
第1—17题只有一个正确选项
1、判断大理石“溶于”稀盐酸是化学变化的依据是
A.溶液质量增加 B.溶液温度升高
C.产生能使澄清石灰水变浑浊的气体 D.固体消失
2、属于物质化学性质的是
A.颜色 B.密度 C.熔点 D.助燃性
3、物质名称与化学式相符合的是
A.水银:Ag B.氧化钠:Na2O2 C.氯化镁:MgCl D.生石灰:CaO
4、下列物质中含有氧分子的是
A.O2 B.H2O2 C.SO2 D.CO2
5、Cr2O3可作为某些化学反应的催化剂,其中Cr元素的化合价为
A. +2 B.+3 C. +5 D.+6
6、下列变化中属于化合反应是
A.甲烷+氧气二氧化碳+水 B.二氧化碳+氢氧化钙碳酸钙+ 水
C.氧化汞 汞+氧气 D.氧气+氢气 水
7、霓虹灯中填充的气体是
A.氧气 B.二氧化碳 C.稀有气体 D.氮气
8、氧元素由游离态变成化合态的变化是
A.氧气变成液氧 B.氯酸钾制氧气 C.双氧水制氧气 D.镁带燃烧
9、如图●和○分别表示两种不同元素的原子,其中表示由不同单质组成的混合物的是
A. B. C. D.
10、在1.0l×105 Pa时,升高温度,液态空气依次先后分离出来的顺序是
A.氮气、氩气、氧气
B.氧气、氩气、氮气
C.氮气、氧气、氩气
D.氧气、氮气、氩气
11、美国发明的月球制氧机可利用太阳光产生的高温使月球土壤发生化学反应而释放出氧气,由此可以推断月球土壤中一定含有
A.氧分子 B.氧元素 C.氯酸钾 D.双氧水
12、为了延缓食品变质,包装时不会采用
A.充入氧气 B.充入氮气 C.放入一小包干燥剂 D.真空包装
13、下图表示初中化学常见实验操作,其中正确的是
14、实验室用酒精在浓硫酸做催化剂和加热到170℃的条件下制取乙烯气体,与选择制取乙烯的发生装置无关的信息是
A.反应物的状态 B.反应温度 C.乙烯的密度 D.催化剂的状态
15、实验室制取氧气,既可用过氧化氢,也可采用分解氯酸钾的方法。两种方法的共同点有
①采用MnO2均可改变其反应速率 ②反应都不需加热
③都利用含氧化合物分解来达到目的 ④两种方法所需仪器相同
A.①③ B.③④ C.①② D.②④
16、做空气中氧气含量测定的实验装置如右图。下列有关说法正确的是
A.选用红磷是因为反应可以耗尽O2,生成固态的P2O5
B.燃烧匙中的红磷可以换成硫或木炭
C.燃烧匙中的红磷越多,水位上升越高
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
17、如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子,则以下对该反应的说法正确的是
A.是化合反应 B.有两种物质生成
C.反应前后分子种类不变 D.参加反应的两种分子个数比为4:1
第18—20题有1—2个正确选项。
18、下列有关CO2的叙述正确的是
A.CO2的摩尔质量是44g B.1mol CO2中含有2mol O
C.CO2的物质的量是CO2的质量 D.CO2中C与O的物质的量之比为1:2
19、关于化学方程式S+O2SO2的描述错误的是
A.此化学反应的基本类型是氧化反应
B.硫燃烧会生成无色无味的气体
C.每1 mol硫和1 mol氧气点燃后反应生成1 mol二氧化硫
D.每1 g硫和1 g氧气反应生成2 g二氧化硫
20、一定质量的碳粉与硫粉混合物,与0.2mol氧气恰好完全反应,全部生成CO2和SO2气体的物质的量共
A.0.05mol B.0.1mol C.0.2mol D.介于0.05mol与0.1mol之间
二、填空题(共20分)
21、如右图所示,“树”的“根部”吸收所需的“营养”元素,在“树”上开出了5朵美丽的“花朵”。请按要求填写相应“花朵”的化学式:
(1) ,
(2) ,
(3) ,
(4) ,
(5) 。
22、化学与生活息息相关,我们的衣食住行都离不开化学。
(1) 如果没有化学的发展,世界就不可能像今天这样丰富多彩。下列事实与化学没有密切关
系的是 。
A.食物、衣料和日常用品的丰盛 B.新材料的开发和利用
C.环境污染的预防和治理 D.物质机械运动的规律
(2) 炎热的夏季自行车胎容易爆裂,原因是 。
(3) 车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料。
乙醇汽油属于 (填“纯净物”或“混合物”);乙醇由 种元素组成,乙醇分子中碳、氢、氧原子的物质的量之比为 ;乙醇中碳元素与氢元素的质量比为 ;乙醇的摩尔质量为 ;92克乙醇中所含分子个数为 。
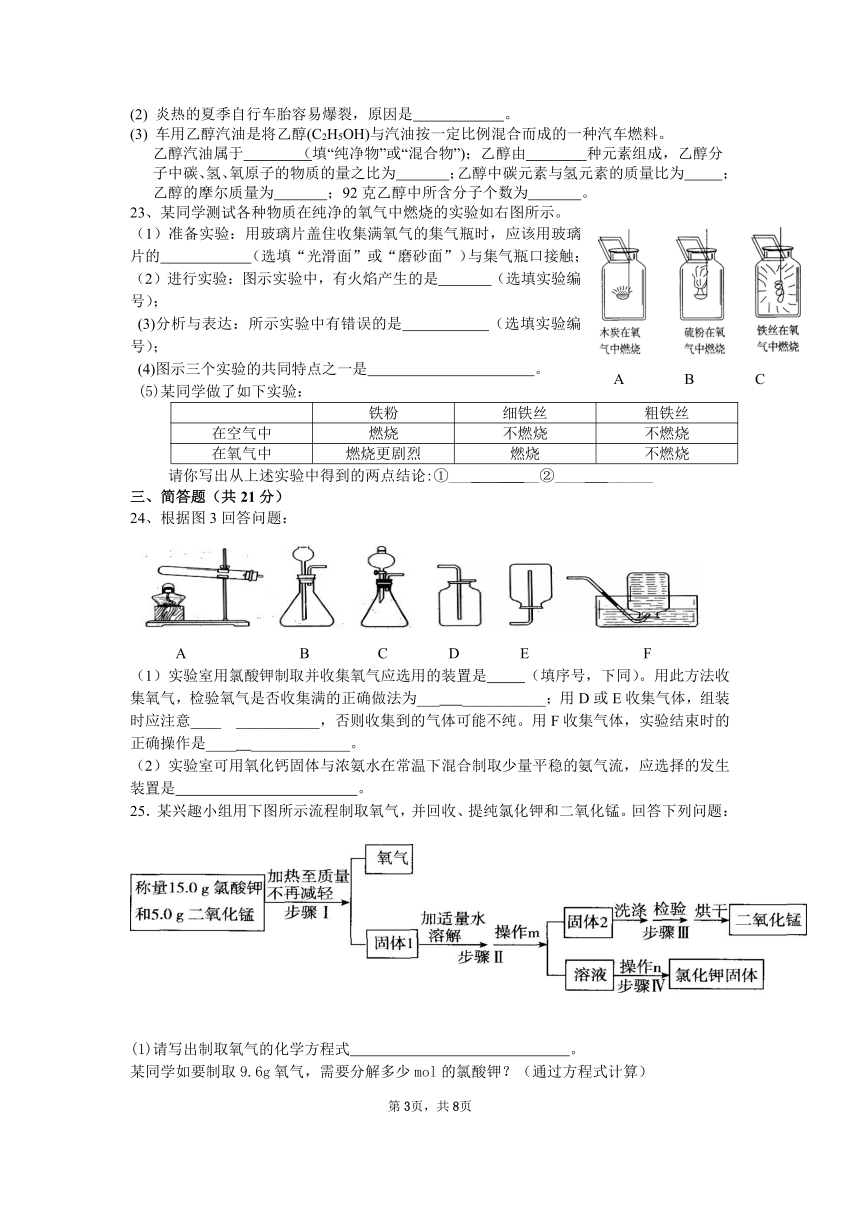
23、某同学测试各种物质在纯净的氧气中燃烧的实验如右图所示。
(1)准备实验:用玻璃片盖住收集满氧气的集气瓶时,应该用玻璃片的 (选填“光滑面”或“磨砂面”)与集气瓶口接触;
(2)进行实验:图示实验中,有火焰产生的是 (选填实验编号);
(3)分析与表达:所示实验中有错误的是 (选填实验编号);
(4)图示三个实验的共同特点之一是 。
(5)某同学做了如下实验:
铁粉 细铁丝 粗铁丝
在空气中 燃烧 不燃烧 不燃烧
在氧气中 燃烧更剧烈 燃烧 不燃烧
请你写出从上述实验中得到的两点结论:①____ _____②____ ______
三、简答题(共21分)
24、根据图3回答问题:
A B C D E F
(1)实验室用氯酸钾制取并收集氧气应选用的装置是 (填序号,下同)。用此方法收集氧气,检验氧气是否收集满的正确做法为___ ___________;用D或E收集气体,组装时应注意____ ___________,否则收集到的气体可能不纯。用F收集气体,实验结束时的正确操作是____ _____________。
(2)实验室可用氧化钙固体与浓氨水在常温下混合制取少量平稳的氨气流,应选择的发生装置是 。
25.某兴趣小组用下图所示流程制取氧气,并回收、提纯氯化钾和二氧化锰。回答下列问题:
(1)请写出制取氧气的化学方程式 。
某同学如要制取9.6g氧气,需要分解多少mol的氯酸钾?(通过方程式计算)
(2)在该反应中二氧化锰的作用是 ,在反应中二氧化锰的质量分数不再变化的实验判断依据是 。
(3)在回收提纯的过程中需要控制水的用量,原因有 (填标号)。
A.提高实验效率 B.保证固体1全部溶解 C.节约能源
(4)为完成上述实验,需要用50 mL的量筒量取30 mL的水,读数时量筒内的液体凹液面最低处与右图中 (填“a”或“b”)处刻度线保持水平。
(5)写出右图中仪器a、b的名称:
a ,b 。
(6)步骤Ⅱ中的操作m应选择右图中 (填“甲”或“乙”)装置,该操作中玻璃棒的作用是 。
(7)实验结束后,称得回收到的氯化钾的质量比理论值小,可能的原因有 (写一点)。
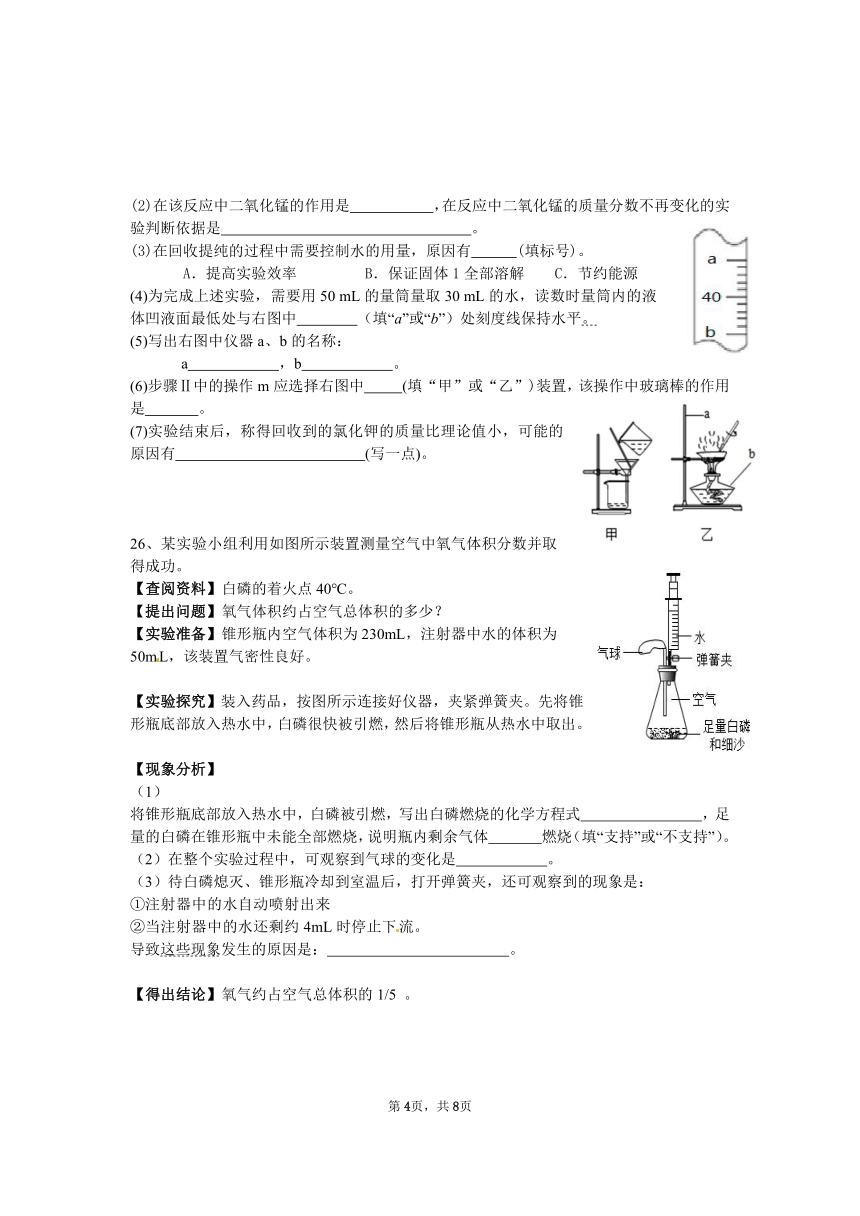
26、某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功。
【查阅资料】白磷的着火点40℃。
【提出问题】氧气体积约占空气总体积的多少?
【实验准备】锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。
【实验探究】装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】
将锥形瓶底部放入热水中,白磷被引燃,写出白磷燃烧的化学方程式 ,足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体 燃烧(填“支持”或“不支持”)。
(2)在整个实验过程中,可观察到气球的变化是 。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:
①注射器中的水自动喷射出来
②当注射器中的水还剩约4mL时停止下流。
导致这些现象发生的原因是: 。
【得出结论】氧气约占空气总体积的1/5 。
一、选择题(共20分,每空1分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C D D A B D C D C A
题号 11 12 13 14 15 16 17 18 19 20
答案 B A B C A A A B、D A、B C
二、填空题20分 答案 得分 说明
1 H2 1分
2 O2 1分
3 CaO 1分
4 CO2 1分
5 CaCO3 1分
6 D 1分
7 分子间间隙变大 1分
8 混合物 1分
9 三/3 1分
10 2:6:1 1分
11 24:6 (4:1) 1分
12 46 g/mol 1分
13 1.204×1024 1分
14 磨砂面 1分
15 B 1分
16 C 1分
17 都是化合反应;都有氧气参与反应;都是氧化反应;生成物都是氧化物;都需要点燃才能反应 1分 合理给分
18 接触面积越大,反应越剧烈 1分 18、19答案可互换
19 在氧气中的反应比空气中反应更剧烈(反应物浓度越大,反应越剧烈) 1分
三、简答题20分 答案 得分 说明
1 AE 或 AF 1分 一个即可
2 带火星的木条伸入集气瓶,木条复燃集气瓶口有气泡往外冒 1分 与前一空答案对应
3 导管伸入集气瓶底部 1分
4 先将导管移出水槽,再熄灭酒精灯 1分
5 C 1分
6 2KClO32KCl+3O2↑ 1分
7 计算过程: 9.6g ÷32 g/mol = 0.3mol2KClO32KCl+3O2↑ 2 3 x 0.3 = (比例式1分) x=0.2 (计算结果1分) 2分
8 催化剂(加快反应速率) 1分
9 固体质量不再减轻 1分
10 A、B、C 1分
11 b 1分
12 铁架台 1分
13 酒精灯 1分
14 甲 3分
15 引流 1分
16 水太少,氯化钾没有完全溶解;未过滤完开始蒸发;蒸发时未搅拌,有液体飞溅 1分 合理给分
17 4P + 5O2 点燃 2P2O5 1分 合理给分
18 不支持 1分
19 先鼓后瘪 1分 合理给分
20 ①白磷燃烧消耗了锥形瓶中的氧气,使瓶中气压降低;
②锥形瓶中氧气约占46mL,当注射器中的水进入锥形瓶约46mL后,瓶中气压与外界相当. 1分 两点需答全,合理给分
注意:整卷方程式没有配平、加条件或标注生成物状态统扣1分
点燃
点燃
加热
A B C
2 3 乙量性质l 乙量性质l
x 0.3
第1页,共6页
(满分60分,考试时间40分钟)
本卷可能用到的相对原子质量:H—1 C—12 O—16 Mg-24 S—32 Cl—35.5 K--39
选择题(共20分)
第1—17题只有一个正确选项
1、判断大理石“溶于”稀盐酸是化学变化的依据是
A.溶液质量增加 B.溶液温度升高
C.产生能使澄清石灰水变浑浊的气体 D.固体消失
2、属于物质化学性质的是
A.颜色 B.密度 C.熔点 D.助燃性
3、物质名称与化学式相符合的是
A.水银:Ag B.氧化钠:Na2O2 C.氯化镁:MgCl D.生石灰:CaO
4、下列物质中含有氧分子的是
A.O2 B.H2O2 C.SO2 D.CO2
5、Cr2O3可作为某些化学反应的催化剂,其中Cr元素的化合价为
A. +2 B.+3 C. +5 D.+6
6、下列变化中属于化合反应是
A.甲烷+氧气二氧化碳+水 B.二氧化碳+氢氧化钙碳酸钙+ 水
C.氧化汞 汞+氧气 D.氧气+氢气 水
7、霓虹灯中填充的气体是
A.氧气 B.二氧化碳 C.稀有气体 D.氮气
8、氧元素由游离态变成化合态的变化是
A.氧气变成液氧 B.氯酸钾制氧气 C.双氧水制氧气 D.镁带燃烧
9、如图●和○分别表示两种不同元素的原子,其中表示由不同单质组成的混合物的是
A. B. C. D.
10、在1.0l×105 Pa时,升高温度,液态空气依次先后分离出来的顺序是
A.氮气、氩气、氧气
B.氧气、氩气、氮气
C.氮气、氧气、氩气
D.氧气、氮气、氩气
11、美国发明的月球制氧机可利用太阳光产生的高温使月球土壤发生化学反应而释放出氧气,由此可以推断月球土壤中一定含有
A.氧分子 B.氧元素 C.氯酸钾 D.双氧水
12、为了延缓食品变质,包装时不会采用
A.充入氧气 B.充入氮气 C.放入一小包干燥剂 D.真空包装
13、下图表示初中化学常见实验操作,其中正确的是
14、实验室用酒精在浓硫酸做催化剂和加热到170℃的条件下制取乙烯气体,与选择制取乙烯的发生装置无关的信息是
A.反应物的状态 B.反应温度 C.乙烯的密度 D.催化剂的状态
15、实验室制取氧气,既可用过氧化氢,也可采用分解氯酸钾的方法。两种方法的共同点有
①采用MnO2均可改变其反应速率 ②反应都不需加热
③都利用含氧化合物分解来达到目的 ④两种方法所需仪器相同
A.①③ B.③④ C.①② D.②④
16、做空气中氧气含量测定的实验装置如右图。下列有关说法正确的是
A.选用红磷是因为反应可以耗尽O2,生成固态的P2O5
B.燃烧匙中的红磷可以换成硫或木炭
C.燃烧匙中的红磷越多,水位上升越高
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
17、如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子,则以下对该反应的说法正确的是
A.是化合反应 B.有两种物质生成
C.反应前后分子种类不变 D.参加反应的两种分子个数比为4:1
第18—20题有1—2个正确选项。
18、下列有关CO2的叙述正确的是
A.CO2的摩尔质量是44g B.1mol CO2中含有2mol O
C.CO2的物质的量是CO2的质量 D.CO2中C与O的物质的量之比为1:2
19、关于化学方程式S+O2SO2的描述错误的是
A.此化学反应的基本类型是氧化反应
B.硫燃烧会生成无色无味的气体
C.每1 mol硫和1 mol氧气点燃后反应生成1 mol二氧化硫
D.每1 g硫和1 g氧气反应生成2 g二氧化硫
20、一定质量的碳粉与硫粉混合物,与0.2mol氧气恰好完全反应,全部生成CO2和SO2气体的物质的量共
A.0.05mol B.0.1mol C.0.2mol D.介于0.05mol与0.1mol之间
二、填空题(共20分)
21、如右图所示,“树”的“根部”吸收所需的“营养”元素,在“树”上开出了5朵美丽的“花朵”。请按要求填写相应“花朵”的化学式:
(1) ,
(2) ,
(3) ,
(4) ,
(5) 。
22、化学与生活息息相关,我们的衣食住行都离不开化学。
(1) 如果没有化学的发展,世界就不可能像今天这样丰富多彩。下列事实与化学没有密切关
系的是 。
A.食物、衣料和日常用品的丰盛 B.新材料的开发和利用
C.环境污染的预防和治理 D.物质机械运动的规律
(2) 炎热的夏季自行车胎容易爆裂,原因是 。
(3) 车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料。
乙醇汽油属于 (填“纯净物”或“混合物”);乙醇由 种元素组成,乙醇分子中碳、氢、氧原子的物质的量之比为 ;乙醇中碳元素与氢元素的质量比为 ;乙醇的摩尔质量为 ;92克乙醇中所含分子个数为 。
23、某同学测试各种物质在纯净的氧气中燃烧的实验如右图所示。
(1)准备实验:用玻璃片盖住收集满氧气的集气瓶时,应该用玻璃片的 (选填“光滑面”或“磨砂面”)与集气瓶口接触;
(2)进行实验:图示实验中,有火焰产生的是 (选填实验编号);
(3)分析与表达:所示实验中有错误的是 (选填实验编号);
(4)图示三个实验的共同特点之一是 。
(5)某同学做了如下实验:
铁粉 细铁丝 粗铁丝
在空气中 燃烧 不燃烧 不燃烧
在氧气中 燃烧更剧烈 燃烧 不燃烧
请你写出从上述实验中得到的两点结论:①____ _____②____ ______
三、简答题(共21分)
24、根据图3回答问题:
A B C D E F
(1)实验室用氯酸钾制取并收集氧气应选用的装置是 (填序号,下同)。用此方法收集氧气,检验氧气是否收集满的正确做法为___ ___________;用D或E收集气体,组装时应注意____ ___________,否则收集到的气体可能不纯。用F收集气体,实验结束时的正确操作是____ _____________。
(2)实验室可用氧化钙固体与浓氨水在常温下混合制取少量平稳的氨气流,应选择的发生装置是 。
25.某兴趣小组用下图所示流程制取氧气,并回收、提纯氯化钾和二氧化锰。回答下列问题:
(1)请写出制取氧气的化学方程式 。
某同学如要制取9.6g氧气,需要分解多少mol的氯酸钾?(通过方程式计算)
(2)在该反应中二氧化锰的作用是 ,在反应中二氧化锰的质量分数不再变化的实验判断依据是 。
(3)在回收提纯的过程中需要控制水的用量,原因有 (填标号)。
A.提高实验效率 B.保证固体1全部溶解 C.节约能源
(4)为完成上述实验,需要用50 mL的量筒量取30 mL的水,读数时量筒内的液体凹液面最低处与右图中 (填“a”或“b”)处刻度线保持水平。
(5)写出右图中仪器a、b的名称:
a ,b 。
(6)步骤Ⅱ中的操作m应选择右图中 (填“甲”或“乙”)装置,该操作中玻璃棒的作用是 。
(7)实验结束后,称得回收到的氯化钾的质量比理论值小,可能的原因有 (写一点)。
26、某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功。
【查阅资料】白磷的着火点40℃。
【提出问题】氧气体积约占空气总体积的多少?
【实验准备】锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。
【实验探究】装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】
将锥形瓶底部放入热水中,白磷被引燃,写出白磷燃烧的化学方程式 ,足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体 燃烧(填“支持”或“不支持”)。
(2)在整个实验过程中,可观察到气球的变化是 。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:
①注射器中的水自动喷射出来
②当注射器中的水还剩约4mL时停止下流。
导致这些现象发生的原因是: 。
【得出结论】氧气约占空气总体积的1/5 。
一、选择题(共20分,每空1分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C D D A B D C D C A
题号 11 12 13 14 15 16 17 18 19 20
答案 B A B C A A A B、D A、B C
二、填空题20分 答案 得分 说明
1 H2 1分
2 O2 1分
3 CaO 1分
4 CO2 1分
5 CaCO3 1分
6 D 1分
7 分子间间隙变大 1分
8 混合物 1分
9 三/3 1分
10 2:6:1 1分
11 24:6 (4:1) 1分
12 46 g/mol 1分
13 1.204×1024 1分
14 磨砂面 1分
15 B 1分
16 C 1分
17 都是化合反应;都有氧气参与反应;都是氧化反应;生成物都是氧化物;都需要点燃才能反应 1分 合理给分
18 接触面积越大,反应越剧烈 1分 18、19答案可互换
19 在氧气中的反应比空气中反应更剧烈(反应物浓度越大,反应越剧烈) 1分
三、简答题20分 答案 得分 说明
1 AE 或 AF 1分 一个即可
2 带火星的木条伸入集气瓶,木条复燃集气瓶口有气泡往外冒 1分 与前一空答案对应
3 导管伸入集气瓶底部 1分
4 先将导管移出水槽,再熄灭酒精灯 1分
5 C 1分
6 2KClO32KCl+3O2↑ 1分
7 计算过程: 9.6g ÷32 g/mol = 0.3mol2KClO32KCl+3O2↑ 2 3 x 0.3 = (比例式1分) x=0.2 (计算结果1分) 2分
8 催化剂(加快反应速率) 1分
9 固体质量不再减轻 1分
10 A、B、C 1分
11 b 1分
12 铁架台 1分
13 酒精灯 1分
14 甲 3分
15 引流 1分
16 水太少,氯化钾没有完全溶解;未过滤完开始蒸发;蒸发时未搅拌,有液体飞溅 1分 合理给分
17 4P + 5O2 点燃 2P2O5 1分 合理给分
18 不支持 1分
19 先鼓后瘪 1分 合理给分
20 ①白磷燃烧消耗了锥形瓶中的氧气,使瓶中气压降低;
②锥形瓶中氧气约占46mL,当注射器中的水进入锥形瓶约46mL后,瓶中气压与外界相当. 1分 两点需答全,合理给分
注意:整卷方程式没有配平、加条件或标注生成物状态统扣1分
点燃
点燃
加热
A B C
2 3 乙量性质l 乙量性质l
x 0.3
第1页,共6页
同课章节目录
